酚醛树脂-重氮萘醌正型光刻胶是由线性酚醛树脂、重氮萘醌型感光剂、添加剂以及溶剂构成.曝光时,重氮萘醌基团转变成烯酮,与水接触时,进一步转变成茚羧酸,从而使曝光区在用稀碱水显影时被除去,显影后得到的图形与掩膜版一样,故酚醛树脂-重氮萘醌光刻胶属于正型光刻胶.此类正胶用稀碱水显影时不存在胶膜溶胀问题,因此分辨率较高,且抗干法蚀刻性较强,故能满足大规模集成电路及超大规模集成电路的制作.紫外正型光刻胶根据所用曝光波长的不同,又可分为g-line(436 nm) 正胶、i-line(365 nm)正胶.两者虽然都是用线型酚醛树脂做成膜树脂,重氮萘醌型酯化物作感光剂,但在酚醛树脂及感光剂在微观结构上均有变化,因此两者性能,尤其是分辨率不一样,应用场合也不同.g-line正胶,适用0.5 μm以上集成电路的制作,而i-line正胶,适用0.30—0.5 μm集成电路的制作.紫外正胶还用于液晶平面显示器等较大面积的电子产品制作.
i-line 光刻技术80年代中期进入开发,90年代初进入成熟,90年代中期进入昌盛并取代了g-line光刻胶的统治地位.i-line光刻胶最初分辨率只能达到0.5 μm,随着i-line 光刻机的性能改进,i-line正胶亦能制作线宽为0.35 μm的集成电路.i-line光刻技术目前仍是最广泛应用的光刻技术,i-line光刻胶仍将在较长一段时间内持续占据相当数量的市场份额.
我国光刻胶的研究始于上个世纪70年代,最初阶段与国际水平相差无几,几乎和日本同时起步,但由于种种原因,差距愈来愈大.国外用于193 nm浸没式光刻的光刻胶早已产业化, EUV(极紫外)光刻胶也日渐成熟,而我国IC(集成电路)用i-line光刻胶全部需要进口.因此,在国内进行i-line光刻胶的研究,进而实现产业化生产是当务之急.
与g-line光刻胶相比,i-line光刻胶仍然是由酚醛树脂、感光剂、添加剂和溶剂等组成,但酚醛树脂的微观结构、感光剂的载体化合物有些发展变化. 2 从 g-line到 i-line,树脂的发展变化
从显影时溶解抑制机理来看,树脂结构和组成的不同造成了对光刻胶性能的影响,主要有两方面的因素:(1)甲酚异构体的结构及甲叉键的位置;(2)树脂的分子量及分子量分布.这些因素影响着显影过程的溶解促进和溶解抑制,从而影响分辨率. 2.1 从g-line发展到 i-line,树脂的邻-邻′相连程度提高
正型光刻胶中的成膜树脂一般为间甲酚、对甲酚与甲醛的缩合物.甲酚异构体具有 不同的活性点,间甲酚具有3个活性点(图1),当间甲酚与其他酚反应时,甲叉键的位置 图1 间甲酚异构体的结构及其甲叉键的位置 Isomeric structure of m-cresol and methylene bond position 图2 对甲酚异构体的结构及其甲叉键的位置 Isomeric structure of p-cresol and methylene bond position 有3种:邻-邻′相连、邻-对相连、邻′-对相连.对甲酚只有两个活性点(图2),甲叉键的位置只有邻-邻′相连.在间/对甲酚体系中,随着对甲酚含量的增加,邻-邻′相连程度增加,聚合物的规整性和刚性增加,在显影液中扩散速度慢,胶膜的溶解速率下降,感光度下降,但感光剂与高邻-邻′相连的树脂间由于氢键作用强,而展示高的溶解抑制性,使曝光区与非曝光区的溶解速率反差增大,胶的分辨率提高.因此,从g-line发展到 i-line,为追求更高的分辨率,树脂的邻-邻′相连程度不断提高.
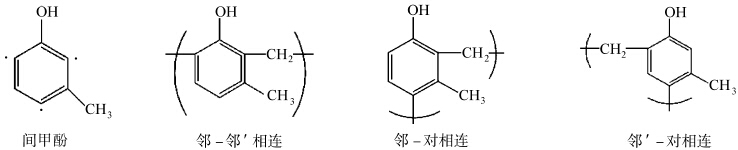 | 图1 间甲酚异构体的结构及其甲叉键的位置 Isomeric structure of m-cresol and methylene bond position |
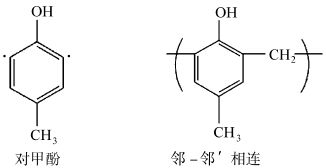 | 图2 对甲酚异构体的结构及其甲叉键的位置 Isomeric structure of p-cresol and methylene bond position |
获得高邻-邻′相连树脂的传统方法是在间甲酚/对甲酚体系中提高对甲酚的投料比.由于间甲酚的反应活性比对甲酚高,在间-对甲酚反应体系中,间甲酚的反应速度大约是对甲酚的9倍,间甲酚先被消耗完,残余的对甲酚要通过高温蒸馏除去,高温蒸馏时,酚醛树脂会发生重排,分子量分布变宽.而且传统的一步法是两相反应,缩聚过程中会引起甲醛的损失,因此传统的一步法制备出的酚醛树脂,分子量大小及分子量分布重复性差,批与批之间质量不稳定.这些树脂还要经过分级,变成Tandem型树脂(树脂的中间分子量所占比例下降),才能得到性能优异的i-line光刻胶[1].分级的产率只有40%—50%,造成树脂的大量浪费,并产生大量的废液.用双官能团单体BHMPC(2,6-双羟甲基-对-甲酚)替代部分对甲酚,可合成出高邻-邻′相连的树脂,分子量及分子量分布低,无对甲酚富集的齐聚物,树脂重复性好,无需分级可直接使用.与传统树脂相比,这种BHMPC树脂具有更好的光刻性能[2].
BHMPC树脂是采用两步缩合法来制备的(图3).第一步:对甲酚预缩合,制备BHMPC单体;第二步:BHMPC单体与间甲酚缩合,得BHMPC树脂.或者间-对甲酚先合成低分子量齐聚物,齐聚物再与BHMPC单体聚合[3,4].
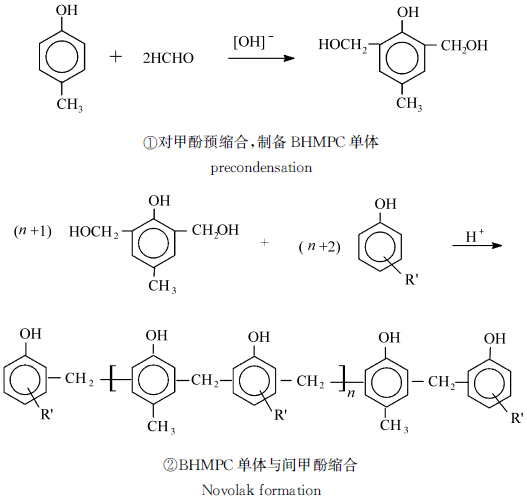 | 图3 BHMPC树脂的两步合成法 Two-step reaction pathway of the novolak synthesis |
如果在聚合体系中引入特定的端基,如2,4-二甲酚、2,6-二甲酚、2,5-二甲酚、3,4-二甲酚等,来控制树脂的分子量和溶解性质,制备出的树脂既具有高邻-邻′相连度的主体结构,而端基又提供了良好的溶解性和感光速度,由此而制备出的i-line正胶分辨率达0.25 μm[5,6].在聚合体系中引入二甲酚端基,还可提高树脂的耐热性. 3 从 g-line到 i-line,感光剂的发展变化
感光剂的作用是促进曝光区的溶解,抑制非曝光区的溶解.重氮萘醌型感光剂的溶解抑制不仅是因为感光剂的疏水性,还有感光剂与树脂的多种作用,如重氮萘醌基团的氢键作用、磺酰酯的氢键作用、静电作用、碱催化偶合反应等有关.感光剂的骨架结构及酯化度会影响这些作用.
与g-line胶相比, i-line胶对感光剂有以下新要求:
(1)光漂白后在365 nm残余吸收小,透过性高.这要求感光剂的骨架在365 nm吸收小,透过性高.
(2)酯化度高,重氮萘醌基团的数目多.
(3)重氮萘醌基团间的距离大,重氮萘醌基团相互之间尽可能远.
(4)感光剂的疏水性大. 3.1 感光剂的骨架在365 nm吸收小,透过性高
传统的二苯甲酮型骨架在g-line是完全透过的,但在i-line有较强的非光漂白性吸收,感光剂的光敏性降低,图形侧壁角减小,分辨率下降,甚至产生footing(底脚)缺陷.通过减少体系离域化程度,可使在i-line的吸收最小化,比如用长链烷基替换一个苯基(见图4),由骨架引起的非漂白吸收大部分被除去了[7].许多非二苯甲酮型化合物在i-line是完全透过的(见图5).
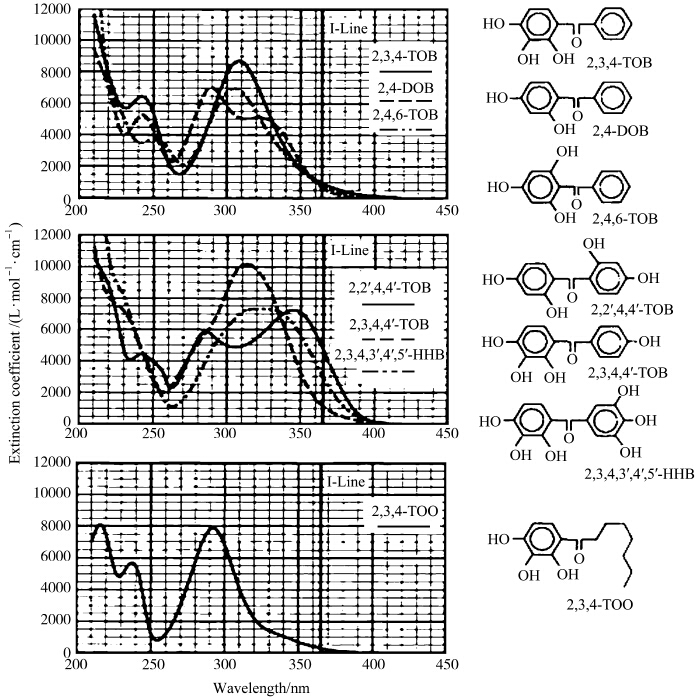 | 图4 羟基苯甲酮的 UV图谱 UV spectra of hydroxyl-substituted benzophenone bakebones |
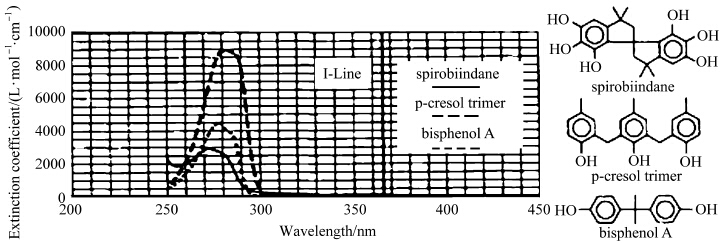 | 图5 非苯甲酮化合物的 UV图谱 UV spectra of non-benzophenone bakebones |
除了考虑感光剂的吸收特性,还要考虑感光剂中重氮萘醌基团间的邻近度.酚醛树脂需要一个空间与重氮萘醌基团形成一个协同球(图6),当重氮萘醌基团靠得太近,协同球相互重叠交叉, 重氮萘醌基团与树脂的接触面积减小,单位重氮萘醌基团的抑制效率下降.而远距离的重氮萘醌基团,协同球在空间上不相连,单位重氮萘醌基团有更大的溶解抑制效率.图5中螺旋二茚衍生出的感光剂,重氮萘醌单元密集,溶解抑制效率低,光刻性 能受到限制.双酚A、对甲酚三聚体、重氮萘醌基团与基团间距离远,溶解抑制效率高.
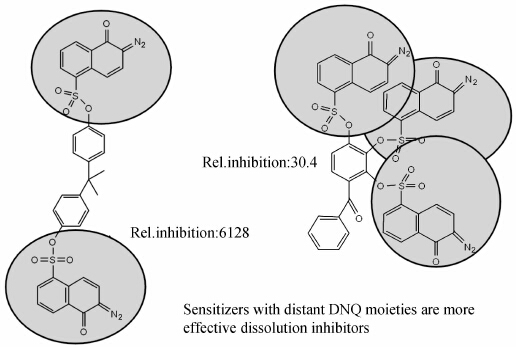 | 图6 重氮萘醌基团邻近度影响示意图[8] Schematic representation of the effect of chromophore(DNQ) proximity |
感光剂的酯化度越高,对树脂的溶解抑制性越强,胶的分辨率高,所以从g-line发展到i-line,感光剂的酯化度呈升高趋势.但感光剂的酯化度升高时,其光敏性下降,溶解性变差.事实上,全酯化的感光剂由于难于溶解而无法实用.
单个—OH由于空间位阻而未被酯化的感光剂与全酯化感光剂相比,溶解抑制作用 没有下降,仍具有高的溶解反差,高分辨力,但光敏性、溶解性更好.这个—OH由于周围 有空间位阻导致不同位置上的OH可选择性酯化.但当未被酯化的—OH超过一个时,感光剂的溶解抑制作用迅速下降.通过感光剂的骨架结构设计及优化反应条件可以实现选择性酯化,制备出单个—OH未被酯化的的感光剂[9,10,11,12,13].
同样的酯化度,疏水性增加(例如在骨架上引入烷基),感光剂的溶解抑制作用增强.
骨架的高透过性、高疏水性,重氮萘醌基团与基团之间布局遥远,单个位阻—OH未被酯化,沿着这一设计准则,研究者们开发了许多高性能的非二苯甲酮系感光剂,图7为一些高性能感光剂的骨架化合物[14,15,16,17,18,19,20,21].
 | 图7 高性能感光剂的骨架化合物 Backbones of high performance photoactive compounds |
传统的高分辨率i-line光刻胶是由高分子量分级树脂与小分子量溶解速率促进剂混合而成 [22,23].树脂分级后,由于低分子量组分被除去,树脂的光敏性下降;光刻胶与基板的粘附性变差,蚀刻时易发生钻蚀、剥离现象,导致抗蚀性下降.在胶中加入具有2—7个酚型羟基官能团并且分子量<1000的芳香族多羟基化合物,不但可提高胶的粘附性,还提高胶的光敏性[24,25,26,27,28].
溶解促进剂必须符合曝光区溶解速率的增加大于非曝光区溶解速率的增加的要求.酚羟基的极性大小决定了它提供H的能力,如感光剂会优先与供H能力最强的酚类化合物形成氢键,因此非曝光区的溶解速率降低;而曝光区,由于感光剂的分解,无氢键作用,低分子量酚类化合物会增加曝光区的溶解速率,从而提高曝光区与非曝光区的溶解速率反差,达到提高分辨率的目的.
一些溶解促进剂的结构如下所示[29,30,31,32,33,34,35]:
 | 图8 溶解促进剂 Dissolution promoter |
i-line 光刻胶还可根据需要加入其他添加剂,如加入表面活性剂来提高胶的流平性,防止条痕的产生,提高膜厚均匀性;加入粘附促进剂,提高光刻胶与基板的粘附性;加入紫外线吸收剂,防止因光的反射而形成驻波. 5 化学增幅型i-line光刻胶
化学增幅型光刻胶具有感光速度快、分辨率高的特点.如果化学增幅型光刻胶能用于i-line光刻,那么i-line光刻胶的性能将得到提高.但传统的产酸剂在紫外区吸收低,造成感光灵敏度低,限制了化学增幅型i-line光刻胶的发展.随着一些在i-line具有高灵敏度、高产酸效率的产酸剂的开发,化学增幅型i-line光刻胶已成为可能[36].
线性酚醛树脂,三嗪类产酸剂、胺类交联剂组成的化学增幅型负型i-line光刻胶,不仅具有感光速度快、分辨率高的特点,而且能经受苛刻的离子注入工艺,已广泛地应用于LED(发光二极管)制造中.线性酚醛树脂或聚羟基苯乙烯树脂、噻吩类产酸剂、双乙烯醚类交联剂组成化学增幅型正型光刻胶,采用高温前烘工艺,使酚醛树脂或聚羟基苯乙烯树脂与双乙烯醚类交联剂在前烘时发生交联.在PEB(曝光后烘烤)期间,在曝光区,酸催化已交联的树脂分解,得高灵敏度(<30 mJ/cm2)、高分辨率正图(分辨率可达0.25 μm),且具有高耐热性(>140℃)[37].理论上讲,用于248 nm、193 nm及EUV光刻中的化学增幅型光刻胶中的聚合物,如果匹配在i-line具有高产酸效率的产酸剂,均有可能用于i-line光刻,如t-BOC protected tetra-C-methyl calix[4](特-丁氧基羰基保护的-C-甲基杯芳烃[4])与产酸剂diphenyliodonium 9,10-dimethoxy anthracene-2-sulfonate(二苯基碘鎓9,10-二甲氧基蒽-2-磺酸酯)组成的光刻胶在i-line曝光,灵敏度高达13 mJ/cm2,图形反差高达12.6[38].然而这些为248 nm、193 nm及EUV光刻设计的聚合物,制备费用比酚醛树脂昂贵得多,这也是化学增幅型正胶没有成为i-line光刻胶主流的原因.
随着集成电路集成度的提高、加工线宽的缩小,对光刻胶分辨率的要求越来越高.根据瑞利原则,缩短曝光波长可以提高光刻分辨率,因此光刻技术经历了从g-line、i-line光刻,到深紫外248 nm、 193 nm光刻以及即将量产化的EUV光刻,相对应于各曝光波长的光刻胶也应运而生.随着曝光波长变化,光刻胶的组成与结构也不断地变化,以使光刻胶的综合性能满足对应集成工艺制程的要求.我国的光刻胶也必然从g-line、i-line光刻胶朝着深紫外248 nm、 193 nm光刻胶以及EUV光刻胶的方向发展.
| [1] | Hanabata M, Oi F, Furuta A. Novolak design for high-resolution positive photoresists (IV): tandem-type novolak resin for high-performance positive photoresists[J].Proc. SPIE,1991,1466:132-140. |
| [2] | Jeffries A, Brzozowy D, Greene N, Kokubo T, Tan S. Novel novolac resins produced from 2,6-bishydroxymethyl-p-cresol, p-cresol, and m-cresol: a method to more evenly distribute p-cresol units throughout a novolac resin[J]. Proc. SPIE,1993,1925:235-245. |
| [3] | Baehr G, Westerwelle U, Gruetzner G.Tailoring of novolac resins for photoresist applications using a two-step synthesis procedure[J].Proc. SPIE, 1997,3049:628-638. |
| [4] | 东京应化工业株式会社.正型光致抗蚀剂组合物以及抗蚀剂图形的形成方法.中国专利,200410005582.9, 2004-02-18. Tokyo Ohka Kogyo Co.Ltd. Positive photoresist composition and process for forming resist pattern. China patent, 200410005582.9, 2004-02-18. |
| [5] | Xu C B, Zampini A, Sandford H F, Lachowski J, Carmody J. Sub-0.25-μm i-line photoresist: the role of advanced resin technology[J].Proc. SPIE,1999,3678:739-750. |
| [6] | Zampini A, Monaghan M J, Xu C B, Cardin W J. Effect of end group on novolak resin properties[J]. Proc. SPIE, 1998,3333: 1241-1250. |
| [7] | Brunsvold W R, Eib N K, Lyons C F, Miura S S, Plat M V, Dammel R R. Novel DNQ PACs for high-resolution i-line lithography[J]. Proc.SPIE, 1992,1672: 273-285. |
| [8] | Uenishi K, Kawabe Y, Kokubo T, Slater S G, Blakeney A J. Structural effects of DNQ-PAC backbone on resist lithographic properties[J].Proc. SPIE, 1991,1466: 102-116. |
| [9] | Jeffries A T, Brzozowy D J, Naiini A A, Gallagher P M. Novel combination of photoactive species: photoresists formed from selectively esterified novolacs and polyfunctional photoactive compounds[J]. Proc. SPIE, 1997,3049: 746-756. |
| [10] | Hanawa R, Uetani Y, Hanabata M. Design of PACs for high-performance photoresists (I): role of di-esterified PACs having hindered -OH groups[J]. Proc. SPIE, 1992,1672: 231-241. |
| [11] | Uenishi K,SakaguchiS, Kawabe Y, Kokubo T, Toukhy M A, Jeffries A T, Slater A G, Hurditch R J. Selectively DNQ-esterified PAC for high-performance positive photoresists[J]. Proc. SPIE, 1992,1672: 262-272. |
| [12] | Hanawa R, Uetani Y, Hanabata M. Design of PACs for high-performance photoresists (II): effect of number and orientation of DNQs and -OH of PACs on lithographic performances[J]. Proc. SPIE, 1993,1925: 227-234. |
| [13] | Pandya A, Trefonas P,Zampini A, Turci P. Highly regioselective PACs for i-line resist design: synthetic reaction model, dissolution kinetics and lithographic response[J]. Proc. SPIE, 1994,2195: 559-575. |
| [14] | Tokyo Ohka Kogyo Co.Ltd.Positive photoresist composition and processing and synthesizing polyphenol compound. US patent, 6492085,2001-12-10. |
| [15] | 三星电子株式会社. 光刻胶组合物、其制备方法和用其形成图纹的方法. 中国专利, 00118160.2,2000-03-30. Samsung Electronics Co., Ltd. Photoresist composition, method of preparation thereof and process for forming resist pattern. China patent, 00118160.2,2000-03-30. |
| [16] | Fuji Photo Film Co.Ltd. Micropattern-forming material having a low molecular weight novolak resin,a quinone diazide sulfonyl ester and a solvent. US patent, 5380618,1995-01-10. |
| [17] | Tokyo Ohka Kogyo Co.Ltd. Positive working photosensitive resin composition containing 1,2-naphthoquinone diazide esterification product of triphenylmethane compound. US patent, 5401605, 1995-03-28. |
| [18] | Tokyo Ohka Kogyo Co.Ltd. Positive photoresist composition and processing and synthesizing polyphenol compound. US patent, 6106994,2000-08-22. |
| [19] | Tokyo Ohka Kogyo Co.Ltd. Positive photoresist composition and process for forming contact hole. US patent, 6177226,2001-01-23. |
| [20] | Tokyo Ohka Kogyo Co.Ltd. Positive photoresist composition. US patent, 6312863,2001-11-06. |
| [21] | Tokyo Ohka Kogyo Co.Ltd. Positive photoresist composition and process for forming resist pattern. US patent, 6406827,2002-06-18. |
| [22] | Rahman M D, Lu P H, Cook M M, Kim W K,Khanna D N. Novolak resin for ultrafast high-resolution positive i-line photoresist compositions[J]. Proc. SPIE, 1998,3333: 1189-1200. |
| [23] | Yu J J, Meister C C, Vizvary G, Xu C B, Fallon P. Sub-0.30-μm i-line photoresist: formulation strategy and lithographic characterization[J].Proc. SPIE, 1998,3333: 1365-1380. |
| [24] | Uetani Y, Tomioka J, Moriuma H, Miya Y.Contrast enhancement by alkali-decomposable additives in quinonediazide-type positive resists[J].Proc. SPIE, 1998,3333: 1280-1287. |
| [25] | Wanat S F, Rahman M D, Dixit S S, Lu P H, McKenzie D S, Cook M M. Novel novolak block copolymers for advanced i-line resists[J]. Proc. SPIE, 1998,3333: 1092-1102. |
| [26] | Cook M M, Rahman M D, Lu P H.Effects of structural differences in speed enhancers (dissolution promoters) on positive photoresist composition[J]. Proc. SPIE, 1998,3333: 1180-1188. |
| [27] | Miyamoto H, Nakamura T, Inomata K, Ota T, Tsuji A. Study for the design of high-resolution novolak-DNQ photoresist: the effects of low-molecular-weight phenolic compounds on resist systems[J]. Proc. SPIE, 1995,2438:223-234. |
| [28] | Shih H I, Reiser A. Dissolution promotion in novolac-diazoquinone resists[J]. Proc. SPIE,1997,3049: 340-344. |
| [29] | 东京应化工业株式会社. 正型光致抗蚀剂组合物以及抗蚀剂图形的形成方法. 中国专利, 03154301.4,2003-08-14. Tokyo Ohka Kogyo Co.Ltd. Positive photoresist composition and process for forming resist pattern.China patent, 03154301.4,2003-08-14. |
| [30] | Tokyo Ohka Kogyo Co.Ltd. Positive working naphthoquinone photoresist containing a cyclohexyl-substituted triphenylmethane compound. US patent, 5501936,1996-03-26. |
| [31] | Miyamoto H, Nakamura T, Inomata K, Ota T, Tsuji A. Study for the design of high-resolution novolak-DNQ photoresist: the effects of low-molecular-weight phenolic compounds on resist systems[J]. Proc. SPIE, 1995, 2438: 223-234. |
| [32] | Kawabe Y, Tan S, Nishiyama F, Sakaguchi S, Kokubo T, Blakeney A J, Ferreira L. Effect of low-molecular-weight dissolution-promoting compounds in DNQ-novolac positive resist[J]. Proc. SPIE, 1996, 2724: 420-437. |
| [33] | 东京应化工业株式会社.正型光致抗蚀剂组合物.中国专利, 200410071372.X,2004-07-23. Tokyo Ohka Kogyo Co.Ltd. Positive photoresist composition. China patent, 200410071372.X,2004-07-23. |
| [34] | Tokyo Ohka Kogyo Co.Ltd. Positive photoresist composition. US patent, 5702861,1997-12-30. |
| [35] | Tokyo Ohka Kogyo Co.Ltd. Positive photoresist composition and process for forming resist pattern using same. US patent, 6379859,2002-04-30. |
| [36] | Asakura T, Yamato H, Matsumoto A, Ohwa M. Novel photoacid generators for chemically amplified resists with g-line, i-line and DUV exposure[J]. Proc. SPIE, 2001, 4345: 484-493. |
| [37] | 东京应化工业株式会社.正型光致抗蚀剂组合物. 中国专利, 200510064839.2,2005-07-23. Tokyo Ohka Kogyo Co.Ltd. Positive photoresist composition. China patent, 200510064839.2,2005-07-23. |
| [38] | Kwon Y G,Kim J K, Fujigaya T, Shibasaki Y,Ueda M. A positive-working alkaline developable photoresist based on partially tert-Boc-protected calix[4] resorcinarene and a photoacid generator[J]. J. Mater. Chem., 2002, 12: 53-57. |



