2. 中国科学院 研究生院, 北京 100049
2. Graduate University of Chinese Academy of Sciences, Beijing 100049, P. R. China
随着大规模集成电路的快速发展,针对光刻技术的要求也在摩尔定律[1]的指引下不断提高[2,3,4].从上世纪80年代开始,光刻技术所使用的光源波长从G线(438 nm)、I线(365 nm),逐步推进到深紫外(DUV,248 nm和193 nm)波长,目前正在发展极紫外(EUV,13.5 nm)技术.虽然光刻分辨率已经进入纳米量级,然而随着纳米器件的发展,不仅要求特征尺寸越来越小,而且要能够实现包括从二维到三维的复杂纳米微结构与器件的制备[5].基于非线性光学原理的飞秒激光多光子光刻技术,由于其不仅可以突破光学衍射极限实现纳米尺度的光刻,还具有实现任意三维复杂结构的加工能力[6],已经成为纳米结构与器件加工中行之有效的手段.
多光子光刻技术的发展和应用需要高性能的光刻胶与之匹配.目前应用于多光子光刻技术的光刻胶多数是基于高分子材料的商品化光刻胶,如SCR500、SU8等负性光刻胶[7],以及Marder等[8,9]报道的高分子正性光刻胶.尽管无定形的高分子光刻胶材料有柔性、易加工等特点[10,11],但是因其分子量较大和分子量分布较宽而造成线边缘粗糙度较大,难以满足纳米加工进一步提高分辨率与光刻质量的要求[12,13,14,15,16].
光刻胶的分辨率和线边缘粗糙度是由主体材料的分子大小所决定的.近年来,针对高分子材料的不足,在光刻胶的研究中已发展出了分子玻璃光刻材料.分子玻璃是无定形的有机小分子化合物,具有确定的分子结构、单一分子量分布和小的分子尺寸,分子间无链缠结.因此,在要求高分辨率和低线边缘粗糙度的纳米加工中,分子玻璃材料比高分子材料更具有潜在的优势[17,18,19].目前,分子玻璃作为光刻胶主体材料已经被应用到电子束(EB)和极紫外(EUV)光刻等研究中,并获得了较高的加工精度和较低的线边缘粗糙度[20,21].Shirota等[22,23,24]相继设计并合成了几种星型多酚类分子玻璃材料,此类化合物在EB光刻中可得到分辨率分别为150 nm、70 nm、40 nm和25 nm的图像.Ober等[25]合成了一系列多酚树脂型分子玻璃光刻胶主体材料,得到了适用于EB和EUV光刻的正性光刻胶.
在多光子光刻技术中,利用分子玻璃光刻胶的特点,有望实现低线边缘粗糙度和高精度的多光子微纳加工,其中,设计并制备可应用于多光子光刻中的分子玻璃正性光刻胶是实现高精度多光子正胶光刻不可或缺的重要材料基础.本文设计合成了杯芳烃衍生物作为分子玻璃的主体材料,与光生酸剂(Photoacid generator,PAG)三氟甲磺酸三苯锍鎓盐进行复配,制备了适合于多光子光刻技术的分子玻璃正性光刻胶.利用1HNMR、FT-IR、DSC、TGA等手段对杯芳烃类衍生物进行了结构鉴定和性能表征,并对光刻胶的成分以及紫外光曝光下的显影工艺进行了优化.在此基础上使用780 nm波长的飞秒激光对杯[4]芳烃分子玻璃正性光刻胶的多光子光刻性能进行了评价. 1 实验部分 1.1 材料与试剂
光生酸剂三氟甲磺酸三苯锍鎓盐(Triphenysulfonium triflate),分析纯,购自Sigma-Aldrich公司;四甲基氢氧化铵(TMAH)溶液(质量分数为10 %),分析纯,购自北京兴福精细化学研究所;对羟基苯甲醛、间苯二酚、4-二甲氨基吡啶、二碳酸二叔丁基酯、无水硫酸镁、N-甲基吡咯烷酮、无水乙醇、乙酸乙酯等为分析纯,环戊酮为化学纯,均购自蓝弋化学试剂公司,使用时未经纯化;DMSO-d6,CDCl3(≧99.8%),由Cambridge Isotope Laboratories Inc提供. 1.2 仪器与测试
紫外可见吸收光谱使用日本Shimadzu公司UV-2550紫外可见分光光度计测定;红外光谱使用美国Varian公司生产的Excalibur 3100傅里叶红外光谱仪测量;1HNMR用德国Bruker公司的AvanceII-400核磁共振波谱仪测量;热重分析(TGA)使用美国TA 仪器公司的Q5000示差热分析仪测量;示差扫描量热分析(DSC)使用美国TA 仪器公司Q2000 量热计测定;紫外高压汞灯,购自北京电光源研究所,波长范围:300 nm—400 nm,功率为32.5 mW/cm2;KW-4A型匀胶机,购自中科院微电子所;X4数字显示熔点仪,购自北京福凯科技发展有限公司;飞秒激光多光子光刻实验在本实验室的纳米光子学超细微加工系统上完成;所有扫描电子显微镜(SEM)照片采用日本Hitachi公司S-4300扫描电子显微镜获取. 1.3 分子玻璃主体材料的合成
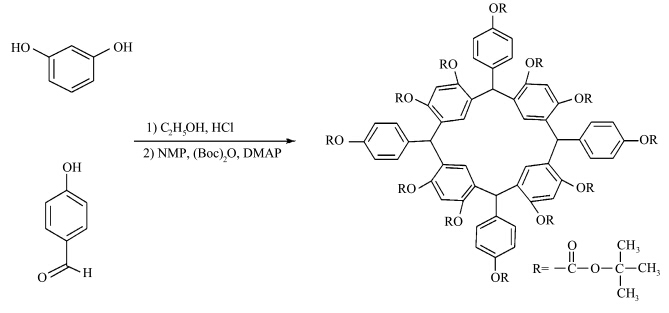
本文中使用间苯二酚和p-羟基苯甲醛在浓盐酸催化的条件下,反应生成周环含有12个酚羟基的杯[4]芳烃化合物;经过叔丁氧基羰基(t-Boc)进行基团保护,得到目标化合物,即t-Boc基团保护的杯[4]芳烃衍生物.根据文献[26]报道,该类化合物具有非平面结构和无定形性特性.合成路线如图1所示
(1)2,8,14,20-四(p-羟基苯基)杯[4]芳烃的合成及结构鉴定
在250 mL三颈瓶中加入间苯二酚(16.572 g,150 mmol),完全溶解于150 mL无水乙醇中,冰水浴条件下加入36%(质量分数)的浓盐酸25 mL,磁力搅拌10 min.然后缓慢加入对羟基苯甲醛(18.302 g,150 mmol),混合液由浑浊变为澄清,加热回流6 h,停止反应并冷却至室温,产生大量固体,抽滤后得到粉红色固体物质,将滤饼用乙醇(100 mL)洗涤两次,丙酮(150 mL)洗涤两次,然后产物在50℃真空烘箱中干燥24 h,得到粉红色固体产物I 27.503 g,产率:85.6%,熔点(DSC数据):404℃.
1HNMR (400 MHz,DMSO-d6):2.50(bs,24H),5.40(s,1H),5.49(s,1H),5.89(m,1H),6.28(m,4H).
产物2,8,14,20-四(p-羟基苯基)杯[4]芳烃的红外光谱图(KBr,cm-1)如图2(A)所示,图中的主要吸收峰包括3386 cm-1处化合物周环上12个酚—OH的伸缩振动峰,1508 cm-1、1431 cm-1、1373 cm-1苯环上CC的伸缩振动峰,1078 cm-1处—C—O伸缩振动峰.
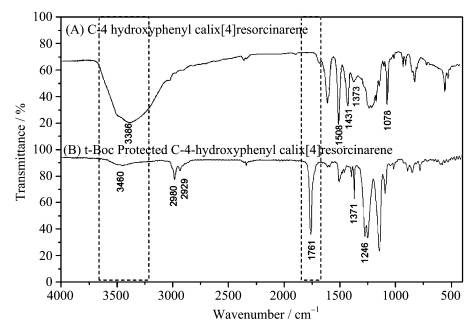 | 图2 (A) 2,8,14,20-四(p-羟基苯基)杯[4]芳烃;(B)t-Boc基团保护的杯[4]芳烃衍生物的红外光谱图 FT-IR spectrum:(A)C-4-hydroxyphenyl calix[4]resorcinarene,(B) t-Boc protected C-4-hydroxyphenyl calix[4]resorcinarene |
(2)t-Boc基团保护的杯[4]芳烃衍生物
在250 mL三颈瓶中将产物I(5.023 g,5.85 mmol)和4-二甲氨基吡啶(0.294 g,2.35 mmol)溶解于100 mL的N-甲基吡咯烷酮中,磁力搅拌,将二碳酸二叔丁基酯(17.144 g,79 mmol)溶解于50 mL N-甲基吡咯烷酮溶液中,并使用恒压滴液漏斗缓慢滴加至三颈瓶中的反应体系,产生大量CO2气体,室温下搅拌24 h,然后将黄色反应液倒入600 mL去离子水中,产生大量沉淀,抽滤得到淡黄色固体,将其溶解于150 mL乙酸乙酯中,并依次用去离子水250 mL洗涤3次,饱和食盐水250 mL洗涤一次,分液得到的有机相用无水硫酸镁干燥,过滤并旋蒸,所得固体在50℃真空烘箱中干燥12 h,得到淡黄色固体产物9.739 g,产率:80.6%.
1HNMR (400 MHz,CDCl3):1.19(s,18H),1.25(s,18H),1.34(s,18H),1.42(s,18H),1.54(s,18H),1.58(s,18H),5.67(s,2H),5.77(s,2H),6.27(dd,4H),6.84(m,16H),7.07(m,4H)
产物t-Boc基团保护的杯[4]芳烃衍生物的红外光谱图(KBr,cm-1)如图2(B)所示.
图2虚线内所示,与2,8,14,20-四(p-羟基苯基)杯[4]芳烃相比,1761 cm-1为t-Boc基团上—CO伸缩振动峰,而未保护的的化合物在该位置附近没有出现峰值,说明了2,8,14,20-四(p-羟基苯基)杯[4]芳烃分子中的—OH t-Boc被基团保护;3460 cm-1处的—OH的伸缩振动峰变得很弱,说明分子中的—OH已经大部分或者全部被基团保护;此外,2980 cm-1、2929 cm-1为t-Boc基团上—CH3的C—H伸缩振动峰,1371 cm-1为t-Boc基团上—CH3的C—H弯曲振动峰,1246 cm-1为C—O伸缩振动峰,以上吸收峰波数基本符合t-Boc基团保护的杯[4]芳烃衍生物的结构特征,从而确认了目标化合物的结构. 1.4 光刻胶成分及TMAH显影液浓度的优化 1.4.1 光生酸剂(PAG)载入量
PAG与主体材料的比例影响着主体材料分子中酸敏t-Boc基团能否被光生酸充分脱保护,从而改变光刻胶材料在显影液中的溶解性.我们考察了不同成分的分子玻璃光刻胶在紫外光下曝光显影的情况,其中分子玻璃主体材料t-Boc保护的杯[4]芳烃衍生物和PAG三氟甲磺酸三苯锍鎓盐的比例如表1所示.将上述两种材料完全溶解于环戊酮中,配制成固含量为3.0%(质量分数)的光刻胶,使用0.22 μm滤膜过滤3次以除去杂质,在玻璃基底上滴加100 μL光刻胶,以4000 rpm/min的转速旋涂30 s,所得薄膜在100℃下前烘2 min,得到300 nm左右的透明薄膜;紫外高压汞灯下样品加掩膜曝光(使用铝箔遮掩部分胶膜,其余部分曝光)5 min;曝光后的胶膜在80 ℃下后烘30 s;使用0.026 mol/L的TMAH水溶液显影3 min,然后,用去离子水清洗、干燥,使用扫描电子显微镜获得曝光图形.
| 表1 生酸剂载入量的优化 The optimization of PAG loaded in resists |
选取PAG三氟甲磺酸三苯锍鎓盐与主体材料t-Boc保护的杯[4]芳烃衍生物比例为10.0%(质量分数)的光刻胶为研究对象,采用与1.4.1 相同的成膜、烘烤和曝光等工艺;分别使用不同浓度的TMAH显影液(如表2所示)显影3 min,然后用去离子水清洗、干燥,使用扫描电子显微镜获得曝光图形.
| 表2 显影液浓度的优化 The optimization of developer’s concentration |
根据光刻胶成分以及显影处理工艺的优化结果,将PAG相对于杯芳烃衍生物主体材料以10.0%溶解于环戊酮溶剂中,配制成固含量为3.0%的光刻胶,完全溶解后使用0.22 μm滤膜过滤3次,在玻璃基底上滴加100 μL的光刻胶溶液,以4000 rpm/min的转速旋涂30 s,所得薄膜在100℃下前烘2 min,得到300 nm左右的薄膜,使用780 nm飞秒激光对薄膜进行多光子曝光,并在80 ℃下后烘30 s,使用浓度为0.026 mol/L的TMAH溶液显影3 min,然后去离子水清洗、干燥,使用扫描电子显微镜观察曝光图形. 2 结果与讨论 2.1 光刻胶成分的性质评价 2.1.1 光生酸剂和杯芳烃主体材料的光谱性质
三氟甲磺酸三苯锍鎓盐的紫外可见吸收光谱如图3(A)所示,其特征吸收峰在232 nm波长处,吸收范围基本上在300 nm波长以下.杯芳烃主体材料的吸收光谱如图3(B)实线所示,其特征吸收峰在272 nm波长处,吸收范围在350 nm以下.
 | 图3 (A)光生酸剂三氟甲磺酸三苯锍鎓盐的紫外可见吸收光谱(乙腈溶液中,2.497╳10-5mol/L) (B)杯芳烃主体材料和光刻胶的紫外可见吸收光谱(乙腈溶液中,主体材料/乙腈为3%,光生酸剂/主体材料为10%) Absorption spectra: (A)photoacid generator(in acetonitrile,2.497mol/L),(B)t-Boc protected calix[4]resorcinarene and molecular glass resist(in acetonitrile,molecular glass/solvent 3%,PAG/molecular glass 10%) |
PAG与主体材料配制成的光刻胶的紫外可见吸收光谱如图3(B)虚线所示,从图中可以看出光刻胶在780 nm波长处没有吸收,表明光刻胶在780 nm飞秒激光照射时发生的是多光子过程.在飞秒激光下光刻时,PAG吸收光子能量并发生均裂,分解生成苯自由基和光生酸剂残留自由基,然后苯自由基与PAG残留自由基继续作用,苯环失氢,体系中生成三氟甲磺酸,在后烘时三氟甲磺酸催化主体材料分子中的t-Boc发生脱保护反应,使主体材料易溶于碱性显影液,从而可以通过显影工艺得到设计加工的图案[19]. 2.1.2 杯芳烃主体材料的热稳定性
在光刻工艺过程中有一些必要的热处理步骤,如前烘、后烘等,为了保持光刻图形在热处理过程中的稳定性和完整性,需要光刻胶主体材料具有较高的玻璃化转变温度(Tg)[27, 28].t-Boc保护的杯芳烃衍生物的差热分析曲线(DSC)如图4(A)所示,结果表明该化合物的Tg在120℃左右;热重分析曲线(TGA)如图4(B)所示,化合物的起始分解温度为150℃,表明该化合物具有较高的热稳定性,能够满足工艺上对光刻胶材料热稳定性的要求,可以用作光刻胶主体材料.
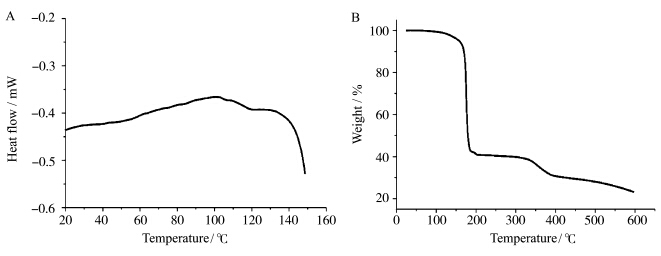 | 图4 (A)t-Boc保护的杯[4]芳烃差热分析图;(B)t-Boc保护的杯[4]芳烃热重分析图 (A)The DSC curve of t-Boc protected calix[4]resorcinarene,(B)The TGA curve of t-Boc protected calix[4]resorcinarene |
此外,从图4(B)可以计算得到化合物的热失重率为59.04%,这与t-Boc基团保护的杯芳烃衍生物的理论热失重率58.90%基本一致,从而进一步证实了该化合物基本上实现了100% t-Boc基团保护. 2.2 光刻胶成分及TMAH显影液浓度的优化 2.2.1 光生酸剂载入量的优化
当PAG载入量为主体材料的5%时(如图5A所示),未曝光区域保留比较完整,但曝光区域有较多残留.当PAG载入量增加至10%时(如图5B所示),未曝光区域仍然完整,而曝光区域清洗相对比较彻底,但是仍有部分残留光刻胶,这可能是因为显影和清洗不完全,处理过程中光刻胶残留在基底表面,也可能是由于PAG的载入量仍然不足,底层光刻胶未能完全发生脱保护反应.当PAG载入量进一步增加至15%时(如图5C所示),曝光区域清洗彻底,但是未曝光区域破坏比较严重,说明PAG载入量过高.因此可以认为PAG与主体材料比例为10%时效果较好.
 | 图5 不同PAG载入量下光刻胶的显影结果 The performance of resists with various PAG loading A:5%,B:10%,C:15% |
当显影液TMAH水溶液浓度为0.013 mol/L和0.026 mol/L时,未曝光区域胶膜保留比较完整,同时曝光区域完全溶解,从而产生较好的对比度(如图6A,6B);当显影液浓度增加到0.065 mol/L以上时,尽管曝光区域溶解完全,但是同时未曝光区域也有不同程度的溶解和破坏(如图6C,6D,6E).综合各种浓度显影液的显影效果,选定0.026 mol/L的TMAH水溶液作为显影液.
 | 图6 不同显影液浓度下光刻胶的显影结果 The performance of resists processed in developers with various TMAH concentrations A-E: 0.013,0.026,0.065,0.13,0.26 mol/L |
使用纳米光子学超细微加工系统,对三氟甲磺酸三苯锍鎓盐和t-Boc基团保护的杯芳烃衍生物配制的分子玻璃光刻胶进行多光子光刻实验.首先,采用不同的曝光功率加工线条结构,得到清晰完整的线条图形.如图7A结果所示,随着飞秒激光加工功率的降低,得到的线宽不断减小,其中最大线宽为806 nm,最细线条线宽为180 nm.图7B是加工的线宽随激光功率的变化曲线,从中可以看出,线宽与激光功率之间呈非线性关系,进一步对激光功率与线宽进行拟合,得到如下的关系式:

式(1)中W为线宽,P为激光功率,a,b均为常数,拟合值分别为590.0和0.1233,这与多光子加工负胶所得到的功率线宽关系相吻合[29, 30].此外,使用适中的激光功率20.2 mW进行多光子光刻,得到线宽为393 nm清晰完整的螺旋线二维图形,如图7C所示;进一步加工得到了尺寸为30.34 μm×28.95 μm的本实验室徽标,如图7D所示.以上光刻实验结果说明该分子玻璃正性光刻胶,可以应用于复杂结构的多光子光刻.
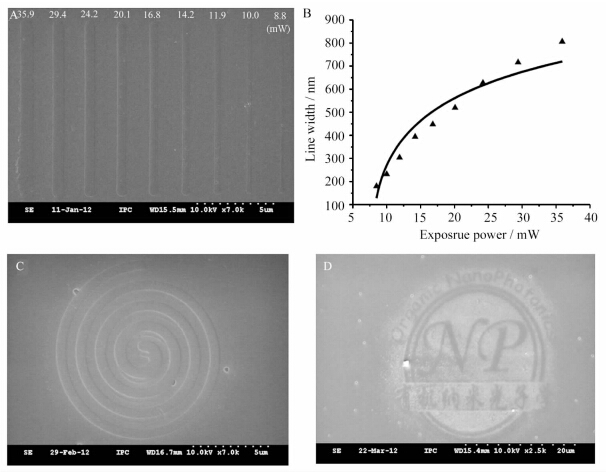 | 图7 (A) 不同曝光功率下的线条(35.9 mW—8.5 mW);(B)曝光功率和线宽的关系; (C)固定功率下(20.2 mW)曝光得到螺旋线;(D)固定功率下(20.2 mW)得到的实验室徽标 SEM images of pattern with multi-photon lithography(A)line/space pattern with various exposure dose(35.9 mW—8.5 mW),(B)the relationship between exposure power and line width, (C)spiral lines with fixed exposure dose(20.2 mW),(D)LaONP logo with fixed exposure dose(20.2 mW) |
通过间苯二酚和p-羟基苯甲醛的酸催化反应,设计合成了具有较高Tg的t-Boc基团保护的杯[4]芳烃功能化衍生物,紫外可见吸收光谱和热稳定性结果表明该化合物是比较理想的光刻胶主体材料.使用三氟甲磺酸三苯锍鎓盐作为光生酸剂与t-Boc保护的杯[4]芳烃主体材料配制成正性分子玻璃光刻胶,使用780 nm波长飞秒激光进行多光子光刻,得到最小线宽在180 nm左右的线条和清晰完整的复杂二维图形.通过优化上述分子玻璃正性光刻胶材料配比和光刻条件,有望进一步提高多光子光刻分辨率,实现纳米尺度高质量光刻图形的制备.
| [1] | Moore G E. Lithography and the future of Moore’s law[J]. Proc. SPIE, 1995, 2438: 2-17. |
| [2] | Wagner C, Harned N. EUV lithography: lithography gets extreme[J]. Nat. Photonics., 2010, 4: 24-26. |
| [3] | Ito T, Okazaki S. Pushing the limits of lithography[J]. Nature, 2000, 406: 1027-1031. |
| [4] | 许 箭,陈 力,杨国强,等. 先进光刻胶材料的研究进展[J], 影像科学与光化学, 2011, 29(6): 417-429. Xu J, Chen L, Yang G Q, et al. Molecular structure of advanced photoresists[J]. Imaging Science and Photochemistry, 2011, 29(6): 417-429. |
| [5] | Pires D, Hedrick J L, Silva A D, Duerig U, Knoll A W. Patterning of molecular resists byscanning probes[J]. Science, 2010, 328: 732-735. |
| [6] | Kawata S, Sun H B, Tanaka T, Takada K. Finer features for functional microdevices[J]. Nature, 2001, 412(6848): 697-698. |
| [7] | 董贤子, 陈卫强, 赵震声, 段宣明. 飞秒脉冲激光双光子微纳加工技术及其应用[J], 科学通报, 2008, 53: 2-13. Dong X Z, Chen W Q, Zhao Z S, Duan X M. Two-photon micro/nano fabrication technology and its applicationby femto-second pulsed laser[J]. Chinese Science Bulletin, 2008, 53: 2-13. |
| [8] | Zhou W H, Ober C K, Perry J W, Marder S R. An efficient two-photon-generated photoacid applied to positive-tone 3D microfabrication[J]. Science, 2002, 296: 1106-1109. |
| [9] | Yu T Y, Ober C K, Marder S R, Perry J W. Chemically amplified positive resists for two-photon three-dimensional microfabrication[J]. Adv. Mater., 2003, 15(6): 517-521. |
| [10] | Yang D, Chang S W, Ober C K. Molecular glass photoresists for advanced lithography[J]. J. Mater. Chem., 2006, 16: 1693-1696. |
| [11] | 刘 娟,孔繁荣,余金星,王力元. 含碘鎓盐光产酸剂和增感染料的化学增幅性i-线正性光致抗蚀剂[J]. 影像科学与光化学, 2011, 29(6): 430-437. Liu J, Kong F R, Yu J X, Wang L Y. Chemically amplified positive i-line photoresist containing iodonium salt PAG and dye sensitizers[J]. Imaging Science and Photochemistry, 2011, 29(6): 430-437. |
| [12] | Cao H B, Roberts J M, Rice B J, et al. Highly sensitive positive-working molecular resist based on new molecule [J]. Proc. SPIE, 2003, 5039: 484. |
| [13] | Cobb J L, Brainard R L, Dentinger P M, et al. EUV lithography: patterning to the end of the road[J]. Mater. Res. Soc. Symp. Proc., 2002, 705: 91. |
| [14] | Prabhu V M, VanderHart D L, Wu W L, et al. Photoresist latent and developer images as probed by neutron reflectivity methods[J]. Adv.Mater., 2011, 23: 388-408. |
| [15] | Pfeiffer F, Felix N M, Ober C K, Schmidt H M. Physical vapor deposition of molecular glass photoresists: a new route to chemically amplified patterning[J]. Adv.Funct. Mater., 2007, 17(14): 2336-2342. |
| [16] | VanderHart D L, Prabhu V M, Silva A D, Felix N M, Ober C K. Solid state NMR investigation of photoresist molecular glasses including blend behavior with a photoacid generator[J]. J. Mater. Chem., 2009, 19: 2683-2694. |
| [17] | Hattori S, Koshiba T, Nakasugi T. High resolution positive-working molecular resist derived from truxene[J]. J. Photopolym. Sci. Technol., 2009, 22(5): 609-614. |
| [18] | Nishikubo T, Kudo H J. Recent development in molecular resists for extreme ultraviolet lithography[J]. J. Photopolym. Sci. Technol., 2011, 24: 9-18. |
| [19] | Dai J, Chang S W, Hamad A, Yang D, Felix N, Ober C K. Molecular glass resists for high-resolution patterning[J]. Chem. Mater., 2006, 18(15): 3404-3411. |
| [20] | KadotaT, Kageyama H, Wakaya F, Gamo K, Shirota Y. Amorphous molecular materials: development of novel negative electron-beam molecular resists[J]. Mater. Sci. Eng., C, 2001, 16(1-2): 91-94. |
| [21] | Yasuhiko S. Photo- and electroactive amorphous molecular materials molecular design, syntheses, reactions, properties, and applications[J]. J. Mater. Chem., 2005, 15(1):75-93. |
| [22] | Yoshiiwa M, Kageyama H, Shirota Y, Wakaya F, Gamo K, Takai M. Novel class of low molecular-weight organic resists for nanometer lithography[J]. Appl. Phys. Lett.,1996, 69(17): 2605-2607. |
| [23] | Yasuhiko S.Organic materials for electronic and optoelectronic devices[J]. J. Mater. Chem., 2000, 10(1): 1-25. |
| [24] | Kadota T, Kageyama H, Wakaya F, Gamo K, ShirotaY. Novel electron-beam molecular resists with high resolution and high sensitivity for nanometer lithography[J]. Chem. Lett., 2004, 33(6): 706-707. |
| [25] | Seung W C, Ramakrishnan A, Daniel B, DaY, Nelson F, Heidi B C, Hai D, Ober C K. Sub-50 nm feature sizes using positive tone molecular glass resists for EUV lithography[J]. J. Mater. Chem., 2006, 16(15): 1470-1474. |
| [26] | Kudo H, Nishikubo T, et al. Molecular waterwheel (Noria) from a simple condesion of resorcinol and an alkanedial[J]. Angew. Chem. Int. Ed., 2006, 118: 8116-8120. |
| [27] | Felix N M, Silva A D, Ober C K. Calix[4] resorcinarene derivatives as high resolution resist materials for supercritical CO2 processing[J]. Adv.Mater., 2008, 20: 1303-1309. |
| [28] | Sha J, Prabhu V M, Bonnesen P V, Ober C K. Architectural effects on acid reaction-diffusion kinetics in molecular glass photoresists[J]. Chem. Mater., 2010, 22: 3093-3098. |
| [29] | Dong X Z, Zhao Z S, Duan X M. Improving spatial resolution and reducing aspect ratio in multiphoton plolymerization nanofabrication[J]. Appl. Phys. Lett., 2008, 92: 091113. |
| [30] | Serbin J, Chichkov B N, Houbertz R, Popall M. Femtosecond laser-induced two-photon polymerization of inorganic-organic hybrid materials for applications in photonics[J]. Opt. Lett., 2003, 28(5): 301-303. |