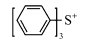
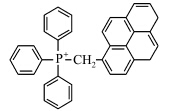
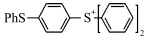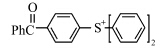紫外光(UV)固化具有环境污染少、固化速度快、能源消耗低等优点,广泛应用于涂料、油墨、胶黏剂等领域.紫外光固化树脂体系主要由光引发剂、反应性低聚物、活性稀释剂和其它添加剂组成[1].光引发剂是紫外光固化树脂体系的关键组分,它对光固化起决定性作用.按反应机理的不同,光引发剂可分为自由基型和阳离子型两种.阳离子光引发剂主要有芳基重氮盐、二芳基碘鎓盐、三芳基硫鎓盐和芳基茂铁盐等.芳基茂铁盐[2]是新开发的阳离子光引发剂,它的最大吸收峰波长大于360 nm,甚至可延伸至可见光区,能够与紫外光源的发射光谱相匹配,然而其摩尔消光系数低,引发速率慢,工业化产品较少.芳基重氮盐光解时会释放出氮气,在固化物中形成气泡,目前已被淘汰.二芳基碘鎓盐和三芳基硫鎓盐[3, 4] 光引发活性高,是阳离子光引发剂的主要商品.
阳离子光引发剂产生的活性种寿命长,具有后固化作用,且阳离子光固化体积收缩小,内应力低,尺寸精度高,性能独特.鎓盐光引发剂是目前快速成型光固化树脂体系的最佳候选引发剂.然而,一般UV固化光源的主发射波长在365 nm附近,用于快速成型的激发光源辐射一般为355 nm的单色激光,而鎓盐光引发剂的吸收波长多在250—300 nm,与UV固化光源的发射光谱不匹配.为了提高光引发速率和光能利用率,许多科技工 作者努力研究阳离子光引发剂及其敏化[5].本文着重介绍了阳离子光引发剂敏化的研究进展. 1 阳离子光引发剂的敏化
阳离子光引发剂敏化的常用方法有:(1)添加光敏剂;(2)扩大引发剂分子的共轭程度,使吸收光谱红移;(3)键合生色基团.以下针对这3个方面进行介绍. 1.1 添加光敏剂
光敏剂[6]是指能扩大光引发剂光谱响应范围的物质,可分为化学光敏剂和光谱光敏剂.化学光敏剂可提高光子的量子效率;而光谱光敏剂可扩大体系的吸收波长范围.一般用于阳离子光引发剂的是光谱光敏剂,其敏化作用主要有4种途径,以下分别介绍它们的敏化机理. 1.1.1 能量转移机理
光敏剂吸收光子达到激发态,然后受激光敏剂分子和光引发剂分子发生共振或电子交换,将激发能转移到引发剂分子,其敏化过程如图1所示.能量转移是经典的敏化机理,可以通过激发单重态或三重态进行,三重态的寿命较长,能量转移更普遍.
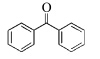
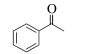
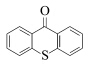
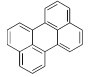
能量转移的必备条件是光敏剂的激发能大于或等于光引发剂的激发能,即E*(S)≥E*(I).表1列出了一些光引发剂和光敏剂的吸收峰波长、消光系数和激发态能量.
| 表1 部分鎓盐和光敏剂激化态能量和最大吸收波长[10,11,12] Triplet or singlet excitation energies and absorption maxima of photoinitiators and photosensitizers[10,11,12] |
光敏剂受紫外光激发产生自由基,自由基作为电子给体还原鎓盐光引发剂,从而产生碳阳离子活性中心,引发单体聚合[13].Timpe等[14]研究了安息香双甲醚(BDMK)、安息香异丙基醚(BIPE)和α-苯基苯偶姻(α-PhB)对苯基缩水甘油醚/二芳基碘鎓盐体系光引发聚合反应的影响.通过测量反应物的聚合速率和量子产率,得出敏化效果依次为BDMK>BIPE>α-PhB的结论.Yagci等[15]在乙烯基醚/碘鎓盐体系中添加α,α-二甲基苯偶酰缩酮(DMPA)、二苯甲酮和噻吨酮,在高压汞灯光化学反应器中照射一段时间,分离反应产物,测定单体转化率和产物分子量及分子量分布.结果表明DMPA、二苯甲酮和噻吨酮都使单体转化率和产物分子量分布增加.他们认为体系发生了多步反应,光敏剂首先吸收光子,光解产生自由基,然后碘鎓盐夺取该自由基上的电子,产生正碳活性中心,引发乙烯基醚单体聚合.此类光敏剂除了常用的自由基光引发剂外,还包括一些 染料.Narewska等[16]制备了荧黄素染料,把它添加到鎓盐引发的1,2-环氧环己烷(cyclohexene oxide,CHO)树脂体系中,室温下在高压汞灯光反应器中反应一段时间,分离反应产物,测定单体转化率和光引发剂的量子产率,用傅利叶实时红外跟踪反应过程.结果表明,加入荧黄素染料可以提高光引发剂的量子产率和CHO的聚合速率.他们认为荧黄素染料在受到光照后激发光解,随即与鎓盐分子通过电子转移发生光氧化还原反应,生成新的自由基阳离子活性中心,引发环氧环己烷单体聚合.近年来,有人开始研究由复合光敏剂组成的多组分光固化体系.Cook等[17]通过Photo-DSC研究樟脑醌(CQ)、二芳基碘鎓六氟磷酸盐(Ph2I+PF6-)和胺衍生物组成的三元引发体系,结果表明CQ/ Ph2I+PF6-/amine三元体系引发单体的聚合速率远高于CQ/amine和CQ/Ph2I+PF6-体系.CQ在紫外光照下会发生褪色反应,当没有胺存在时,CQ的光致褪色有一个诱导期,导致CQ/Ph2I+PF6-体系聚合速率不高,而三元体系有高的聚合速率.他们认为CQ/ Ph2I+PF6-/amine体系的引发机理为,首先CQ吸收光子达到激发态,然后激发态CQ分子与胺发生氧化还原反应,生成羰基自由基和胺烷基自由基,生成的羰基自由基再与碘鎓盐反应,形成具有高活性的反应中心,引发单体聚合.
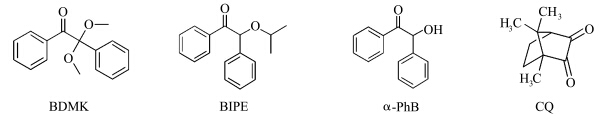 | 图2 BDMK、BIPE、α-PhB和CQ分子结构式 Structural formula of BDMK,BIPE,α-PhB and CQ |
鎓盐的还原电势与它自身的吸电子能力相关.二芳基碘鎓盐具有相对高的还原电势,一般自由基光引发剂都可提高碘鎓盐的光引发速率.而三芳基硫鎓盐的还原电势较低,只能用强亲核性的自由基还原,提高光引发速率[18]. 1.1.3 激发态复合物电子转移机理
光敏剂吸收紫外辐射跃迁至激发态,受激光敏剂分子与基态光引发剂分子络合,形成激发态复合物;然后激发态复合物发生内部电子转移,光敏剂分子跃迁回基态,光引发剂分子达到激发态.其敏化机理如图3所示,光敏剂PS在紫外光照下吸收光子跃迁到激发态,之后与鎓盐分子形成激发态复合物,最后激发态复合物发生电子转移并分解产生阳离子活性中心,引发单体聚合.
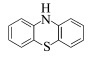
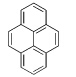
此类光敏剂有二苯酮、蒽、芘、苝、硫杂蒽酮、吩噻嗪和乙烯基咔唑等稠环类芳烃化合物[20].蒽和吩噻嗪[21]与光引发剂分子之间发生电子转移的吉布斯自由能变化较小,光敏化更容易,是鎓盐体系的有效光敏剂.Crivello[22]把苯并吩噻嗪和苯并吩噁嗪添加到三芳基硫鎓盐中,对比光照前后紫外吸收光谱,发现光照后体系在长波范围有明显的吸收,用红外测温仪监测聚合反应过程中的热效应,发现加入光敏剂后反应物温度明显增加,表明苯并吩噻嗪和苯并吩噁嗪提高了反应速度.他们还研究染料作为鎓盐的电子转移光敏剂[23],将姜黄色素及其衍生物添加到环氧化合物/碘鎓盐体系,用高压汞灯或LED激发体系反应,用红外测量实时监测反应物温度和Photo-DSC分析树脂体系的反应热.实验结果证明姜黄色素提高反应物温度,是一种有效的电子转移光敏剂.Gomurashvili等[24]证明吩噻嗪是鎓盐体系优良的电子转移光敏剂.
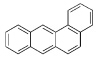
研究人员在光敏剂的分子设计和合成方面进行了大量尝试,James等[25]合成了几种蒽的衍生物,研究它们在各种单体中的反应活性,评价它们对碘鎓盐和硫鎓盐的敏化效果,发现9,10-二烷氧基蒽具有很好的光敏化效果.他们也考察了芳烃和芳酮对硫鎓盐的敏化效果及机理[26],芳烃类光敏剂包括苯并蒽、六苯并苯、苝、芘和吩噻嗪等;芳酮类光敏剂包括蒽醌、苯甲酮、硫杂蒽酮、芴酮等.Bulut等[27]制备了两种苯并三唑衍生物BEBT和HTBT,分子共轭程度高,对340—460 nm的光具有较强的吸收,把它们添加到二芳基碘鎓盐环氧化合物体系中,发现该体系光引发速率大大提高.
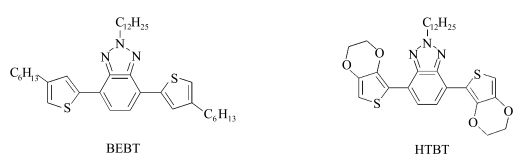 | 图4 苯并三唑衍生物BEBT和HTBT分子结构式 Structural formula of benzotriazole derivatives BEBT and HTBT |
光敏剂分子的光解碎片与光引发剂分子发生加成反应,从而使光引发剂激发.Denizligil等[28, 29] 在烯丙基硫鎓盐光引发体系中加入苯偶姻或酰基磷氧化物(TMDPO),研究其光化学反应,提出了碎片加成敏化新机理,其敏化机理示意于图5.
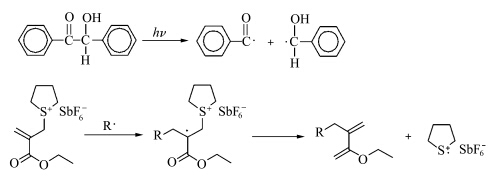 | 图5 碎片加成敏化示意图 Schematic diagram of addition fragmentation reactions |
由图5可知碎片加成过程主要分三步:第一步,自由基光引发剂分子在紫外光的照射下发生碳碳键的均裂,生成活性自由基R·;第二步,生成的活性自由基R·加成到烯丙基硫鎓盐分子上的双键,在β位产生一个自由基,形成自由基中间体;第三步,由于该中间体不稳定,会进一步分解,生成具有更高引发活性的自由基阳离子活性中心,引发阳离子聚合反应.
Reetz等[30]合成了一种新型的阳离子光引发剂烯丙氧基-甲基吡啶鎓盐(MAP+SbF6-),分子中引入了可加成的烯丙基双键,其最大吸收波长小于300 nm,当加入苯偶姻作为光敏剂时,吸收波长可延伸至370 nm.
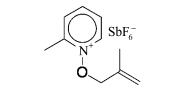 | 图6 MAP+SbF6-分子结构式 Structural formula of the molecule MAP+SbF6- |
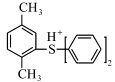
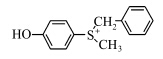
早期开发的阳离子光引发剂结构简单,它们的吸收光谱一般在远紫外区.扩大生色基团的共轭程度,可使引发剂的吸收光谱红移,同时增大消光系数.Crivello等[31,32,33]把苯甲酰甲基、2-茚酮基和4-甲氧基苯甲酰甲基等基团键合到硫鎓盐的生色基团上,得到了一系列共轭程度不同的光引发剂,测试它们的紫外吸收光谱.所得光谱特性如表2所示,随着取代基共轭程度增加,光引发剂的紫外吸收峰红移增加.
| 表2 含不同取代基鎓盐分子的吸收波长和消光系数 Absorption and extinction coefficients of onium salt molecules with different substituent group |
在添加光敏剂的体系中,光敏化过程是多分子作用的结果,有赖于分子的扩散,敏化效果受体系黏度的影响.将生色基团键合到鎓盐分子上可以克服体系黏度的影响,产生分子内敏化.若键入的生色基团与鎓盐硫原子相隔三到四个饱和碳原子,如图7 (a)所示,键入的生色基团与硫原子轨道空间交叠,更有利分子内电荷转移,提高敏化效率[35].常用的生色基团有蒽、吩噻嗪等稠环化合物,如图7(b).它们的吸收光谱类似于蒽,但比蒽红移约10 nm,在350—410 nm处有强吸收.
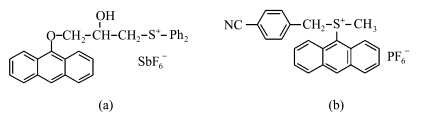 | 图7 蒽生色团键合鎓盐光引发剂分子结构式[34] Structural formula of onium salt molecules bonding anthracene chromophore[34] |
Yagci等[36, 37] 把二苯甲酮生色团键合到具有光引发活性的烯丙基铵盐分子上,合成了一种新型的光引发剂BPEA,分子结构如图8(a),并研究了它引发环氧化合物和乙烯基醚化合物聚合的反应.他们认为二苯甲酮片段先受到紫外辐射达到激发态, 然后处于激发态的二苯甲酮片段提取基态BPEA分子上的氢,从而产生活性自由基,该自由基加成到烯丙基双键上生成不稳定的中间体,该中间体很快分解形成新的阳离子活性中心,引发阳离子聚合.阳年发等对普通碘鎓盐结构进行改造,把二苯甲酮生色团键合到碘鎓盐分子中,设计出了一种新型的碘鎓盐,其结构式如图8(b).其最大吸收波长在260—320 nm,比原碘鎓盐红移10—70 nm.键入二苯甲酮的碘鎓盐无需另外添加光敏剂,可在普通高压汞灯照射下引发阳离子光聚合,提高引发效率.
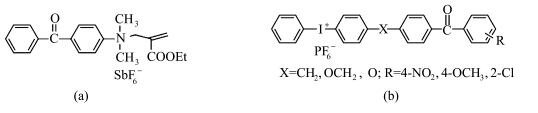 | 图8 二苯甲酮生色团键合鎓盐光引发剂分子结构式[38] Structural formula of onium salt molecules bonding benzophenone chromophore[38] |
Kreutzer等[39]制备了一种键合双生色基团的阳离子光引发剂BDMPP+SbF6-(见图9),其最大吸收峰位于350 nm.该引发剂分子结构中既含有苯甲酰基又含有鎓盐结构,可作自由基和阳离子光引发剂,引发丙烯酸酯单体自由基聚合,环氧化物的阳离子聚合以及丙烯酸酯/环氧化物的杂化聚合.
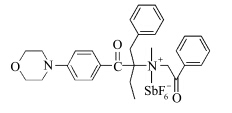 | 图9 BDMPP+SbF6-阳离子光引发剂分子结构式 Structural formula of cationic photoinitiator BDMPP+SbF6- |
阳离子光固化体系具有体积收缩小、不受氧阻聚、活性中心寿命长,以及能延时固化、对基材附着力强等优点.阳离子光引发剂作为阳离子光固化体系的重要组分,近年受到广泛的关注.针对多数阳离子光引发剂吸收光谱与紫外光源的发射光谱不匹配、引发 速率和引发效率低的问题,科学家们经过不懈努力提出了上述解决方案.此外,还通过改变中心原子来增强鎓盐的光引发特性,已知的中心原子除I、S外还有Se、P、As、Bi等.预计阳离子光引发体系发展趋势是开发低毒性、低迁移率、少污染、高引发效率和良好溶解性的新型光引发体系,如高分子化阳离子光引发剂和自由基-阳离子光引发剂的杂化.阳离子光固化材料已在多个领域得到工业应用,特别是快速生成具有高度交联的多功能高分子材料,在微电子领域的重要性和应用前景也日益显现.随着对阳离子光引发体系的深入研究,各种高性能光引发体系将会不断涌现,阳离子光固化的应用领域也将不断拓宽.
| [1] | 魏杰,金养智. 光固化涂料[M]. 北京: 化学工业出版社, 2005. 52-59. Wei J, Jin Y Z. Photocurable Coatings[M]. Beijing: Chemical Industry Press, 2005. 52-59. |
| [2] | 王涛,黄毓礼,师树简. 芳茂铁阳离子聚合光引发剂引发活性研究[J]. 高等学校化学学报,2003,(4): 735-738. Wang T, Huang Y L, Shi S J. Studies on the photosensitivity of cationic polymerization photoinitiator BF4-[J]. Chemical Journal of Chinese Universities, 2003,(4): 735-738. |
| [3] | 周健,张秋禹,张和鹏. 鎓盐类阳离子光引发剂的研究进展[J]. 材料导报,2011, 25(1): 16-21. Zhou J, Zhang Q Y, Zhang H P. The development of onium salt cationic photoinitiators[J]. Materials Review, 2011, 25(1): 16-21. |
| [4] | 张变香,魏保利. 紫外阳离子光引发剂及其发展动态[J]. 中国涂料,2011, 26(4): 31-54. Zhang B X, Wei B L. UV cationic photo-initiator and the development trend[J]. China Paint, 2011, 26(4): 31-54. |
| [5] | Crivello J V, Ahn J. Synthesis and characterization of second-generation S,S-dialkyl-S-(dimethylhydroxyphenyl)sulfonium salt photoinitiators[J]. Journal of Polymer Science Part A: Polymer Chemistry, 2003, 41(16): 2556-2569. |
| [6] | 凌华招,谢川. 改善鎓盐类阳离子光引发剂光敏性的研究概况[J]. 信息记录材料,2005,(3): 27-30. Ling H Z, Xie C. Development of enhancing photosensitivity of onium salts cationic photoinitiators[J]. Information Recording Materials, 2005,(3): 27-30. |
| [7] | Dektar J L, Hacker N P. Comparison of the photochemistry of diarylchloronium, diarylbromonium, and diaryliodonium salts[J]. The Journal of Organic Chemistry, 1991, 56(5): 1838-1844. |
| [8] | Dektar J L, Hacker N P. Photochemistry of diaryliodonium salts[J]. The Journal of Organic Chemistry, 1990, 55(2): 639-647. |
| [9] | Dektar J L, Hacker N P. Triphenylsulfonium salt photochemistry. new evidence for triplet excited state reactions[J]. The Journal of Organic Chemistry, 1988, 53(8): 1833-1835. |
| [10] | Crivello J V, Lam J H W. Diaryliodonium salts. a new class of photoinitiators for cationic polymerization[J]. Macromolecules, 1977, 10(6): 1307-1315. |
| [11] | Yaci Y, Reetz I. Externally stimulated initiator systems for cationic polymerization[J]. Progress in Polymer Science, 1998, 23(8): 1485-1538. |
| [12] | Akhtar S R, Crivello J V, Lee J L. Synthesis of aryl-substituted sulfonium salts by the phosphorus pentoxide-methanesulfonic acid promoted condensation of sulfoxides with aromatic compounds[J]. The Journal of Organic Chemistry, 1990, 55(13): 4222-4225. |
| [13] | Yagci Y, Schnabel W. New aspects on the photoinitiated free radical promoted cationic polymerization[J]. Makromolekulare Chemie. Macromolecular Symposia, 1992, 60(1): 133-143. |
| [14] | Timpe H J, Rajendran A G. Light-induced polymer and polymerization reactions-42. A kinetic study of cationic photopolymerization with (benzoin derivative)/(onium salt) systems[J]. European Polymer Journal, 1991, 27(1): 77-83. |
| [15] | Kahveci M U, Tasdelen M A, Yagci Y. Photochemically initiated free radical promoted living cationic polymerization of isobutyl vinyl ether[J]. Polymer, 2007, 48(8): 2199-2202. |
| [16] | Narewska J, Strzelczyk R, Podsiady R. Fluoflavin dyes as electron transfer photosensitizers for onium salt induced cationic photo polymerization[J]. J. Photochem. Photobiol. A, 2010, 212: 68-74. |
| [17] | Cook W D, Chen F. Enhanced photopolymerization of dimethacrylates with ketones, amines, and iodonium salts: the CQ system[J]. Journal of Polymer Science Part A: Polymer Chemistry, 2011, 49(23): 5030-5041. |
| [18] | Johnen N, Kobayashi S, Yagci Y, et al. Substituted vinyl bromides as photoinitiators for cationic polymerizations[J]. Polymer Bulletin, 1993, 30(3): 279-284. |
| [19] | Dossow D, Qin Q Z, Hizal G, et al. Photosensitized cationic polymerization of cyclohexene oxide: a mechanistic study concerning the use of pyridinium-type salts[J]. Polymer, 1996, 37(13): 2821-2826. |
| [20] | Cho J, Hong J. Photocuring kinetics for the UV-initiated cationic polymerization of a cycloaliphatic diepoxide system photosensitized by thioxanthone[J]. Eur. Polym. J., 2005, 42(1): 367-374. |
| [21] | Cho J, Kim E, Kim H, et al. An investigation of the surface properties and curing behavior of photocurable cationic ?lms photosensitized by anthracene[J]. Polymer Testing, 2002, 21: 781-791. |
| [22] | Crivello J V. Benzophenothiazine and benzophenoxazine photosensitizers for triarylsulfonium salt cationic photoinitiators[J]. Journal of Polymer Science Part A: Polymer Chemistry, 2008, 46(11): 3820-3829. |
| [23] | Crivello J V, Bulut U. Curcumin: a naturally occurring long-wavelength photosensitizer for diaryliodonium salts[J]. Journal of Polymer Science Part A: Polymer Chemistry, 2005, 43(21): 5217-5231. |
| [24] | Gomurashvili Z, Crivello J V. Phenothiazine photosensitizers for onium salt photoinitiated cationic polymerization[J]. Journal of Polymer Science Part A: Polymer Chemistry, 2001, 39(8): 1187-1197. |
| [25] | Crivello J V, Jang M. Anthracene electron-transfer photosensitizers for onium salt induced cationic photopolymerizations[J]. Journal of Photochemistry and Photobiology A: Chemistry, 2003, 159(2): 173-188. |
| [26] | Crivello J V, Lee J L. Photosensitized cationic polymerizations using dialkylphenacylsulfonium and dialkyl(4-hydroxyphenyl)sulfonium salt photoinitiators[J]. Macromolecules, 1981, 14(5): 1141-1147. |
| [27] | Bulut U, Balan A, Caliskan C. Benzotriazole derivatives as long wavelength photosensitizers for diaryliodonium salt initiators[J]. Journal of Polymer Science Part A: Polymer Chemistry, 2011, 49(3): 729-733. |
| [28] | Yaci Y, önen A. An allylic pyridinium salt: radical promoted latent thermal catalyst for cationic polymerization[J]. Journal of Polymer Science Part A: Polymer Chemistry, 1996, 34(17): 3621-3624. |
| [29] | Denizligil S, Yagci Y, Mcardle C. Photochemically and thermally induced radical promoted cationic polymerization using an allylic sulfonium salt[J]. Polymer, 1995, 36(16): 3093-3098. |
| [30] | Reetz I, Bacak V, Yagci Y. Addition fragmentation reactions for cationic polymerization using a novel allyloxy-picolinium salt[J]. Polymer International, 1997, 43(1): 27-32. |
| [31] | Crivello J V, Kong S. Long-wavelength-absorbing dialkylphenacylsulfonium salt photoinitiators: synthesis and photoinduced cationic polymerization[J]. Journal of Polymer Science Part A: Polymer Chemistry, 2000, 38(9): 1433-1442. |
| [32] | Crivello J V, Lam J H W. Photoinitiated cationic polymerization by dialkylphenacylsulfonium salts[J]. Journal of Polymer Science: Polymer Chemistry Edition, 1979, 17(9): 2877-2892. |
| [33] | Crivello J V, Lam J H W. Photoinitiated cationic polymerization with triarylsulfonium salts[J]. Journal of Polymer Science: Polymer Chemistry Edition, 1979, 17(4): 977-999. |
| [34] | Peter Pappas S, Tilley M G, Pappas B C. Anthracene-bound sulfonium salts: highly efficient photoinitiators for cationic polymerization: a new synthesis of sulfonium salts which avoids the use of silver salts[J]. Journal of Photochemistry and Photobiology A: Chemistry, 2003, 159(2): 161-171. |
| [35] | 洪啸吟,Pappas S P. 分子内敏化鎓盐的合成及光敏性研究[J]. 感光科学与光化学,1993, 11(3): 256-263. Hong X Y, Pappas S P. Studies on synthesis and photoactivity of some onium salts with built-in photosensitizer[J]. Photographic Science and Photochemistry, 1993, 11(3): 256-263. |
| [36] | Yurteri S, Onen A, Yagci Y. Benzophenone based addition fragmentation agent for photoinitiated cationic polymerization[J]. European Polymer Journal, 2002, 38(9): 1845-1850. |
| [37] | Onen A, Yagci Y. Synthesis of a novel addition-fragmentation agent based on Michler's ketone and its use as photo-initiator for cationic polymerization[J]. Polymer, 2001, 42(16): 6681-6685. |
| [38] | 阳年发,曹靖,杨利文. 自由基和阳离子杂化光固化引发剂及其制备方法和用途. 中国专利,02114033.2. 2002-10-30. Yang N F, Cao J, Yang L W. Synthesis and application of free radical and cationic hybrid photoinitiator. China patent, 02114033.2. 2002-10-30. |
| [39] | Kreutzer J, Demir K D, Yagci Y. Synthesis and characterization of a double photochromic initiator for cationic polymerization[J]. European Polymer Journal, 2011, 47(4): 792-799. |