聚离子复合物(PIC)是近年来高分子自组装领域研究的一个热点. 它是由两种带相反电荷的全亲水性嵌段聚合物在水溶液中通过静电作用复合成的纳米材料,其性质受阴/阳聚离子比例、聚合物链的柔性、离子强度、温度等因素的影响[1,2,3],可以通过改变阴/阳离子的比例来调节它的聚集行为[4]。聚离子复合物是一种性能优良的医学材料,可作为生物活性分子,如药物、蛋白质和基因[5,6,7]等的纳米载体. 近年来,聚离子复合物聚集体包载光敏剂体系既具有聚离子复合物聚集体的肿瘤靶向作用,又提高了光敏剂在靶向细胞内的光毒性,进而提高了其光动力疗效,这一体系呈现出新颖的光、电性能,从而引起了人们广泛的关注[8, 9]. 光敏剂分子在聚离子复合物聚集体内核这一“空间受限”体系(10—100 nm)中具有邻近效应,有望获得高的能量传递或电子转移效率[10]. 通过设计聚离子复合物的组成,改变聚集体内核微环境的空间尺寸、极性和粘度等性质,可进一步拓展聚离子复合物聚集体/光敏剂体系在光生物、光功能材料领域的应用[11].
光动力疗法在肿瘤治疗方面的应用备受关注[12,13,14],它利用可见光敏化位于人体病变组织(如肿瘤组织)内部的光敏剂而杀死病变组织. 聚合物聚集体形成的载药体系对实体瘤具有高通透性和滞留效应(EPR),有望实现靶向给药[15,16]. 聚合物包载光敏剂体系制备简单、易于保存、光动力活性良好,所以近年来利用聚离子复合物聚集体作为载体来增强细胞内的光动力疗效成为研究的热点[12,17]. 许多证据表明,在大多数情况下光动力疗法是通过机制II(type II )起主导作用的,即光动力作用的效果取决于1O2的产率,因此提高光敏剂产生单重态氧的产率有助于增强其光敏剂的光敏活性[18,19]. 富勒烯和卟啉类化合物在光照条件下能够产生多种活性氧[20,21],但是其水溶性较差、可见光区吸收弱等特点限制了它们的进一步应用. 本文利用ATRP方法合成了聚苯乙烯-聚丙烯酸叔丁酯(PSt-PtBuA),在酸性条件下水解得到聚苯乙烯-聚丙烯酸(PSt-PAA). PSt-PAA在缓冲溶液中能自组装形成以聚苯乙烯为疏水内核、聚丙烯酸为亲水外壳的两亲性聚合物聚集体. 富勒烯或卟啉类化合物(图1)可包载于PSt-PAA两亲性聚合物聚集体的内核中. 加入阳离子聚合物(PMADQUAT)形成聚离子复合物后,聚集体内核微环境和空间尺寸发生变化,可大幅提高富勒烯或卟啉类化合物的单重态氧产率.
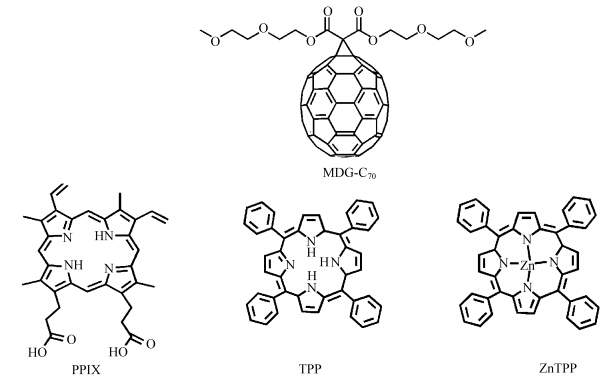 | 图1 C70衍生物和卟啉类化合物结构式 The chemical structures of C70 and porphyrin derivatives |
二乙二醇单甲醚、丙二酸均购自国药集团; 苯乙烯、丙烯酸叔丁酯、2-甲基丙烯酰氧基乙基三甲基氯化铵(MADQUAT)均购自Sigma公司; 原卟啉(PPIX)、四苯基卟啉(TPP)、四苯基锌卟啉(ZnTPP)、 N-N-N′N′-N″-五甲基二乙烯三胺(PMDETA)、2-溴正丁酸乙酯(EBnB)和CuCl均购自Acros公司; 9,10二甲氧基蒽-2-磺酸钠(MAS)购自Aldrich公司; PMADQUAT参照文献[22]合成. 所有有机溶剂均经过无水处理,使用前重蒸. 水溶液采用二次蒸馏水配制,所用缓冲溶液均为Tris-HCl缓冲溶液(10 mmol/L,pH = 7.0).
所用仪器:Bruker AVANCE 500超导核磁共振仪,25 ℃下用Φ5 mm管在多核宽带BBO探头中测定,以CDCl3为溶剂,TMS为内标; Hitachi U-3010紫外-可见吸收光谱仪,日本,采用1 cm石英比色皿; Hitachi F-4600荧光分光光度计,日本,采用1 cm石英比色皿,发射波长为371 nm,狭缝宽度为2.5 nm; Philips CM 120透射电子显微镜(TEM),将聚合物溶液滴加到铜网上,常温晾干后观察聚集体的形貌; Dawn EOS型凝胶渗透色谱/多角度激光光散射(SEC/MALLS)联用仪,色谱柱型号为:MZ 103 (300 × 8.0 mm),美国Wyatt公司,测定分子量及分子量分布,操作条件为温度40 ℃,流速0.5 mL/min,进样量150 μL,流动相为四氢呋喃(THF). 1.2 化合物合成
化合物MDG-C70: 参照文献合成[23,24]. 将50 mg (0.069 mmol) C70、45 mg (135.5 mmol) CBr4溶于50 mL重蒸甲苯中,在N2保护下加入32.7 mg (0.106 mmol)二乙二醇单甲醚丙二酸酯和1,8-二氮杂环[5, 4, 0]+-烯-7(DBU)(24.3 mg,0.16 mmol),室温下避光反应6 h. 减压除去溶剂,用柱层析法纯化得到棕色固体化合物24 mg MDG-C70,产率35.5%. 1HNMR (CDCl3): 4.60—4.62 (m,4H),3.86—3.88 (m,4H),3.68—3.70 (m,4H),3.55—3.57 (m,4H),3.38 (s,6H).
聚合物PSt-PAA的合成(图2): 将8 mL (0.070 mol)苯乙烯,142 μL (0.0007 mol) N-N-N′-N′-N″-五甲基二乙烯三胺,100 μL (0.0007 mol)2-溴正丁酸乙酯溶于8 mL苯甲醚中,冷冻条件下通N2抽真空,反复3次,除去体系中的氧气,加入0.068 g (0.0007 mol) CuCl,在N2保护下110℃反应45 h. 反应结束后静置在冰水浴中使反应终止,采用中性氧化铝柱层析,用THF作洗脱剂除去催化剂及配体,所得洗脱液减压浓缩,用甲醇洗涤、透析、干燥得5.789 g聚合物PSt-Br,产率81.58%. GPC: Mn=18310,Mw=16290,PDI=1.124.
 | 图2 聚合物PSt-PAA的合成路线 Synthesis of polymer PSt-PAA |
将6 mL (0.042 mol)丙烯酸叔丁酯,1 g聚合物PSt-Br,88.6 μL (0.00042 mol) N-N-N′-N′-N″-五甲基二乙烯三胺溶于6 mL苯甲醚中,冷冻条件下通N2抽真空,反复3次,除去体系中的氧气,加入0.042 g (0.0007 mol) CuCl,在氮气保护下110 ℃反应8 h. 反应结束后静置在冰水浴中使反应终止. 采用中性氧化铝柱层析,用THF作洗脱剂除去催化剂及配体,所得洗脱液减压浓缩,用甲醇洗涤、透析、干燥得到3.9 g聚合物PSt-PtBuA,产率74%. GPC: Mn=57490,Mw=43110,PDI=1.334. 1HNMR (CDCl3): 7.09—6.40 (m,Ar—H),2.30 (m,—CH2CH—),1.85 (m,—CH2CH—),1.89 (m,—CH2CH—),0.91 (s,—C(CH3)3).
将3.9 g PSt-PtBuA溶于30 mL 1,4-二氧六环中,滴加入6 mL浓盐酸,90 ℃下反应48 h,减压除去溶剂,透析,干燥得3.0 g聚合物PSt-PAA,产率77%. GPC: Mn=36670,Mw=38920,PDI=1.061. 1HNMR (CDCl3): 7.05—6.55 (m,Ar—H),2.34 (m,—CH2CH—),1.84 (m,—CH2CH—),1.89 (m,—CH2CH—). 1.3 PSt-PAA聚合物及聚离子复合物溶液的制备
PSt-PAA溶液通过透析方法制备[25,26]. 将10 mg的PSt-PAA溶于1 mL N,N-二甲基甲酰胺(DMF)中,将其转移至透析袋中,置于pH=7.0、浓度为10 mmol/L的Tris-HCl缓冲溶液中透析,透析过程中多次更换缓冲溶液,48 h后用缓冲溶液配成一定浓度的PSt-PAA溶液.
同样的方法将透析后得到的0.05 g/L的PMADQUAT溶液与0.05 g/L的PSt-PAA溶液在超声条件下以不同比例混合得到阳/阴聚离子质量比为0—6的聚离子复合物溶液. 1.4 PSt-PAA及聚离子复合物临界聚集浓度(CAC)测定
将1×10-3 mol/L芘的乙醇溶液注入样品瓶中,自然挥发掉乙醇溶剂. 将指定浓度的聚合物溶液注入样品瓶,荧光测试溶液芘的浓度保持在2×10-6 mol/L[27]. 测试前溶液搅拌过夜,使溶液达到平衡. 发射波长设定为371 nm,狭缝宽度为2.5 nm,测定芘的激发光谱随聚合物浓度的变化. 1.5 单重态氧(1O2)的测定
MDG-C70及卟啉类化合物的1O2产率采用9,10二甲氧基蒽-2-磺酸钠(MAS)光氧化法测定(图3)[28,29]. 固定MAS的浓度为8×10-5 mol/L,采用400 W高压钠灯照射(λ> 400 nm)样品,每隔3 min取样检测紫外-可见吸收光谱. 利用MAS在382 nm处吸收值降低程度与光照时间的关系可比较不同光敏剂产生单重态氧的相对产率.
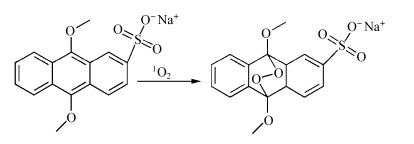 | 图3 MAS光氧化反应方程式 The photo-oxidation reaction of MAS |
ATRP方法合成的高分子具有分子量分布窄、分子量可控的特点,本实验先合成苯乙烯-丙烯酸叔丁酯嵌段聚合物PSt-PtBuA,经酸性水解而转变为苯乙烯-丙烯酸嵌段聚合物PSt-PAA,1HNMR结果显示PSt-PtBuA中的叔丁酯几乎为定量水解,具体合成步骤见图2.
图4是三种聚合物的GPC图,由图可以看出分子量越大,出峰时间越短,且都呈现正态分布而且分布都比较窄. 详细的分子量及分布见表1.
 | 图4 PSt-Br大分子引发剂、PSt-PtBuA和PSt-PAA嵌段共聚物的GPC图 GPC traces of PSt-Br macroinitiators,PSt-PtBuA andPSt-PAA block copolymer |
| 表1 PSt-Br大分子引发剂,PSt-PtBuA和PSt-PAA嵌段共聚物的分子量和分子量分布 Characteristics of the molecular weights and molecular weight distributions of PSt-Br macroinitiators,PSt-PtBuA and PSt-PAA block copolymers |
TEM实验结果表明PSt-PAA形成的聚集体为明显的球形(图5a),平均粒径约为47 nm,加入阳离子聚合物PMADQUAT后,聚集体粒径变小,当m(PMADQUAT)/m(PSt-PAA)=3时,聚集体的平均粒径约为36 nm (图5 b). 形成聚离子复合物后聚集体粒径变小可能是两者的静电相互作用引起的[30].
 | 图5 (a)聚合物PSt-PAA和(b)聚离子复合物(m(PMADQUAT)/m(PSt-PAA)=3)水溶液中聚集体的TEM图 TEM images of aggregates prepared from polymer (a)PSt-PAA and (b) PIC(m(PMADQUAT)/m(PSt-PAA)=3) aqueous solutions |
以芘为荧光探针可以测定聚合物在水中形成聚集体的CAC[31,32,33,34]. 芘在水溶液中的溶解度极低,而当被增溶到疏水区域后,周围环境极性发生改变,因此芘的激发谱的强度会发生变化并伴随谱带的红移. 以芘的激发光谱在339 nm与336 nm处的强度的比值(I339/I336)随聚合物浓度的变化作图,得到图6. 在聚合物浓度较低时,芘的I339/I336基本保持不变,表明聚合物以分散状态存在于水中. 逐渐增大聚合物浓度时,芘的I339/I336突然增大,表明体系中形成了核壳结构的聚集体,芘被增溶到了聚集体的疏水内核. 测定结果表明,PSt-PAA的CAC为0.015 g/L,而m(PMADQUAT)/m(PSt-PAA)=3时,聚离子复合物的CAC为0.005 g/L. 两种聚集体都有较低的CAC,意味着在稀释环境下两种聚集体都有很好的耐稀释稳定性,加入阳离子聚合物后,使得疏水核内静电排斥力减小,降低了屏蔽效应而更容易形成聚集体
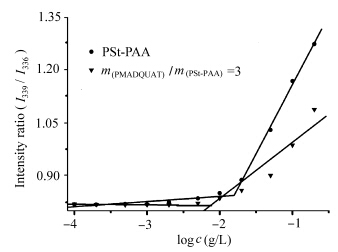 | 图6 芘的激发谱中339与336 nm处强度比 (I339/I336) 值随logc(PSt-PAA) 和logc(mPMADQUAT/mPSt-PAA=3)变化的曲线 Plot of intensity ratio I339/I336 of pyrene excitation spectra versus logc for PSt-PAA and m(PMADQUAT)/m(PSt-PAA)=3 [pyrene]=2×10-6 mol/L |
光敏剂吸收光以后,由基态跃迁到寿命较短的激发单重态,激发单重态经过系间窜越生成寿命较长的激发三重态. 光敏剂的激发三重态直接与氧发生能量转移反应,生成单重态氧[35]. 而单重态氧是一种具有高反应活性、高氧化性的活性氧,它具有亲电性,能高效氧化生物分子,如不饱和脂肪酸、蛋白质、核酸等,是在光动力疗法中损伤靶目标的最重要的活性反应物种之一. 因此,提高光敏剂产生单重态氧的量子效率有助于增强其光敏活性. 水溶性蒽类化合物MAS与1O2反应后,将引起MAS在382 nm处的吸收下降. 利用MAS在382 nm处吸收值降低程度与光照时间的关系可比较相同浓度条件下光敏剂在不同聚集体中光敏化产生1O2的产率. 图7a中插图为光照后MAS 在m(PMADQUAT)/m(PSt-PAA)=3的聚离子复合物聚集体包载MDG-C70体系中340—430 nm范围内的吸收光谱变化. 具有醚链结构的MDG-C70在缓冲溶液中有一定的溶解度,可产生单重态氧. 利用PSt-PAA聚集体或聚离子聚集体(m(PMADQUAT)/m(PSt-PAA)=3)包裹后,其单重态氧产率得到大幅提高(图7a). 富勒烯本身具有很强的疏水性,在极性溶剂中易于簇集,从而猝灭了富勒烯的激发态,不利于富勒烯产生单重态氧. 经过聚合物聚集体包裹后,富勒烯主要位于聚合物聚集体的疏水部分,可以较好地分散,有利于富勒烯单重态氧的产生[36]. MDG-C70在聚离子复合物聚集体中的单重态氧产率要高于PSt-PAA中的产率(图7b和表2),当PMADQUAT与PSt-PAA的质量比为3时,单重态氧的产率达到最大值. 这可能是过量的阳离子聚合物使得PSt-PAA聚集体的壳核结构微环境发生变化,反而不利于单重态氧的产生,具体机理有待于进一步研究.
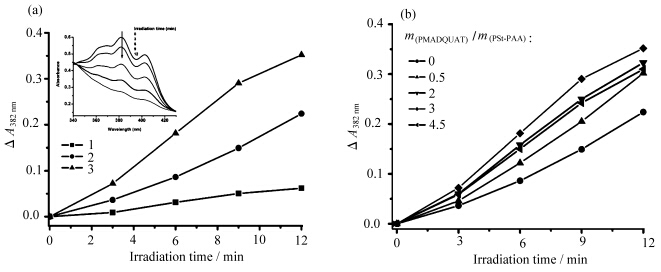 | 图7 (a)MDG-C70在不同溶液中的单重态氧产率 1.Tris-HCl(pH=7.0)缓冲溶液;2.PSt-PAA溶液;3.聚离子复合物溶液(m(PMADQUAT)/m(PSt-PAA)=3) (b) MDG-C70在具有不同PMADQUAT和PSt-PAA质量比聚合物溶液中的单重态氧量子产率 插图为MAS在m(PMADQUAT)/m(PSt-PAA)=3溶液包载MDG-C70体系中的吸收光谱随光照时间的变化 (a) The yields of 1O2 of MDG-C70 in different solutions 1.Tris-HCl; 2. PSt-PAA and 3. polyion complex solutions (m(PMADQUAT)/m(PSt-PAA)=3) (b) The yields of 1O2 of MDG-C70 in polyion complex solutions with different mass tratio of PMADQUAT and PSt-PAA [MDG-C70]=10-6 mol/L,[PSt-PAA] =0.05 g/L Inset: absorption spectra of MAS bleaching system of MDG-C70 illuminated at 0,3,6,9,12 min in m(PMADQUAT)/m(PSt-PAA)=3 solution |
卟啉类化合物作为第一代光动力光疗药物在临床上被用于恶性肿瘤的治疗已有多年,但其作为光疗药物存在许多缺陷,如水溶性差、在水溶液中易聚集等. 采用聚合物聚集体包裹的ZnTPP、PPIX和TPP卟啉类化合物在PSt-PAA聚集体和聚离子复合物聚集体溶液中表现出了良好的单重态氧产率(表2). 与MDG-C70相似,卟啉类化合物在聚离子复合物聚集体中的单重态氧量子产率要高于单纯的PSt-PAA聚集体. MDG-C70、ZnTPP、PPIX和TPP在m(PMADQUAT)/m(PSt-PAA)=3的聚离子复合物聚集体溶液中的单重态产率最高,分别是相关光敏剂在PSt-PAA聚集体中的1.64、2.60、2.63和2.20倍. 进一步说明聚离子复合物聚集体更有利于光敏剂产生单重态氧.
| 表2 ZnTPP、PPIX和TPP在不同质量比例聚离子复合物溶液(m(PMADQUAT)/m(PSt-PAA))中的 单重态氧量子产率a The yields of 1O2 of ZnTPP,PPIX and TPP in polyion complex solutions with different mass ratio of PMADQUAT and PSt-PAA ([MDG-C70] =[ZnTPP]=[PPIX]=[TPP]=10-6 mol/L) |
采用ATRP方法合成了PSt-PtBuA,通过酸性条件下水解得到PSt-PAA,在pH=7.0的Tris-HCl缓冲溶液中形成两亲性聚合物聚集体,加入阳离子聚合物PMADQUT后,可通过静电相互作用组装形成聚离子复合物,改变了聚集体的尺寸及内微环境. 光敏剂富勒烯和卟啉类化合物在水中溶解度较小,且限制了其光动力疗效,本实验制备的聚离子复合物聚集体增强了其溶解能力,并研究了不同比例的聚离子复合物聚集体溶液中富勒烯和卟啉类化合物产生单重态氧产率的能力. 结果表明,聚离子复合物聚集体既增加了富勒烯和卟啉类化合物的溶解能力,又保持了其光化学特征,且MDG-C70、ZnTPP、PPIX和TPP在m(PMADQUAT)/m(PSt-PAA)=3的聚离子复合物聚集体溶液中的单重态氧产率分别是相关光敏剂在PSt-PAA聚集体溶液中的1.64、2.60、2.63和2.20倍.
| [1] | Matsumoto S, Christie R J, Nishiyama N, et al. Enviroment-responsive block copolymer micelles with a disulfide cross-linked core for enhanced siRNA delivery[J]. Biomacromolecules, 2009, 10(1): 119-127. |
| [2] | Chelushkin P S, Lysenko E A, Bronich Y K, et al. Polyion complex nanomaterials from block polyelectrolyte micelles and linear polyelectrolytes of opposite charge. 2. dynamic properties[J]. J. Phys. Chem. B, 2008, 112(26): 7732-7738. |
| [3] | Park J S, Akiyama Y, Yamasaki Y, et al. Preparation and characterization of polyion complex micelles with a novel thermosensitive poly(2-isopropyl-2-oxazoline) shell via the complexation of oppositely charged block lonomers[J]. Langmuir, 2007, 23(1): 138-146. |
| [4] | Anraku Y, Kishimura A, Oba M, et al. Spontaneous formation of nanosized unilamellar polyion complex vesicles with tunable size and properties[J]. J. Am. Chem. Soc., 2010, 132(5): 1631-1636. |
| [5] | Ohya Y, Takeda S, Shibata Y, et al. Evaluation of polyanion-coated biodegradable polymeric micelles as drug delivery vehicles[J]. J. Contr. Release, 2011, 155(1): 104-110. |
| [6] | Ji W H, Panus D, Palumbo R N, et al. Poly(2-aminoethyl methacrylate) with well-defined chain length for DNA vaccine delivery to dendritic cells[J]. Biomacromolecules, 2011, 12(12): 4373-4385. |
| [7] | Tamura A, Oishi M, Nagasaki Y. Enhanced cytoplasmic delivery of siRNA using a stabilized polyion complex based on PEGylated nanogels with a cross-linked polyamine structure[J]. Biomacromolecules, 2009, 10(7): 1818-1827. |
| [8] | Zhang G D, Harada A, Nishiyama N, et al. Polyion complex micelles entrapping cationic dendrimer porphyrin: effective photosensitizer for photodynamic therapy of cancer[J]. J. Contr. Release, 2003, 93(2): 141-150. |
| [9] | Ideta R, Tasaka F, Jang W D, et al. Nanotechnology-based photodynamic therapy for neovascular disease using a supramolecular nanocarrier loaded with a dendritic photosensitizer[J]. Nano Lett., 2005, 5(12): 2426-2431. |
| [10] | Niedermair F, Sandholzer M, Kremser G, et al. Solution self-assembly and photophysics of platinum complexes containing amphiphilic triblock random copolymers prepared by ROMP[J]. Organometallics, 2009,28(9): 2888-2896. |
| [11] | Wu W C, Chen C Y, Tian Y Q, et al. Enhancement of aggregation-induced emission in dye-encapsulating polymeric micelles for bioimaging[J]. Adv. Funct. Mater., 2010, 20(9): 1413-1423. |
| [12] | Herlambang S, Kumagai M, Nomoto Y, et al. Disulfide crosslinked polyion complex micelles encapsulating dendrimer phthalocyanine directed to improved efficiency of photodynamic therapy. J. Contr. Release, 2011, 155(3): 449-457. |
| [13] | Tsai H C, Tsai C H, Lin S Y, et al. Stimulated release of photosensitizers from graft and diblock micelles for photodynamic therapy[J]. Biomaterials, 2012, 33(6): 1827-1837. |
| [14] | Nishiyama N, Morimoto Y, Jang W D, et al. Design and development of dendrimer photosensitizer-incorpora-ted polymeric micelles for enhanced photodynamictherapy[J]. Adv. Drug Del. Rev., 2009, 61(4): 327-338. |
| [15] | Duncan R. Polymer conjugates for tumour targeting and intracytoplasmic delivery. The EPR effect as a common gateway[J]. Pharm. Sci. Technol. Today, 1999, 2(11): 441-449. |
| [16] | Maeda H, Bharate G Y, Daruwalla J. Polymeric drugs for efficient tumor-targeted drug delivery based on EPR-effect[J].Eur. J. Pharm. Biopharm., 2009, 71(3): 409-419. |
| [17] | Jang W D, Nakagishi Y, Nishiyama N, et al. Polyioncomplexmicelles for photodynamictherapy: incorporation of dendritic photosensitizer excitable at long wavelength relevant to improved tissue-penetrating property[J]. J. Contr. Release, 2006, 113(1): 73-79. |
| [18] | Bonnett R. Photosensitizers of the porphyrin and phthalocyanine series for photodynamic therapy[J]. Chem. Soc. Rev., 1995, 24(1): 19-33. |
| [19] | Henderson B W, Dougherty T J. How does photodynamic therapy work[J]. Photochem. Photobiol., 1992, 55(1): 145-157. |
| [20] | Nakamura E, Isobe H. Functionalized fullerenes in water. The first 10 years of their chemistry, biology, and nanoscience[J].Acc. Chem. Res., 2003, 36(11): 807-815. |
| [21] | Arbogast J W, Foote C S. Chemistry of singlet oxygen. 36. Singlet molecular oxygen (1Δg) luminescence in solution following pulsed laser excitation. Solvent deuterium isotope effects on the lifetime of singlet oxygen[J]. J. Am. Chem. Soc., 1982, 104(7): 2069-2070. |
| [22] | Khutoryanskiy V V, Kujawa P, Nurkeeva Z S, et al. Radiation synthesis of linear and crosslinked polytrimethylammonium chloride and complex formation with potassium hexacyanoferrates (II, III) in aqueous solutions[J]. Macromol. Chem. Phys., 2001, 202(7): 1089-1093. |
| [23] | 高云燕, 刘丽华, 欧植泽, 等. 胆固醇修饰富勒烯/γ-环糊精包结复合物的生物活性[J]. 物理化学学报, 2010, 26(2): 495-501. Gao Y Y, Liu L H, Ou Z Z, et al. Biological activity of a cholesterol modified fullerene γ-cyclodextrin inclusion complex[J]. Acta Phys. Chim. Sin., 2010, 26(2): 495-501. |
| [24] | Gao Y Y, Wang Z L, Ou Z Z, et al. Regulation of glucose oxidase activity through interaction with fullerene derivatives[J]. Chin. J. Chem., 2012, 30(2): 418-426. |
| [25] | Zhang L F, Eisenberg A. Multiple morphologies and characteristics of "Crew-Cut" micelle-like aggregates of polystyrene-b-poly(acrylic acid) diblock copolymers in aqueous solutions[J]. J. Am. Chem. Soc., 1996, 118(13): 3168-3181. |
| [26] | Arimura H, Ohya Y, Ouchi T, et al. Formation of core-shell type biodegradable polymeric micelles from amphiphilic poly(aspartic acid)-block-polylactide diblock copolymer[J].Biomacromolecules, 2005, 6(2): 720-725. |
| [27] | Zhang D W, Zhang H, Nie J, et al. Synthesis and self-assembly behavior of pH-responsive amphiphilic copolymers containing ketal functional groups[J]. Polym. Int., 2010, 59(7): 967-974. |
| [28] | Miyamoto S, Martinez G R, Medeiros M G, et al. Singlet molecular oxygen generated from lipid hydroperoxides by the russell mechanism: studies using 18O-labeled linoleic acid hydroperoxide and monomol light emission measurements[J]. J. Am. Chem. Soc., 2003, 125(20): 6172-6179. |
| [29] | Miyamoto S, Martinez G R, Rettori D, et al. Linoleic acid hydroperoxide reacts with hypochlorous acid, generating peroxyl radical intermediates and singlet molecular oxygen[J]. Proc. Nat. Acad. Sci. USA, 2006, 103(2): 293-298. |
| [30] | Yan Y, Keizer A, Stuart M C, et al. Stability of complex coacervate core micelles containing metal coordination polymer[J]. J. Phys. Chem. B, 2008, 112(35): 10908-10914. |
| [31] | Ohya Y, Takeda S, Shibata Y, et al. Preparation of highly stable biodegradable polymer micelles by coating with polyion complex[J]. Macromol. Chem. Phys., 2010, 211(16): 1750-1756. |
| [32] | Astafieva I, Zhong X F, Eisenberg A. Critical micellization phenomena in block polyelectrolyte solutions[J]. Macromolecule, 1993, 26(26): 7339-7352. |
| [33] | Wilhelm M, Zhao C L, Wang Y C, et al. Poly(styrene-ethylene oxide) block copolymer micelle formation in water: a fluorescence probe study[J]. Macromolecules, 1991, 24(5): 1033-1040. |
| [34] | Yang H, Hu C C, Wu X, Chen H B, et al. pH and salt effects on the aggregation behavior of star polymer with G1 polyamidoamine core and terminal amphiphilic blocks[J]. Supramol. Chem., 2010, 22(9): 477-482. |
| [35] | 谢 洁, 何慧珠. 一种可生产单重态氧的新型光敏剂-类卟啉大环金属配合物[J]. 感光科学与光化学, 1996, 14(3): 212-217. Xie J, He H Z. New photosensitizers for efficient production of singlet oxygen-porphyrin-like macrocycle metal complexes[J]. Photographic Science and Photochemistry, 1996, 14(3): 212-217. |
| [36] | Wang X S, Metanawin T, Zheng X Y, et al.Structure-defined C60/polymer colloids supramolecular nanocomposites in water [J]. Langmuir, 2008, 24(17): 9230-9232. |




