2. 中国科学院大学, 北京 100049
2. University of Chinese Academy of Sciences, Beijing 100049, P. R. China
Hydrotrope是一类具有特殊性能的两亲化合物(Amphiphile),因其具有突出的助水溶性能,中文称为助水溶剂[1,2]. 助水溶剂使用时只需要将难溶的溶质与助水溶剂在水中以合适的比例混合即可,操作简单;使用后将助溶体系适当稀释,即可释放出被溶物[3],易于回收. 此外,助水溶剂还具有选择性高、助溶量大的特点[3,4,5].Shukla M[6]等对比不同助溶技术对药物Glipizide助溶性能时发现各种方法的增溶量次序:助水溶剂助溶>固体分散>胶束增溶.特别是对一些难水溶的芳香族化合物,助水溶剂表现出很好的助溶效果.因此,助水溶剂在生物、医药及日化等领域有着极大的应用前景[7].
相对其广泛开展的应用方面研究,关于助水溶剂的理论研究较为薄弱,特别是其在水溶液中自缔合行为方面的研究.这是因为助水溶剂虽具有类似于表面活性剂的分子结构,在水溶液中会发生自缔合现象.但助水溶剂的疏水基部分比较小,不能形成像表面活性剂胶束那样结构明确的聚集体[8, 9],这给其水溶液中聚集体的检测带来了困难.目前,灵敏的荧光探针技术已被广泛用于微环境的表征和两亲化合物聚集行为的研究[10,11],选取合适的荧光探针,将有助于进一步认识助水溶剂分子的助溶性能和自缔合行为,为其实际应用提供理论指导.
近年来,出现了新型的可聚合助水溶剂,其通过聚合制备得到具有同样助溶能力的两亲聚合物[7,12].从而克服小分子助水溶剂在医药应用中出现的一些副作用,如致毒反应和细胞损伤[13].除助溶作用外,这类可聚合助水溶剂也是一类功能性的添加剂,可以和表面活性剂或两亲聚合物复合,协同产生不同的聚集体,例如worm-like胶束或囊泡,并通过聚合锁定相应的超分子聚集体.因此,可聚合型助水溶剂引起了广泛的研究兴趣.
本文制备了一系列具有不同烷芳基基团的可聚合阳离子型助水溶剂(PCHs),其化学结构式见图1(左).选取染料尼罗红为探针(结构见图 1(右)),采用吸收和发射光谱测定方法,研究了PCHs的助溶作用、自缔合行为和相应的聚集体的结构变化,并讨论了分子缔合的作用机制.此外,通过自由基聚合得到相应的两亲聚合物,并初步评价了其对尼罗红的助溶作用.
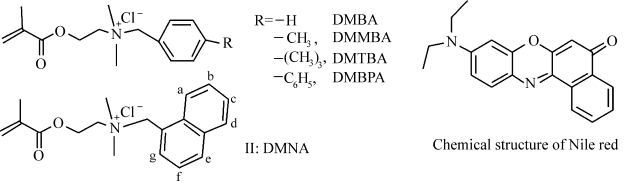 | 图1 PCHs结构(左)和染料尼罗红的结构(右) Structures of PCHs (left) and Nile red (right) |
甲基丙烯酸-N,N-二甲基氨乙酯(DMAEMA,分析纯,北京化学试剂厂);氯化苄(BC),对甲基苄氯(MBC),对叔丁基苄氯(TBC)和4-氯甲基联苯(PBC)均为分析纯试剂,购于Sigma-Aldrich 公司;1-氯甲基萘,尼罗红(分析纯,百灵威科技有限公司);偶氮二异丁脒盐酸盐(AIBA,分析纯,Aldrich公司产品),二氯甲烷和丙酮(分析纯,北京化学试剂厂);合成使用的溶剂均经过除水和蒸馏处理,所有光谱测试用水均使用超纯水(Millipore Milli-Q水净化器处理)制备,并在室温下测试. 1.2 合成方法与表征
各种可聚合阳离子型助水溶剂(PCHs),按文献[14, 15]方法合成.产物结构经1HNMR,13CNMR和IR鉴定.其中未见诸于报道的DMNA的结构表征如下:
DMNA:1HNMR(400 MHz,D2O):8.24(nap-Hg,d,1H),8.15(nap-Hd,d,1H),8.06(nap-Hc,d,1H),7.79(nap-Ha,d,1H),7.73(nap-Hf,m,1H),7.65(nap-He,Hb,t,2H),6.15(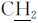 =C,s,1H),5.76(
=C,s,1H),5.76(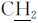 =C,s,1H),5.11(nap-
=C,s,1H),5.11(nap-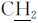 ,s,2H),3.14 (N(
,s,2H),3.14 (N(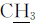 )2,s,6H),4.69(O—
)2,s,6H),4.69(O—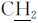 —CH2—N,t,2H),3.92(O—CH2—
—CH2—N,t,2H),3.92(O—CH2—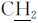 —N,t,2H),1.92(
—N,t,2H),1.92(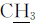 —C,s,3H);
—C,s,3H);
13CNMR(400 MHz,D2O,二氧六环为内标):168.91(O—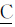 =O),135.82(CH2=
=O),135.82(CH2=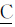 ),134.78,134.49,133.30,132.83,130.14,128.73(2C),127.41,126.129,123.86,123.43(
),134.78,134.49,133.30,132.83,130.14,128.73(2C),127.41,126.129,123.86,123.43(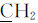 =C),66.18(nap-
=C),66.18(nap-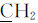 ),63.91(O—
),63.91(O—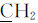 —CH2—N),59.18(
—CH2—N),59.18(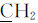 —CH2—N),51.26(N(
—CH2—N),51.26(N(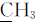 )2),18.19(
)2),18.19(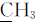 —C).
—C).
IR(KBr):1720.5,1635.6,1481,1296,1163,808,783 cm-1.
两亲聚合物的制备:40 mL浓度为0.5 mol/L的助水溶剂水溶液,置于50 mL试管中,向溶液中通入20 min的氮气去除反应体系中的氧气,加入引发剂AIBA(单体摩尔浓度的2%).密封试管,置于50 ℃的恒温水浴中聚合10 h.将产物用丙酮沉淀纯化,真空干燥至恒重.
1.3 仪器与测试助溶曲线的测定,步骤如下:精确移液0.2 mL尼罗红的二氯甲烷溶液(5×10-3 mol/L)至5 mL容量瓶中,减压除去溶剂,加入5 mL不同浓度的PCHs水溶液,将配制的溶液振荡24 h后,测试前用0.22 μm亲水滤膜过滤.利用Hitachi U-3900紫外-可见分光光度计和Hitachi F-4500荧光光谱仪测定尼罗红在PCHs溶液中的吸光度和荧光发射强度.
两亲聚合物的分子量通过激光光散射的方法测试得到.将聚合物样品溶解于0.1 mol/L的氯化钠(NaCl)水溶液中,以690 nm的激光作为光源,采用美国Wyatt公司的DAWN EOS型激光光散射仪测定,以测试得到的Zimm图为模型,计算得到聚合物的分子量.测试结果得到PDMBA、PDMMBA和PDMNA的重均分子量(Mw)分别为3.8×105 g/mol、2.6×105 g/mol、3.6×105 g/mol.两亲聚合物的助溶作用按上述程序测定. 2 结果与讨论 2.1 助溶作用
光谱测量法是确定溶质浓度的简单又精确的方法. 这里采用油溶性的尼罗红染料为探针(溶质),测定它在PCHs水溶液中的吸收光谱.以DMBA为例,如图2所示,当DMBA浓度较低时,尼罗红的吸光度很弱,随着DMBA浓度的增大,尼罗红的吸光度明显增大,表明溶液中溶解的染料分子增多,出现助溶作用.图3展示了尼罗红的光密度与PCHs浓度对数的关系.当PCHs的浓度达到某一浓度后,染料的光密度大幅度地升高,表现出显著的助溶作用.这个阈值浓度即助水溶剂的最小助溶浓度(MHC).
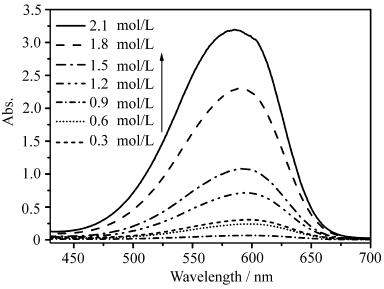 | 图2 在不同浓度DMBA水溶液中尼罗红的吸收光谱 Absorption spectra of Nile red in various concentrations of DMBA aqueous solutions |
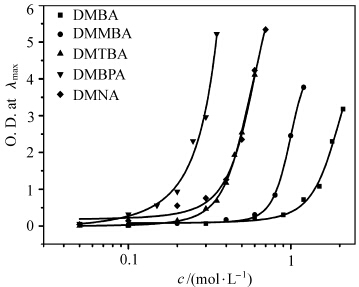 | 图3 尼罗红的光密度(O.D.)与PCHs浓度对数的关系 The relationship between optical density(O.D.) value of Nile red and the logarithm concentration of PCHs (c) |
由图3可计算PCHs的MHC值.另外,通过助溶曲线和MHC值还可求得PCHs的Setschenow常数.以上数据均列于表1.
| 表1 各种PCHs的助溶作用和缔合作用的参数 The solubilization parameters (MHC,CAC) for PCHs |
Setschenow常数(Ks),是反映助水溶剂助溶效率的重要参数[16,17],其表达式如下:
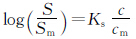
其中,S、c为染料的溶解度和助水溶剂的浓度;Sm、cm为MHC处染料的溶解度和助水溶剂的浓度. 由表1数据分析这类PCHs的助溶能力与其结构的关系,若按MHC值排列,DMBA>DMMBA>DMTBA>DMNA>DMBPA,即随着化合物上苯环取代基的尺寸增大而下降,这反映了随着助水溶剂分子的疏水性提高,其更容易发生分子缔合,从而更容易产生助溶作用.影响助溶作用的另外一个重要因素是助水溶剂本身的溶解度.按Ks常数比较,DMBPA和DMTBA大于DMNA,说明萘环和苯环对助溶作用的贡献存在差别:含有萘环的助水溶剂DMNA,具有较强的π-π相互作用,在较低浓度下,即能形成聚集体,但其形成的聚集体结构较疏松,因此增溶效率要低于DMBPA和DMTBA. 综合考虑疏水性和聚集体结构的影响,总体评价,DMBA助溶效果一般,DMTBA和DMNA较好,DMBPA最佳. 2.2 自缔合行为
PCHs分子结构中含亲水的季胺阳离子基团和疏水的烷芳基基团,在水溶液中易发生自缔合行为而引起其宏观性能的显著变化.为进一步了解PCHs的助溶作用机制,这里采用荧光探针法,从分子水平上研究它们在溶液中的自缔合行为与浓度之间的关系.
油溶性尼罗红染料是一种很灵敏的中性荧光探针,被广泛的用于各种聚集体内部极性的测定.它的荧光发射峰位于600 nm以上,能级较低,适用于本文这种含有芳环基团化合物的聚集体系.测定尼罗红在不同浓度PCHs中的荧光光谱,图4表示尼罗红的荧光发射峰强度与PCHs浓度的关系.值得注意的是,不同于助溶曲线上观察到的单一增长趋势,随浓度增大,荧光发射峰强度呈现出先增大后急剧减小的趋势,具有两个转折点阈值浓度.由前面对增溶曲线的分析可知,尼罗红在PCHs中的增溶浓度随着PCHs浓度的增大逐渐增大.由于荧光光谱的灵敏度高,能检测到更低浓度增溶在PCHs聚集体内的尼罗红染料分子,反映出PCHs开始缔合的阈值浓度,称之为临界缔合浓度(CAC)。随着增溶于聚集体中的尼罗红染料分子的增多,局部浓度过大,导致染料激发态分子的自猝灭现象,当尼罗红染料增溶浓度增大产生的自猝灭作用超过了其对发射光强的贡献时,荧光发射峰强度曲线就发生翻转,出现最大值.由图4得到的各助水溶剂的CAC值和cmax值列于表 1中,对比发现,cmax数值和染料助溶法求得的MHC数值基本一致.而CAC值则明显低于MHC值.由此说明助水溶剂分子类似表面活性剂分子,在比较低的浓度条件就开始分子自缔合(CAC).然而它们又不同于表面活性剂,只有当分子缔合达到一定程度(MHC)时,其宏观性质,包括助溶性、表面活性、电导率等才开始发生变化.本工作澄清了一些文献报导误将CAC和MHC混为一谈的观念[18].这二种阈值浓度的差异是因为助水溶剂分子结构中,疏水部分比较小,分子的亲水疏水平衡值(HLB)较大,疏水缔合作用比较弱,不可能形成表面活性剂胶束那样具有确定结构的分子聚集体,而是通过分子堆砌形成疏松结构的聚集体.同时,随着浓度增加,分子缔合程度不断提高,引起分子聚集体结构的变化,达到一定程度时,开始引起宏观性能的重要变化.这一现象类似于表面活性剂的“预胶束化”过程[19].
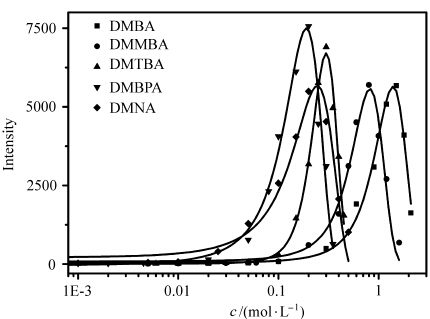 | 图4 尼罗红荧光强度随PCHs浓度的变化 Plots of fluorescent intensity of Nile red as a function of the concentration of PCHs |
分子聚集体的微环境极性是表征聚集体结构的重要参数,应用现代荧光探针技术可以简便又无损地测得分子聚集体的微环境的极性.尼罗红染料不仅是油溶性荧光染料,同时也是对极性十分敏感的显色染料[20].它的吸收或发射带波长随环境的极性减小而显著蓝移,因此尼罗红染料探针被广泛的应用于各种分子聚集体的内部微环境极性的测定[10, 11].表3列出各助水溶剂MHC值附近尼罗红的最大吸收波长和荧光发射光波长,由最大吸收波长和极性的相关曲线,可以得到相应分子聚集体微环境的极性[20].表2中的数据显示这类PCHs聚集体的极性都较高,说明形成的聚集体结构比较疏松,含有相当程度渗入内部的水分子,但这样极性变化程度已足以引起助溶性能的显著提高.
| 表2 PCHs 在MHC值处对应尼罗红的最大吸收波长、荧光发射波长和微环境极性 Absorption wavelength maximum (λamax),emission wavelength maximum (λfmax) and the polarity ER value of the probable solubilizaiton site of Nile red in PCHs (at MHC) obtained from λamax value |
PCHs缔合过程中形成的分子聚集体的微环境的极性随着浓度的增大发生变化.以DMTBA为例,它的发射波长变化的情况如图5所示:当浓度低于CAC值,染料的波长保持不变;当浓度超过CAC,随着浓度增加,缔合程度提高,染料的波长不断地下降,表明随着分子缔合过程,微环境极性不断下降.同时在MHC处也未观察到十分明显的转折,表明聚集体的生长是逐步缔合过程.在本组的另外一篇报道中,通过对相同类型的Hydrotrope两亲化合物(AEBA)聚集体的分子聚集数(Nagg)的测定,证明在CAC以后,分子聚集数随浓度而逐步增大[21].根据以上结果,证实这类PCHs在水溶液中缔合形成比较疏松的聚集体结构,随着浓度提高和缔合程度增加,聚集体分子结构的有序性和堆砌密度不断升高,当达到一定程度产生分子间的协同作用,宏观性质发生显著变化,这就是在MHC阈值浓度范围观察到的现象.
 | 图5 尼罗红的最大吸收波长,荧光发射波长随DMTBA浓度的变化 Variation in the absorption wavelength maximum (λamax) and emission wavelength maximum (λfmax) of the probe Nile red as a function of the concentration of DMTBA |
上述PCHs分子结构中含有可聚合基团甲基丙烯酰基,因此通过自由基聚合可得到相应的两亲聚合物.所得聚合物可视为PCHs的集合体,因此具有类似的助溶功能.如图6所示,在相同浓度(0.1 mol/L)下(聚合物以单体摩尔质量计算),聚合物对尼罗红的助溶量均高于单体,显示出具有更强的助溶作用.此外,尼罗红的最大吸收峰和荧光发射峰的位置在聚合物溶液中相对PCHs溶液发生蓝移(表3),说明在聚合物溶液体系中,染料分子所处的微环境极性更低.这是由于聚合物在水溶液中具有很高的局部浓度效应,促进了疏水基团间的相互缔合而形成比较密切的聚集体,因此疏水微区的极性较低[22].
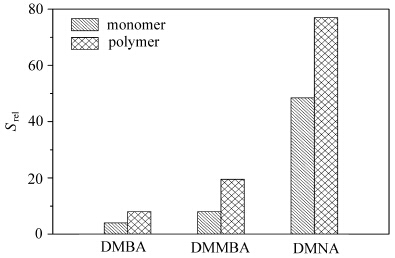 | 图6 尼罗红在不同PCHs和相应聚合物水溶液中的助溶倍数(0.1 mol/L) Solubility enhancement of Nile red at PCHs and their polymers aqueous solutions(0.1 mol/L) |
| 表3 尼罗红在不同PCHs及相应聚合物水溶液中的最大吸收波长和荧光发射波长(0.1 mol/L) Absorption wavelength maximum (λamax) and emission wavelength maximum (λfmax) of Nile red at PCHs and their polymers aqueous solutions (0.1 mol/L) |
应用多功能探针技术,研究了具有不同烷芳基疏水体结构的可聚合阳离子型Hydrotrope的自缔合行为、微环境极性和助溶作用.结果表明在这类功能化合物的分子缔合过程中存在二个转变点,位于低浓度(10-1—10-2mol/L)的CAC和位于较高浓度(>10-1 mol/L)的MHC.当助水溶剂浓度超过CAC后,分子间将发生缔合,随着浓度增加,分子缔合度升高,聚集体结构中芳环排列的有序性不断提高.助水溶剂浓度达到(MHC)时,产生分子间协同作用,引起助溶作用的发生.本文阐明了这类助水溶剂的自缔合作用的机制和CAC与MHC的物理意义.聚集体微环境极性的测定表明这类助水溶剂缔合形成比较疏松的结构,且其分子堆砌密度随聚集体的增大而逐步升高.为进一步发展高质量、多功能的Hydrotrope型两亲化合物材料提供了有价值的依据.
| [1] | Neuberg C.Hydrotropic phenomena[J]. Journal of Chemical Society, 1916, 110: 555-559. |
| [2] | Neuberg C. Hydrotropy[J]. Biochemische Zeitschrift, 1916, 76: 107-108. |
| [3] | Gaikar V, Sharma M. Separations with hydrotropes[J]. Separation and Technology, 1993, 3(1): 2-11. |
| [4] | Kabir-ud-Din, Parveen N, Naqvi A Z. Hydrotropic behavior of sodium salicylate in presence of additives[J]. Journal of Dispersion Science and Technology, 2009,30(10): 1500-1505. |
| [5] | Jain P, Goel A, Sharma S, et al. Solubility enhancement techniques with special emphasis on hydrotrophy[J]. International Journal of Pharma Professional's Research, 2010, 1(1): 34-45. |
| [6] | Shukla M, Rathore P, Jain A, et al. Enhanced solubility study of glipizide using different solubilization techniques[J]. International Journal of Pharmacy and Pharmaceutical Sciences, 2010, 2(2): 46-48. |
| [7] | Pinal R, Kim J Y, Kim S, et al. Hydrotropic solubilization of poorly water-soluble drugs[J]. Journal of Pharmaceutical Scienecs, 2010, 99(9): 3953-3965. |
| [8] | Kaler E W, Hodgdon T K. Hydrotropic solutions[J]. Current Opinion in Colloid and Interface Science, 2007, 12(3): 121-128. |
| [9] | Friberg S E, Lochhead R V, Blute I, et al. Hydrotropes-performance chemicals[J]. Journal of Dispersion Science and Technology, 2004, 25(3): 243-251. |
| [10] | 袁 钊,曾 毅,陈金平,等.以尼罗红为探针对新型两亲性树枝形聚合物微环境的研究[J].影像科学与光化学,2010, 28(5): 343-353. Yuan Z, Zeng Y, Chen J P, et al. Investigation of the microenvironment of novel amphiphilic dendrimers with nile red as a probe[J]. Imaging Science and Photochemistry, 2010, 28(5): 343-353. |
| [11] | 姜小明,宋 磊, 赵 濉.荧光探针法研究双子型阳离子表面活性剂与明胶的相互作用[J].影像科学与光化学,2012. 30(3): 175-181. Jiang X M, Song L, Zhao S.Interaction between gemini cationic surfactants and gelatin investigation by fluorescence[J]. Imaging Science and Photochemistry, 2012, 30(3): 175-181. |
| [12] | Park K, Lee S C, Huh K M, et al. Hydrotropic polymeric micelles for enhanced paclitaxel solubility: in vitro and in vivo characterization[J]. Biomacromolecules, 2007, 8(1): 202-208. |
| [13] | Lee S C, Acharya G, Lee J, et al. Hydrotropic polymers:synthesis and characterization of polymers containing picolylnicotinamide moieties[J]. Macromolecules, 2003, 36(7): 2248-2255. |
| [14] | Wang G X, Zhang Y X, Wu F P. Cationic surfmers with benzyl groups: Synthesis and copolymerization with acrylamide[J]. Chinese Journal of Polymer Science, 2011, 29(3): 352-359. |
| [15] | 王桂霞,李万刚,张玉玺,等.阳离子型共聚物AM/DMBAC疏水微嵌段结构的分析[J].高分子学报, 2010,(4): 435-441. Wang G X, Li W G, Zhang Y X, et al. Studies of microblock structure of AM/DMBAC cationic copolymers[J]. Acta Polymerical Sinica, 2010,(4): 435-441. |
| [16] | May W E, Wasik S P, Freeman D H. Determination of the solubility behavior of some polycyclic aromatic hydrocarbons in water[J]. Analytical Chemistry, 1978, 50(7): 997-1000. |
| [17] | Gandhi N N, Meyyappan N. Solubility and mass transfer coefficient enhancement of benzyl acetate in water through hydrotropy[J]. Journal of Chemical Engineering Data, 2004, 49(5): 1290-1294. |
| [18] | Neumann M G, Schmitt C C, Prieto K R, et al. The Photophysical determination of the minimum hydrotrope concentration of aromatic hydrotropes[J]. Journal of Colloid Interface Science, 2007, 315(2): 810-813. |
| [19] | 姜永才,吴世康.在胶束形成前染料分子的能量转移与预胶束基本性质的研究[J]. 化学学报, 1990, 48(5): 447-451. Jiang Y C, Wu S K. A study on the basic properties of premicelle and the energy transfer of dyes before micellar formation[J]. Acta Chimica Sinica, 1990, 48(5): 447-451. |
| [20] | Deye J F, Berger T A, Anderson A G. Nile red as a solvatochromic dye for measuring solvent strength in normal liquids and mixtures of normal liquids with supercritical and near critical fluids[J]. Analytical Chemistry, 1990, 62(6): 615-622. |
| [21] | 李 晶,吴飞鹏,王尔鉴. Hydrotrope型两亲化合物的合成和自缔合研究[J]. 影像科学与光化学,2009. 27(4): 287-295. Li J, Wu F P, Wang E J. Synthesis and self-association property of a novel hydrotrope amphiphilic compound[J]. Imaging Science and Photochemistry, 2009, 27(4): 287-295. |
| [22] | Li J, Wu F P,Wang E J.Studies on self-associative behavior of a novel cation amphiphilic polymer[J]. Chinese Journal of Polymer Science, 2009, 27(4): 593-596. |




