2. 南开大学泰达应用物理学院弱光非线性光子学教育部重点实验室, 天津 300457
2. The Key Laboratory of Weak-Light Nonlinear Photonics, Ministry of Education, Applied Physics School, Teda College, Nankai University, Tianjin 300457, P. R. China
TiO2光催化剂具有光催化效率高、化学稳定性强等特点,多年来在光催化研究领域倍受重视[1,2,3].然而,纯TiO2的禁带宽度为3.2 eV,只能够吸收波长小于387.5 nm的紫外光(太阳光谱中紫外光部分仅占8%,而可见光占45%以上),因此,以TiO2为基础的可见光催化剂的研制已成为该领域的研究热点.
近年来,利用金属或非金属离子掺杂技术,制备高活性的TiO2基可见光催化剂已取得了良好的效果,如掺杂Sn[4]、Fe[5]、Zr[6]、W[7]和Cu[8]等金属元素以及N[9]、C[10]、F[11]和B[12]等非金属元素.实验表明,金属或者非金属离子的掺杂能够改变TiO2的晶体结构、能带结构和表面微结构,对催化剂的紫外、可见光催化活性产生重大的影响.
Si掺杂TiO2催化剂的研究已有报道.Anderson和Bard[13, 14]发现Si掺杂的TiO2催化剂的紫外光催化活性高于P25,而且在Si掺杂TiO2催化剂的表面能够形成Si—O—Ti结构.Reddy等[15]发现锐钛矿TiO2中掺杂Si后具有更好的热稳定性.Fu等人[16]的研究发现采用溶胶凝胶法制备的Si掺杂TiO2催化剂,其紫外光催化活性提高源于比表面积的增加和热稳定性的增强.Shinji Iwamoto和Masashi Inoue[17]等利用XPS和XANES技术研究了Si掺杂TiO2中Si离子的掺杂方式,发现在Si掺杂的TiO2中,Si离子是高度分散的,形成Si—TiO2固溶体结构.Li等[18]采用水热法制备出Si掺杂TiO2催化剂,研究结果表明Si的掺杂在TiO2表面形成Ti—O—Si结构并形成SiO2,而且Si掺杂导致了TiO2催化剂禁带宽度增加. Si掺杂TiO2催化剂表现出高的紫外光催化活性,主要归因于催化剂热稳定性的增强.直至目前,Si掺杂TiO2催化剂的结构和掺杂方式在文献中存在不同报道,而且Si掺杂对-TiO2能带结构的影响和光催化机理缺乏深入研究,而且具有可见光响应的Si掺杂TiO2催化剂的报道尚少.
本文采用溶胶-凝胶法制备出具有高活性的Si4+离子掺杂TiO2可见光催化剂.利用XRD、XPS、UV-Vis DRS等表征技术,确定了可见光催化剂的结构、Si的掺杂方式和能带结构,分析讨论了Si掺杂TiO2可见光催化剂降解对-氯苯酚的可见光催化机理. 1 实验部分 1.1 催化剂的制备
采用溶胶凝胶法,以Ti(OC4H9)4为前驱物、正硅酸乙酯((C2H5O)4Si)为掺杂剂,制备出Si掺杂纳米TiO2可见光催化剂.首先量取一定体积的(C2H5O)4Si溶于40 mL的无水乙醇中,在强烈搅拌下加入1 mL的浓盐酸和12 mL的钛酸四丁酯,然后加入5 mL去离子水,持续搅拌直至TiO2凝胶为止.将凝胶放置陈化24 h,100 ℃烘干,450 ℃煅烧2.5 h,得到Si掺杂纳米TiO2催化剂,放入干燥器中备用.在相同的条件下,改变(C2H5O)4Si的加入量,即可得到一系列TiO2-xSi催化剂.样品标记为TiO2-xSi催化剂(x代表Si离子与Ti离子的摩尔百分比).纯TiO2的制备方法同上,只是没有加入(C2H5O)4Si.N掺杂的TiO2(TiO2-N)的制备:在没有加入(C2H5O)4Si的前提下,在TiO2溶胶中加入一定量NH3·H2O,产生浅黄色沉淀,制备出TiO2-N催化剂,其它制备方法同上.1.2 光催化反应
通过光催化降解对-氯苯酚溶液来评价纯TiO2、TiO2-N和TiO2-xSi催化剂的可见光催化活性.可见光催化实验在圆柱形玻璃反应器(70 mL)中进行,以400 W高压汞灯(Philips HPA400/30S)作为外照光源,用400 nm的截止滤光片滤掉紫外光,反应器距光源15 cm;催化剂用量为10 mg,对-氯苯酚溶液浓度为5×10-5 mol/L,体积为40 mL(pH=5.74),溶液中通氧量为5 mL·min-1,磁力搅拌保持反应体系中溶液浓度与温度(25±2 ℃)平衡.采用4-氨基氨替吡啉比色法测定对-氯苯酚剩余浓度.实验所用化学试剂均为分析纯,实验用水为ρ=18.2 MΩ·cm-1去离子水. 1.3 物性表征
X 射线粉末衍射谱(XRD,Rigaku D/max-2500,Cu靶,Kα线)测定TiO2和TiO2-xSi催化剂的晶体结构,粒子的平均粒径根据德拜-谢乐公式(D=kλ/Bcosθ)计算获得;等温氮气吸附-脱附分析(Micromeritics Automatic Surface Area Analyzer Gemini 2360, Shimadzu)测得所有催化剂的比表面积(BET);X射线光电子能谱(XPS)的测试在PHI1600型X-光电子能谱仪(Mg-Al靶, Kα线)上进行,所有的谱图都根据C1s (284.8 eV)进行校正;用KBr压片法在傅里叶变换红外光谱仪(MAGNA-560,Nicolet)上测得样品的红外光谱;紫外-可见分光光度计(U-4100, Hitachi)测定样品的紫外可见漫反射吸收光谱.2 结果与讨论 2.1 催化剂结构
图1为纯TiO2和TiO2-xSi样品的XRD谱,所有样品在25.3°、37.8°、48.0°、53.9°和62.7°出现的衍射峰表明纯TiO2和TiO2-xSi样品均为四方晶系锐钛矿结构.然而,纯TiO2在27.3°出现了一个弱的衍射峰,表明纯TiO2样品中含有微量的金红石结构.与纯TiO2比较,TiO2-xSi样品没有发现与Si4+离子相关的衍射峰,如SiO2等,而且TiO2-xSi样品的衍射峰没有出现明显的移动(见插图),其晶胞参数和晶胞体积基本不变(见表1),因此证明掺入的Si4+离子并没有以取代式或间隙式的掺杂方式进入TiO2晶格,可能是以Si的相关物种的形式,如Ti—O—Si结构,存在于TiO2粒子的表面.另外,TiO2-xSi样品没有金红石的衍射峰,而且相对于纯TiO2平均粒径减小,比表面积相对增加(见表1);原因在于在水解反应过程中TiO2表面Ti—O—Si结构的形成阻止表面金红石相的生成和晶粒的生长[19,20,21].
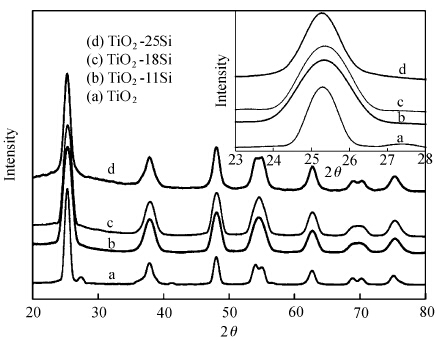 | 图1 TiO2和TiO2-xSi样品的XRD谱图,插图为各样品在2θ=25.3°附近的衍射峰 XRD patterns of TiO2 and TiO2-xSi samples, the inset shows the enlarged version of the peak near 25.3° |
| 表1 TiO2和TiO2-xSi样品的晶胞参数、晶胞体积、粒径和比表面积 Cell parameters, cell volume, crystallite size and specific surface area of TiO2and TiO2-xSi samples |
图2为纯TiO2和TiO2-xSi样品的FT-IR光谱.所有的样品在400—800 cm-1、1642 cm-1和3400 cm-1出现了3个较强的吸收带,400—800 cm-1的吸收带为Ti—O和Ti—O—Ti伸缩振动; 1620 cm-1和3400 cm-1的吸收带分别为吸附在催化剂表面的水分子的弯曲振动和伸缩振动[22, 23].与纯TiO2相比,TiO2-xSi样品在940和1120 cm-1附近出现的两个新的强吸收带分别被归属为Ti—O—Si和Si—O—Si的伸缩振动[24,25,26],而在1450 cm-1附近新的弱吸收带归结为Si—CHx (x=2或3)伸缩振动[27],表明掺杂的Si4+离子主要是以Ti—O—Si和Si—O—Si结构的形式存在于TiO2表面,同时TiO2表面存有微量的Ti—O—Si—CHx结构.
 | 图2 TiO2和TiO2-xSi样品的傅里叶红外光谱 The FT-IR transmission spectra of TiO2 and TiO2-xSi samples |
图3为纯TiO2和TiO2-18Si样品的Si2p的XPS谱.在图3中,纯TiO2没有Si2p峰出现,而TiO2-18Si样品Si2p3/2的结合能为102.5 eV,表明TiO2-18Si样品中掺入的Si离子为4+.另外,TiO2-18Si样品Si2p3/2的结合能(102.5 eV)低于SiO2的Si2p3/2结合能(103.60 eV),因此证明掺入的Si4+离子在TiO2粒子表面主要是以Ti—O—Si结构形式存在,而没有形成SiO2结构层.因为在TiO2粒子表面Ti—O—Si结构中Ti的电负性(1.54)小于SiO2 中Si—O—Si结构Si的电负性(1.90),所以TiO2-18Si样品表面Ti—O—Si的Si2p3/2的结合能(102.5 eV)低于SiO2中Si2p3/2的结合能(103.60 eV).图4为纯TiO2和TiO2-18Si样品O 1s的XPS谱,并采用Xpsaks 软件,以相同条件(峰位和半峰宽相等)对两样品的O 1s谱进行拟合.对于纯TiO2,结合能是530 eV的峰为TiO2晶格氧[28],而531.2 eV附近的峰被归结为表面含氧物种的氧,如表面桥氧和羟基(OH).对于TiO2-18Si样品,除530 eV和531.2 eV的峰外,结合能532 eV的峰被归结为TiO2表面Ti—O—Si结构的氧[17, 29],进一步证明掺入Si4+离子在TiO2粒子表面主要形成Ti—O—Si结构.另外,通过XPS定量计算可知,TiO2-18Si样品的表面桥氧和羟基的含量(15.89%)高于纯TiO2(4.68%),说明Si4+离子的掺杂有助于TiO2的表面羟基化.
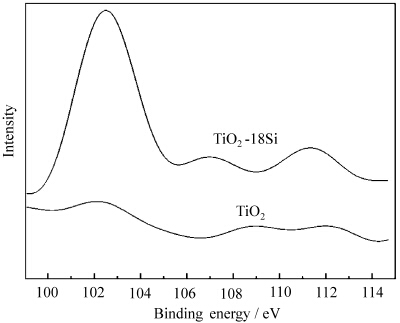 | 图3 TiO2和TiO2-18Si样品的Si 2p谱 The Si 2p peaks of TiO2 and TiO2-18Si samples |
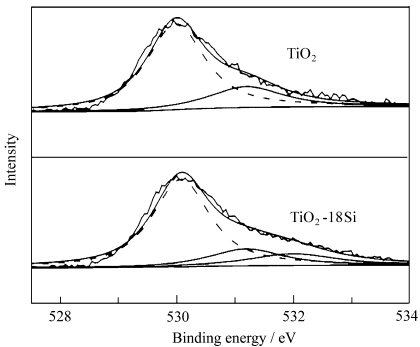 | 图4 TiO2和TiO2-18Si样品的O 1s 谱 The O 1s peaks of TiO2 and TiO2-18Si samples |
TiO2-18Si样品的FT-IR光谱分析可知,掺杂的Si4+离子在TiO2粒子表面主要形成Ti—O—Si和Si—O—Si两种结构,而Si2p的XPS谱的结果证明Si4+离子在TiO2粒子表面主要是以Ti—O—Si形式存在,没有形成SiO2结构。综合以上分析,在TiO2粒子表面可能Ti—O—Si结构之间由—O—(桥氧)连接(一个—O—连接2个Ti—O—Si结构,一个Ti—O—Si结构在四配位的Si位由3个—O—连接3个Ti—O—Si结构),形成表面Ti—O—Si—O—Si—O—Ti网络结构(Ti—O—Si)x.
图5为TiO2和TiO2-xSi样品的漫反射紫外可见吸收光谱,350 nm附近的强峰为TiO2和TiO2-xSi样品的带带跃迁,起峰阈值分别为409 nm和407 nm.根据文献[30]中的禁带宽度计算方法可得出TiO2和TiO2-xSi样品的禁带宽度分别为3.03 eV和3.05 eV,表明掺入的Si4+离子在TiO2粒子表面主要形成Ti—O—Si结构,不能改变TiO2的禁带宽度.报道指出[31,32,33,34],TiO2表面Ti—O—Si结构的存在会在TiO2导带和价带之间引入新的束缚态能级.其中,非金属离子形成的表面结构的能级一般位于TiO2价带上方而金属离子形成的表面结构的能级一般位于TiO2导带下方。因此,TiO2-xSi样品在400—650 nm可见光区出现明显的吸收被归结为电子从TiO2的价带到Ti—O—Si表面结构能级(表面态能级)的跃迁,该表面态能级主要集中在导带下0.2—0.6 eV区域.
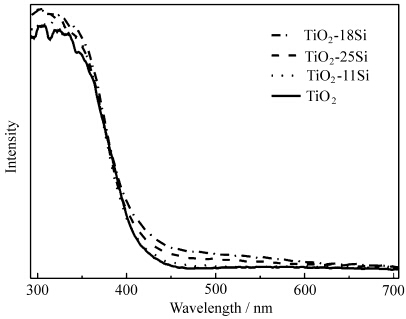 | 图5 TiO2和TiO2-xSi样品的漫反射紫外-可见吸收谱 Diffuse reflectance UV-Vis spectra of TiO2 and TiO2-xSi samples |
图6为TiO2 、TiO2-N和TiO2-xSi样品的可见光催化降解对-氯苯酚的浓度与降解时间(c-t)曲线,其可见光催化活性见表2. 结果表明,可见光空白实验只有微弱的光解,TiO2-xSi样品的可见光活性(降解率(Δc/c0)、反应速率常数(k)、半衰期(t1/2)、比活性)均明显高于纯TiO2和TiO2-N样品. 纯TiO2 的8 h降解率为10%,TiO2-N的8 h降解率为26.9%, 而TiO2-18Si样品8 h降解率为78.2%,分别是纯TiO2的7倍和TiO2-N的3倍.TiO2、TiO2-N和TiO2-xSi样品的ln (c0/c)~t 之间呈现直线关系,说明其光催化反应为一级动力学反应.
 | 图6 TiO2和TiO2-18Si样品的可见光催化降解对氯苯酚的c-t曲线 Comparison of photocatalytic degradation of 4-chlorophenol in the presence of TiO2 and TiO2-18Si samples under visible light irradiation |
| 表2 TiO2和TiO2-xSi催化剂的可见光催化活性 Photodegradation of 4-chlorophenol under visible light irradiation |
根据以上的表征结果,并结合光催化基本原理,TiO2-xSi催化剂比纯 TiO2可见光催化活性提高的主要原因如下:由于纯TiO2的禁带宽度只有3.03 eV(λ= 409 nm),对λ>400 nm的可见光吸收较弱(见图6),因此可见光活性较低.对于TiO2-xSi样品,由于掺入的Si4+离子在TiO2粒子表面形成Ti—O—Si结构,在导带下0.2—0.6 eV区域形成该结构的表面态能级,价带到表面态能级的跃迁(400—650 nm)产生可见光响应,实现了催化剂表面光生载流子的直接分离,从而提高了催化剂的可见光催化活性。其可见光催化的机理如下:在光催化反应过程中,由于可见光照射,TiO2-xSi催化剂的价带到Ti—O—Si表面态能级的跃迁导致了光生载流子在催化剂表面直接发生分离,跃迁到Ti—O—Si表面态能级的光生电子能够被表面吸附的O2分子俘获形成O-2,在固液界面发生如下反应:
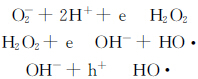
以Ti(OC4H9)4为前驱物、正硅酸乙酯((C2H5O)4Si)为掺杂剂,采用溶胶-凝胶法制备出Si4+离子掺杂的TiO2可见光催化剂(TiO2-xSi).光催化降解对-氯苯酚的实验表明,该催化剂的可见光催化活性远高于纯TiO2和N掺杂的TiO2(TiO2-N)催化剂. 研究结果表明,掺入的Si4+离子主要是以Ti—O—Si结构形式存在于TiO2粒子表面,在导带下0.2—0.6 eV区域形成表面态能级,价带到表面态能级的跃迁产生可见光吸收,使催化剂光谱响应范围拓宽到可见区,从而导致了光生载流子在催化剂表面的直接分离,实现了催化剂的可见光催化.另外,Si4+离子的掺杂增加了催化剂的表面羟基等活性物种, 增强了表面吸附能力和氧化还原能力,有效地提高了催化剂的可见光催化活性.
| [1] | Fujishima A, Honda K. Electrochemical photolysis of water at a semiconductor electrode[J]. Nature, 1972, 238: 37. |
| [2] | Thompson T L, Yates Jr J T. Surface science studies of the photoactivation of TiO2-new photochemical process[J]. Chemical Reviews, 2006, 106: 4428. |
| [3] | Chen X B and Mao S S. Titanium dioxide nanomaterials: synthesis, properties, modifications, and applications[J]. Chemical Reviews, 2007, 107: 2891. |
| [4] | Cao Y, Yang W, Zhang W, et al. Improved photocatalytic activity of Sn4+doped TiO2 nanoparticulate films prepared by plasma-enhanced chemical vapor deposition[J]. New journal of Chemistry,2004, 28: 218. |
| [5] | Zhu J, Ren J, Huo Y, et al. Nanocrystalline Fe/TiO2 visible photocatalyst with a mesoporous structure prepared via a nonhydrolytic sol-gel toute[J]. The Journal of Physical Chemistry C,2007, 111: 18965. |
| [6] | 王恩君,杨辉云,曹 亚. Zr离子掺杂TiO2可见光光催化剂光催化活性的研究[J].化学学报,2009,67: 2759. Wang E, Yang H, Cao Y. Photocatalytic activity of visible-light-driven zirconium doped TiO2 photocatalysts[J]. Acta Chimica Sinica, 2009, 67: 2759. |
| [7] | Yang Y, Wang H, Li X, et al. Electrospun mesoporous W6+-doped TiO2 thin film for efficient visible-light photocatalysis[J]. Materials Letters,2009,63:331-333. |
| [8] | Nagaveni K, Hegde M S, Madras G S. Stucture and photocatalytic activity of Ti1-xMxO2±δ (M=W, V, Ce, Zr, Fe, and Cu) synthesized by solution combustion method[J]. The Journal of Physical Chemistry B, 2004, 108: 20204-20212. |
| [9] | Asahi R, Morikawa T, Ohwaki T, et al. Visible-light photocatalysis in nitrogen-doped titanium oxides[J].Science, 2001, 293: 269-271. |
| [10] | Chen D, Jiang Z, Geng J, et al. Carbon and nitrogen co-doped TiO2 enhance visible-light photocatalytic activity[J]. Industrial & Engineering Chemistry Research,2007, 46: 2741. |
| [11] | 黄冬根,廖世军,党 志.氟掺杂锐钛矿型TiO2的制备、表征及催化性能[J]. 化学学报, 2006, 64: 1805. Huang D G, Liao S J, Dang Z. Preparation, characterization and photocatalytic performance of anatase F doped TiO2 sol[J]. Acta Chimica Sinica,2006, 64: 1805. |
| [12] | 龙绘锦,孟庆巨,元 晶,杨文胜,曹亚安.B离子掺杂TiO2催化剂(TiO2-xBx)光催化活性的研究[J]. 化学学报, 2008, 66: 657 Long H, Meng Q, Yuan J, et al. Study on photocatalytic activity of boron doped TiO2 catalyst(TiO2-xBx)[J]. Acta Chimica Sinica,2008, 66: 657. |
| [13] | Anderson C, Bard A J. An improved photocatalyst of TiO2/SiO2 prepared by a sol-gel synthesis[J]. The Journal of Physical Chemistry,1995, 99: 9882. |
| [14] | Anderson C, Bard A J. Improved photocatalytic activity and characerization of mixed TiO2/SiO2 and TiO2/Al2O3 materials[J]. The Jounal of Physical Chemistry B, 1997, 101: 2611-2616. |
| [15] | Reddy B M, Mehdi S, Reddy E P. Dispersion and thermal stability of vanadium oxide catalysts supported on titania mixed oxide[J]. Catalysis Letters,1993, 20:317. |
| [16] | Fu X, Clark L A, Yang Q. Anderson M A. Enhanced photocatalytic performance of Titania-based binary metal oxides: TiO2/SiO2 and TiO2/ZrO2[J]. Environmental Science & Technology,1996, 30: 647-653. |
| [17] | Shinji I,Seiu I,Masashi I. XANES and XPS study of silica-modified Titanias prepared by the glycothermal method[J]. Chemistry of Materials,2005, 17:650-655. |
| [18] | Li J, Hou B, Xu Y,et al. Hydrothernal synthesis, characterization, and photocatalytic performance of silica-modified titanium dioxide nanoparticles[J]. Journal of Colloid and Interface Science,2005, 288: 149-154. |
| [19] | Zhang H, Banfield J F. Thermodynamic analysis of phase stability of nanocrystalline titania[J]. Journal of Materials Chemistry,1998, 8:2073-2076. |
| [20] | Kumar S R, Suresh C, Vasudevan K A, et al. Phase transformation in sol-gel titania containing silica[J]. Materials Letters,1999, 38: 161-166. |
| [21] | Pabon E,Retuert J,Quijada R, et al. TiO2-SiO2 mixed oxides prepared by a combined sol-gel and polymer inclusion method[J]. Microporous Materials,2004, 67:195-203. |
| [22] | Yu J G, Yu H G, Cheng B, et al. The effect of calcination temperature on the surface microstucture and photocatalytic activity of TiO2 thin film prepared by liquid phase deposition[J]. The Journal of Physical Chemistry B,2003, 107:13871. |
| [23] | Hong X, Wang Z, Cai W, et al. Visible-light-activated nanoparticle photocatalyst of lodine-doped Titanium dioxide[J]. Chemistry of Materials,2005, 17:1548-1552. |
| [24] | Duran A,Serna C,Fornes V, et al. Structural considerations about SiO2 glasses prepared by sol-gel[J]. Journal of Non-Crystalline Solids,1986, 82: 69-77. |
| [25] | Belhekar A, Awate S, Anand R. Photocatalytic activity of titania modified mesoporous silica for pollution control[J]. Catalysis Communication, 2002, 3: 453-458. |
| [26] | Yamashita H, Kawasaki S, Ichihashi Y, et al. Characterization of Titanium-silicon binary oxide catalysts prepared by the sol-gel method and their photocatalytic reactivity for the liquid-phase oxidation of 1-Octanol[J].The Journal of Physical Chemistry B,1998, 102: 5870-5875. |
| [27] | Chung Y, Richard A B, Susan M K, et al. Synthesis of alkyl-terminated silicon nanoclusters by a solution route[J]. The Journal of the American Chemical Society,1999, 121(22):5191-5195. |
| [28] | Cao Y, Meng Q, Yang W, et al. Effect of plasma treatment on surface properties of TiO2 nanoparticulate films[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2005, 262: 181. |
| [29] | Chen Q, Jiang D, Shi W, et al. Visible-light-activated Ce-Si co-doped TiO2 photocatalyst[J].Applied Surface Science, 2009, 255: 7918-7924. |
| [30] | Surolia P, Tayade R, Jasra R. Photocatalytic degradation of nitrobenzene in an aqueous system by transition-metal-exchanged ETS-10 zeolites[J]. Industrical & Engineering Chemistry Research, 2010, 49: 3961-3966. |
| [31] | Wang E, He T, Zhao L, Chen Y, Cao Y. Improved visible light photocatalytic activity of titania doped with tin and nitrogen[J]. Jounal of Materials Chemictry, 2010, 21:144-150. |
| [32] | Wang E, Zhang P, Chen Y, Liu Z, He T, and Cao Y. Improved visible-light photocatalytic activity of titania activated by nitrogen and indium modification[J]. Jounal of Materials Chemictry, 2012, 22: 14443-14449. |
| [33] | Rehm J, McLendon G, Nagasawa Y, Yoshihara K, Moser J, and Gr tzel. Femtosecond electron-transfer dynamics at a sensitizing dye-semiconductor(TiO2) interface[J]. The Journal of Physical Chemistry, 1996, 100: 9577-9578. |
| [34] | Mao L, Li Q, Zhang. Study on surface states of Pt/TiO2 thin film in different atmospheres[J]. Solar Energy, 2007, 81: 1280-1284. |




