2. 中国科学院大学, 北京 100049;
3. 北京师范大学化学学院, 北京 100875
2. University of Chinese Academy of Sciences, Beijing 100049, P.R. China;
3. Beijing Normal University, College of Chemistry, Beijing 100875, P. R. China
光产酸剂(Photo-acid Generator,简称PAG)是一类在光、射线、等离子体等辐射下能够分解生成特定酸的化合物,所产生的酸可使酸敏树脂发生分解或者交联反应,从而使光照部分与非光照部分溶解反差增大.光产酸剂被广泛应用于阳离子光固化材料、热敏印刷版材及化学增幅抗蚀剂等成像体系中.目前用于感光成像体系的主要产酸剂分为离子型和非离子型两大类.传统的离子型光产酸剂,主要有重氮盐、二芳基碘鎓盐、三芳基硫鎓盐等,这几类光产酸剂产酸效果良好,工艺成熟,但稳定性和溶解性较差,吸收波长范围较短(<300 nm),限制了其应用[1,2,3,4].在此基础上发展起来的分子内增感硫鎓盐产酸剂,即敏化作用发生在分子内,分子内发生电荷转移,有单分子反应的特点,不受扩散速度的影响.依靠分子内增感作用使其吸收波长红移至400 nm左右,但是合成步骤复杂、成本昂贵[5,6].非离子型产酸剂主要有N-羟基酰亚胺磺酸酯、亚胺磺酸酯、硝基苄苯磺酸酯和磺酸肟酯类等,通过引入不同结构的生色团和不同强弱的酸根,可以改变吸收波长及产酸率.非离子型产酸剂较离子型产酸剂在有机溶剂和聚合物膜中的溶解性好,并具有产酸毒性小、吸收光谱较宽、合成简单等特点,随着光聚合体系的不断发展,在紫外光固化和微电子领域的应用备受关注[7,8,9,10,11].
2001年,Asakura等[12]报道了的一种磺酸肟酯化合物(5-甲基磺酸酯亚胺-5H-噻吩-2-亚胺)-甲基苯乙腈(MTMA),见结构式1.其在g线(436 nm)、i线(365 nm)和深紫外(DUV,248nm)都有很好的光产酸率,这种产酸剂在一般溶剂中有较好的溶解性,在酚醛树脂体系中有很好的稳定性(分解温度可达140℃),可用于正性和负性的抗蚀剂中.但其在可见光区的吸收很差,不能满足410 nm等新型紫光LED光源的使用要求.

结构式1 (5-甲基磺酸酯亚胺-5H-噻吩-2-亚胺)-甲基苯乙腈
本文利用两种生色团与3种磺酰氯化合物进行组合,通过用不同生色团来改变光产酸剂的吸收波长,而不同种类的磺酰氯化合物可以产生不同强度的酸根.合成了4种该系列的非离子型光产酸剂,用核磁氢谱确认了产物结构,并对其热稳定性、紫外可见吸收特性、产酸效率及引发阳离子聚合性能进行了测试. 1 实验部分 1.1 仪器与试剂
化学试剂:噻吩、冰醋酸、浓硝酸(95%)、甲醇、苯乙腈、四氢呋喃、三乙胺、对甲基苯磺酸、苯、氢氧化钾、乙酸乙酯、罗丹明B(RB)、庚烷、丙酮,均购自北京蓝弋化工产品有限责任公司;硝基苯,购自北京偶合科技有限公司;对甲基苯磺酰氯、甲基磺酰氯、对三氟甲基苯磺酰氯,为AlfaAesar公司产品.
实验仪器:紫外吸收采用TU-1901紫外-可见分光光度计.1HNMR采用Avame PRX500 Bruker-HNMR,以CDCl3、DMSO为溶剂.热稳定性测定采用ZRY-2P型综合热分析仪.实时傅立叶红外光谱采用Niolet 5700 FT-IR(KBr分束器,MTC/A检测器,数据采集间隔为0.3985 s,分辨率4 cm-1),美国热电公司;紫外光点光源为配有320—480 nm滤光片的EFOSLite点光源,光纤直径为5 mm,EXFOPSD,加拿大;UV-A光强计,北京师范大学光电仪器厂. 1.2 4种非离子型光产酸剂的合成
合成的4种磺酸肟酯类非离子型光产酸剂包括:(5-对甲基苯磺酸酯亚胺-5H-噻吩-2-亚胺)-苯乙腈(P-1)、(5-对三氟甲基苯磺酸酯亚胺-5H-噻吩-2-亚胺)-苯乙腈(P-2)、(4-甲基磺酸酯亚胺-环己醇-2,5-二亚乙胺基)-(2-苯基)-乙腈(P-3)、(4-对甲基苯磺酸酯亚胺-环己醇-2,5-二亚乙基胺基)-(2-苯基)-乙腈(P-4),结构式如图1所示.
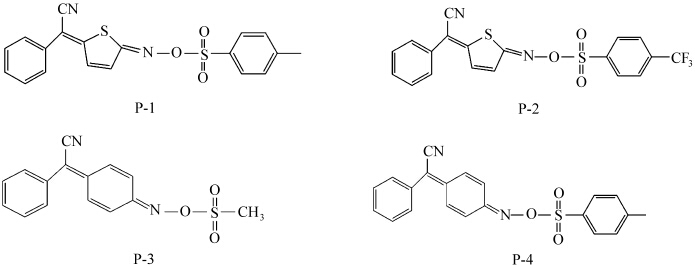 | 图1 4种磺酸肟酯类光产酸剂的结构式 Structure formula of four oxime sulfonates photoacid generators |
(1)中间产物a的合成[13]:6.45 g(0.05 mol)硝基噻吩于甲醇溶解,室温下加入30 g四甲基氢氧化铵,溶解后加入11.5 mL(0.1 mol)苯乙腈.反应3 h,浓盐酸调节pH至5,倒入水中,CHCl3萃取,无水MgSO4干燥,减压蒸馏,甲醇重结晶得棕黄色晶体,产率46%.
(2)目标产物P-1的合成:将中间产物a 5.6 g(0.02mol)和50 mL四氢呋喃在冰水浴搅拌下,加入10 mL三乙胺,再滴入3 mL(0.02 mol)对甲基苯磺酰氯,反应2 h.将反应液倒入水中,所得固体用甲苯重结晶,得棕黄色晶体,产率48%.
1HNMR(400 MHz,DMSO-d6):2.36(s,3H),6.61(d,1H),6.86(d,1H),7.21(d,2H),7.54—7.59(m,5H),7.93(d,2H).
(3)目标产物P-2的合成:将中间产物a 0.5g溶于50 mL苯中,注入2.4 mL对三氟甲基苯磺酰氯,50 ℃下反应1 h.加入30 mL苯稀释后,用50 mL,15%的Na2CO3溶液洗涤,水洗,无水Na2SO4干燥过夜,得黄色固体,再用庚烷重结晶,得棕黄色晶体,产率26%.
1HNMR(400 MHz,DMSO-d6):6.59(d,1H),7.20—7.21(d,1H),7.54—7.59(m,5H),7.92(d,2H),7.94—7.95(d,2H).19F(400 MHZ,DMSO-d6,113 ppm).
1.2.2 P-3及P-4的合成:(1)中间产物b的合成[13]:10 g氢氧化钾和55 mL甲醇搅拌溶解,55 ℃下依次加入6.2 mL(0.045mol)苯乙腈和4.5mL硝基苯,反应4 h后冷却至室温,倒入水中,并以醋酸和水进行酸化(测定pH呈酸性),黄色固体产物以甲醇和水洗涤,以苯重结晶,得黄色固体,产率42%.
(2)目标产物P-3的合成:将中间产物b 1.0 g和20 mL四氢呋喃加入三口瓶中,5℃下滴加0.95 mL三乙胺,再加入溶有1.0 g甲基磺酰氯的四氢呋喃溶液,反应2 h.将反应液倒入水中,固体用甲苯重结晶,得黄色晶体,产率38%.
1HNMR(400 MHz,CDCl3): 3.25(s, 3H), 6.79—6.82(d, 1H), 7.23—7.25(d, 1H), 7.30—7.33(s, 1H),7.51(s, 5H), 7.58—7.61(d, 1H).
(3)目标产物P-4的合成:将中间产物b 1.0g和20 mL四氢呋喃加入三口瓶中,5℃下滴加0.95 mL三乙胺,再加入溶有2.0 g对甲苯磺酰氯的四氢呋喃溶液,反应2 h.将反应液倒入水中,固体用甲苯重结晶,得黄色晶体,产率30%.
1HNMR(400 MHz,CDCl3):3.6(3H),6.7(1H),6.9—7.0(2H),7.3—7.5 (8H),7.9 (1H),8.5 (1H). 1.3 结构表征与性质测定
1HNMR采用Avame PRX500 Bruker-HNMR,以CDCl3、DMSO为溶剂,表征化合物结构.热稳定性测定采用ZRY-2P型综合热分析仪.紫外可见吸收光谱测定采用TU-1901紫外-可见分光光度计,溶剂为乙腈. 1.4 光产酸效率的评价 1.4.1 测试原理
本文采用罗丹明B(RB)指示剂法测定4种光产酸剂的产酸效率.由于这几种光产酸剂紫外光谱的最大吸收峰在410 nm、365 nm附近,所用指示剂必须对350—450 nm范围内的波长基本无吸收,并且能通过其吸光度的改变反映酸度的变化.RB在非质子溶剂中为内酯型结构的隐染料,遇酸后,RB隐染料发生开环反应成为羧酸型结构(见反应式1),555 nm处的吸光度明显增大.前人实验表明:随着酸浓度的增加,RB在555 nm处的吸收峰值也随之增加[14 ,15,16],是测定光产酸效率的合适染料.RB(隐)与酸的反应式如下:

反应式1罗丹明B隐染料遇酸后的开环反应
将对甲基苯磺酸和RB分别溶解在有机溶剂中,配制成一系列浓度的溶液.将一系列不同浓度的酸与一定浓度的RB溶液反应混合,用紫外-可见光分光光度计跟踪不同浓度条件下RB的吸光度变化ΔAbs,在一定浓度范围内,以RB特征峰吸光度的变化为纵坐标,以酸的浓度为横坐标,绘制曲线,RB的活性吸收峰值随酸浓度的变化呈现良好的线性关系,即可得到所谓的标准工作曲线. 1.4.3 光产酸效率的测定
将RB溶于已知浓度的光产酸剂的乙腈溶液,置于比色皿中,再用已经分别放置了420 nm和365 nm滤光片的紫外灯对其进行曝光,曝光能量均为47.4 mJ/cm2,测定曝光后样品的吸光度,再以标准工作曲线为参比,根据ΔAbs即可得到对应的酸的浓度Δc,c0为光产酸剂初始浓度,然后根据公式(1)计算可以得到光产酸剂在溶液中的产酸效率.

本工作的光聚合体系由上述光产酸剂和本实验室合成的乙烯基醚类单体DVE[17](见结构式2)组成.乙烯基醚单体在近红外谱图中碳碳双键的特征吸收峰在1616 cm-1处,随着光固化反应的进行,碳碳双键变成碳碳单键,双键的吸收峰强度随光照时间增加而变弱,所以可利用碳碳双键的特征吸收峰的变化来监视其聚合反应的变化程度.双键转化率(DC%)和聚合速率(R)由Origin6.1数据处理软件和OMNIC7.1红外软件结合公式(2)和公式(3)计算得到[18, 19].

结构式2 DVE单体
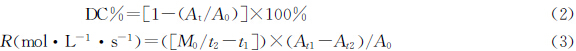
上两式中,A0为样品在固化前、At为样品在固化过程中任意时刻单体双键特征吸收峰的面积,[M0]为所选单体双键官能团的初始浓度. 2 结果与讨论 2.1 理化性质测定 2.1.1 热稳定性
采用热重分析法以研究几种光产酸剂的热稳定性,图2为P-1、P-2、P-3、P-4的热分解曲线.由此可以看出4种光产酸剂初始分解温度分别为178 ℃、165 ℃、160 ℃、150 ℃,其热稳定性均较好.
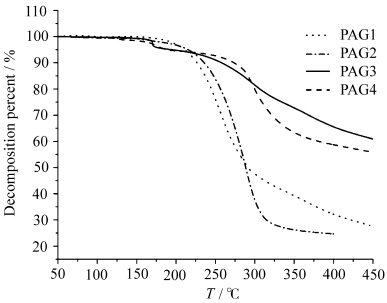 | 图2 4种光产酸剂的热重曲线图 TG curve of four photoacid generators |
图3为4种光产酸剂的紫外吸收光谱图,浓度为8×10-5mol/L,由此谱图可以看出它们的紫外吸收光谱较宽.
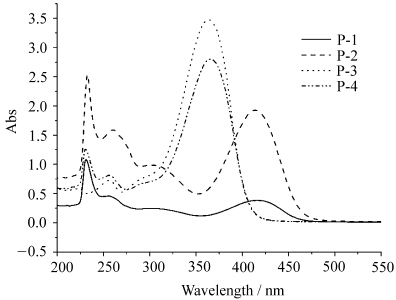 | 图3 4种引发剂的的紫外吸收光谱图 UV absorption spectrum of four photoacid generators |
下表1为4种光产酸剂的吸收波长及相对应的摩尔消光系数.
| 表1 4种光产酸剂的紫外吸收波长及摩尔消光系数 Maximum absorptions and molar extinction coefficient of four photoacid generators |
图4为不同浓度对甲基苯磺酸下的RB的吸收光谱图.从图4可得图5所示的标准工作曲线.可以看出:RB的活性吸收峰强度与对甲基苯磺酸浓度(c=10-5 mol/L)呈现良好的线性关系。由标准工作曲线可以测定出光产酸剂的光照产酸量,根据产酸效率公式(1)可求出产酸剂的产酸效率。
 | 图4 RB的活性吸收峰值对酸(对甲基苯磺酸)的浓度关系图 Absorption spectra of RB base with different concentration p-Toluene sulfonic acid |
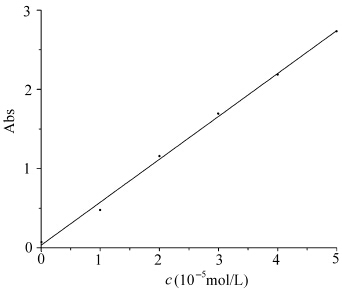 | 图5 标准工作曲线 Standard working curve |
将RB(隐)和光产酸剂的混合溶液在紫外灯下曝光,通过测定RB活性吸收峰的变化,可以得到光产酸剂的产酸量随曝光时间的变化图,结合前面测得的工作曲线,得到各光产酸剂的产酸率(cH+/c总),即产生酸的浓度与光产酸剂的浓度之比,结果见表2.
| 表2 4种光产酸剂在不同波长下的产酸率 The acid yield of four photoacid generators under different wavelength |
从表2可以看出,P-1和P-2在365 nm和420 nm的紫外光照射下均有较高的产酸率,而P-3和P-4产酸率则较低,说明产酸率与产酸剂的结构有很大关系.受到与N相连的噻吩环和苯环的不同影响,中间体为噻吩环型的光产酸剂P-1,由于S原子的吸电子性要比C原子强,使得噻吩环在N处的电子云密度变小,从而导致N-O键更加容易断裂.
以P-1为例,光产酸剂在光照下分解生成酸的机理[9]如反应式2所示.
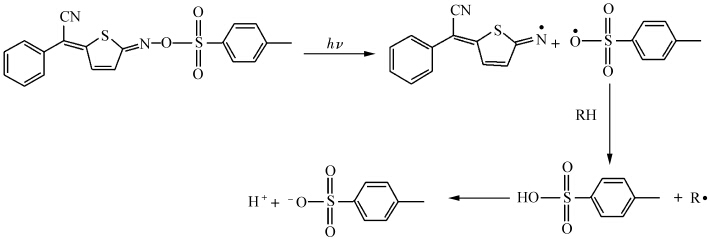
反应式2 P-1的光解机理(RH为供氢体)
配制4个质量浓度为10%的DVE丙酮溶液,分别加入P-1、P-2、P-3、P-4,使光产酸剂占单体质量的3%,涂于KBr盐片上,然后放入Nicolet5700中,用紫外光点光源照射固化,光照波长为365 nm,紫外光强为30 mW/cm2,DVE的双键转化率和聚合速率曲线分别如图6、7所示.
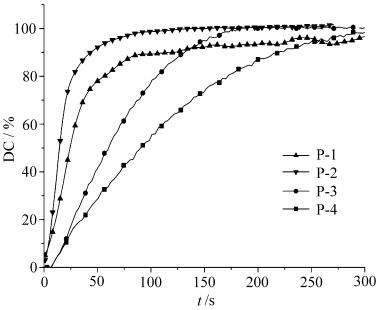 | 图6 P-1—P-4引发DVE聚合时的双键转化率(DC%) Conversion rate of DVE for P-1-P-4 |
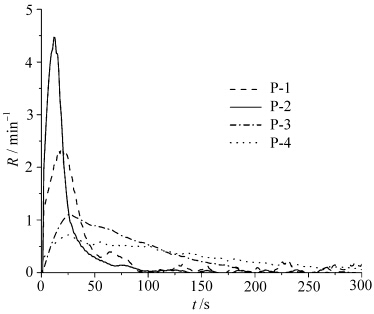 | 图7 P-1—P-4引发DVE聚合时的聚合速率 Polymerization rate of DVE for P-1-P-4 |
由图6可知,P-1—P-4引发单体聚合反应,双键转化率达到50%的时间,分别是24 s、14 s、60 s、90 s;由图7(聚合速率曲线图)可知,最大聚合速率从大到小排列依次是P-2>P-1>P-3>P-4,达到最大聚合速率的时间分别是19 s、12 s、24 s、25 s;与产酸率的大小趋势一致,即产酸率大的引发单体聚合反应的双键转化率高,聚合较完全,最大聚合速率快,达到最大聚合速率的时间短,产酸率最大的P-2引发单体聚合反应的聚合速率也最大.说明了在光产酸剂浓度占单体的质量分数为3%时,合成的几种光产酸剂均能引发乙烯基醚类单体聚合,但产酸率高的P-1和P-2,引发单体聚合反应的速率明显高于产酸率低的P-3和P-4. 2.3.2 光产酸剂P-1浓度对单体光聚合反应的影响
配制5个质量浓度为10%的DVE丙酮溶液,分别加入P-1,使P-1占单体质量的1%、2%、3%、4%、5%,涂于KBr盐片上,然后放入Nicolet5700中,用紫外光点光源照射固化,光照波长为365 nm,紫外光强为30 mW/cm2,DVE的双键转化率和聚合速率曲线分别如图8、9所示.
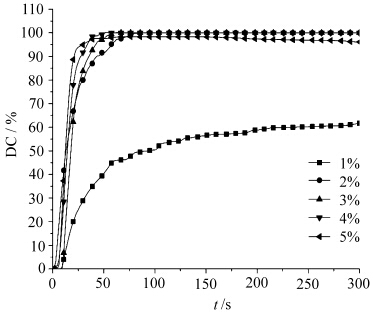 | 图8 P-1浓度对DVE双键转化率(DC%)的影响 Effect of P-1’s concentration on DC% of DVE |
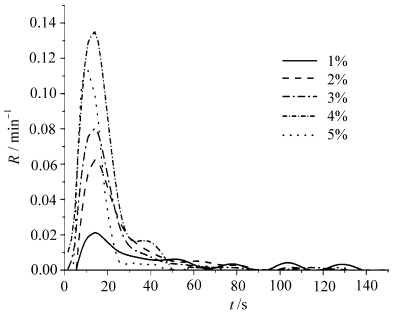 | 图9 P-1浓度对DVE聚合速率的影响 Effect of P-1’s concentration on polymerization rate of DVE |
由图8、9可知,在一定范围内,随着光产酸剂P-1浓度(质量分数)增大,DVE的聚合速率及双键转化率逐渐增高,这主要是因为P-1在紫外光照射下可产生强酸对甲苯磺酸,使DVE单体质子化,生成一个C+中心,然后DVE在阳离子链末端不断加成,生成高分子聚合物,所以随着P-1浓度的增加,P-1在紫外光照射下产生的活性种对甲苯磺酸浓度也增加,DVE的聚合速率也相应增加.研究中发现浓度为2%时,光照30 s即能达到80%的双键转化率,而引发剂浓度(质量分数)从4%增加到5%时,DVE的双键转化率有下降的趋势,这是由于引发剂对光有较强的吸收,在引发剂浓度过高时存在自屏蔽效应,使得引发剂的引发效率降低、产生的活性中心浓度并没有等比增加,最终导致聚合反应速率增加缓慢. 3 结论
本文合成了4种磺酸肟酯类非离子型光产酸剂,并对其结构进行了表征.这些化合物热分解温度可达150 ℃以上,在248 nm、365 nm等处有较强吸收,应用前景较广.其中分子内含有噻吩环的P-1和P-2不仅吸收光谱拓展到410 nm等可见光区,其光产酸效率也优于分子内含有苯环的P-3和P-4.以P-1为对象进行了光聚合动力研究,发现P-1浓度为2%时,光照30 s双键转化率(DC%)即能达到80%.
致谢:感谢北京化工大学材料科学与工程学院聂俊教授在实时红外测试方面提供的指导和帮助.
| [1] | 周 健,张秋禹,张和鹏,刘 清,王为强,周艳阳. 鎓盐类阳离子光引发剂的研究进展[J]. 材料导报A:综述篇, 2011,25(1):16-21. Zhou J, Zhang Q Y, Zhang H P, Liu Q, Wang W Q, Zhou Y Y. The development of onium salt cationic photoinitiators[J]. Materials Review, 2011, 25(1):16-21. |
| [2] | 张雅静,邹应全. 光致阳离子聚合引发剂的进展[J]. 信息技术材料,2006, 7(1). Zhang Y J, Zou Y Q. The development of photoinitiator for cationic polymerization[J]. Information Recording Materials,2006, 7(1). |
| [3] | Shirai M, Tsunooka M. Photoacid and photobase generators: prospects and their use in the development of polymeric photosensitive systems[J]. Bulletin of the Chemical Society of Japan,1998, 71(11): 2483-2507. |
| [4] | 蔡晓路,陆明湖.阳离子光引发剂的发展动态[J]. 感光材料,1999, 79-82. Cai X L, Lu M H. The development of cationic photoinitiators[J]. Image Materials, 1999,79-82. |
| [5] | 洪啸吟,Pappas S P. 分子内敏化鎓盐的合成及光敏性研究[J]. 感光科学与光化学,1993,11(3):256-263. Hong X Y, Pappas S P. Studies on synthesis and photoactivity of some onium salts with built-in photosensitizer[J]. Photographic Science and Photochemistry, 1993,11(3):256-263. |
| [6] | 王美丽,王文广,韩元利,蒲嘉陵. 新型硫鎓盐光生酸剂的合成及产酸性能研究[J]. 影像科学与光化学,2008, 26(2): 88-93. Wang M L, Wang W G, Han Y L, Pu J L. Studies on synthesis of sulfonium salts and their properties as photo-acid generator[J]. Imaging Science and Photochemistry, 2008, 26(2): 88-93. |
| [7] | Shirai M, Tsunooka M. Photoacid and photobase generators: chemistry and applications to polymeric materials[J]. Progress in Polymer Science, 1996,21(1):1-45. |
| [8] | Zhou W H, Kuebler S M, Braun K L, et al. An efficient two-photon-generated photoacid applied to positive-tone 3D microfabrication[J]. Science, 2002, 296(5570):1106-1109. |
| [9] | Shirai Masamitsu, Okamura Haruyuki. I-line sensitive photoacid generators for UV curing[J]. Progress in Organic Coatings, 2009, 64(2-3):175-181. |
| [10] | Okamura H, Sakai K, Tsunooka M. I-line sensitive photoacid generators and their use for photocrosslinking of polysilane/diepoxyfluorene blend[J]. Journal Photopolymer Science and Technology, 2003,16(1): 87-90. |
| [11] | Ortica F, Scaiano J C, Pohlers G. Laser flash photolysis study of two aromatic N-oxyimidosulfonate photoacid generators[J]. Chemistry of Materials, 2000, 12(2):414-420. |
| [12] | Asakura T, Yamato H, Matsumoto A, Ohwa M. Novel photoacid generators for chemically amplified resists with g-line, i-line and DUV exposure[J]. Proc. SPIE, 2001,4345:484-493. |
| [13] | Hyogo H Y, Bleier H.Oxime sulfonates and the use thereof as latent sulfonicaids. US patent, 6004724, 1999-12-21. |
| [14] | Pohlers G, Scaiano J C. A novel photometric method for the determination of photoacid generation efficencies using benzothiazole and xanthene dyes as acid sensors[J]. Chemistry of Materials, 1997,(9):3222-3230. |
| [15] | 王 健,张伟民,王文广,蒲嘉陵.光生酸剂产酸效率的研究[J].北京印刷学院学报,2006,14(2):15-18. Wang J, Zhang W M, Wang W G, Pu J L. The methods of evaluation on the acid-generation efficiency of PAGs[J]. Journal of Beijing Institute of Graphic Communication, 2006,14(2):15-18. |
| [16] | 韩元利, 王文广, 王美丽, 蒲嘉陵. 高效光生酸剂的设计合成与性能研究[J]. 影像技术,2007,(4),13-16.Han Y L, Wang W G, Wang M L, Pu J L, Design and synthesis of photoacid generator with high efficiency and research on performance[J]. Image Technology, 2007,(4):13-16. |
| [17] | 辛阳阳, 肖时卓, 周树云, 陈 萍, 邹应全. 氨基甲酸酯乙烯基醚类化合物光聚合性能研究[J]. 影像科学与光化学,2012, 30(6):463-470. Xin Y Y, Xiao S Z,Zhou S Y, Chen P, Zou Y Q. Study on photopolymerization properties of vinyl ether monomers with different functionalities[J]. Imaging Science and Photochemistry, 2012, 30(6):463-470. |
| [18] | Decker C, Moussa K. Real-time kinrtic-study of laser-induced polymerization[J]. Macromolecules, 1989,22(12):4455-4462. |
| [19] | Christian Decker, Trieu Nguyen Thi Viet, Hong Pham Thi. Photoinitiated cationic polymerization of epoxides[J]. Polymer International, 2001, 50(9):986-997. |




