氟离子是人体所必需的微量元素,适量的氟离子摄入有益于牙齿和骨骼的健康.美国环保署(EPA)规定安全饮用水中氟离子的最大浓度为4 mg/L(4 ppm或211 μmol/L)[ 1 ],过多或过少摄入氟离子都会对人体产生不良影响,例如:氟中毒、尿结石、肿瘤、骨质疏松等[ 2,3,4 ],所以研究快速便捷的水相中氟离子定性和定量检测方法有重要的意义.
传统的氟离子检测方法有氟离子选择性电极和离子色谱法等,但存在着成本高、操作复杂、不易携带等缺点[ 5,6,7 ],相比之下,荧光化学传感器具有方便、快捷、灵敏度高等优点,近些年来得到了快速发展.尽管基于氢键、路易斯酸碱或离子-π相互作用机理设计的传感器被证实可有效地检测氟离子[ 8,9,10,11,12,13,14 ],但是多数只能用于有机相中对四丁基氟化铵(TABF)的识别,并且会受到H2PO4-、AcO-、以及CN-的干扰,限制了这类荧光化学传感器在纯水体系中的应用;2003年,Swager和Kim首次报道利用硅氟间化学反应对氟离子实现了专一性识别[ 15 ],最近,中科院化学所的杨国强等人以分子内质子转移化合物为发色团,利用氟离子对硅氧键的断裂反应实现了在水相中对氟离子快速、专一性检测[ 16 ].香豆素是一类强荧光发色团,研究表明,硅烷基保护的7-羟基香豆素衍生物荧光很 弱,在氟离子作用下硅氧键断裂,脱保护后香豆素阴离子可以发射很强的荧光,在有机相中对氟离子的响应极快(~10 s),但在纯水相中响应时却需要~4 h[ 17 ].
本工作设计合成了香豆素衍生物7-(二叔丁基(对硝基苯醚)硅醚)-4-甲基-香豆素(DTBPC),研究了DTBPC在水中对氟离子的响应.研究结果表明,在表面活性剂十六烷基溴化铵的存在下,DTBPC可以高灵敏、快速、专一性地识别氟离子,为新型氟离子荧光传感器的发展提供了新的实验基础. 1 实验部分 1.1 仪器及主要试剂
Bruker Avance Π-400 核磁共振仪;Waters LCT Premier XE高分辨液质联用仪;日本岛津UV-2550型紫外可见吸收光谱仪;日立F-4500荧光光谱仪;北京电光科学仪器厂XT4-100X显微熔点仪.
四氢呋喃(THF)、三乙胺(Et3N)、乙酸乙酯、石油醚、二氯甲烷(CH2Cl2)、甲醇(CH3OH)、无水Na2SO4等均为国药集团北京化学试剂公司分析纯或化学纯产品,四氢呋喃用金属钠干燥回流后重蒸,三乙胺经氢化钙干燥后重蒸. 1.2 DTBPC的合成
DTBPC的合成路线如图1所示.
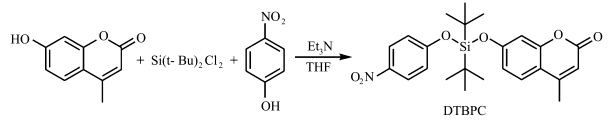 | 图1 DTBPC合成路线 Synthetic Route of DTBPC |
将660 mg (3.75 mmol) 4-甲基-7羟基香豆素、520 mg (3.75 mmol)对硝基苯酚、8.6 mmol (1.0 mL)TEA置于50 mL的三口瓶中,向瓶中加入20 mL干燥重蒸的THF,搅拌待体系完全溶解后,迅速加入1.2 mL (5 mmol)二氯二叔丁基硅烷,回流搅拌24 h停止反应;过滤,滤液旋干后用二氯甲烷溶解,饱和食盐水洗涤3次,无水Na2SO4干燥,过滤浓缩后柱层析分离(乙酸乙酯:石油醚 = 1 : 5),得到白色固体产物600 mg,重结晶(CH2Cl2: CH3OH=3∶7)得到570mg白色针状固体,产率33.5%,熔点:138—139℃.1HNMR (400 MHz,CDCl3) :1.12 (s,18H,SiCCH3),2.41 (s,3H,coumarin-CH3),6.18 (s,1H,coumarin-H3),6.88 (dd,J=8.7 Hz,J=2.4 Hz,1H,coumarin-H6),6.94 (d,J =2.3 Hz,1H,coumarin-H8),7.06 (d,J=9.2 Hz,2H,p-nitrophenol-H2),7.49 (d,J=8.7 Hz,1H,coumarin-H5),8.18 (d,J=9.2 Hz,2H,p-nitrophenol-H3);MS (ESI-TOF): m/z calcd: 478.165 [M + Na]+,found: 478.1654. 2 结果与讨论 2.1 DTBPC在THF中对氟离子响应研究
首先检测了DTBPC在四氢呋喃中对氟离子的响应行为.向DTBPC的四氢呋喃溶液中(1×10-5 mol/L)加入氟离子(四丁基氟化铵,5×10-5mol/L),测定体系的吸收和荧光发射光谱,10 s体系达到平衡,图2为体系中加入氟离子10 s后的吸收和荧光发射光谱.加入氟离子前后体系的吸收和发光都有明显改变,加入氟离子前,DTBPC的最大吸收在~300 nm处,以310 nm的光激发,体系表现为最大发射峰在375 nm的香豆素发射,但荧光很弱,分析是由于分子内电子转移,硝基苯猝灭了香豆素大部分的荧光.加入氟离子后,体系的最大吸收红移到415 nm,荧光光谱除最大发射峰红移到464 nm处,发光大大增强.根据文献可以推断,体系中氟离子的加入使DTBPC分子中Si—O键断裂,释放出香豆素阴离子(1),体系表现为香豆素阴离子的吸收和发光,基于分子内电荷转移(ICT)机制的香豆素阴离子的吸收和发光相比香豆素本身均有较大程度的红移.结果表明,实验条件下化合物DTBPC与氟离子的作用非常快(≤10 s),结合与氟离子作用前后荧光光谱的显著变化,说明DTBPC具有作为turn-on型荧光探针检测氟离子的能力.
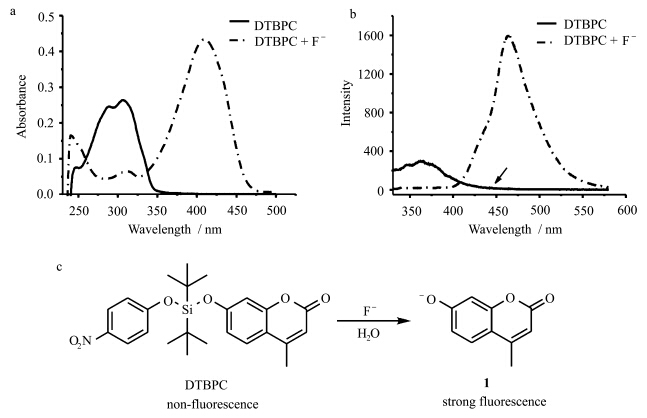 | 图2 四氢呋喃溶液中加入F-前后化合物DTBPC的吸收光谱(a)和荧光发射光谱(b) λex=310 nm,[DTBPC] = 1×10-5 mol/L,[F-] = 5×10-5 mol/L; (c) 氟离子检测机理 Absorption (a) and fluorescence (b) spectra of DTBPC (1×10-5 mol/L) in THF before and after addition of F- (5×10-5 mol/L); (c) the sensing mechanism of DTBPC for the detection of F- |
虽然化合物DTBPC在四氢呋喃有机溶剂中对氟离子有极为快速和灵敏的响应,但氟离子检测主要在水中进行.由于化合物DTBPC在水中溶解度差,为了实现在水相中对氟离子的检测,在阳离子表面活性剂十六烷基三甲基溴化铵(CTAB)的存在下,我们在水相中制备了DTBPC分散体系.配置浓度均为2.0×10-3mol/L的十六烷基三甲基溴化铵(CTAB)的水溶液和化合物DTBPC的THF溶液,用微量注射器取DTBPC的THF溶液100 μL,快速注入到10 mL高速搅拌的CTAB水溶液中,持续搅拌30 s,得到DTBPC水相分散体系[ 16 ].
向制备的DTBPC水相分散体系(2 × 10-5 mol/L)中加入不同量的氟离子(NaF),3 min后测定体系吸收和荧光发射光谱,如图3所示.没有加入氟离子时,体系的最大吸收峰在310 nm处,随着氟离子的加入,310 nm的吸收峰逐渐降低并略微红移,同时在长波长方向出现了最大峰为380 nm的新吸收峰,而体系的荧光光谱显著增强,最大峰在450 nm.图3b的插图直观的给出该体系在加入氟离子前后荧光由“off”到“on”的变化.显然,DTBPC在水相分散体系中氟离子作用下同样可以发生Si—O键断裂反应,生成香豆素阴离子,从而使体系表现为香豆素阴离子分子内电荷转移态的吸收和荧光发射.
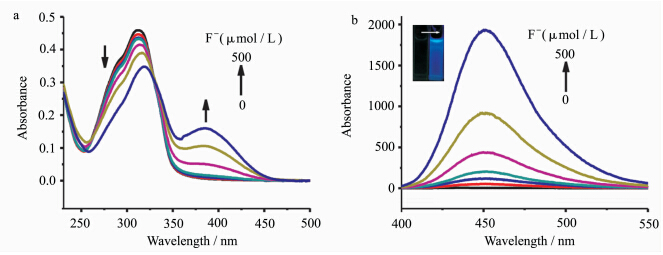 | 图3 DTBPC(2 × 10-5 mol/L)加入不同浓度的氟化钠3 min后的吸收(a)和荧光发射光谱(b) Absorption (a) and fluorescence (b) spectra of the DTBPC (2 × 10-5 mol/L) aqueous dispersion after 3 min upon addition of F- at 20 ℃,λex = 380 nm |
为了评估化合物DTBPC用于氟离子检测的能力,研究了化合物DTBPC水相分散体系对氟离子响应的选择性.向DTBPC(2 × 10-5 mol/L)水分散体系中分别加入100当量的常见阴离子(Br-,Cl-,F-,H2PO4-,HSO4-,AcO-,NO3-,SO42-,钠盐形式),10 min后检测体系的荧光光谱,只有加入F-的体系显示出明显的荧光增强,其它阴离子的加入对体系的荧光发射强度几乎没有影响,说明DTBPC水分散体系对氟离子的识别具专一选择性,可在众多阴离子中选择性识别氟离子.
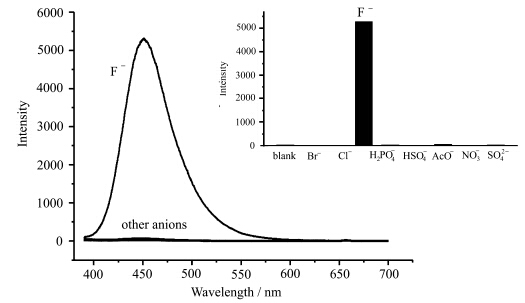 | 图4 DTBPC(2 × 10-5 mol/L)水分散体系分别加入100当量不同阴离子(Br-,Cl-,F-, H2PO4-,HSO4-,AcO-,NO3-,SO42-)10 min后的荧光发射光谱 插图为不同阴离子存在下体系450 nm发光强度,λex=380 nm Fluorescence spectra of DTBPC (2 × 10-5 mol/L) aqueous dispersions upon addion of 100 equiv of Br-,Cl-,F-,H2PO4-,HSO4-,AcO-,NO3-,SO42- The inset shows the selectivity for fluoride ions (monitoring the emission at 450 nm),λex =380 nm |
为了解DTBPC分散体系在水中对氟离子检测的灵敏度,我们计算了DTBPC在水相中对氟离子的检测限.当DTBPC浓度为2 × 10-5 mol/L、检测时间为3 min时,将体系450 nm处的荧光强度的变化对氟离子浓度,得到如图5所示的结果,体系在450 nm处的荧光强度的变化与氟离子浓度之间呈现很好的线性关系.利用检测限(limit of detection,LOD)计算公式(LOD=3*S.D./K,S.D.为未添加氟离子时探针分子荧光光谱变化的标准偏差,K为曲线斜率),计算得到探针分子的检测限60 ppb,说明探针分子DTBPC在水相中检测氟离子具有很好的灵敏度.
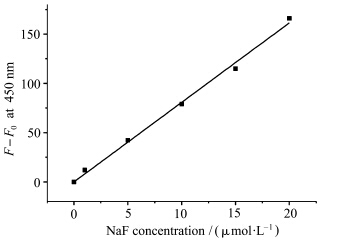 | 图5DTBPC(2×10-5 mol/L)水分散体系450 nm处荧光强度随加入氟离子浓度 (0—20×10-6 mol/L)变化关系,λex=380 nm The change of fluorescence intensities at 450 nm of DTBPC aqueous dispersion (2×10-5 mol/L) as a function of fluoride concentration (0—20 × 10-6 mol/L),λex = 380 nm |
设计合成了香豆素衍生物DTBPC,基于氟硅特殊的相互作用,以DTBPC为探针分子研究了其在水相中识别氟离子的方法,检测响应时间从文献中类似探针分子的4 h缩短到3 min,检测限达到60 ppb,对氟离子的检测具有专一的选择性.为进一步研究可用于水相氟离子检测的新型turn-on型荧光传感器提供了实验依据.
| [1] | Carton R J. Review of the 2006 united states national research council report: fluoride in drinking water[J]. Fluoride, 2006, 39(3): 163-172. |
| [2] | Kobayashi C A N, Leite A L, Silva T L, Dos Santos L D, Nogueira F C S, Santos K S, De Oliveira R C, Palma M S, Domont G B, Buzalaf M A R. Proteomic analysis of urine in rats chronically exposed to fluoride[J]. Journal of Biochemical and Molecular Toxicology, 2011, 25(1): 8-14. |
| [3] | Singh P, Barjatiya M, Dhing S, Bhatnagar R, Kothari S, Dhar V. Evidence suggesting that high intake of fluoride provokes nephrolithiasis in tribal populations[J]. Urological Research, 2001, 29(4): 238-244. |
| [4] | Bassin E B, Wypij D, Davis R B, Mittleman M A. Age-specific fluoride exposure in drinking water and osteosarcoma (United States)[J]. Cancer Causes & Control, 2006, 17(4): 421-428. |
| [5] | De Marco R, Clarke G, Pejcic B. Ion-selective electrode potentiometry in environmental analysis[J]. Electroanalysis, 2007, 19(19-20): 1987-2001. |
| [6] | Breadmore M C, Palmer A S, Curran M, Macka M, Avdalovic N, Haddad P R. On-column ion-exchange preconcentration of inorganic anions in open tubular capillary electrochromatography with elution using transient-sotachohoretic gradients. 3. Implementation and method development[J]. Analytical Chemistry, 2002, 74(9): 2112-2118. |
| [7] | Van den Hoop M A G T, Cleven R F M J, Van Staden J J, Neele J. Analysis of fluoride in rain water comparison of capillary electrophoresis with ion chromatography and ion-selective electrode potentiometry[J]. Journal of Chromatography A, 1996, 739(1): 241-248. |
| [8] | Guha S, Saha S. Fluoride ion sensing by an anion-π interaction[J]. Journal of the American Chemical Society, 2010, 132(50): 17674-17677. |
| [9] | Wang J, Yang L, Hou C, Cao H. A new N-imidazolyl-1,8-naphthalimide based fluorescence sensor for fluoride detection[J]. Organic & Biomolecular Chemistry, 2012, 10(31): 6271-6274. |
| [10] | Liu X M, Zhao Q, Song W C, Bu X H. New highly selective colorimetric and ratiometric anion receptor for detecting fluoride ions[J]. Chemistry-A European Journal, 2012, 18(10): 2806-2811. |
| [11] | Ke I S, Myahkostupov M, Castellano F N, Gabbai F O P. Stibonium ions for the fluorescence turn-on sensing of F- in drinking water at parts per million concentrations[J]. Journal of the American Chemical Society, 2012, 134(37): 15309-15311. |
| [12] | Kubo Y, Kobayashi A, Ishida T, Misawa Y, James T D. Detection of anions using a fluorescent alizarin-phenylboronic acid ensemble[J]. Chemical Communications, 2005, (22): 2846-2848. |
| [13] | Koskela S J M, Fyles T M, James T D. A ditopic fluorescent sensor for potassium fluoride[J]. Chemical Communications, 2005, (7): 945-947. |
| [14] | Liu X Y, Bai D R, Wang S. Charge-transfer emission in nonplanar three-coordinate organoboron compounds for fluorescent sensing of fluoride[J]. Angewandte Chemie International Edition, 2006, 118(33): 5601-5604. |
| [15] | Kim T H, Swager T M. A Fluorescent Self-amplifying wavelength-responsive sensory polymer for fluoride ions[J]. Angewandte Chemie International Edition, 2003, 42(39): 4803-4806. |
| [16] | (a) Hu R, Feng J, Hu D, Wang S, Li S, Li Y, Yang G. A rapid aqueous fluoride ion sensor with dual output modes[J]. Angewandte Chemie International Edition, 2010, 49(29): 4915-4918. (b) Xiong L, Feng J, Hu R, Wang S, Li S, Li Y, Yang G. Sensing in 15 s for aqueous fluoride anion by water-insoluble fluorescent probe incorporating hydrogel[J]. Analytical Chemistry, 2013, 85(8): 4113-4119. |
| [17] | (a) Kim S Y, Park J, Koh M, Park S B, Hong J I. Fluorescent probe for detection of fluoride in water and bioimaging in A549 human lung carcinoma cells[J]. Chemical Communications, 2009, (31): 4735-4737. (b) Sokkalingam P, Lee C H. Highly sensitive fluorescence "turn-on" indicator for fluoride anion with remarkable selectivity in organic and aqueous media[J]. The Journal of Organic Chemistry, 2011, 76(10): 3820-3828. |
| [18] | Thomsen V, Schatzlein D, Mercuro D. Limits of detection in spectroscopy[J]. Spectroscopy, 2003, 18(12): 112-114. |




