2. 山西省化工设计院, 山西 太原 030024;
3. 山西省环境保护技术评估中心, 山西 太原 030024
2. Shanxi Provincial Chemical Design Institute, Taiyuan 030024, Shanxi, P. R. China;
3. Environmental Protection Technology Evaluation Center, Taiyuan 030024, Shanxi, P. R. China
近年来,阴离子在生命科学、药物领域、化学催化、环境科学等研究领域的重要作用已被逐渐认识,阴离子的识别已成为超分子化学研究的热点之一.比色法检测某些阴离子,因其操作简单、无需贵重仪器等优势,更是得到国内外化学工作者的高度重视[ 1,2,3,4 ].
F-是最小的阴离子且电负性强,具有特殊的化学性质,在生物学、医学、食品科学以及环境科学中都有重要的作用.人体缺乏氟时易发生龋齿,过量又会发生氟中毒,因此对氟的检测显得尤为重要,有关F-化学传感器的设计合成已引起众多研究者的兴趣[ 5,6,7,8,9,10,11 ].
10-羟基苯并喹啉羟基的对位易于偶氮化,可连接其它的基团而形成延伸共轭体系.因此本工作设计合成了7-(4-氯苯)偶氮-10-羟基苯并喹啉(化合物1),该化合物具有较大的π电子共轭体系,并且结构中含有生色团—CC—,助色团—HO,杂原子N、O,芳香族基团及—NN—双键,易发生分子内电荷转移(ICT)使其吸收光谱位于可见光区[ 12,13,14,15 ].实验结果表明合成的化合物1可以选择性识别氟离子,能使溶液颜色发生显著的变化,从而实现对氟离子的裸眼检测. 1实验部分 1.1仪器与试剂
UV-2450紫外-可见分光光度计(日本岛津);ZF-20D暗箱式紫外分析仪(巩义予华仪器厂);Bruker DRX-300核磁共振仪(瑞士);8300型红外光谱仪(岛津,日本).
苯胺、亚硝酸钠、氢氧化钠(分析纯,北京化工厂);二氧六环、苯、正己烷、氯仿、石油醚、乙腈(分析纯,天津天大试剂厂);四丁基醋酸铵和四丁基氯化铵(98%,TCI公司);四丁基溴化铵、四丁基碘化铵、四丁基氟化铵、四丁基硫酸氢铵(99%,J & K公司). 1.2 实验过程 1.2.1 化合物1的合成
合成路线如图1所示.
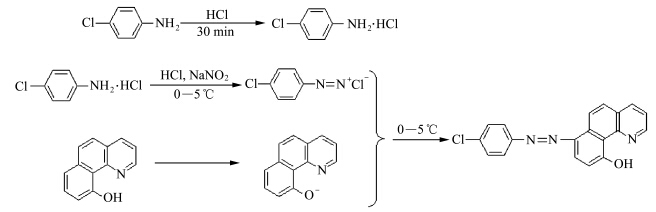 | 图1 化合物1的合成 Synthesis of compound 1 |
(1) 对氯苯胺盐酸盐的制备
将对氯苯胺2.0 g加入到5 mL蒸馏水和5 mL 37%的浓盐酸中,室温下搅拌30 min,过滤晶体并用乙醇洗3次,烘干,得1.98 g固体,产率74%.
(2) 重氮化
取对氯苯胺盐酸盐0.72 g在5 mL蒸馏水和5 mL 37%的浓盐酸中溶解,冷却到0—5 ℃(冰水浴),缓慢滴加NaNO2水溶液(0.5 g NaNO2溶于10 mL水中),至淀粉碘化钾试纸刚刚变蓝为止,维持0—5 ℃继续反应30 min.
(3) 偶联
取0.5 g的10-羟基苯并喹啉(HBQ),溶于10 mL蒸馏水和10 mL二氧六环的混合溶液中,保持0—5 ℃,体系用氢氧化钠调节至pH=8,剧烈搅拌下将HBQ溶液缓慢加入(2)的体系中,继续反应2—3 h;冰水浴中静置2 h,减压过滤,得橙色固体,依次用水、苯-正己烷(1∶10)洗涤,红外干燥,得粗品.
(4) 柱层析分离
氯仿-石油醚体系(3∶2)柱层析分离,经干燥后得重氮化目标产物0.48 g,产率59.5%.熔点为204—205 ℃.
1HNMR (300 MHz,CDCl3) ∶15.82 (s,1H),9.09 (d,1H),9.06 (d,1H),8.87 (d,1H),8.35 (t,1H),8.23 (d,1H),7.94 (d,2H),7.65 (d,2H),7.46 (d,2H). IR (KBr) : 3434.98,1620.09,1475.44cm -1. 1.2.2 实验部分
配置1.0×10-4mol/L化合物1的乙腈储备液.配置0.2 mol/L的四丁基铵盐的乙腈溶液.准确移取2.0 mL的化合物1储备液于比色杯中,并逐渐滴加不同体积的阴离子储备液,摇匀.然后进行紫外测定. 2结果与讨论 2.1 化合物1对F-的选择性识别作用
如图2(a)所示,在化合物1的乙腈溶液中,随着F-离子的加入,化合物1在390 nm处的吸收峰强度明显下降,在530 nm附近出现新的吸收峰,加入其它阴离子Cl-、Br-、I-、Ac-、HSO4-对化合物1的吸收光谱基本无明显影响.图2(b)插图为化合物1与不同阴离子作用的裸眼识别照片,由图可知化合物1在加入F-后溶液颜色由黄色变成红色,而加入其它阴离子则基本无颜色变化,说明化合物1对碱性较强的F-有选择性识别作用,而对其它阴离子基本上不识别,从而可以实现对F-的裸眼识别.
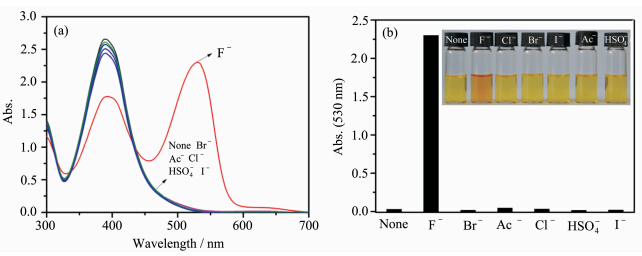 | 图2 (a) 阴离子对化合物1吸收光谱的影响 (b) 化合物1的乙腈溶液中加入不同阴离子后的吸光度及颜色变化 (a) Absorption spectra of 1 in the presence of anions (b) Absorption spectra and color changes of 1 upon addition of various anions in acetonitrile [ 1 ]=1.0×10-4 mol·L-1; [F-]=35 equiv. of 1 |
在乙腈溶液中,测定了不同浓度的氟离子对化合物1的紫外吸收光谱的影响.结果如图3(a)所示,随着氟离子浓度的增加,390 nm处的吸光度逐渐减小,530 nm处的吸光度逐渐增强,在435 nm出现1个等吸收点,表明化合物1与F-形成了确定化学计量比的配合物.图3a插图为化合物1与不同浓度F-的裸眼识别照片,随着F-浓度的不断增加,溶液颜色由黄色逐渐变橙最终变成红色.如图3(b)所示,体系的吸光强度A530nm/A390nm与[F-]在5.0×10-4 —3.0×10-3 mol/L的范围内呈线性关系(R=0.9824).由此可以实现化合物1在乙腈体系中对F-的定量检测.检测限为1.9×10-5 mol/L,在[F-]的检测浓度为3.0×10-3 mol/L时,5次重复测定的标准偏差为1.4%.
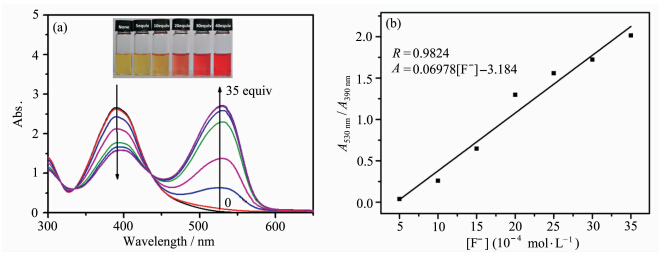 | 图3 (a) 不同浓度F-对化合物1紫外光谱的影响 (b) 化合物1对F-检测的线性图 (a) The absorption changes of compound 1 (100 μmol·L-1) with increasing concentrations of F-(0—35 equiv. of 1) (b) Linear graph of compound 1 with increasing concentrations of F- (0—35 equiv. of 1) |
主体化合物分子1与F-共存溶液显红色,当向其共存溶液中加入少量质子性溶剂甲醇后,溶液颜色由化合物1与F-共存时的红色变为黄色(图4),即化合物1本身的颜色,且吸收光谱恢复为化合物1本身的吸收光谱.这可能是由于甲醇加入后,甲醇分子与F-结合,破坏了主体化合物分子1与F-二者的共存体系
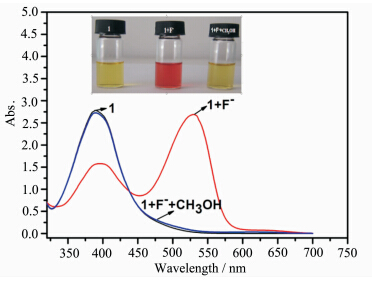 | 图4 化合物1与F-的体系中加入少量CH3OH的吸收光谱及颜色变化 Absorption spectra and color changes of 1 and F- upon addition of CH3OH |
为进一步阐明主体化合物1与F-间的氢键作用本质,作者进行了1HNMR(TMS)滴定实验,见图5,以DMSO-d6为溶剂,图5(a)中主体化合物1中的-OH质子化学位移为16.01.当加入35倍主体化合物1浓度的氟化四丁基铵盐后,如图5(b)中所示,—OH的质子峰消失,同时苯环上质子的化学位移向高场移动.因为F-的加入破坏了化合物1的分子内氢键,—OH的质子脱去,促进了主体化合物1分子内电荷转移,使得苯环上电荷密度增大,芳香质子的化学位移向高场移动.
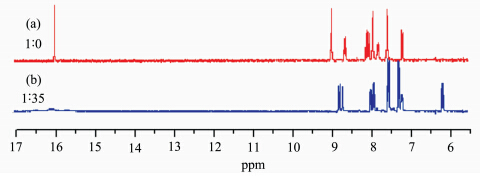 | 图5 DMSO-d6中主体化合物1及其在F-存在时的1HNMR谱 1HNMR spctra of receptor 1 and in the presence of F- in DMSO-d6 [F-]=35equiv. of 1 |
本文合成了一种对F-有选择性识别作用的化合物7-(4-氯苯)偶氮-10-羟基苯并喹啉.利用紫外-可见吸收光谱考察了其与F-、Cl-、Br-、I-、AcO-、HSO4-的作用.结果表明该化合物分子与F-形成稳定配合物.同时加入F-时,溶液立刻由黄色变为红色,而加入其它阴离子则无变化,从而实现了对F-的选择性识别.
| [1] | 周公度. 超分子结构化学[J]. 大学化学, 2002, 17(5): 1-12. Zhou G D, The structural chemistry of supramolecular[J]. University Chemistry, 2002, 17(5): 1-12. |
| [2] | Pietrangeli D, Ricciardi G. Synthesis of porphyrazines bearing thioalkylthiol tethers:useful building blocks for supramolecular chemistry[J]. Tetrahedron Letters, 2011, 52: 1105-1107. |
| [3] | 张来新, 杨琼, 赵卫星. 超分子化学研究的新进展[J]. 应用化工, 2010, 39(11): 1759-1765. Zhang L X, Yang Q, Zhao W X. Recent research progress of supramolecular chemistry[J]. Applied Chemical Industry, 2010, 39(11): 1759-1765. |
| [4] | Yu E, Alexeev B I, Kharisov T C, García H, Garnovskiia A D .Coordination motifs in modern supramolecular chemistry[J]. Coordination Chemistry Reviews, 2010, 254: 794-831. |
| [5] | Kim S H, Hwang I J, Gwon S Y, Burkinshaw S M, Son Y A. An anion sensor based on the displacement of 2,6-dichlorophenol-indo-o-cresol sodium salt from a water-soluble tetrasulfonated calix |
| [6] | arene[J]. Dyes and Pigments, 2011, 88: 84-87. |
| [7] | Kaur K, Kumar S. 1-Aminoanthracene-9,10-dione based chromogenic molecular sensors:effect of nature and number of nitrogen atoms on metal ion sensing behavior [J]. Tetrahedron, 2010,66: 6990-7000. |
| [8] | Shao J, Lin H , Cai Z S, Lin H K. A simple colorimetric and ON-OFF fluorescent chemosensor for biologically important anions based on amide moieties [J]. Journal of Photochemistry and Photobiology, 2009, 95: 1-5. |
| [9] | Lee S K, Kang J. A new macrocyclic anion receptor utilizing amide, amine, and 9-anthracenyl hydrogens[J]. Tetrahedron Letters, 2011, 52: 5192-5195. |
| [10] | Tavallali H, Rad G D, Parhami A, Abbasiyan E. A new application of bromopyrogallol red as a selective and sensitive competition assay for recognition and determination of acetate anion in DMSO/water media[J]. Dyes and Pigments, 2012, 94: 541-547. |
| [11] | 吴瑛, 张圣慈, 马洪坤. 香豆素衍生物对阴离子的识别特性[J]. 影像科学与光化学, 2012, 30(1): 43-52. Wu Y, Zhang S C, Ma H K, Coumarin derivatives of anion recognition characteristics[J]. Imaging Science and Photochemistry, 2012, 30(1): 43-52. |
| [12] | Liu Z H, Devaraj S, Yang C R, Yen Y P. A new selective chromogenic and fluorogenic sensor for citrate ion[J]. Sensors and Actuators, B. 2012, 174: 555-562. |
| [13] | Wang L L, Li B, Zhang L M, Li P, Jiang H. An optical anion chemosensor based on a europium complex and its molecular logic behavior[J]. Dyes and Pigments, 2013, 97: 26-31. |
| [14] | Gao W Z, Wang S R, Xiao Y, Li X G. Study on synthesis and properties of novel luminescent hole transporting materials based on N, N-di(p-tolyl)-N, N-diphenyl -1,10-biphenyl-4, 40-diamine core[J]. Dyes and Pigments, 2013, 97: 92-99. |
| [15] | Helal A, Kim H S. Carbazole incorporated ratiometric chemosensor for Zn2+[J]. Spectrochim. Acta, Part A,2013, 105: 273-279. |
| [16] | Wen X H, Tan F, Jing Z J, Liu Z Y. Preparation and study the 1:2 inclusion complex of carvedilol with β-cyclodextrin[J]. Journal of Pharmaceutical and Biomedical Analysis, 2004, 34: 517-523. |




