光致变色(Phtochromism)[1]是指一个化合物在某一波长光的照射下,发生了特定的化学变化转变成另一种状态,在这个过程中,引起了化合物吸收光谱的变化,而在加热或另一波长光的照射下,又恢复到起始状态(图1)。光致变色材料以光作为调控手段,已在光信息存储、光开关材料、光学器件、光信息基因材料等方面得到了成功应用[2]。
 | 图1 光致变色反应过程中紫外-可见吸收光谱的变化 Absorption spectral change in the photochromic process |
在光致变色化合物中,二芳乙烯是一类热不可逆的光致变色材料,其光致变色异构体对热稳定,只有在不同波长光的照射下才能发生可逆的开关环反应。二芳乙烯的光致变色现象最早由日本化学家Irie报道[3],从此揭开了二芳乙烯化合物的研究热潮。二芳乙烯类光致变色反应的机制是光环化反应,即二芳乙烯分子的开环态在光照 的条件下,发生顺旋关环反应,生成共轭体系增大的闭环化合物(图2)。由于共轭体系增大,使得二芳乙烯的最大吸收峰从紫外区红移至可见区。在可见光照射下,通常有色的闭环态可恢复到无色或浅色的开环态。二芳乙烯化合物因本身所具有的响应时间快、热稳定性好、抗疲劳性强等优点,越来越受到研究者的重视。二芳乙烯化合物的光开关功能及其他特性可以通过适当的结构修饰进行调控,主要有两种手段:(1)在乙烯基的两端引入不同的取代基或镶嵌不同的杂环;(2)在芳基的一端或两端进行修饰,连接不同的功能基团,引进诸如磁性、荧光、探针、液晶等功能,并通过光开关环化反应进行调控。
 | 图2 二芳乙烯类化合物光致变色过程示意图 The structural change of diarylethenein the photochromic process |
荧光探针是一类以荧光信号为输出信息且能够特异性识别目标分子的荧光材料[4]。荧光检测技术相对于其它检测技术具有成本低、灵敏度高、选择性强、操作方便等优点,在环境、生物、化工、医药等众多领域都有着广泛的应用[5]。近年来,荧光探针在疾病诊断方面的应用也越来越受到人们的关注。具有可调控能力的荧光材料成为当下研究的热点。通过在荧光探针分子中引入对荧光可以进行调控的基团(如二芳乙烯)起到荧光开关的作用,这在信息的输入、输出和存储中有着重要的应用。
荧光开关是荧光可以被外界刺激所调控的分子,在二芳乙烯分子的端基或者环上连接荧光基团,当荧光基团的发射光谱与光开关前后的一种状态的吸收光谱发生能级匹配时,光开关的同时就会产生荧光的变化,用此机理可以有效地构筑荧光开关。在通常的二芳乙烯体系中,开环态通常具有强荧光,即荧光信号处于ON的状态,而关环态具有弱荧光,即荧光信号处于OFF状态。荧光开关还可以与其他识别基团相连构筑具有识别功能的荧光探针开关分子,用于特定靶标分子的识别和跟踪。目前的荧光开关分子在应用上主要存在两个问题:(1)用于开关环反应的激发波长往往与开环态荧光激发的波长非常接近,导致在荧光信号读出的过程中,开环态分子已经变成了关环态分子而导致荧光的猝灭,不利于信息的存储和读取;(2)荧光开关及探针最期待的应用是在生物检测和成像领域,这就需要克服目前荧光开关材料生物相容性差等问题。
在过去的10年中,作者课题组在二芳乙烯荧光开关体系的研究方面做了较为系统的工作,为解决荧光开关的非破坏性读出,及荧光开关在生物成像方面的应用等问题,发展了新的荧光开关体系,本文主要针对这几年的研究成果和进展进行简要的综述。
1 具有非破坏性读出能力的二芳乙烯荧光开关材料我们通过分子间超分子相互作用及不同组分间的能量传递,将荧光开关的荧光激发波长移至可见区和近红外区,获得了具有非破坏性读出能力的凝胶开关材料和杂化纳米材料。
1.1 二芳乙烯凝胶开关材料在超分子自组装领域,有机小分子凝胶的研究引起人们广泛的兴趣,并且于近年得到了很大的发展,主要应用于药物释放[6, 7]、传感[8]、纳米材料的模板试剂[9,10,11]等。在凝胶体系中,分子间通过非共价键的聚集组装会导致荧光强度和波长的位移,起到荧光调控的作用[12]。由于二芳乙烯分子含有平行、反平行两种构象,并且都是扭曲的柔性结构,分子间作用的空间位阻较大,通常难以形成稳定的有机凝胶。荷兰的Feringa课题组利用手性酰胺基团首次获得了含二芳乙烯的凝胶材料,在溶胶、凝胶状态均能进行光致变色[13, 14],并且在凝胶状态下呈现Cotton效应,但这类化合物没有荧光性质。田禾教授课题组制备了基于胆甾和萘酐荧光基团的光致变色凝胶因子[15],该化合物在溶胶状态下有强的荧光,但凝胶状态下的荧光较弱,且光致变色前后荧光强度变化不大。
我们通过大量的尝试,利用二酰胺环己烷通过长烷基链与二芳乙烯吡啶正盐连接,构筑了一类凝胶能力较强的二芳烯化合物(图3)[16]。其中二酰胺环己烷之间可通过强烈的互补双氢键作用产生有序排列,而长烷基链的引入减少了二芳乙烯基团的空间位阻。凝胶测试结果表明,单边连接二芳乙烯的化合物1能够交联多种有机溶剂,尤其以乙腈、丙酮的效果最佳,并且放置一个星期凝胶的外观没有发现任何变化。而双边连接二芳乙烯的化合物2的凝胶稳定性远远不如化合物1,可能源于吡啶正盐间的电荷排斥作用减弱了化合物的有序排列。化合物 1 不仅可以在凝胶中实现良好的荧光开关,并且也有效地实现了荧光的非破坏性激发(图4)。
 | 图3 化合物1和2的结构 The structure of compounds 1 and 2 |
 | 图4 化合物1 的光致变色:(A)可逆光环化反应,(B)对应的荧光开关成像图,365光照射下(C)吸收和(D)荧光光谱变化 Photochromism of compound 1 :(A) reversible photo cyclization process upon irradiation, (B) the related fluorescent images of open and closed form,(C) the related absorption and (D)emission spectral change |
通过实验发现,化合物1的荧光光谱具有浓度依赖行为,随着浓度的增加,虽然吸收光谱没有显著的变化,但荧光激发光谱的最大峰值却从稀溶液的370nm逐渐红移至凝胶的470nm,荧光发射波长也红移了近20nm(图5)。化合物1在乙腈溶液和凝胶状态都具有良好的光致变色性能,在365和620nm光的交替照射下,可以实现颜色的变化和荧光开关功能。开环态的发射波长由稀溶液中的605nm,红移至623nm。在365nm紫外光使之关环后,发生分子内的能量转移荧光被有效猝灭(96%被猝灭)。由于凝胶状态下最佳的荧光激发波长在470nm附近,远离365nm的关环波长,对于实现荧光的非破坏性读出非常有利。如图5C,用470nm光分别照射开环态和光稳态的化合物一个小时,可见区的吸收基本上没有变化,可以有效地在凝胶状态下实现荧光信号的非破坏性读出。因此,采用365 nm紫外光进行 信息写入;470 nm光对化合物 1的橙红色荧光进行读出;620nm的可见光能够有效地将信息擦除,再用365nm光记录信息,实现了一个可写-读-擦多次循环的信息存储体系。
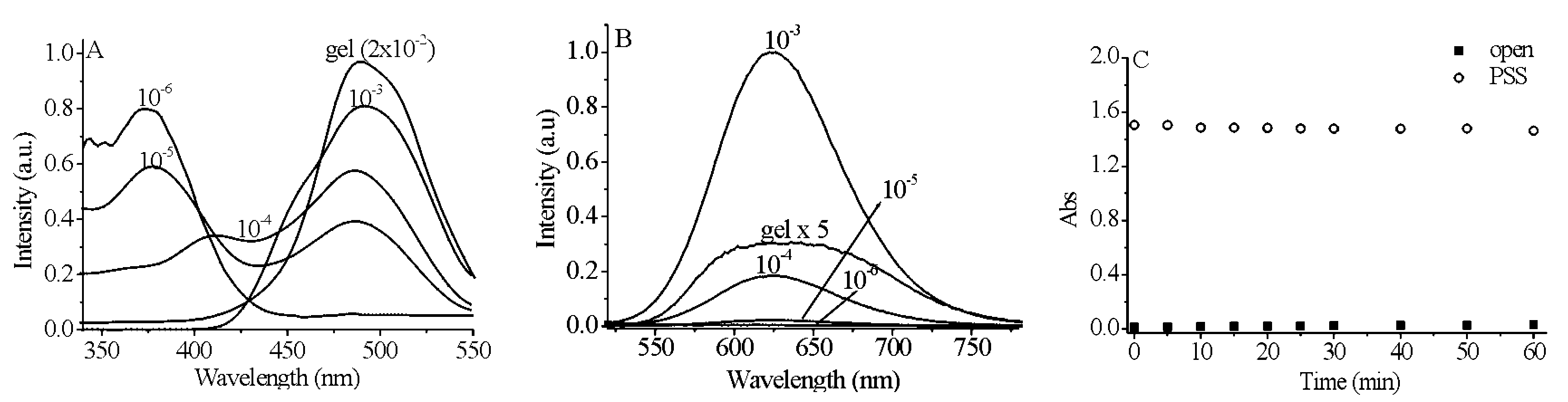 | 图5 (A)化合物 1 不同浓度的荧光激发光谱(Em:620 nm);(B)化合物 1 在乙腈中不同浓度的发射光谱(Ex:470 nm); (C)化合物 1 开环态及光稳态在470 nm光照下620 nm处的吸收随时间的变化 (A) Concentration-dependent excitation (Em: 620 nm) and (B)Emission spectra of 1 ; (C)Absorption change of open state and PSS of 1 at 620 nm under 470 nm irradiation |
在以上研究工作基础上,我们进一步将单组份的光致变色凝胶体系扩展至多组份多功能的超分子体系[17],利用荧光生色团萘酰亚胺与三聚氰胺基团强烈的三氢键作用,设计合成了带萘酰亚胺基团的凝胶因子( 3 )和接三聚氰胺基团的二芳乙烯(DTE),两者所形成的自组装体系在紫外光和可见光的照射下不仅呈现出荧光的可逆变化,同时产生形貌和表面亲疏水性的变化。
实验发现,化合物 3 可在多种非质子溶剂中形成稳定的凝胶,其中在乙酸乙酯中的成胶浓度可以低到8.5 mg·mL-1。当向化合物3形成的凝胶中加入DTE后,两者之间通过氢键形成配合物,配合物的溶解度有了较大的提高,可在乙酸乙酯中形成半凝胶。我们通过核磁滴定分析和红外光谱对化合物 3 和 DTE的自组装形式进行了研究,验证了分子3和DTE之间通过形成三氢键形成如示意图6中的自组装模式。通过荧光共聚焦显微镜(CLSM)和SEM对化合物 3 在 DTE 加入 前后的凝胶样品形貌进行观察,发现加入 DTE后,凝胶 3 的形貌结构由块状变为带有小孔的薄膜状结构,当用365 nm的紫外灯照射后,该薄膜状结构转变为不规则的片状结构(图7)。这说明光照在化合物 3 和 DTE 自组装形成的配合物的形貌调节中起着关键作用。
 | 图6 化合物 3 与 DTE 自组装及光致变色示意图 Chemical structure and photochromic process of 3+DTE |
 | 图7 (a-c) 化合物 3及3+DTE 在乙酸乙酯中的SEM 图以及 3及3+DTE 紫外光照后的SEM图(标尺分别为5、10和2 μm);(d,e) 化合物 3及3+DTE 的薄膜在光照前后的水接触角;(f) 3及3+DTE 的荧光强度随紫外光和可见光交替照射后的变化 (a-c) SEM images of gels of 3 and 3+DTE from ethyl acetate before and after 365 nm light irradiation (scale bar: 5,10and 2 μm,respectively,from left to right); (d,e) water contact angle of 3+DTE before and after 365 nm light irradiation; (f) the fluorescence changes under alternating UV/Vis light irradiation |
我们也对化合物 3和DTE 自组装形成的配合物进行了荧光开关实验。用紫外光照射后,3及3+DTE 在500 nm左右的吸收逐渐增强,达到光稳态之后,80%的荧光得到猝灭。进行了7次光循环之后,依然保留着原来80%的荧光强度,说明了化合物 DTE具有良好的抗疲劳性。同时,由于光照前后化合物膜的表面形貌和粗糙度发生了变化,因而其薄膜的水接触角和疏水性在光照后也明显增大,可以构筑荧光和表面性质变化的双通道开关。
1.2 基于有机纳米粒子的荧光非破坏性读出在自组装功能材料的诸多应用中,强荧光材料是一个广受人们关注的领域。虽然现今已开发出众多的强荧光物质,但它们的荧光往往仅限于稀溶液中,在固态下会浓度猝灭。为了解决浓度猝灭问题,有几个课题组设计了结构新颖的聚集态荧光增强材料[18,19,20,21,22,23,24,25]。二芳乙烯由于具有较快的响应时间和良好的抗疲劳性,在调控荧光性能方面得到了大量的应用,但在固态荧光调控方面的报道则很少见。本课题组2007年报道了利用分子间氢键形成的自主装体系调控聚集态荧光行为的研究[26]。我们设计合成了带有吡啶基的二芳乙烯分子( 4 )和带有羧基的化合物( TDBA,BF2 )(图8),通过氢键自组装,研究了这些自组装体系的光化学和光物理特性。
 | 图8 自组装示意图 The process of the self-assemblies |
化合物4本身荧光比较弱,与羧酸形成自组装体系后荧光明显增强。我们采用共沉淀法,在水和四氢呋喃的混合溶剂中制备了摩尔比为1∶2的 4-TDBA 的纳米粒子,平均粒径为200 nm,该纳米粒子在开环态的吸收峰位于276 nm,相对于溶液中有6 nm的红移;但在335 nm处有一明显的肩峰,比溶液中红移了18 nm,并且峰形明显宽化。用365 nm的光照至光稳定态后,闭环态的最大吸收峰位为580 nm,由溶液中的紫红色变为蓝色,相对于稀溶液中红移了20nm。在纳米粒子中,荧光的变化更为显著,开环态纳米粒子的荧光发射位于47 nm,相对于稀溶液红移了55nm,使其荧光的发射和闭环态的吸收在能量上能够很好匹配,构成了良好的荧光开关,且能循环多次(图9A),但在溶液状态下,由于能量不匹配,荧光开关不明显。该纳米分散体系具有很好的成膜性,在固态膜中的荧光和光致变色现象与纳米粒子呈现出类似的特性(图9B)。
 | 图9 (A) 4-TDBA 溶液及纳米粒子光致变色中的荧光变化; (B) 4-TDBA 纳米膜的光致变色及荧光开关行为(插图为分别用紫外365 nm和可见光580 nm循环照射的荧光变化); (C)固态 BF2和4-BF2 纳米粒子的吸收和荧光光谱;(D) 4-BF2 纳米粒子的荧光开关行为 (A) Fluorescent spectra of 4-TDBA in THF solution and the nano particles suspended in THF water; (B) Absorption (red line) and fluorescent (black line) spectral changes of solid film of 4-TDBA upon irradiation of 365 nm light. Inset: Fluorescence switch cycles upon alternating irradiation of UV and visible light; (C) Individual absorption and emission spectra in solid film; a.emission of 4 (Ex 365 nm),b.absorption of 4-BF2 ,c. emission of 4-BF2 (Ex 365 nm),d.emission of BF2 (Ex 480 nm); (D) Fluorescent changes of 4-BF2 during photochromism process (Ex: 365 nm; inset: Ex under 480 nm and switched under 365 nm) |
为进一步将激发波长移至可见区,构建非破坏性读出的荧光开关材料,选择了发射在红光区 域的硼氟化合物 BF2 作为客体荧光分子构筑了4-BF2 纳米粒子,硼氟化合物具有荧光发射强,发射波长可调和斯托克位移小等优势,但该类荧光化合物的一个缺点是固态下显著的荧光猝灭行为,我们利用形成主客体的有机纳米复合物,有效抑制了 BF2 在高浓度下的猝灭。如图9C可见,纳米复合物的荧光位于610 nm处,与纯固态的 BF2 染料相比蓝移了60 nm,且荧光强度显著提高,同时因其最大吸收波长位于480 nm,可以用480 nm作为荧光的读出光源,用365 nm进行光致变色(写入)(图9D),600 nm进行回复(擦除),有效地实现了荧光信息的非破坏性读出,构筑了具有非破坏读出能力的有机纳米荧光开关材料。
1.3 基于杂化纳米粒子的非破坏性读出为进一步将激发波长移至近红外区,提高荧光非破坏性读出的稳定性,我们成功地将稀土上转换纳米粒子引入荧光开关体系,构筑了近红外激发的荧光开关材料。上转换稀土纳米晶(UCNP)具有反斯托克位移的特点,在980 nm激光泵浦下可以同时吸收两个或多个近红外区低能量光子并转化为可见区的发射[27],有望实现从UCNP到二芳烯的能量转移。为此,我们将稀土纳米晶(LaF3:Yb,Ho;NaYF4:Yb,Er)掺杂到具有光致变色性能的米基硼-二芳乙烯(化合物 5 )的聚合物薄膜中,利用分子之间的能量转移实现了近红外激发的非破坏性上转换荧光开关(图10)[28]。
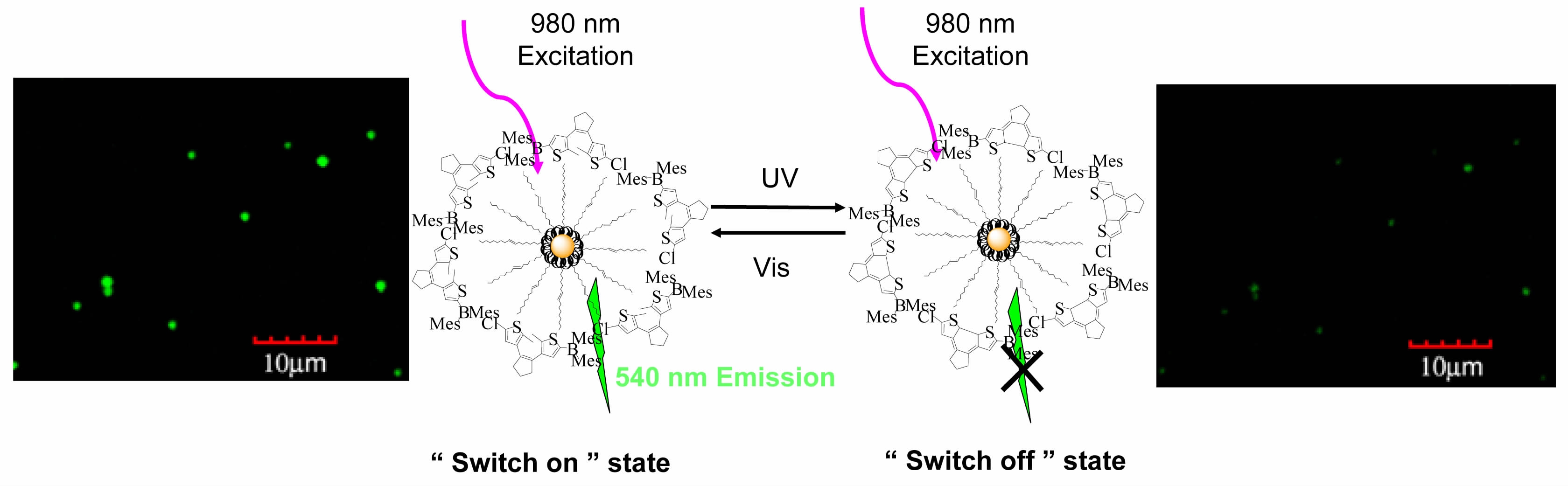 | 图10 上转换荧光开关原理示意图Principle of the up-conversion luminescent switch |
在开环状态下,二噻吩乙烯的吸收光谱与UCNP的荧光发射没有重叠,因此呈现典型的UCNP的上转换荧光发射,此时荧光开关处于“On”的状态,而在关环状态下,二噻吩乙烯的吸收与UCNP的荧光发射具有明显的光谱重叠(图11),因此,UCNP的荧光发射被猝灭,此时荧光开关处于“Off”的状态,荧光信号可以用980 nm进行读出,该过程可以多次反复,而且用980 nm分别照射开环态和关环态样品50h,其荧光光谱基本没有变化,说明该体系具有很好的光稳定性。
 | 图11 (A)杂化纳米晶 5 /LaF3: Yb、Ho在PMMA薄膜中365 nm光照前后的吸收光谱及980 nm 激发后开环态的荧光光谱(插图为近红外激发上转换发光);(B)杂化纳米晶的非破坏性读出行为及980 nm照射后的光稳定性 (A) UV-visible absorption spectra of -loaded PMMA film before (dash line) and after (solid line) irradiation with 365 nm light for 30 min,and the normalized up-conversion luminescence spectra of the prepared film (dotted line,λex= 980 nm). Inset shows the image of the up-conversion emission;(B)Nondestructive readout capability of the film in the open state ( □ ) and PSS state ( ■ ),λex=980 nm. Inset graph shows the modulated up-conversion luminescence intensity at 540 nm of the film during alternating UV and visible light irradiation |
二芳乙烯对光有响应能力,在光的照射下可发生开关环变化,从而实现对光学性质的调控,如果在二芳乙烯分子引入其他刺激响应基团,例如其他的光响应基团或化学响应基团,则可以实现多响应的分子开关。
2005年,本课题组报道了连有香豆素的二芳乙烯分子对光的响应行为(图12)[29]。众所周知,香豆素也是一种常见的对光敏感的基团,它可以在光的照射下发生单体的聚合,主要以二聚的形式存在[30,31,32]。但香豆素对光的响应需要在Lewis酸的催化下才能进行,因此,可以独立地对单个香豆素或二芳乙烯光响应基团进行调控。在不加入Lewis酸的情况下,用365 nm和620 nm的光进行交替照射,可以实现二芳乙烯单元的开关环。当加入Lewis酸后,在紫外光的照射下,香豆素发生单体的聚合,聚合对吸收光谱和荧光光谱都有一定程度的影响,对荧光的影响尤为显著。
 | 图12 化合物 6o 对外部刺激的响应过程 Four states of compound 6o responding to external stimuli |
通过1HNMR以及ESI-Mass,证实了该体系中的香豆素基团在光照后主要以三聚体的形式存在。香豆素聚合之后,解离成单体的过程相当困难,需要在小于300 nm的光长时间照射,才能回到单体状态。香豆素和二芳乙烯分子对光的响应过程可归纳为图12中的4个状态,即开环态单体、闭环态单体、开环态三聚体和闭环态三聚体。各种状态的转换除吸收光谱变化外,荧光光谱也发生了很大的变化。开环态 6o 明显有两个荧光发射峰,分别位于488 nm及380 nm处,对应于二芳乙烯单元和香豆素基团的发射。在香豆素单体态,由于分子内的能量转移过程,紫外光照使二芳乙烯的荧光部分猝灭。加入Lewis酸光照使香豆素二聚后,在405 nm处出现香豆素聚合物的荧光。在620 nm光的照射下,二芳乙烯开环,488 nm处二芳烯的荧光又增强。这样我们通过两个光开关基团的结合,构筑了多级开关响应的荧光开关体系。
通过连接对质子或离子响应的基团,也可以实现对pH或离子的选择性响应。为了实现对pH值的响应,我们将带有咪唑基邻菲啰啉基团引入二芳乙烯化合物(化合物 7和8 ,图13)[33]。咪唑基上的N—H是比较活泼的基团,在碱的作用下可以脱质子。通过核磁滴定实验,证实加入碱之后发生了脱质子,使得π体系的电子离域程度增加,邻菲罗啉上各质子的化学环境更趋向于一致,这些变化在吸收和荧光光谱上得到了体现。随着碱的加入,荧光强度逐渐降低,吸收峰蓝移。由于对光和酸碱都有响应,于是就构成了对酸碱和光响应的多响应分子开关(图14)。
 | 图13 化合物 7和8 的结构 Structure of compounds 7 and 8 |
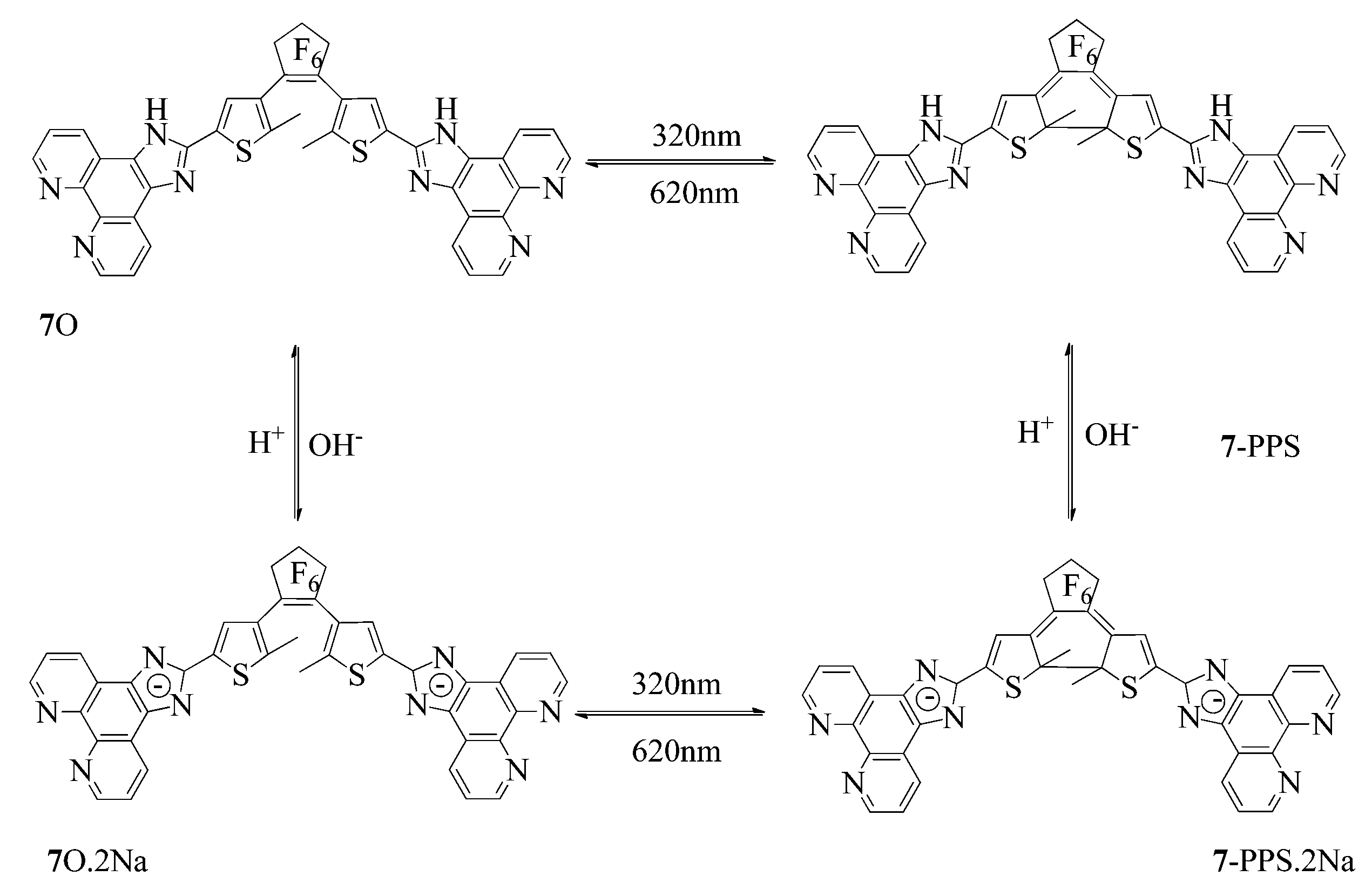 | 图14 多响应分子开光示意图 The four states of 7 upon photochromism and deprotonation |
化合物 8和7 类似,都能对酸碱和光有响应,稍有不同的是,化合物 8 在碱的作用下,对荧光的猝灭比化合物 7 更显著,由此,我们利用光和酸碱作为输入信号,以荧光变化作为输出信号,建立了逻辑门。
2006年,本课题组成功地将具有光致变色性能的二噻吩乙烯和具有氟离子响应的米基硼单元连接在了一起,合成了米基硼-二噻吩乙烯的衍生物 BTE-1B [34]。 BTE-1B 不仅具有优良的光致变色性能,而且对氟离子有特异性响应,氟离子的存在同时影响其光致变色的性能。当 BTE-1B 处于开环态时,在氟离子的作用下340 nm处的吸收峰消失,当用紫外光照至光稳态时,氟离子的加入使最大吸收峰由560 nm蓝移到490 nm,颜色由蓝色变为黄色(图15)。通过实验发现,该化合物对氟离子具有较高的选择性。
 | 图15 氟离子对 BTE-1B 光致变色性能的调控示意图 Photochromic property of BTE-1B modulated by a fluoride ion |
荧光成像作为一种重要的生物监测手段在生物领域得到了广泛的研究,并取得了很好的效果[35]。目前,用于荧光成像的材料主要包括荧光蛋白[36]、纳米发光材料[37]、有机小分子染料[38]等。在有机小分子染料中,主要的荧光基团有罗丹明类[39]、花菁类[40]等。但是这些染料分子也有一定的局限性,例如小分子有机染料的光稳定性一直是成像研究的主要障碍;绿色荧光蛋白也存在生物背景噪音干扰等问题。利用光稳定性好的响应材料作为生物成像的探针材料不仅能够克服光漂白性和生物体系的噪音干扰,同时通过引入适当的靶向基团可以实现对特定生物分子或生理过程的动态跟踪。
二芳乙烯类的衍生物在生物方面的应用研究较少,主要是由于其生物相容性和水中的荧光猝灭问题。Irie课题组在2007年首次将生物分子基团和荧光团同时引入二芳乙烯的两端,实现了生物分子的体外荧光标记[41]。之后,本课题组将亲水的醚链和疏水的烷基链连接到二芳烯分子两端(化合物 9 ,图16),通过分子间的超分子组装作用解决了二芳乙烯分子的亲水性和生物相容性的问题,实现了二芳乙烯化合物的细胞成像[42]。 化合物 9 具有两亲性分子的特点,在水中可以自组装形成分散性良好的囊泡,使荧光基团吡啶正盐镶嵌于疏水的长烷基链中,避免了荧光在水中的猝灭,实验证明,该化合物在水体系中的荧光强度显著高于在有机溶剂甲醇中的荧光强度,且该化合物在水中有显著的荧光开关行为。通过对化合物 9 的细胞毒性试验证实其具有较低的细胞毒性,能作为荧光探针用于生物成像。
 | 图16 化合物 9 的光致变色过程及在水中的自组装 Structure,photochromism and self-assembly process of 9 |
化合物 9 能够进入细胞胞浆并在细胞体内实现荧光开关。而且在405 nm和633 nm光的交替照射下,可以实现多次开关环的循环,显示了二芳乙烯分子良好的抗疲劳性和光稳定性(图17)。之后,Branda课题组将二芳乙烯的吡啶盐作用于蠕虫,在蠕虫的活体内实现了光致变色和荧光开关[43]。
 | 图17 化合物 9o (20 μmol/L PBS溶液)在25 ℃孵育KB细胞20 min后的共聚焦荧光(A~D)和相应荧光、明场叠加图像(E~H) (A)初始成像图;(B)选中细胞用405 nm光照3 min,功率为2 mW;(C)所有细胞用405 nm光照3 min;(D)用633 nm光照1 h CLSM image (above) and the overlay image (bottom) of KB living cells incubated with 9o for 20 min at 25 ℃ (A) original state,(B) irradiated by 405 nm light (2 mW) for a single cell,(C) all cells,and (D) recovered by 633 nm light |
在此基础上,我们对二芳乙烯分子在生物领域方面的应用进行了深入的研究,希望在生物静态成像的基础上,通过对二芳乙烯分子的设计实现光可控生理过程的动态捕捉。我们将三联吡啶引入到二芳乙烯分子中设计合成了化合物 10 (图18)[44]。其中三联吡啶是一种很好的金属配体,尤其是对金属铜离子和锌离子有着良好的配位能 力[45],当二芳乙烯分子的两端连有三联吡啶与金 属离子形成配合物时,可以通过二芳乙烯开关功能对其配合物的性质进行调控[46, 47]。在该分子中,二芳乙烯单元能在紫外光和可见光的照射下实现开关环,紫外光照射达到光稳态后,95%的荧光被猝灭。除了对光的效应外,化合物 10o 对金属锌离子也有很强的响应能力,三联吡啶部分可以与金属锌离子进行配位,配位后荧光减弱,然后在EDTA的作用下,荧光又得到恢复。其光致变色和离子识别过程如图18所示。
 | 图18 化合物 10 的结构变化 Chemical structure changes of compound 10 |
我们进一步通过共聚焦荧光成像记录了锌离子被转运进入细胞的过程(图19),并利用荧光强度的变化直观、定性地反映了转运的动态过程,这为检测金属离子的跨膜运输提供了可视工具。化合物 10o 作为双控荧光开关探针,不仅自身荧光可逆,对特定刺激也有响应,在可视化生物过程中有潜在的应用前景。
 | 图19 用化合物 10o (10 μmol/L PBS/DMSO,100:2,v/v)在25 ℃孵育20 min后KB细胞共聚焦图像 (A、F)细胞明场图;(B)细胞明场(A)和荧光(C)成像叠加图;(C)初始成像图;(D)选中细胞用405 nm光照3 min,功率为2 mW; (E)选中细胞用633 nm光照40 min,功率为0.7 mW;(G)初始成像图;(H)加入Zn2+溶液50 μmol/L;(I)加入Zn2+溶液100 μmol/L; (I)加入EDTA溶液500 μmol/L;(K)、(L)、(M)、(N)分别为对应(G)、(H)、(I)、(J)的荧光强度分布 CLSM images of KB cells incubated with 10o for 20 min at 25℃(1×10-5 mol/L in PBS/ DMSO,100∶2,v/v) (A,F) Brightfield image of KB cells. (B) Overlay image of A and C.Confocal fluorescence image of (C) original state, (D) irradiated by 405 nm light (2 mW,3 min) for one selected cell and (E) recovered by 633 nm light (0.7 mW,40 min). Confocal fluorescence image of (G) original state of F,and incubation by Zn2+solution with the concentrations of (H) 5×10-5mol/L,(I) 1×10-4 mol/L. (J) Recovered by 5×10-4 mol/L EDTA solution. (K),(L),(M),(N) were the distribution of fluorescence intensity of (G),(H),(I),(J),respectively |
二芳乙烯作为一种经典的光致变色化合物,是一种非常有价值的功能材料。虽然从光致变色现象的发现至今已有100多年的历史,但对于二芳乙烯化合物的研究以及应用才刚刚开始。二芳乙烯类化合物已经被证实在分子开关、信息存储、防伪等方面具有巨大的应用潜能[48],在生物领域方面,二芳乙烯分子的应用还相对较少,鉴于二芳乙烯类化合物卓越的抗疲劳性能和良好的荧光开关行为,通过合理的分子设计和化学修饰,该类化合物预期将在生物检测、生理过程跟踪及生物存储等方面获得广泛的应用。
致谢: 以上研究得到了国家973项目(2013CB733700)、国家自然科学基金项目(21125104,91022021,51373039)、教育部博士点优先发展计划(20120071130008)、上海市优秀学术带头人计划(12XD1405900)的资助,在此表示感谢!| [1] | Irie M. Diarylethenes for memories and switches[J]. Chemical Reviews,2000,100(5): 1685-1716. |
| [2] | Tian H,Yang S J, Recent progresses on diarylethene based photochromic Switches [J]. Chemical Society Reviews, 2004, 33(2): 85-97. |
| [3] | Irie M, Mohri M, Thermally irreversible photochromic systems. Reversible photocyclization of diarylethene derivatives [J]. The Journal of Organic Chemistry,1988, 53(4): 803-808. |
| [4] | Vendrell M, Zhai D, Er J C,et al. Combinatorial strategies in fluorescent probe development [J]. Chemical Reviews,2012,112(8): 4391-4420. |
| [5] | Kobayashi H, Ogawa M, Alford R, et al. New strategies for fluorescent probe design in medical diagnostic imaging [J]. Chemical Reviews,2010, 110(3): 2620-2640. |
| [6] | Dai H, Chen Q, Qin H,et al. Temperature-responsive copolymer hydrogel in controlled drug delivery [J]. Macromolecules,2006,39(19): 6584-6589. |
| [7] | Ramanan R M K, Chellamuthu P, Tang L,et al. Development of a temperature-sensitive composite hydrogel for drug delivery applications [J]. Biotechnology Progress,2006,22(1): 118-125. |
| [8] | Li S, John V T, Irvin, G C, Rachakonda, S H, McPherson G L,et al. Synthesis and magnetic properties of a novel ferrite organogel [J]. Journal of Applied Physics,1999,85(8): 5965-5967. |
| [9] | Jung J H, Ono Y, Shinkai S. Sol-gel polycondensation in a cyclohexane-based organogel system in helical silica: creation of both right- and left-handed silica structures by helical organogel fibers [J]. Chemistry - A European Journal,2000,6(24): 4552-4557. |
| [10] | Kobayashi S, Hanabusa K, Hamasaki N, et al. Preparation of TiO2 hollow-fibers using supramolecular assemblies [J]. Chemistry of Materials,2000,12(24): 1523-1525. |
| [11] | Kobayashi S, Hamasahi N, Suzuki M,et al. Preparation of helical transition-metal oxide tubes using organogelators as structure-directing agents [J]. Journal of the American Chemical Society, 2002, 124(23): 6550-6551. |
| [12] | (a)Yang H, Yi T, Zhou, Z,et al. Switchable fluorescent organogels and mesomorphic superstructure based on naphthalene derivatives [J].Langmuir, 2007, 23(15): 8224-8230. (b) Shu T, Wu J, Lu M,et al.Tunable red-green-blue fluorescent organogels on the basis of intermolecular energy transfer [J].Journal of Materials Chemistry, 2008, 18(8): 886-893. |
| [13] | (a) De J J J D, Lucas L N, Kellogg R M,et al.Reversible optical transcription of supramolecular chirality into molecular chirality [J]. Science,2004,304(5668): 278-281. (b) De J J J D, Hania P R, Pugzlys A,et al, Light-driven dynamic pattern formation [J]. Angewandte Chemie International Edition,2005,44(16): 2373-2376. |
| [14] | De J J J D, Tiemersma-Wegman T D, Van E J H,et al. Dynamic chiral selection and amplification using photoresponsive organogelators [J]. Journal of the American Chemical Society,2005,127(40): 13804-13805. |
| [15] | Wang S, Shen W, FengY, Tian H. A multiple switching bisthienylethene and its photochromic fluorescent organogelator [J]. Chemical Communications,2006, 1497-1499. |
| [16] | Xiao S, Zou Y, Yu M,et al. A photochromic fluorescent switch in an organogel system with nondestructive readout ability [J].Chemical Communications, 2007, 4758-4760. |
| [17] | Cao X, Zhou J, Zou Y,et al. Fluorescence and morphology modulation in a photochromic diarylethene self-assembly system [J]. Langmuir,2011,27(8): 5090-5097. |
| [18] | Deans R, Kim J, Machacek M R,et al. A poly(p-phenyleneethynylene) with a highly emissive aggregated phase [J]. Journal of the American Chemical Society,2000,122(35): 8565-8566. |
| [19] | Precup-Blaga F S, Garcia-Martinez J C, Schenning A P H J,et al. Highly emissive supramolecular oligo(p-phenylene vinylene) dendrimers [J]. Journal of the American Chemical Society,2003,125(42): 12953-12960. |
| [20] | Mutai T, Satou H, Araki K. Reproducible on-off switching of solid-state luminescence by controlling molecular packing through heat-mode interconversion [J]. Nature Materials,2005,4(9): 685-687. |
| [21] | Kishimura A, Yamashita T, Yamaguchi K, et al. Rewritable phosphorescent paper by the control of competing kinetic and thermodynamic self-assembling events[J]. Nature Materials,2005,4(7):546-549. |
| [22] | Hulvat J F,Sofos M,Tajima K,et al. Self-assembly and luminescence of oligo(p-phenylene vinylene) amphiphiles[J]. Journal of the American Chemical Society,2005,127(1):366-372. |
| [23] | Lim S J,An B K,Jung S D,et al.Photochromism: photoswitchable organic nanoparticles and a polymer film employing multifunctional molecules with enhanced fluorescence emission and bistable photochromism[J]. Angewandte Chemie International Edition,2004,43(46):6346-6350. |
| [24] | Sheikh-Ali B M, Weiss R G. Effects of aggregation and mesomorphic order on the photophysical properties of 4-alkyl-n-(p-cyanophenyl)piperidines. Molecules capable of forming intramolecular charge transfer states[J].Journal of the American Chemical Society,1994,116(14):6111-6120. |
| [25] | Abraham S, Mallia V A, Ratheesh K V,et al. Reversible thermal and photochemical switching of liquid crystalline phases and luminescence in diphenylbutadiene-based mesogenic dimers [J]. Journal of the American Chemical Society,2006,128(23): 7692-7698. |
| [26] | Xiao S, Zou Y, Wu J,et al. Hydrogen bonding assisted switchable fluorescence in self-assembled complexes containing diarylethene: controllable fluorescent emission in the solid state [J]. Journal of Materials Chemistry, 2007, 17(24): 2483-2489. |
| [27] | Zhou J, LiuZ, Li F. Upconversion nanophosphors for small-animal imaging [J]. Chemical Society Reviews,2012, 41(3): 1323 1349. |
| [28] | Zhou Z, Hu H, Yang H,et al.Up-conversion luminescent switch based on photochromic diarylethene and rare-earth nanophosphors [J]. Chemical Communications, 2008,4786-4788 |
| [29] | Xiao S, Yi T, Li F,et al. A multi-photo responsive photochromic dithienylethene-containing coumarin derivative [J]. Tetrahedron Letters,2005, 46(52): 9009-9012. |
| [30] | Hammond G S, Stout C A, Lamola A A. Mechanisms of photochemical reactions in solution. XXV. The photodimerization of coumarin [J]. Journal of the American Chemical Society,1964,86(15): 3103-3106. |
| [31] | Hoffman R.Wells P, Morrison H. Organic photochemistry. XII. Further studies on the mechanism of coumarin photodimerization, observation of an unusual "heavy atom" effect [J]. The Journal of Organic Chemistry, 1971,36(1): 102-108. |
| [32] | Morrison H A, Curtis H, McDowell T. Solvent effects on the photodimerization of coumarin[J]. Journal of the American Chemical Society,1966,88(23): 5415-19. |
| [33] | Xiao S, Yi T, Zhou Y,et al. Multi-state molecular switches based on dithienylperfluorocyclopentene and imidazo phenanthroline [J]. Tetrahedron, 2006, 62(43): 10072-10078. |
| [34] | Zhou Z, Xiao S, Xu J,et al. Modulation of the photochromic property in an organoboron-based diarylethene by a fluoride ion [J]. Organic Letters,2006, 8(18): 3911-3914. |
| [35] | Finley K R, DavidsonA E, Ekker S C. Three-color imaging using fluorescent proteins in living zebrafish embryos [J]. Biotechnology Progress,2001,31(1): 66-72. |
| [36] | (a) Chalfie M, Tu Y, Euskirchen G,et al. Green fluorescent protein as a marker for gene expression [J]. Science,1994, 263(5148): 802-805. (b) Orlic D, Kajshura J,Chimenti S,et al. Bone marrow cells regenerate infarcted myocardium [J]. Nature,2001, 410(6829): 701-705. |
| [37] | Michalet X, Pinaud F F, Bentolila A,et al. Quantum dots for live cells, in vivo imaging, and diagnostics [J]. Science,2005,307(5709): 538-544. |
| [38] | (a) Gao X, Cui Y, Levenson R M,et al. In vivo cancer targeting and imaging with semiconductor quantum dots [J]. Nature Biotechnology,2004,22(8): 969-976. (b) Medintz I L, Uyeda HT, Goldman E R,et al. Quantum dot bioconjugates for imaging, labelling and sensing [J]. Nature Materials,2005,4(6): 435-446. (c) Xiong L, Yang T, Yang Y,et al.Long-term in vivo biodistribution imaging and toxicity of polyacrylic acid-coated upconversion nanophosphors [J]. Biomaterials,2010,31(27): 7078-7085. (d) Xiong L-Q, Chen Z G, Yu M-X, et al.Synthesis, characterization, and in vivo targeted imaging of amine-functionalized rare-earth up-converting nanophosphors [J]. Biomaterials,2009,30(29): 5592-5600. (e) Sun Y, Yu M, Liang S, et al.Fluorine-18 labeled rare-earth nanoparticles for positron emission tomography (PET) imaging of sentinel lymph node [J]. Biomaterials,2011,32(11): 2999-3007. |
| [39] | Zhang M, Yu M, Li F,et al.A highly selective fluorescence turn-on sensor for cysteine/homocysteine and its application in bioimaging [J]. Journal of the American Chemical Society,2007,129(34): 10322-10323. |
| [40] | Carreon J R, Stewart K M, Mahon K P,et al. Cyanine dye conjugates as probes for live cell imaging [J]. Bioorganic & Medicinal Chemistry Letters,2007,17(18): 5182-5185. |
| [41] | Soh N, Yoshida K, Nakajima H, et al. A fluorescent photochromic compound for labeling biomolecules [J]. Chemical Communications,2007, 5206-5208. |
| [42] | ZouY, Yi T, Xiao S,et al. Amphiphilic diarylethene as a photoswitchable probe for imaging living cells [J]. Journal of the American Chemical Society,2008,130(47): 15750-15751. |
| [43] | Al-Atar U, Fernandes R, Johnsen B,et al. A photocontrolled molecular switch regulates paralysis in a living organism [J]. Journal of the American Chemical Society,2009,131(44): 15966-15967. |
| [44] | Piao X, Zou Y, Wu J,et al. Multiresponsive switchable diarylethene and its application in bioimaging [J]. Organic Letters,2009,11(17):3818-3821. |
| [45] | Barboiu M, Prodi L, Montalti M, et al. Dynamic chemical devices: modulation of photophysical properties by reversible, ion-triggered, and proton-fueled nanomechanical shape-flipping molecular motions[J]. Chemistry- A European Journal,2004, 10(12): 2953-2959. |
| [46] | Yam V, Ko C, Zhu N. Photochromic and luminescence switching properties of a versatile diarylethene-containing 1,10-phenanthroline ligand and its rhenium(I) complex [J]. Journal of the American Chemical Society,2004,126(40): 12734-12735. |
| [47] | Ko C-C, Kwok W-M, Yam V, et al. Triplet MLCT photosensitization of the ring-closing reaction of diarylethenes by design and synthesis of a photochromic rhenium(I) complex of a diarylethene-containing 1,10-phenanthroline ligand [J]. Chemistry-A European Journal,2006,12(22): 5840-5848. |
| [48] | Zhang J J, Zou Q, Tian H. Photochromic materials: more than meets the eyes [J]. Advanced Materials,2013, 25(3): 378-399. |




