氰化物对人体及绝大多数生命体具有强烈毒性[1],但是在工业生产中,依然广泛存在氰化物的使用和含氰废物的排放[2]。化学合成纤维的生产,矿物浮选,冶金过程当中使用和排放的氰化物,以及在杀虫剂和除草剂中含有的少量氰化物,都有可能对食物、水体及周围环境造成污染,从而严重威胁健康及生命安全[3]。此外,氰化物作为某些细菌及真菌的代谢产物广泛存在于自然界中,烟草燃烧之后其烟雾中也含有氰化物,吸烟时血液中的氰化物含量会显著提高。而且氰化物的过量摄入会影响人体心血管功能,破坏中枢神经系统和视觉神经系统,扰乱人体新陈代谢。其最 大的影响,在于抑制细胞内线粒体的呼吸作用,氰化氢对人体的LD50值为 1.0 mg/kg。美国环保局 (The United States Environmental Protection Agency) 规定了饮用水中氰化物的最高含量为 0.2 ppm[1]。
氰化物的检测主要依靠电化学及离子色谱。但是这类传统方法对仪器设备的依赖性较大,成本较高,耗时长。而化学传感器则具有成本低、设备简单、检测速度快,及灵敏度高的特点[4]。在过去10年中,针对不同的检测对象,研究人员合成 了具有各种光谱性能的化合物,化学传感器领域 的研究获得了广泛的关注和发展[5,6,7,8,9]。
化学传感器主要由识别单元和信号单元两部分组成,通过共价键、配位或分子间作用,组合成完整的传感体系。当识别单元与检测目标发生相互作用之后,信号单元发出检测信号[10]。而化学反应型传感器,即通过识别单元与检测目标发生专一性化学反应,从而实现对待测物定性及定量识别的传感体系[11]。由于化学反应本身所具备的微量反应特征,相比金属配位、氢键及立体效应等其他非反应型识别原理,易于实现更高的灵敏度。检测信号主要通过紫外可见吸收光谱、激发光谱、荧光及磷光发射光谱、荧光寿命等光谱变化来表达。得益于这几类光谱,尤其是荧光发射光谱灵敏度的不断提高,化学传感器也得到了长足的发展和进步。荧光增强型化学传感器相对荧光猝灭型传感器而言,灵敏度更高。这是由于增强的荧光信号能够更好地排除仪器噪声的影响,减小测量误差。
吩嗪作为一类天然产物的衍生物,具有合成简单、易于修饰的特点[12]。在与强吸电子基团结合之后,吸收光谱红移,表现出很强的分子内电荷转移吸收,吩嗪本身的荧光则表现出明显的猝灭。基于这一特点,我们设计合成了以吩嗪作为荧光团,吲哚磺酸作为吸电子基团和识别基团的反应型化学传感器 PDSI 。由于吲哚氮原子具有正电荷,所以在750 nm表现出很强的ICT吸收,也使得吲哚的C N双键亲电活性大大增加。氰根进攻C N双键的C原子,发生亲核加成,破坏了吲哚双键,阻断了分子内电荷转移过程,从而恢复吩嗪荧光,实现了荧光增强的信号表达。
1 实验部分 1.1 试剂与仪器核磁共振1HNMR 和13CNMR,使用Bruker AM 400 MHz 核磁共振谱仪,TMS作为内标;吸收光谱使用Varian Cary 500 UV-Vis光谱仪;荧光光谱使用Horiba Fluoromax-4型荧光光谱仪;质谱使用Waters Micromass LCT 质谱仪。
DMF用氢化钙重蒸处理,其它试剂由Aldrich公司购买,未经进一步纯化。
1.2 化合物PDSI的合成吩嗪经保险粉还原生成还原吩嗪 1。1 在空气中易被氧化,干燥后迅速与碘丁烷进行烷基化反应,生成烷基化产物 2。2 为墨绿色透明晶体,在空气中不稳定,通过Vilsmeier-Haack 反应形成稳定的醛基化产物 3。3 为橙黄色固体粉末,与2,3,3-三甲基吲哚磺酸盐在哌啶催化下发生1∶2的Knoevenagel反应生成产物 PDSI ,如图1所示。产物 3和4 的结构均通过核磁共振氢谱进行了表征,PDSI 也通过核磁共振氢谱和质谱进行了表征。
1.2.1 二丁基吩嗪二醛 ( 3 ) 的合成将2.84 g (15.8 mmol) 吩嗪溶解在70 mL乙醇当中,在氩气保护下,加热至回流,搅拌15 min后,加入保险粉水溶液 (28.4 g,0.16 mol,125 mL),体系由淡黄色透明溶液迅速变为淡绿色悬浊液,继续回流2 h,停止加热。待温度降至室温后,抽滤得到固体,滤饼用水洗涤,经真空干燥后得到2.0 g中间体还原吩嗪粗产品 ( 1 )。迅速将2.0 g (10.9 mmol) 1 溶于30 mL DMSO当中,加入1.2 g (30 mmol) NaOH、0.2 g (0.6 mmol) 四丁基溴化铵、1.5 mL水,常温下搅拌5min后,加入2.5mL(21.8mmol)碘代正丁烷,加热至40℃搅拌,反应4h。待体系降至室温后,将其倒入饱和食盐水中,用二氯甲烷萃取,中性氧化铝柱层析纯化,得到墨绿色晶体(2),约2.2g(7.7mmol)。由于2在空气中不稳定,迅速投入下一步反应。将2溶于14mLDMF中,在冰浴和氩气保护下,缓慢滴加1mL三氯氧磷,继续在冰浴下搅拌15min后,升温至90℃,搅拌反应6h。待降至室温,将反应体系倒入冰水中,搅拌,用1N NaOH水溶液调节pH至中性。过滤得到橙黄色滤饼,用二氯甲烷溶液,柱层析纯化,得到产物 3 (0.8 g),产率30%。
 | 图1 化合物 PDSI 的合成路线Synthesis process of PDSI(i) Na2S2O4,EtOH,H2O,80 ℃; (ii) n-butyl iodide,NaOH,TBAB,DMSO,H2O,r.t. 40 ℃;(iii) phosphorus oxychloride,DMF,ice bath to 90℃,6h; (iv) piperidine,CH3CN,80 ℃,10 h |
1HNMR (400 MHz,CDCl3):9.59 (s,2H,CHO),7.10 (dd,J=8.1,1.6 Hz,2H,Ar-H),6.72 (d,J=1.6 Hz,2H,Ar-H),6.27 (d,J=8.2 Hz,2H,Ar-H),3.44 (m,4H),1.63 (m,4H),1.48 (dq,J=14.6,7.3 Hz,4H),1.04 (t,J=7.3 Hz,6H)。13CNMR (101 MHz,CDCl3 ) : 189.81,142.52,135.18,130.17,109.77,108.25,45.77,31.44,26.47,25.62,22.67。Mass (ESI,m/z) [M+H]+ calcd for C22H27N2O2+: 351.2. Found: 351.2。
1.2.2 吲哚磺酸盐 ( 4 ) 的合成将1.22 g (7.6 mmol) 2,3,3-三甲基-3H吲哚和0.46 g (3.7 mmol) 1,3-丙烷磺内酯加入10 mL甲苯中,回流反应12 h。待降至室温后,抽滤,滤饼用二氯甲烷洗涤,真空干燥,得到固体产物 4 ,0.9 g (3.3 mmol),产率90%。
1HNMR (400 MHz,DMSO) :8.06 (m,1H,Ar-H),7.83 (m,1H,Ar-H),7.62 (s,2H,Ar-H),4.66 (s,2H),2.84 (s,3H),2.63 (s,2H),2.16 (s,2H),1.53 (s,6H)。
1.2.3 产物 PDSI 的合成将350 mg (1.0 mmol)3和420mg(1.5mmol)4加入20mL乙腈中,搅拌均匀之后,滴入两滴哌啶,在氩气保护下,加热回流10 h,体系由橙色悬浊液逐渐变为墨绿色溶液。反应完毕后,待降至室温,旋除溶剂,柱层析提纯,洗脱液为 CH2Cl2 : EtOH = 20∶1。得到终产物 PDSI ,260 mg (0.3 mmol),产率30%。
1HNMR (400 MHz,DMSO) :8.17 (d,J=15.6 Hz,2H,Ar-H),7.84 (dd,J=18.4,7.5 Hz,4H,Ar-H),7.69 (d,J=8.3 Hz,2H,Ar-H),7.56 (m,6H,Ar-H),7.31 (s,2H),6.70 (d,J=8.8 Hz,2H),4.76 (t,4H),3.91 (t,4H),2.63 (t,4H),2.15 (m,4H),1.77 (s,12H),1.58 (m,8H),0.96 (s,6H)。Mass (ESI,m/z) [M+H]+ calcd for C50H61N4O6S2: 877.4033. Found: 877.4030。
2 结果与讨论 2.1 PDSI对氰根离子的紫外可见吸收光谱响应如图2所示,在紫外可见吸收光谱中,10 μmol/L PDSI 的DMSO溶液,表现出两个主要吸收峰,分别位于438 nm和750 nm。ICT作用表现为750nm处的最大吸收峰,截止波长达到900nm。当加入氰根离子后,由于双键被破坏,吲哚基团上氮原子的正电荷被中和,吸电子能力迅速降低,750nm处的ICT吸收带吸光度相应下降。同时,由于整个分子的电荷转移作用逐渐消失,438nm处吸收出现蓝移和减弱,在488nm处出现一个等吸收点,这表示体系逐渐生成了新的反应产物。由于红外区域吸光度的剧烈下降,肉眼可明显观察到溶液体系的颜色由绿色逐渐变为淡黄色,从而实现了对氰根离子直观的颜色响应。
由图2右图可以看到,当加入0.1~1.2当量氰根时,750nm处吸光度剧烈变化,变化率呈线性增加的趋势。当加入的氰根总当量达到1.6时,变化率逐渐降低,2.0当量时,反应基本进行完全,加入2.4个当量,反应达到饱和点,吸光度不再发生变化。
 | 图2 左:在 PDSI (10 μmol/L) DMSO溶液中,加入0~2.4eq氰根离子 (氰化四丁基铵水溶液),紫外光谱的变化;右:750nm处最大吸收强度变化率,随着加入氰根离子浓度的变化曲线,内图:加入氰根前后溶液颜色对比。 Left: UV-Vis spectra of PDSI (10 μmol/L) in DMSO with different equivalent of CN- in water.Right: Plot of change ratio at 750 nm according to CN- concentration,inset: photo of PDSI solvent (20 μmol/L in DMSO) color change before and after addtion of CN- |
如图3所示,由于吲哚磺酸基团的强拉电子作用,PDSI 的DMSO溶液没有明显的荧光,仅仅在580 nm处表现出极微弱的发射。这是由于ICT过程通常会降低荧光量子产率,猝灭分子的荧光。随着氰根离子的加入,由于吲哚C N+ 双键与氰根离子发生亲核加成反应,缺电子的氮正离子变为电中性,同时C N+ 双键被破坏,形成新的C—N单键,分子内电荷转移作用逐渐消失,表现出明显的荧光增强。位于580nm处的最大发射波长,强度增大超过20倍。与吸收光谱的变化规律比较,可以看出,同样在加入0.1~1.4倍当量的过程中,580nm处荧光强度呈现线性增大,当加入1.8个当量之后,变化趋于平缓,加入2.2个当量之后,反应达到饱和点,荧光强度不再变化。
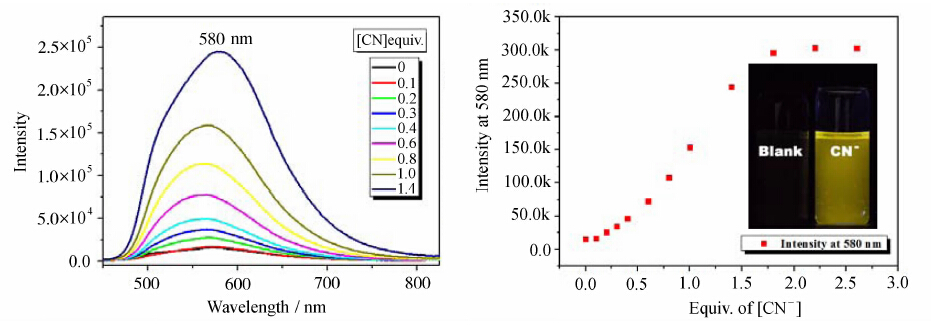 | 图3左:在PDSI(10μmol/L)DMSO溶液中,加入0~2.4eq氰根离子,荧光光谱的变化;右:580nm处最大发射强度随着加入氰根离子浓度的变化曲线,内图:加入氰根前后溶液的荧光对比。激发波长:438 nm Left: Fluorescence spectra of PDSI (10 μmol/L) in DMSO with different equivalent of CN- in water.Right: Change plot of emission intensity at 580 nm concomitant with CN- equivalent,inset: photo of PDSI solvent (10 μmol/L in DMSO) fluorescence change before and after addition of CN-.Ex =438 nm - |
为了更加直观地研究反应型探针的反应机理,进行了核磁滴定实验。如图4所示,对照反应 前后的1HNMR谱图,可以明显看出反应前后分子结构发生的变化。在DMSO-d6中,加入2.2 eq CN-,反应10 min后,6.69~8.18ppm范围的苯环及烯烃的相应谱峰均移向高场,表现出非常明显的屏蔽化效应,表明原先由吸电子基团的诱导效应导致的去屏蔽化作用消失。与此同时,N+—CH在4.76 ppm处的三重峰Ha,以及S—CH在3.91 ppm处的三重峰Hb分别向高场移动至3.25ppm和3.05ppm。这两个烷基H化学位移的变化进一步佐证了与氰根反应后的N+电荷被中和,失去诱导效应。同时,通过核磁滴定谱图,也可看出,在10 min的反应时间内,体系中的 PDSI 已经反应完全。
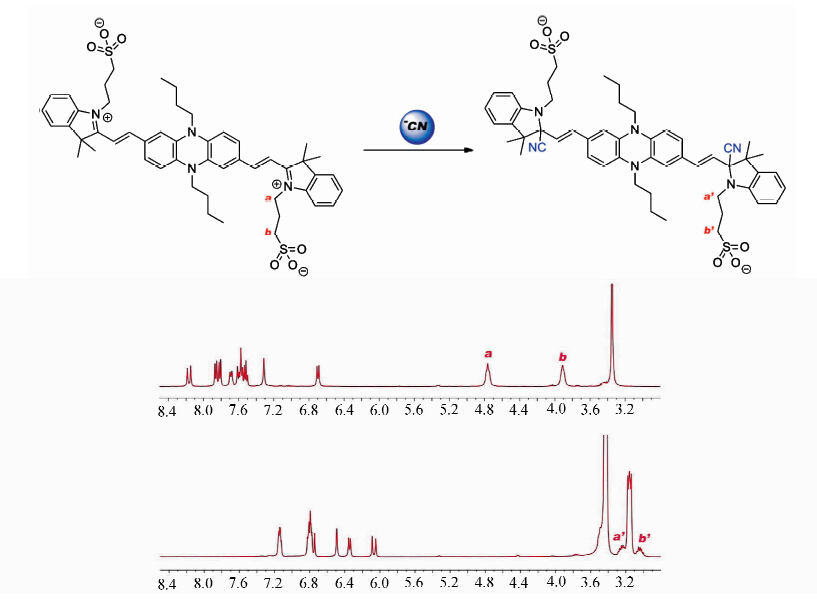 | 图4 PDSI 与CN-的反应过程示意图及1HNMR滴定谱图 Reaction process of PDSI toward cyanide anion and 1HNMR titration spectra |
利用曲线拟合荧光强度变化曲线,计算化合物 PDSI 对氰根离子的检出限,如图5。线性拟合得到的曲线斜率为k=17403.67398。仪器测量标准差由七次平行测试580 nm处荧光强度计算得到 σ=120.3911。由3σ/k计算得到检出限为0.02 μmol/L。
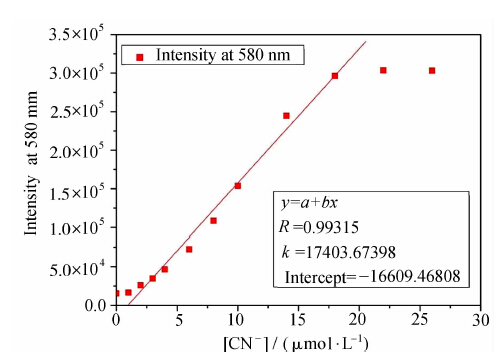 | 图5 PPDSI 在580 nm发射波长随氰根离子浓度变化曲线及线性拟合 Change plot of emission intensity of PDSI at 580 nm toward cyanide anion concentration and its linear fit measurement |
选择性是荧光传感器的重要性能参数。如图6所示,只有加入氰根离子时,PDSI溶液才表现出明显的荧光增强,增强幅度超过20倍。这主要是由于氰根相比其他阴离子具有更强的亲核反应性,同时吲哚磺酸盐的双键结构恰好对于氰根离子具有更强的亲电反应性能。为了进一步测试不同阴离子的存在是否会对 PDSI 对氰根离子的响 应造成影响,进行了抗干扰测试。如图7所示,分别加入10 eq不同阴离子之后,再加入2 eq氰根离子,PDSI 体系表现出基本相同的荧光增强,其它阴离子的存在并没有对氰根的检测造成明显影响。由此可见,PDSI 对氰根具有良好的选择性和抗干扰能力。
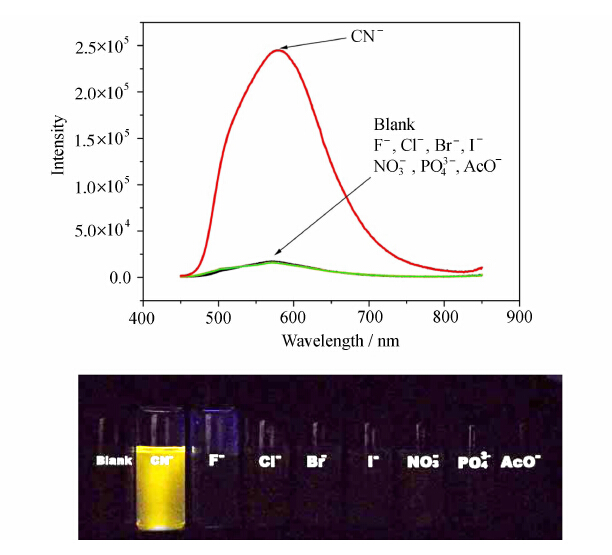 | 图6 PPDSI (10 μmol/L) in DMSO,对不同阴离子的荧光响应:2eq CN-,及10eq F-、Cl-、Br-、I-、NO3-、PO43-、AcO-上图:荧光光谱,Ex=438 nm;下图:365 nm荧光灯下的荧光实拍示意图 Fluorescence spectra (above,Ex=438 nm) and real photo under 365 nm UV lamp (below) of PDSI (10 μmol/L) in DMSO toward CN- and other different anions,respectively: 2eq CN-,10eq F-,Cl-,Br-,I-,NO3-,PO43-,AcO- |
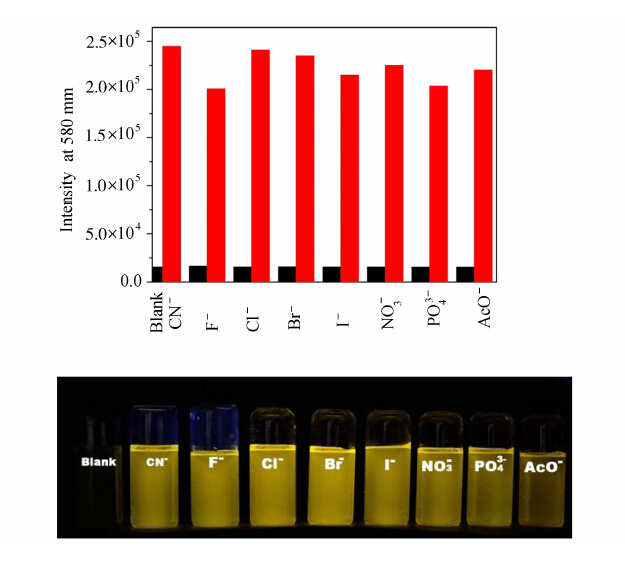 | 图7 PDSI 抗干扰能力测试,上图:黑色表示空白溶液,及加入10eq不同离子时580 nm处荧光强度;红色表示加入2eq氰根后580 nm处荧光强度;下图:365 nm紫外灯下的荧光实拍图像 Anti-interference measurement of PDSI toward variety of anions,(above) black bars represent emission intensity at 580 nm of blank and with 10 eq various anions; red bars: subsequent adding with 2eq cyanide anions; (below) corresponding photo under 365 nm UV lamp |
以吩嗪作为荧光团,设计合成了具有荧光增强性能的化学反应型氰根离子传感器PDSI。通过紫外可见吸收光谱和荧光光谱研究了PDSI对氰根离子的响应。实验表明,氰根离子与PDSI发生亲核加成反应,阻断了分子内电荷转移过程,从而恢复吩嗪荧光,得到荧光增强信号,增强幅度超过20倍,可由肉眼定性观察,检出限达到20nmol/L,低于EPA所规定的饮用水中氰化物的含量上限,同时,PDSI具有良好的选择性和抗干扰能力。综上所述,以吩嗪吲哚菁染料作为氰根离子检测体系,具有很好的应用和发展前景。
| [1] | Xu Z C, Chen X Q, Kim H N, Yoon J Y. Sensors for the optical detection of cyanide ion[J]. Chemical Society Reviews,2010, 39: 127-137. |
| [2] | Kim Y M, Zhao H Y, and Gabbai F P. Sulfonium boranes for the selective capture of cyanide ions in water[J]. Angewandte Chemie International Edition, 2009, 48: 4957-4960. |
| [3] | Pritchard J D. Hydrogen Cyanide Toxicological Overview. U. K.: Health Protection Agency, 2007. |
| [4] | Zou Q, Li X, Zhang J J, Zhou J, Bingbing Sun, Tian H. Unsymmetrical diarylethenes as molecular keypad locks with tunable photochromism and fluorescence via Cu2+ and CN- coordinations[J]. Chemical Communications, 2012, 48: 2095-2097. |
| [5] | Qu Y, Hua J L, and Tian H. Colorimetric and ratiometric red fluorescent chemosensor for fluoride ion based on diketopyrrolopyrrole[J]. Organic Letters, 2010, 12(15): 3320-3323. |
| [6] | Liu J L, Liu Y, Liu Q, Li C Y, Sun L N, Li F Y. Iridium(III) complex-coated nanosystem for ratiometric upconversion luminescence bioimaging of cyanide anions[J]. Journal of the American Chemical Society, 2011, 133: 15276-15279. |
| [7] | Lee C H, Yoon H J, Shim J S, and Jang W D. A boradiazaindacene-based turn-on fluorescent probe for cyanide detection in aqueous media[J]. Chemistry- A European Journal, 2012, 18: 4513-4516. |
| [8] | Lv X, Liu J, Liu Y L, Zhao Y, Sun Y Q, Wang P, Guo W. Ratiometric fluorescence detection of cyanide based on a hybrid coumarin-hemicyanine dye: the large emission shift and the high selectivity[J]. Chemical Communications, 2011, 47: 12843-12845. |
| [9] | Liu Z P, Wang X Q, Yang Z H, He W J. Rational design of a dual chemosensor for cyanide anion sensing based on dicyanovinyl-substituted benzofurazan[J]. The Journal of Organic Chemistry, 2011, 76: 10286-10290 |
| [10] | Robbins T F, Qian H, Su X, Hughes R P, Aprahamian I. Cyanide detection using a triazolopyridinium salt[J]. Organic Letters, 2013, 15(10): 2386-2389. |
| [11] | Yang Y M, Zhao Q, Feng W, Li F Y. Luminescent chemodosimeters for bioimaging[J]. Chemical Reviews, 2013, 113: 192-270. |
| [12] | Yang Y, Li X, Yang G B, Qu Y, Hua J L. Colorimetric and ratiometric near-infrared fluorescent cyanide chemodosimeter based on phenazine derivatives[J]. ACS Applied Materials & Interfaces, 2013, 5: 1317-1326. |




