2. 黑龙江大学 功能无机材料教育部重点实验室, 黑龙江 哈尔滨 150080
2. Key Laboratory of Functional Inorganic Material Chemistry, Ministry of Education, Department of Macromolecular Material and Engineering, Heilongjiang University, Harbin 150080, Heilongjiang, P.R.China
氟离子是人体内重要的微量元素之一,对人体的健康至关重要;同时,临床医学研究表明,一次大剂量的摄入或长期少量的摄入氟离子,将导致人体胃、肾功能的损伤以及引起骨骼氟中毒等。氟离子的含量对环境如人类赖以生存的淡水环境会产生重要的影响,无论从人体健康还是环境保护方面考虑,氟离子的检测都具有重要意义。与传统的氟离子检测手段如离子色谱法相比,荧光化学探针具有检测方便、灵敏度高,可实现活体细胞内氟离子的在线实时检测等优势。目前,科学家们已经开发出许多氟离子荧光和比色法化学探针 [1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20],但很多都主要集中在小分子的化学探针研究上,而对聚合物氟离子化学探针的研究则比较少[9, 10]。
采用RAFT可控/活性自由基聚合方法,可以合成结构和组成可调的、分子量大小可控和分子量分布窄的均聚物、无规共聚物或嵌段共聚物,可系统研究聚合物探针的光物理行为与其分子结构、周围物理及化学环境变化的关系,并为 通过分子结构的设计来调整其传感性能提供必要 的基础。
本文设计合成了以萘酰亚胺为荧光团、苯酰胺为F-识别位点的分子探针Nap,并采用RAFT方法将其与N-异丙基甲基丙烯酰胺(NIPAM)进行共聚,将F-响应单元通过N-异丙基甲基丙烯酰胺单元进行一定程度的稀释和掺杂,改善聚合物薄膜对F-的响应性能。同时,引入N-异丙基甲基丙烯酰胺改善聚合物的成膜性能。
1 实验部分 1.1 仪器与试剂Brucker AV-400核磁共振仪,频率为400 MHz,内标为TMS; JEOL JMS 700质谱分析仪; Varian Cary紫外-可见光谱仪;HORIBA荧光光 谱仪(内置恒温装置); Waters 1515凝胶渗透色谱仪。
AIBN经无水乙醇重结晶后立即使用。NMP(N-甲基吡咯烷酮)减压蒸馏后随即使用。测试和合成过程中使用的水皆为二次蒸馏水。卤素离子选用四丁基铵盐。所用试剂和药品均为分析纯或化学纯,除文中特殊说明外,其它试剂未经进一步提纯直接使用。N-异丙基甲基丙烯酰胺以及聚合物poly(NIPAMm-co-Napn)均按文献采用RAFT方法合成[10, 21](合成路线及其结构见图1),GPC测得Mn = 12500,PDI = 1.20。所得共聚物中单体比例参照文献方法,采用紫外吸收标准曲线进行测定[22],为[NIPAM]/[Nap]=334/1,相应的共聚物记为PNap334,其核磁共振氢谱与红外光谱见图2与图3。
 | 图1 共聚物合成路线及其结构 Synthetic route and chemical structure of PNap334 |
 | 图2 共聚物PNap334在氘代DMSO中的核磁共振氢谱图1HNMR spectra of PNap334 in DMSO-d6 |
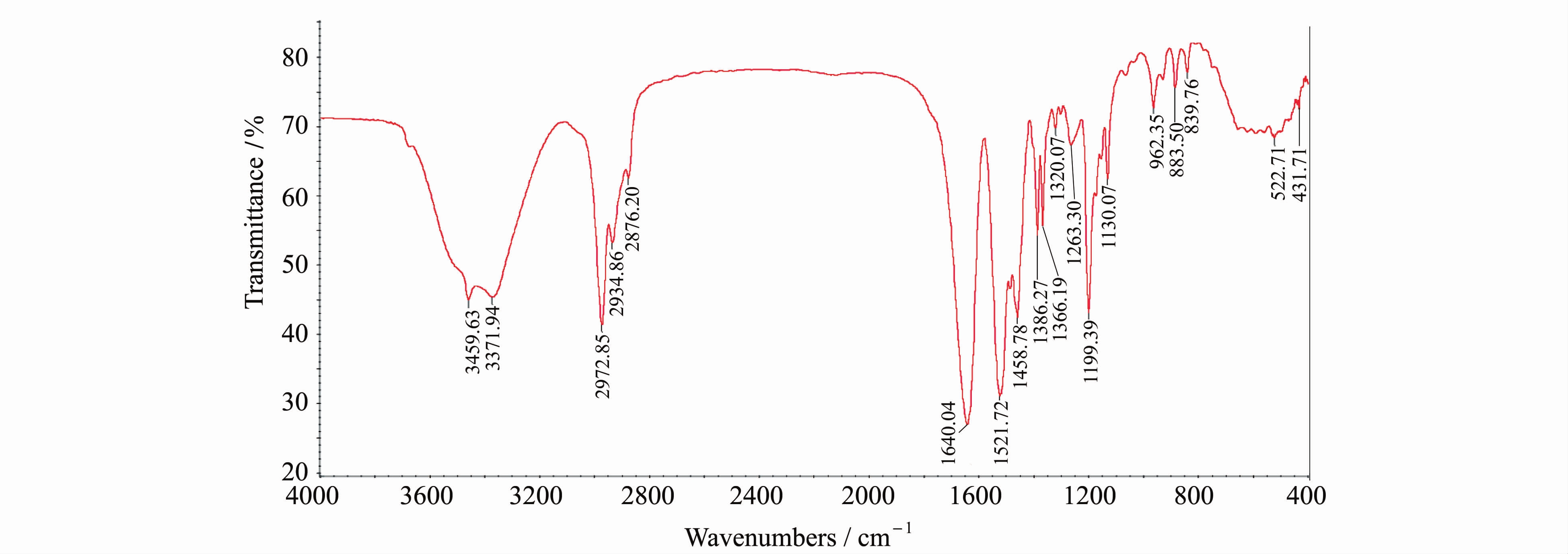 | 图3 共聚物PNap334的红外光谱图 FT-IR spectra of PNap334 |
将待测聚合物用二氯甲烷-二甲亚砜(4∶1,V/V)配制质量浓度为0.5 mg·mL-1的溶液。测试过程中通过恒温水浴控制温度的升降,读数误差为± 0.1 ℃。所有测试溶液现配现用,聚合物 薄膜的制备采用旋涂法,将配好的25.0 mg·mL-1 聚合物二甲亚砜溶液涂到石英玻璃片上,并将其置于水平桌面上,待干燥后测试。测试过程中将涂有聚合物薄膜的石英玻璃片插到四叔丁基氟化铵的乙腈溶液中 (浓度为1.0 × 10-2 mol·L-1)进行相应的光谱测试。薄膜对F-响应性能的测试方法参照文献方法进行[23, 24]。
2 结果与讨论 2.1 F- 对聚合物吸收光谱的影响在PNap334的二氯甲烷-二甲亚砜(9∶1,V/V)溶液(F- 响应单元Nap的浓度为1×10-5mol·L-1) 中加入不同当量的F-。从图4可以看出,随着 F-的加入,360 nm处的吸收峰逐渐减弱,而490 nm 处逐渐形成一个新的吸收峰,并且随着F-浓度的增加而增强,将490 nm处的吸收与360 nm处的吸收比值对F-浓度作图(图4插入图),可以更明显地看到体系吸收随F-浓度的变化,当F-浓度为5×10-5mol/L时,490 nm与360 nm处吸收强度的比值(A490 nm/A360 nm)开始出现变化。吸收光谱变化应该是由于随着F-的加入苯甲酰胺的N—H中的质子与F-形成了氢键(图5),并逐渐发生去质子化作用。
 | 图4 聚合物PNap334的DCM / DMSO (9/1,V/V) 溶液在不同F- 浓度下的紫外-可见吸收光谱 UV-Vis spectra of polymer PNap334 in DCM/DMSO(9/1,V/V) upon addition of F- |
 | 图5 聚合物PNap334与F- 作用机理示意图 Scheme for the interaction mechanism of PNap334 with F- |
甲酰胺的N—H中的质子与F-形成氢键和去质子化作用导致苯甲酰胺的N原子的供电子能力增强,萘酰亚胺与酰胺中的N形成的ICT共轭体系内电子云密度发生了变化,ICT共轭体系内的推拉电子效应增强,导致PNap334体系基态能级的下降,与F-发生作用后PNap334的吸收峰发生红移。其中,340 nm和405 nm处的等吸收点说明F-的加入使溶液平衡体系中存在两种状态 的物质,即PNap334和PNap334-,其中PNap334-的生成对应产生490 nm处的新吸收峰[10]。
氟离子滴定前后酰胺上质子的核磁共振氢谱的变化证实了氢键的形成和去质子化的推测,如图6所示。在滴加1当量的氟离子乙腈溶液时,Nap酰胺上的质子的核磁共振氢谱信号迅速减弱,位移向低场移动,并且峰形明显变宽,这是由于酰胺质子与氟离子形成氢键作用导致;当滴加2当量的氟离子乙腈溶液时,酰胺质子的核磁共振氢谱彻底消失。
 | 图6 单体Nap的酰胺质子核磁共振氢谱的变化(a)加入F-前;(b)加入1当量F-后;(c)加入2当量F-后 1HNMR spectra of Nap before (a) and after (b,1 eq; c,2 eq) the addition of F-- |
图7(a) 是在聚合物的二氯甲烷-二甲亚砜(9/1,V/V)溶液中(Nap单元的浓度为1×10-5 mol·L-1)加入不同当量的F-后,聚合物溶液在340 nm波长的光激发下的荧光谱图变化。随着F-的加入,聚合物中Nap的含量逐渐减少,而Nap-的含量逐渐增多,因而图中465 nm处的峰强度逐渐减小,而580 nm处的峰强度逐渐增大[10]。这里荧光的响应可归结于分子间质子转移和诱导分子内电荷转移[25]。
为了评估聚合物PNap334对氟离子检测的灵敏度,将体系在580 nm处的荧光强度对氟离子浓度作图,如图7(b)所示,体系在580 nm处的荧光强度与氟离子浓度在4×10-5~9×10-5 mol/L范围内呈良好的线性关系,回归方程为:I=32.209c-81.229(I为信号强度,c为F-浓度);线性相关系数r=0.9904\[见图7(b)\]。不加F-时平行测定了11次发光强度,其相对标准偏差为1.134。由此可知,在文中的测试条件下PNap334对F-的检测限为1.05×10-6 mol/L。
 | 图7 (a) 聚合物PNap334的DCM/DMSO (9/1,V/V) 溶液在不同F-浓度下的荧光光谱,激发波长为340 nm; (b)580 nm处的荧光强度与\[F-\]的线性拟合图,由此计算得到PNap334的检测限为1.05 μmol/L(σ=1.134). (a) Fluorescence spectra of polymer PNap334 in DCM/DMSO (9/1,V/V) with different concentrations of F-: λex = 340 nm. (b) Linear fitting chart of fluorescence intensity vs. [F-],and the calculated detection limit of PNap334 is 1.05 μmol/L (σ=1.134) |
为了评估聚合物PNap334用于氟离子检测的能力,还研究了聚合物PNap334对氟离子响应的选择性。在PNap334的DCM/DMSO (9/1,V/V)溶液中分别加入10当量的Cl-、Br-和I-,这些卤素阴离子的加入未引起其荧光光谱的显著变化(图8),只有加入F-的体系显示出明显的荧光光谱变化,465 nm处的荧光强度降低,而580 nm处的荧光强度显著增强。说明PNap334可用于在众多卤素阴离子中对F-的选择性检测。
2.3 F- 对聚合物薄膜的紫外-可见光吸收和荧光发射的影响将涂好聚合物薄膜的石英玻璃浸入四叔丁基氟化铵的乙腈溶液中 (浓度为1.0 × 10-2 mol·L-1),图9为聚合物薄膜在用F-溶液处理前后的紫外-可见吸收光谱变化。从图9很容易看出,用F-处理过后,薄膜在370 nm处的紫外-可见吸收峰减弱,而在490 nm处出现一个新的吸收峰。图10为各聚合物薄膜在用F- 溶液处理前后的荧光光谱变化,用F-处理过后,465 nm处的荧光猝灭,而在580 nm处出现新的荧光发射峰。共聚物薄膜中的Nap荧光基团被NIPAM单元有效地分散,相对稀释了Nap荧光基团,自猝灭作用减弱。
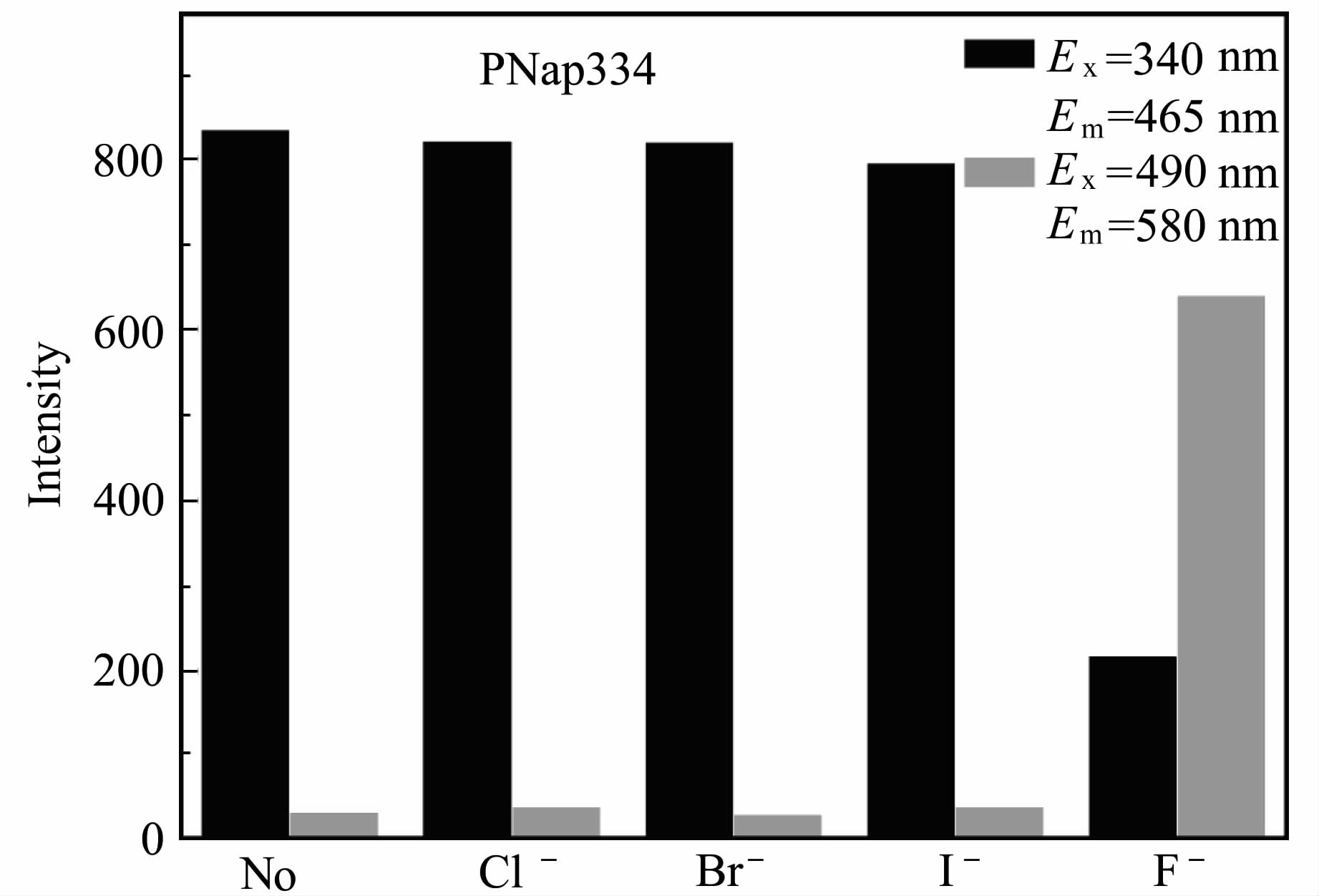 | 图8 聚合物PNap334的DCM/DMSO(9/1,V/V)溶液中分别加入10当量的不同卤素离子 (Cl-、Br-、I-和F-)后荧光强度的变化 Fluorescent intensity of polymer PNap334 in DCM/DMSO (9/1,V/V) upon addition of 10 eq. Cl-,Br-,I- and F- |
 | 图9 加入F-前(实线)后(虚线),聚合物PNap334薄膜的紫外-可见吸收的变化 (F-浓度为1.0×10-2 mol·L-1) UV-Vis spectra of polymer PNap334 films before (solid curve) and after (dot line) the addition of F-(the concentration of F-∶ 1.0× 10-2 mol·L-1) |
 | 图10 加入F-前(实线)后(虚线),聚合物PNap334薄膜的荧光发射的变化(激发波长为370 nm,F- 浓度为1.0×10-2 mol·L-1) Fluorescent spectra of polymer PNap334 films before(solid curve) and after (dot line) addition F-(λex=370 nm,the concentration of F-: 1.0×10-2 mol·L-1) |
本论文利用RAFT方法将NIPAM与1,8-萘酰亚胺衍生物单体(Nap)进行共聚,得到了一种具有F-响应的共聚物PNap334;利用紫外吸收工作曲线测得共聚物中的单体比率为\[NIPAM\]/\[Nap\]=334/1。在PNap334的二氯甲烷-二甲亚砜(9/1,V/V) 溶液中研究发现,聚合物对F-具有很好的选择性识别,而对Cl-、Br-、I-均没有响应;其对F-的检测限为1.05 μmol/L;将聚合物制成固体薄膜后,研究发现聚合物膜对F-亦有很好的识别作用,而共聚单体NIPAM的引入,不仅赋予聚合物更好的成膜性,而且将F- 响应基团稀释,有效地避免了浓度猝灭效应,从而更有利于对F-的识别。
| [1] | Tian H, Liu B. A selective fluorescent ratiometric chemodosimeter for mercury ion[J]. Chemical Communications, 2005, (25): 3156-3158. |
| [2] | Kim Y, Gabbai F P. Cationic boranes for the complexation of fluoride ions in water below the 4 ppm maximum contaminant level[J]. Journal of the American Chemical Society, 2009, 131(9): 3363-3369. |
| [3] | Kubo Y, Yamamoto M, Ikeda M, Takeuchi M, Shinkai S, Yamaguchi S, Tamao K. A colorimetric and ratiometric fluorescent chemosensor with three emission changes: Fluoride ion sensing by a triarylborane-porphyrin conjugate[J]. Angewandte Chemie-International Edition, 2003, 42(18): 2036-2040. |
| [4] | Melaimi M, Gabbai F P. A heteronuclear bidentate Lewis acid as a phosphorescent fluoride sensor[J]. Journal of the American Chemical Society, 2005, 127(27): 9680-9681. |
| [5] | Hudson Z M, Liu X Y, Wang S N. Switchable three-state fluorescence of a nonconjugated donor-acceptor triarylborane[J]. Organic Letter, 2011, 13(2): 300-303. |
| [6] | Yamaguchi S, Akiyama S, Tamao K. Colorimetric fluoride ion sensing by boron-containing pi-electron systems[J]. Journal of the American Chemical Society, 2001, 123(46): 11372-11375. |
| [7] | Xu Z C, Kim S K, Han S J, Lee C, Kociok-Kohn G, James T D, Yoon J. Ratiometric fluorescence sensing of fluoride ions by an asymmetric bidentate receptor containing a boronic acid and imidazolium group[J]. European Journal of Organic Chemistry, 2009, (18): 3058-3065. |
| [8] | Dorsey C L, Jewula P, Hudnall T W, Hoefelmeyer J D, Taylor T J, Honesty N R, Chiu C W, Schulte M, Gabbai F P. Fluoride ion complexation by a B(2)/Hg heteronuclear tridentate lewis acid[J]. Dalton Transactions, 2008, (33): 4442-4450. |
| [9] | Qu Y, Hua J L, Jiang Y H, Tian H. Novel side-chain naphthalimide polyphenyl-acetylene as a ratiometric fluorescent chemosensor for fluoride ion[J]. Journal of Polymer Science Part A-Polymer Chemistry, 2009, 47(6): 1544-1552. |
| [10] | Zhao P, Jiang J B, Leng B, Tian H. Polymer fluoride sensors synthesized by RAFT polymerization[J]. Macromolecular Rapid Communications, 2009, 30(20): 1715-1718. |
| [11] | Li Y, Cao L F, Tian H. Fluoride ion-triggered dual fluorescence switch based on naphthalimides winged zinc porphyrin[J]. Journal of Organic Chemistry, 2006, 71(21): 8279-8282. |
| [12] | Cho E J, Moon J W, Ko S W, Lee J Y, Kim S K, Yoon J, Nam K C. A new fluoride selective fluorescent as well as chromogenic chemosensor containing a naphthalene urea derivative[J]. Journal of the American Chemical Society, 2003, 125(41): 12376-12377. |
| [13] | Gunnlaugsson T, Davis A P, Glynn M. Fluorescent photoinduced electron transfer (PET) sensing of anions using charge neutral chemosensors[J]. Chemical Communications, 2001, (24): 2556-2557. |
| [14] | Pfeffer F M, Lim K F, Sedgwick K J. Indole as a scaffold for anion recognition[J]. Organic & Biomolecular Chemistry, 2007, 5(11): 1795-1799. |
| [15] | Boiocchi M, Del Boca L, Gomez D E, Fabbrizzi L, Licchelli M, Monzani E. Nature of urea-fluoride interaction: incipient and definitive proton transfer[J]. Journal of the American Chemical Society, 2004, 126(50): 16507-16514. |
| [16] | Han F, Bao Y H, Yang Z G, Fyles T M, Zhao J Z, Peng X J, Fan J L, Wu Y K, Sun S G. Simple bisthiocarbonohydrazones as sensitive, selective, colorimetric, and switch-on fluorescent chemosensors for fluoride anions[J]. Chemistry-A European Journal, 2007, 13(10): 2880-2892. |
| [17] | Zhang J F, Lim C S, Bhuniya S, Cho B R, Kim J S. A highly selective colorimetric and ratiometric two-photon fluorescent probe for fluoride ion detection[J]. Organic Letter, 2011, 13(5): 1190-1193. |
| [18] | Bao Y Y, Liu B, Wang H, Tian J A, Bai R K. A "naked eye" and ratiometric fluorescent chemosensor for rapid detection of F(-) based on combination of desilylation reaction and excited-state proton transfer[J]. Chemical Communications, 2011, 47(13): 3957-3959. |
| [19] | Fu L, Jiang F L, Fortin D, Harvey P D, Liu Y. A reaction-based chromogenic and fluorescent chemodosimeter for fluoride anions[J]. Chemical Communications, 2011, 47(19): 5503-5505. |
| [20] | Cao J, Zhao C C, Feng P, Zhang Y, Zhu W H. A colorimetric and ratiometric NIR fluorescent turn-on fluoride chemodosimeter based on BODIPY derivatives: high selectivity via specific Si-O cleavage[J]. RSC Advances, 2012, 2:418-420. |
| [21] | Guo Z Q, Zhu W H, Xiong Y Y, Tian H. Multiple logic fluorescent thermometer system based on N-isopropylmethacrylamide copolymer bearing dicyanomethylene-4H-pyran moiety[J]. Macromolecules, 2009, 42:1448-1453. |
| [22] | Liu G F, Zhou W, Zhang J Q, Zhao P. Polymeric temperature and pH fluorescent sensor synthesized by reversible addition-fragmentation chain transfer polymerization[J]. Journal of Polymer Science Part A-Polymer Chemistry, 2012, 50(11): 2219-2226. |
| [23] | Jin P W, Guo Z Q, Chu J, Tan J, Zhang S L, Zhu W H. Screen-printed red luminescent copolymer film containing cyclometalated iridium(Ⅲ) complex as a high-permeability dissolved-oxygen sensor for fermentation bioprocess[J]. Industrial & Engineering Chemistry Research, 2013, 52:3980-3987. |
| [24] | Jin P W, Chu J, Miao Y, Tan J, Zhang S L, Zhu W H. A NIR luminescent copolymer based on platinum porphyrin as high permeable dissolved oxygen sensor for microbioreactors[J]. AIChE Journal, 59(8):2743-2752. |
| [25] | Yang G Q, Li S Y, Wang S Q, Hu R, Feng J, Li Y, Qian Y. Novel fluorescent probes based on intramolecular charge-and proton-transfer compounds[J]. Pure and Applied Chemistry, 2013, 85(7), 1465-1478. |




