2. 山东农业大学 园艺科学与工程学院, 山东 泰安 271000
2. College of Horticulture Science and Engineering, Shandong Agricultural University, Taian 271018, Shandong, P.R.China
四环素族抗生素因对肺炎球菌、流感菌、革兰氏细菌、破伤风杆菌、布氏杆菌等多种菌类都有广谱抗菌作用而被广泛的应用于畜牧业。其中盐酸四环素是四环素族中最常用的抗生素。近年来因其滥用而导致肉类和奶类食品中抗生素残留,并且造成了食品安全问题。经研究发现四环素能引起肝脏毒性、非酒精性脂肪炎[1,2,3]。为此,美国FDA规定四环素在牛奶中的残留限量小于80 μg/L[4] ;国际卫生组织和欧盟规定在牛奶中的最大残留限量为100 μg/L[5]。尽管残留量的水平通常很低,但这种长期低水平的接触方式也容易产生各种慢性毒性,对人类健康和环境造成危害。因此,建立相应的监控手段和检测方法来控制四环素族抗生素在动物性食品中的残留是非常必要的。目前检测盐酸四环素的常用方法有:高效液相色谱法(HPLC)[6,7,8]、荧光法[9]、传感器法[10]、酶联免疫法(ELISA)、表面等离子体共振法[11]、层析法等一系列方法。虽然这些方法能够精确测量大多样品中抗生素的含量,但存在费力、费时、费钱,仪器设备昂贵,灵敏性差,样品检测需大型分析仪器和在实验室内进行,以及需要专业人员进行操作等缺陷。因此,寻求快速、简便、灵敏度高的盐酸四环素检测方法,以保障人们饮用牛奶的卫生和安全是非常必要的。
荧光探针技术自兴起就被广泛研究[12]。其中稀土镝离子因f电子极少参加化学成键,配位点很丰富,而受到研究者的关注[13]。其荧光光谱基本上保持水合Dy(Ⅲ)的荧光峰波长,荧光强度随配位体的不同而变化,而Dy(Ⅲ)络合物作为扩散控制非辐射能量转移的给予体,只要求研究体系在470~650 nm波长范围内有明显吸收峰就行,这使Dy(Ⅲ)荧光探针的应用范围广泛[14],因此本文构建Dy3+- SSA- TOPO荧光探针检测盐酸四环素。该方法灵敏度高、选择性好、干扰较少、操作简单、加样回收率高等优点。本文成功地将镝荧光探针应用于四环素抗生素的检测,为食品中的四环素族抗生素的残留检测提供了新方法。 1 实验部分 1.1 仪器与试剂
仪器:RF-5301PC型荧光分光光度计(日本岛津公司);PHS-3D pH计(上海精密科学仪器有限公司);BS210S型电子天平(德国赛多利斯公司);TGL-20M高速台式冷冻离心机(湘仪离心机);HJ-3数码恒温磁力搅拌器(常州国华电器有限公司);KQ-200KDE型高功率数控超声波清洗器(昆山市超声仪器有限公司)。
试剂:氧化镝(Dy2O3,上海晶纯试剂有限公司,AR),磺基水杨酸(SSA,天津市博迪化工有限公司,AR),三氯乙酸(CCl3·COOH,上海山浦化工有限公司,AR),浓盐酸(HCl,烟台市双双化工有限公司)。盐酸四环素、土霉素、金霉素、红霉素购于上海晶纯试剂有限公司,USP级;无水乙醇(天津市永大化学试剂有限公司,AR),200mL袋装纯牛奶(购于商场)。实验中所用水均为二次蒸馏水。
1.00×10-2 mol/L DyCl3:准确称取0.3730g的氧化镝于小烧杯中,加入适量浓盐酸,在通风橱中用电热套加热使其溶解,并加热使浓盐酸挥发至近干,然后用无水乙醇定容至100 mL,作为储备液,使用时用无水乙醇稀释。SSA,TOPO试剂用无水乙醇配制成浓度为1.00×10-2 mol/L的储备溶液。300 g/L三氯乙酸溶液:准确称取15.0000 g的三氯乙酸于小烧杯中,用无水乙醇溶解并定容。盐酸四环素用无水乙醇配制为1.00×10-3 mol/L的溶液,并置于冰箱中保存备用。 1.2.2 乙醇体系镝荧光探针的构建
取5支10 mL比色管分别依次加入Dy3+、SSA、TOPO、TC等溶液各1 mL,用无水乙醇定容至刻度线摇匀,放置30 min后,使用荧光分光光度计在波长为200~600 nm范围内测定溶液的荧光光谱,1 cm的荧光池,狭缝为5 nm。根据上述步骤分别测定Dy3++TOPO、Dy3++TC、Dy3++SSA、TC+SSA、SSA+TOPO、Dy3++SSA+TC、SSA+TOPO+TC、Dy3++SSA+TOPO+TC,8个溶液体系的荧光强度。 1.2.3 实验条件的优化
首先研究Dy3+与SSA、TOPO的配比对体系荧光强度的影响,获得最佳配比。其次研究Dy3+与SSA、TOPO、TC等物质加料顺序对体系荧光强度的影响,获得荧光强度最强的加料顺序。最后按最佳配比和顺序在10 mL的比色管中加Dy3+与SSA、TOPO、TC溶液,乙醇定容后每隔10 min测定体系的荧光强度,得出反应时间对体系荧光强度的影响。 1.2.4 选择性实验
固定Dy3+-SSA-TOPO体系的溶液中依次加入土霉素、金霉素、红霉素进行干扰试验。此外研究牛奶中Ca2+、Mg2+、葡萄糖、半乳糖、胆固醇等共存物质对探针测定影响。 1.2.5 牛奶样品加样回收
配制一系列梯度浓度的盐酸四环素溶液,用Dy3++SSA+TOPO荧光探针在最优条件下检测体系在λem =574 nm的荧光强度变化。
按照参考文献[15]方法对牛奶样品进行处理。取5.0 mL牛奶样品置于15 mL的离心管中,加入1.5 mL的300 g/L的三氯乙酸溶液,搅拌1 min后,用低速离心机(3500 r/min)离心5 min后,将上清液小心转移出,静置1 min后,通过0.45 μm的水系醋酸纤维滤膜过滤,收集滤液备用。
牛奶样品的检测:用最优条件下的Dy3++SSA+TOPO作为探针对盐酸四环素处理过的牛奶样品进行检测。在10 mL比色管中,依次加入1 mL 1.0×10-3 mol/L的Dy3+储备液、2.0 mL 1.0×10-3 mol/L的SSA溶液、0.1 mL 10-3 mol/L的TOPO溶液,一定浓度的盐酸四环素溶液、稀释20倍后的牛奶上清液0.5 mL,摇匀。放置30 min后,在λex=305 nm,λem =574 nm处测定溶液的相对荧光强度。 2 结果与讨论 2.1 荧光光谱
图1为Dy3+-SSA体系的荧光光谱图。由图可知体系的激发波长图可知体系的激发波长为305 nm,发射波长为574 nm。
 | 图1 荧光光谱图 Flurescence spectrumDy3+:1.0×10- 4mol/L,SSA:1.0×10-4 mol/L |
以305 nm波长作为激发波长,分别测定了Dy3+、SSA、TC、Dy3++TC、TC+SSA、TOPO、Dy3++TOPO、SSA+TOPO、SSA+TOPO+TC等体系的乙醇溶液中的荧光光谱图,在574 nm处均没有发射峰。单纯Dy3+几乎没有峰这主要是由于在乙醇溶液中,游离态镧系离子的摩尔吸收系数太小,所以直接激发Dy3+时,荧光强度很弱,几乎可以忽略。在体系中存在SSA时,与Dy3+形成配合物后,能够提高溶液中Dy3+配合物的发光效率。单纯的盐酸四环素(TC)在574 nm处并无特征峰出现,将其加入Dy-SSA-TOPO荧光探针所形成的配合物体系中时,可使体系荧光强度减弱(见图2曲线1)。这是由于盐酸四环素对Dy3+-SSA-TOPO荧光探针有荧光猝灭作用,因此可以用Dy3+-SSA-TOPO荧光探针检测TC。
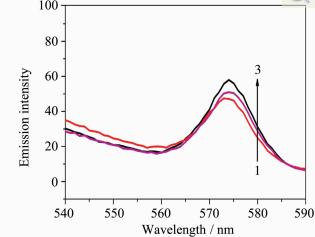 | 图2 不同体系的荧光光谱
Flurescence spectrums of different system 1.Dy3+-SSA-TOPO-TC; 2.Dy3+-SSA; 3.Dy3+-SSA-TOPO Dy3+: 1.0×10-4 mol/L,SSA: 2.0×10-4 mol/L, TOPO: 1.0×10-5 mol/L,TC: 5.0×10-6 mol/L,λex=305 nm |
由图2中曲线2所示,加入SSA后,Dy3+特征峰出现。这是由于当SSA作为配体与Dy3+形成配合物时,提高了对光的吸收,从而提高了溶液中镧系有机配合物的发光效率[16]。并且SSA的激发态与Dy3+激发态的电子能级部分重叠,因此Dy3+荧光可被SSA敏化增强。由曲线3可知,加入TOPO后,Dy3+在574 nm处的荧光强度增大。这也是由于TOPO的加入形成了三元配合物,并且因协同效应荧光强度大于二元配合物。 2.2 实验条件的优化 2.2.1 配比影响
由图3可以看出Dy3+-SSA的配比对体系的荧光强度有很大的影响。由曲线1可以看出,存在Dy3+时,固定其浓度,随着磺基水杨酸含量增加,体系的荧光强度先增大后减小,当达到Dy3+∶SSA=1∶2时,体系的荧光强度值达到最大。SSA用量增大体系的荧光强度下降,可能原因是随SSA浓度增大,分子间形成氢键,或聚集产生相互作用,此作用可能影响SSA与Dy3+配合,进而影响其荧光强度,故本实验选择Dy3+-SSA的配比为1∶2为最佳配比。曲线2可得TOPO的浓度对体系的荧光强度有影响。从图中可以看出,当Dy3+与SSA的浓度一定时,随着TOPO浓度的增加,体系的荧光强度先增大后减小,当TOPO浓度达到1.0×10-5 mol/L时,即Dy3+∶SSA∶TOPO=1∶2∶0.1时,体系的荧光强度值达到最大,故本实验选择Dy3+-SSA-TOPO的配比为1∶2∶0.1为最佳配比。
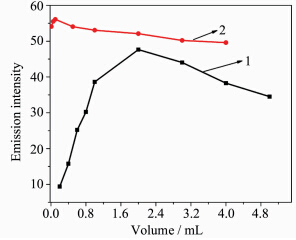 | 图3 荧光强度与Dy3+、SSA和TOPO不同配比的关系
Fluorescence of different ratio of Dy3+,SSA and TOPO 1.Dy3+-SSA; 2.Dy3+-SSA-TOPO Dy3+:1.0×10-4 mol/L,λex/λem=305 nm/574 nm |
由表1可知,不同的加入顺序对体系的荧光强度值If影响不大,这是由于最终发光的体系是由Dy3+与SSA和TOPO形成配合物通过能量变化后发出的荧光,和加样的顺序无关。所以本实验过程中,可以不考虑加入顺序对体系的影响。
| 表1 加入顺序的影响 Effect of the addition order of reagent |
由图4可以看出,时间对Dy3+-SSA-TOPO-TC体系的荧光强度影响不大,本实验选择配好溶液30 min后开始测量。
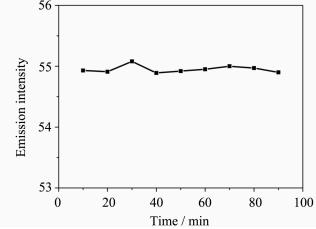 | 图4 反应时间的影响
Effect of the reaction time Dy3+: 1.0×10-4 mol/L,SSA: 2.0×10-4 mol/L,TOPO: 1.0×10-5 mol/L,λex/λem=305 nm/574 nm |
在1.0×10-4 mol/L Dy3+ ,2.0×10-4 mol/L SSA,1.0×10-5 mol/L TOPO的溶液中依次加入土霉素、氯霉素、红霉素进行干扰试验。固定盐酸四环素浓度为1×10-6 mol/L,实验发现当土霉素、金霉素、红霉素的浓度低于10-6 mol/L时,对探针的荧光猝灭作用可以忽略对盐酸四环素的干扰。干扰强度依次为:土霉素>氯霉素>红霉素。由此可知,镝荧光探针在一定的浓度范围内能将目标分子从与它有相似结构的分子中区分出来。此外还考察了牛奶中可能共存物质对探针测定影响,发现加入100倍Ca2+、Mg2+、葡萄糖,50倍的半乳糖、胆固醇不能使探针体系的荧光发生猝灭,对探针的选择性没有干扰。 2.4 牛奶样品中加样回收的检测 2.4.1 标准曲线的绘制
在最优条件下,利用探针Dy3+-SSA-TOPO测定盐酸四环素的浓度与荧光强度值的关系,取得满意结果。从图5中可以看出,体系的荧光强度随盐酸四环素的浓度增加而减小。当盐酸四环 素浓度小于10-6 mol/L时,Dy3+-SSA-TOPO-TC体系的荧光强度值与Dy3+-SSA-TOPO的荧光强度值极为接近;当盐酸四环素的浓度大于5×10-5 mol/L时,探针在574 nm处的特征峰消失。
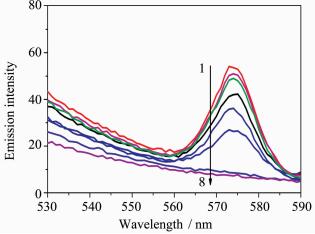 | 图5 盐酸四环素的浓度与荧光强度的关系图
Fluorescence spectrums of the system with different concentration of hydrochloric acid tetracycline Dy3+:1.0×10-4 mol/L ,SSA: 2.0×10-4 mol/L , TOPO: 1.0×10-5 mol/L,λex/λem=305 nm/574 nm 1—8: 1×10-6,3×10-6,5×10-6,1×10-5, 1.5×10-5,2×10-5,5×10-5,1×10-4 mol/L |
 | 图6 肠道形态指标测量取点示意图 Schematic diagram of intestinal morphology |
由于牛奶样品中未检测出四环素,因此我们在牛奶样品中分别加入定量的盐酸四环素进行检测,检测结果如表2所示,回收率在97.5 %~105.2 %之间。由表中数据可知回收率较高,能够定量回收盐酸四环素。由此表明能够通过加样回收的测量检测牛奶样品中盐酸四环素的残留。同时验证了用镝荧光探针检测牛奶中的盐酸四环素的方法能有效、灵敏地检测牛奶中的盐酸四环素含量,灵敏度好并且选择性高。
| 表2 牛奶样品的检测结果 The test results of milk samples |
本文首先选定磺基水杨酸作为配体敏化稀土离子镝的发光,TOPO为协配体,研究了磺基水杨酸、TOPO和稀土离子镝形成的三元配合物体系的荧光光谱特性及实验条件对荧光强度的影响。在Dy3+浓度为1×10-4 mol/L,镝离子与磺基水杨酸和TOPO的浓度比为1∶2∶0.1的最佳条件下,配合物荧光体系可发射镝离子的强特征荧光,其最大的激发和发射波长为305 nm和574 nm。在最佳条件下,以磺基水杨酸和TOPO同稀土离子镝形成的配合物作荧光探针对盐酸四环素标准溶液进行检测。在10-6~2×10-5 mol/L浓度范围内,盐酸四环素浓度与荧光强度呈良好的线性关系,盐酸四环素的检测上限为5×10-5 mol/L,检测下限为10-6 mol/L。通过加样回收实验和干扰实验可知,以稀土离子镝为荧光探针,对盐酸四环素有较高的回收率。因此以Dy3+-SSA-TOPO形成的络合物作为稀土离子荧光探针,能够快速检测出盐酸四环素抗生素,并且具有灵敏度高和选择性好的优点。
| [1] | Yin H Q, Kim M, Kim J H, Kong G, Lee M O, Kang K S, Yoon B I, Kim H L, Lee B H. Hepatic gene expression profiling and lipid homeostasis in mice exposed to steatogenic drug, tetracycline[J]. Toxicological Sciences, 2006, 94(1): 206-216. |
| [2] | Labbe G, Fromenty B, Freneaux E, Morzell V, Letteron P, Berson A, Pessayre D. Effects of various tetracycline derivatives on in vitro and in vivo β-oxidation of fatty acids, egress of triglycerides from the liver, accumulation of hepatic triglycerides, and mortality in mice[J]. Biochemical Pharmacology,1991, 41(4): 638-641. |
| [3] | Fréneaux E, Labbe G, Letteron P, Dinh T L, Degott C, Genève J, Larrey D, Pessayre D. Inhibition of the mitochondrial oxidation of fatty acids by tetracycline in mice and in man: possible role in microvesicular steatosis induced by this antibiotic[J]. Hepatology, 1988, 8(5): 1056-1062. |
| [4] | Carson M C, Ngoh M A, Hardley S W. Confirmation of multiple tetracycline residues in milk and oxytetracycline in shrimp by liquid chromatography-particle beam mass spectrometry [J]. Journal of Chromatography B,1998, 712(1-2): 113-128. |
| [5] | Furusawa N. Rapid liquid chromatographic determination of oxytetracycline in milk [J]. Journal of Chromatography A,1999, 839(1-2): 247-251. |
| [6] | 高福凯,陈璐思,刘永明,刘振波,李桂芝. 四环素类药物在水产品中的存在形态研究及其分析应用[J].分析化学,2013, 41(2): 273-277. Gao F K, Chen L S, Liu Y M, Liu Z B, Li G Z. Study on the Form of Tetracycline Antibiotics in Aquatic Products and Its Analytical Application [J]. Chinese Journal of Analytic Chemistry, 2013, 41(2):273-277. |
| [7] | Tang C M, Yu Y Y, Huang Q X, Peng X Z. Simultaneous determination of fluoroquinolone and tetracycline antibacterials in sewage sludge using ultrasonic-assisted extraction and HPLC-MS/MS [J]. International Journal of Environmental Analytical Chemistry,2012, 92(12): 1389-1402. |
| [8] | 张琰图,章竹君,孙永华. 高效液相色谱化学发光法检测牛奶中残留四环素类化合物的研究[J]. 化学学报, 2006, 64(24): 2461-2466. Zhang Y T, Zhang Z J, Sun Y H, Determination of Tetracyclines Residues in Milk Using High Performance Liquid Chromatography with Chemiluminescence Detection[J]. Acta Chimica Sinica, 2006, 64(24): 2461-2466. |
| [9] | 高 红,赵一兵,郭祥群. 一种测定四环素抗生素的光谱新方法[J]. 光谱学与光谱分析,2006, 26(3): 488-490. Gao H, Zhao Y B, Guo X Q. Determination of Tetracyclines by a New Spectrum Technique[J]. Spectroscopy and Spectral Analysis, 2006, 26(3): 488-490. |
| [10] | Wang S, Yong W, Liu J H, Zhang L Y, Chen Q L, Dong Y Y. Development of an indirect competitive assay-based aptasensor for highly sensitive detection of tetracycline residue in honey[J]. Biosensors and Bioelectronics, 2014, 57: 192-198. |
| [11] | Moeller N, Mueller-Seitz E, Scholz O, Hillen W, Bergwerff A A, Petz M. A new strategy for the analysis of tetracycline residues in foodstuffs by a surface plasmon resonance biosensor [J]. European Food Research and Technology, 2007, 224(3): 285-292. |
| [12] | 姜小明, 张文倩, 宋 磊, 赵 濉.荧光探针法研究连接基团对双子型阳离子表面活性剂聚集行为的影响[J]. 影像科学与光化学,2013, 31(1): 63-68. Jiang X M, Zhang W Q, Song L, Zhao S. Effect of the nature of the spacer on the aggregation properties of cemini cationic surfactants in the aqueous solution investigation by fluoresence[J]. Imaging Science and Photochemistry, 2013, 31(1): 63-68. |
| [13] | Tang J, Hewitt I, Madhu N T, Chastanet G, Wernsdorfer W, Anson C E, Benelli C, Sessoli R, Powell A K. Dysprosium triangles showing single-molecule magnet behavior of thermally excited spin states[J]. Angewandte Chemie International,2006, 45(11): 1729-1733. |
| [14] | 宋玉民,吴锦绣. 稀土芦丁配合物的合成、表征及与血清白蛋白的相互作用[J]. 无机化学学报,2006, 22(12): 2165-2172. Song Y M, Wu J X. Synthesis, Characterization and interaction of rare earth complexes of rutin with HSA and BSA[J]. Chinese Journal of Inorganic Chemistry,2006, 22(12): 2165-2172. |
| [15] | Li L, Li B X, Chena D, Mao L H. Visual detection of melamine in raw milk using gold nanoparticles as colorimetric probe [J]. Food Chemistry,2010, 122(3): 895-900. |
| [16] | Kragh-Hansen U. Molecular aspects of ligand binding to serum albumin[J]. Pharmacological Reviews,1981, 33: 17-53. |




