半导体光催化剂因其在新能源制备及污染物降解等方面具有很大的应用潜力而受到越来越多的关注[1]。到目前为止,已有一百三十多种半导体被用作光催化剂,实现光催化降解过程。TiO2、ZnO等金属氧化物半导体因其较强的化学稳定性,得到了人们的广泛关注[2,3,4]。但是,这种半导体的价带由O2p轨道组成,其导带由一种或多种金属价壳层轨道组成[5],因此,能带宽度较大(一般大于3 eV),只能吸收占太阳光能量4%的紫外光,导致基于这种半导体的光催化剂的效率依然较低。因此,亟需发展能够在可见光或者整个太阳能光谱中都能工作的光催化剂[6]。
目前,制备可见光光催化剂最常用的方法是用敏化剂(例如:染料、量子点)来敏化TiO2、ZnO等宽带隙半导体[7,8];或者通过掺杂的方法来调制这些宽带隙半导体的能带,使能带缩小以吸收可见光[9,10]。通过这些方法,宽带隙半导体的光吸收能力虽然有所提高,但是其光催化效率还不够高,同时又带来了敏化剂不稳定的问题。另外一种制备可见光光催化剂的策略是直接利用窄带隙半导体(例如:α-Fe2O3、Cu2O、CdSe)作为光催化剂[11,12]。但是,这些窄带隙半导体在水相环境中不稳定,容易被光腐蚀[13]。因此,需要寻找新的材料体系来制备高效、稳定的可见光光催化剂。
硅是一种储量丰富,对环境友好的材料。特别是由于其较窄的带隙(1.12 eV),使其具有很强的可见光吸收能力。进一步利用纳米技术得到的硅纳米线阵列,具有减反效应及光自陷效应[14],并且对入射光角度不敏感,可以使吸光效率增加至同厚度平面材料的70倍以上,吸收光谱拓宽至1100 nm[15],因此成为一种备受关注的可见光光催化材料。同时,研究表明,硅作为一种间接带隙半导体,其激发态单重态激子具有特别长的寿命[16,17],因此,在溶液中,硅纳米结构中处于三重态的激子将有可能像染料敏化剂一样,将能量转移给氧气分子(O2),使O2中的电子自旋翻转而被激发为单重态氧1O2[18,19],从而提高降解污染物的效率。但是,硅纳米线阵列作为光催化剂时,最大问题在于其表面不稳定,在水相环境中极易发生光腐蚀,这限制了其在光催化体系中的应用[20]。
在目前的研究中,为了提高基于硅纳米线阵列的光催化剂的稳定性,有研究通过ALD、PECVD等方法在硅纳米线表面修饰贵金属Pt或TiO2等无机半导体材料[21,22]。但是,由于硅纳米线阵列中的硅纳米线分布十分密集,这种昂贵的修饰方法并不能很好地保证硅纳米线被有效包覆,同时,将TiO2等无机半导体材料修饰于硅纳米线表面,还容易带来两种材料间的晶格错位等问题,从而使光催化剂的稳定性及效率均受到影响。另外,这种昂贵的修饰方法及材料显然不能被大规模应用。因此,必须找到新的修饰材料及方法,构造高效稳定的基于硅纳米线阵列的可见光光催化剂。
为了解决以上问题,本工作提出了一种制备基于硅纳米线阵列的可见光光催化剂的策略,这种策略包括两个步骤:首先,将稳定的导电高分子聚(乙撑二氧噻吩)(PEDOT)通过电聚合的方法,包覆于硅纳米线阵列的表面,以提高硅纳米线的稳定性;之后,在表面稳定的硅纳米线阵列上进一步修饰具有等离子体效应的银纳米颗粒(AgNPs),以提高光催化剂的光吸收能力。基于以上策略,我们构建了由AgNPs及PEDOT修饰的硅纳米线阵列(AgNPs/PEDOT/SiNW)的可见光光催化剂,并以罗丹明B(RhB)为模型化合物,研究了该光催化剂的光催化能力。通过研究不同PEDOT修饰厚度及AgNPs担载量对光催化剂的光催化效率的影响,得到了具有最佳光催化能力的光催化剂,并得出了导电高分子修饰厚度、具有等离子体效应的金属纳米颗粒对光催化剂的光催化效率的影响关系。 1 实验部分 1.1 样品的制备
实验中所用的硅纳米线阵列采用文献中普遍使用的金属辅助催化法制得[23]。N型硅片首先用去离子水和丙酮清洗干净,然后在H2SO4(97%) 与H2O2(35%) (V/V=3/1)的混合液中浸泡10 min以去除硅片上所沾染的有机物。洗涤干净的硅片在HF-AgNO3的刻蚀液中,在50℃的水浴中进行刻蚀,HF浓度为5 mol/L,AgNO3的浓度为0.02 mol/L。刻蚀一定时间后(13 min得到10 μm长硅纳米线阵列),将硅片从刻蚀液中取出,用去离子水冲掉附着的絮状物后,将硅片放入王水中浸泡1 h以去除硅纳米线上附着的银。当附着的银在王水中被完全去除后,用水和丙酮将硅纳米线阵列冲洗干净备用。刻蚀好的硅纳米线用HF处理,得到H末端处理的硅纳米线阵列(H-SiNW)。
H-SiNW阵列用水和乙醇清洗干净,吹干后放入电聚合溶液中。电聚合PEDOT过程中,单体EDOT溶于0.01 mol/L的高氯酸锂(LiClO4)乙腈溶液中,采用三电极体系用循环伏安法在H-SiNW阵列表面聚合PEDOT。其中,H-SiNW阵列为工作电极,饱和甘汞电极为参比电极,铂网为对电极。在电聚合过程中,始终向溶液中鼓入氮气,以除去溶液中的氧气。循环伏安法的窗口电压为+1.4 V(vs.SCE)至0.4 V(vs.SCE),扫描速度为100 mV/s。可通过扫描次数来调节PEDOT层的厚度,达到预期厚度后,将修饰后的硅纳米线阵列从溶液中取出,用乙腈冲洗几次,以去除留在硅纳米线阵列上的未聚合的EDOT单体。
银纳米颗粒通过还原金属盐的方法沉积到PEDOT修饰的硅纳米线阵列上。PEDOT修饰的硅纳米线阵列首先浸入柠檬酸钠与硝酸银的水/乙醇混合液中,柠檬酸钠的浓度为:0.2~2 mmol/L,硝酸银的浓度为:0.1~1 mmol/L,水与乙醇的体积比为1比4。在持续搅拌的条件下,将还原剂硼氢化钾加入溶液中,反应在硅纳米线表面生成银纳米颗粒并附着于硅纳米线上。反应后,用水、乙醇冲洗硅纳米线阵列,以去除没有紧密附着的银纳米颗粒。通过改变柠檬酸钠与硝酸银的浓度,调整光催化剂上银纳米颗粒的担载量。 1.2 光催化反应
图1描述了评价光催化剂的光催化能力的方法。光催化过程在室温下进行,氙灯作为光源,调节反应容器与氙灯间的距离,使照射在光催化剂上的光强度达到100 mW·cm-2。基于硅纳米线阵列的光催化剂被切成0.5 cm×0.5 cm 大小,用铁丝固定使之悬于装有3 mL的RhB溶液(2 μmol/L)的石英比色皿中。在实验过程中,始终用磁子对溶液进行搅拌。在光降解实验之前,在暗处将催化剂置于反应体系中并搅拌2 h,以达到催化剂表面的吸附平衡。光催化过程中,经过固定的时间间隔后,将光催化剂从溶液中取出,并用Hitachi UV-3010分光光度计测试溶液的UV-Vis吸收光谱。用RhB的特征峰(553 nm)的强度来表示RhB的浓度,用实时测得的RhB的峰值与光催化降解前RhB的峰值的比值来表示光催化剂的实时光催化降解能力。在测试光催化剂稳定性的实验中,光催化剂完成特定时间的光催化反应后,将其从溶液中取出,用水、乙醇冲洗以去除吸附在光催化剂上的RhB,之后再将该光催化剂放入新鲜的RhB溶液中进行同样条件下的光催化降解测试。
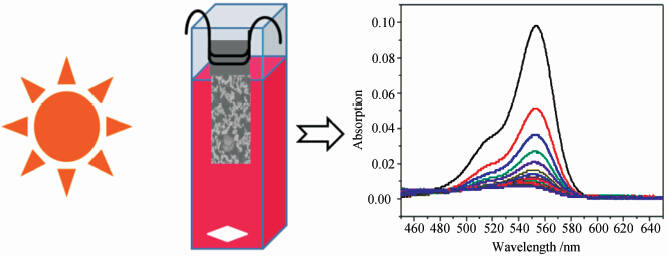 | 图1 光催化降解RhB的过程及评价光催化程度的方法 Schematic diagram of the photodegradation process |
图2a为金属辅助催化法制得的硅纳米线阵列的断面的SEM图片。刻蚀好的硅纳米线用HF处理,得到H末端处理的硅纳米线阵列(H-SiNW)。可以看到,硅纳米线均垂直于硅基底之上,长度约为10 μm。图2b为AgNPs/PEDOT/SiNW的SEM图片。PEDOT通过电化学聚合的方法沉积到H-SiNW的表面,通过改变循环伏安的次数可以调节其厚度。PEDOT是一种惰性稳定的导电高分子,据文献报道可以增强半导体在水溶液中的稳定性。图2c为H-SiNW阵列表面循环伏安法电聚合PEDOT的I-V曲线。循环伏安从1.4 V (vs. SCE)开始向负方向扫描到0.4 V (vs. SCE)后折返,终止于1.4 V(vs. SCE),扫描速度为100 mV/s。图中所示为循环伏安法扫描5圈的I-V曲线。为了确定PEDOT对硅纳米线表面的修饰,PEDOT电聚合的硅纳米线样品通过傅里叶变换红外光谱仪(Excalibur 3100)进行测试。图2d为PEDOT修饰的硅纳米线的红外光谱,628 cm-1处的峰由C—S键的振动引起,1083 cm-1、1111 cm-1及1145 cm-1处的峰由二氧乙烯基的C—O—C键的伸缩引起,1628 cm-1处的峰由噻吩环中的CC键的振动引起。相较于裸硅线的红外光谱,这些特征峰确认了硅纳米线上PEDOT的包覆。
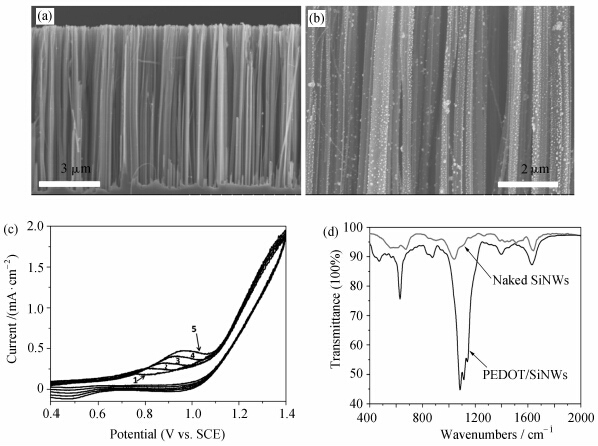 | 图2 (a)为金属辅助催化法制得的硅纳米线阵列的断面的SEM图;(b)为H-SiNW经过修饰后的样品AgNPs/PEDOT/SiNW的SEM图;(c)为H-SiNW阵列表面循环伏安法电聚合PEDOT的I-V曲线;(d)为PEDOT修饰的硅纳米线的红外光谱 (a) Cross-section SEM image of the H-SiNW arrays;(b) Cross-section SEM image of the AgNPs/PEDOT/SiNW arrays; (c) Repeated cyclic voltammograms recorded the first 10 cycles of electro-polymerizaion of PEDOT; (d) The IR of the naked Si nanowires and PEDOT modified Si nanowires |
由于未修饰的H-SiNW阵列在水相环境中不稳定,容易被光腐蚀。为了保证数据的可靠性,我们首先检验了未修饰的H-SiNW 阵列及AgNPs/PEDOT/SiNW阵列降解RhB过程的稳定性。依据之前所述的光催化降解RhB的实验方法,得到了H-SiNW 阵列及AgNPs/PEDOT/SiNW阵列作为光催化剂时的降解曲线(图3)。
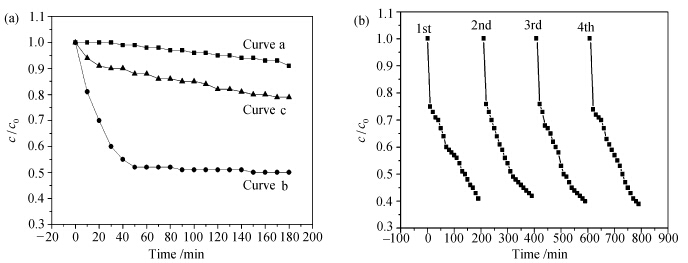 | 图3 (a)曲线a 为RhB在没有光催化剂的情况下自然降解的情况,曲线b和曲线c分别表示H-SiNW 阵列作为光催化剂 在第一轮和第二轮进行降解反应时的降解情况;(b)AgNPs/PEDOT/SiNW样品的光催化能力及稳定性测试 (a) RhB’s nature photodegradation without photocatalyst (curve a); RhB’s photodegradation with H-passivated SiNW arrays as photocatalyst in the 1st cycle (curve b) and in the 2nd cycle (curve c);(b) Stability performance of the AgNPs/PEDOT/SiNW arrays photocatalyst |
如图3所示,在光催化降解RhB过程中,基于硅纳米线阵列的光催化剂均表现出一定的光催化能力。图3(a)中,曲线a为RhB在没有光催化剂的情况下自然降解的情况,可见在没有光催化剂的情况下,RhB在180 min内只有约为5%的降解量。曲线b和曲线c分别表示了H-SiNW 阵列作为光催化剂在第一轮和第二轮进行降解反应时的降解情况。在H-SiNW阵列进行第一次光催化降解RhB的反应中,180 min内,RhB的降解量达到51%(曲线b)。当将该催化剂冲洗干净后置于相同的RhB溶液中,进行第二次降解反应时,180 min后,RhB的降解量只有20%(曲线c)。两次降解反应中,H-SiNW阵列的降解能力的显著降低,这表明未修饰的H-SiNW 阵列在水相环境中极不稳定。因此在利用H-SiNW 阵列为光催化剂的光催化降解实验中,每一轮实验完成后,都用HF对其进行处理后,再进行下一轮实验。
图3(b)为H-SiNW 阵列经过修饰后所得到的样品AgNPs/PEDOT/SiNW 阵列的光催化降解RhB的情况。可以看出,用PEDOT和AgNPs修饰后的样品表现出最强的光催化降解能力,在180 min内,降解量达到60%。对该样品进行稳定性实验,可以看出,同一样品经过4轮共800 min的光催化降解实验,其降解能力并未发生改变。结果表明,PEDOT能保护H-SiNW阵列不被光腐蚀,使其具有良好的稳定性。同时,PEDOT及AgNPs还能提高光催化剂的光催化能力。 2.3 不同银纳米颗粒担载量对AgNPs/PEDOT/SiNW阵列的光催化性能的影响
上述结果已经显示,通过PEDOT及AgNPs的修饰后的硅纳米线阵列的光催化能力及稳定性都有很大的提高。为了得到最优化修饰条件,我们研究了具有不同银纳米颗粒担载量及不同PEDOT膜厚度的AgNPs/PEDOT/SiNW阵列样品的光催化效率。图4为具有不同银纳米颗粒担载量的AgNPs/PEDOT/SiNW光催化剂的SEM图片及其光催化效率。为了保证光催化剂的稳定性,我们首先将SiNW用相同厚度的PEDOT进行修饰,之后,通过改变银纳米颗粒沉积过程中金属盐、表面活性剂及还原剂的浓度,控制AgNPs/PEDOT/SiNW光催化剂的银纳米颗粒的担载量。
 | 图4 具有不同银纳米颗粒担载量的AgNPs/PEDOT/SiNW光催化剂的SEM图及其光催化效率 a为PEDOT修饰H-SiNW阵列后,没有进一步担载银纳米颗粒的样品的SEM图;b为银纳米颗粒担载量极少的样品的SEM图; 随着反应物浓度的提高,AgNPs/PEDOT/SiNW光催化剂上银纳米颗粒的担载量逐渐增多(c~e);f为具有不同银纳米颗粒担载量的光催化剂的k值 (a-e) Cross-section SEM images of five SiNWs array based photocatalysts with the same PEDOT coating and different loading of AgNPs;(f) The rate constant k of RhB photodegradation using different SiNWs array based photocatalysts |
图4a为PEDOT修饰H-SiNW阵列后,没有进一步担载银纳米颗粒的样品的SEM图(样品a)。图4b为银纳米颗粒担载量极少的样品的SEM图,在该样品中,只有在硅纳米线尖端处有少量的银纳米颗粒(样品b)。随着金属盐、表面活性剂及还原剂浓度的提高,光催化剂上银纳米颗粒的担载量逐渐增多(图c至图e)。图4c所示的样品除了尖端的银纳米颗粒量有所增多外,在纳米线阵列内部也有少量银纳米颗粒的分部(样品c)。图4d所示的样品从纳米线阵列的尖端到内部均有大量的银纳米颗粒均匀的担载(样品d),通过对SEM图上的AgNPs进行计数,显示银纳米颗粒的密度达到80颗/μm2。随着反应物浓度的进一步增加,在图4e所示的样品中,银纳米颗粒大量的在硅纳米线尖端聚集成了较大的块状物(样品e)。
为了更清楚地比较这几个样品的光催化效率,我们对光催化过程的数据进行了进一步处理,用一级动力学方程对光催化过程进行拟合,得到ln(c/c0)与时间的关系,拟合所得的直线的斜率即为一级动力学常数k值[24]。图4f列出了不同样品的k值。实验结果显示,随着银纳米颗粒的担载量的增加,k值逐渐增加。当银纳米颗粒在硅纳米线阵列上均匀分布,且担载量达到80颗/μm2时(样品d),光催化剂表现出了最高的光催化能力,而当银纳米颗粒沉积反应的反应物浓度进一步增加,银纳米颗粒在硅纳米线尖端聚集成块时(样品e),k值减小。
由文献研究可知,AgNPs具有最强的表面等离子体效应,常被用于光催化剂及光伏电池材料的制备中,通过表面等离子体共振效应来提高半导体材料的光吸收能力[25,26]。并且,理论研究表面,AgNPs的表面等离子体共振还可直接将硅材料的价电子激发至导带而无需生子辅助[27]。因此,当用银纳米颗粒修饰表面稳定后的硅纳米线阵列时,由于光吸收能力的增强,光催化剂的效率增大。但是,当纳米颗粒在硅纳米线阵列尖端聚集成大颗粒时,影响到硅纳米线对光的吸收,使光催化能力下降。因此,当银纳米颗粒对表面稳定后的硅纳米线表面均匀全面修饰时,光催化剂的光催化能力达到最大值。 2.4 基于不同PEODT厚度的AgNPs/PEDOT/SiNW阵列的光催化剂的性能研究
PEDOT是一种化学稳定的具有高导电性的导电高分子,可用于修饰半导体表面以增强其在水相中的稳定性。为了得到最优化的PEDOT厚度,我们研究了具有不同PEDOT厚度的AgNPs/PEDOT/SiNW光催化剂的光催化性能。图5显示了具有不同PEDOT厚度的AgNPs/PEDOT/SiNW光催化剂的TEM图片及其光催化效率。
 | 图5 具有不同PEDOT厚度的AgNPs/PEDOT/SiNW光催化剂的TEM图及其光催化效率 a为没有修饰PEDOT的硅纳米线的TEM图;随着电聚合过程中循环伏安法的次数的不同,包覆于硅纳米线表面的 PEDOT层的厚度也随之不同(b~e);f为具有不同PEDOT厚度的光催化剂的k值 a: TEM images of H-SiNW which is not coated with PEDOT; b-e: TEM images of five AgNPs/PEDOT/SiNW photocatalysts with the same loading of AgNPs and different PEDOT thickness;f: The rate constant k of RhB photodegradation using different SiNWs array based photocatalysts |
图5a为没有修饰PEDOT的硅纳米线的TEM图。在对硅纳米线阵列表面电聚合沉积PEDOT的过程中,随着电聚合过程中循环伏安法的次数的不同,包覆于硅纳米线表面的PEDOT层的厚度也随之不同(见图5b至图5e)。循环伏安法循环数分别为5圈、10圈、15圈、20圈时,PEDOT厚度分别约为2 nm、4 nm、6 nm、8 nm。PEDOT修饰完成后,再向表面修饰的硅纳米线阵列上修饰同样担载量的银纳米颗粒。最终得到的PEDOT层厚度分别为8 nm、6 nm、4 nm、2 nm的样品,分别被记为样品b′、样品c′、样品d′、样品e′。依照之前所述的数据处理方法,各样品的光催化过程的动力学常数k列于图5f中。
实验表明,随着PEDOT厚度的减小,光催化能力有所增加,在PEDOT厚度2 nm处达到了最大值。这个结果可能是由于在PEDOT膜中载流子的迁移率与膜上的电势梯度有关。在相同的溶液中,PEDOT膜两侧的电势差是一定的,因此,当其厚度越薄,电势梯度就越大,越有利于载流子从光催化剂中导出。这不仅能促使光催化剂产生更多的光生载流子,同时也抑制了激子通过能量转移而失活的过程,使得光催化剂的光催化能力达到最大。 3 结论
本工作提出并证实了一种制备基于硅纳米线阵列的可见光光催化剂的策略。该策略包括两步:第一步为用稳定的导电高分子聚(乙撑二氧噻吩)(PEDOT)修饰硅纳米线阵列,以提高其稳定性;第二步为在表面稳定的硅纳米线阵列上进一步修饰具有等离子体效应的银纳米颗粒(AgNPs),以提高光催化剂的光催化效率。我们以RhB为模型化合物,研究了由AgNPs及PEDOT修饰的硅纳米线阵列的可见光光催化剂的光催化能力,并通过研究不同PEDOT修饰厚度及AgNPs担载量对光催化剂的光催化效率的影响,得到了具有最佳光催化能力的光催化剂。实验表明,当AgNPs对由2 nm厚的PEDOT修饰的硅纳米线阵列均匀修饰,并达到80颗/μm2的担载量时,基于硅纳米线阵列的光催化剂可达到最佳光催化能力。这种先用导电高分子保护,再用具有等离子体效应的金属纳米颗粒活化的修饰策略,还可应用到其他窄带隙半导体的光催化剂的构筑中。
| [1] | Hoffmann M R, Martin S T, Choi W, Bahneman D W. Environmental applications of semiconductor photocatalysis[J]. Chemical Reviews, 1995, 95(1): 69-96. |
| [2] | Fujishima A, Honda K. Fabrication of anatase-type TiO2 films by reactive pulsed laser deposition for photocatalyst application[J]. Nature, 1972, 37(253): 238-240. |
| [3] | Kuo T J, Lin C N, Kuo C L, Huang M H. Growth of ultralong ZnO nanowires on silicon substrates by vapor transport and their use as recyclable photocatalysts[J]. Chemistry of Materials, 2007, 19(21): 5143 5147. |
| [4] | Wu H B, Hng H H, Lou X W. Direct synthesis of anatase TiO2 nanowires with enhanced photocatalytic activity[J]. Advanced Materials, 2012, 24(19): 2567 2571. |
| [5] | Puurunen R L. Surface chemistry of atomic layer deposition: a case study for the trimethylaluminum/water process[J]. Journal of Applied Physics, 2005, 97(12): 121301. |
| [6] | Tong H, Ouyang S, Bi Y, Umezawa N, Oshikiri M, Ye J. Nano-photocatalytic materials: possibilities and challenges[J]. Advanced Materials, 2012, 24(2): 229-251. |
| [7] | Li J, Hoffmann M W G, Shen H, Fabrega C, Prades J D, Andreu T, Hernandez-Ramirez F, Mathur S. Enhanced photoelectrochemical activity of an excitonic staircase in CdS@ TiO2 and CdS@ anatase@ rutile TiO2 heterostructures[J]. Journal of Materials Chemistry, 2012, 22(38): 20472-20476. |
| [8] | Lee Y L, Chi C F, Liau S Y. CdS/CdSe Co-sensitized TiO2 photoelectrode for efficient hydrogen generation in a photoelectrochemical cell[J]. Chemistry of Materials, 2010, 22(3): 922-927. |
| [9] | Ang T P, Toh C S, Han Y F. Synthesis, characterization, and activity of visible-light-driven nitrogen-doped TiO2-SiO2 mixed oxide photocatalysts[J]. The Journal of Physical Chemistry C, 2009, 113(24): 10560-10567. |
| [10] | Sakthivel S, Kisch H. Daylight photocatalysis by carbon-modified titanium dioxide[J]. Angewandte Chemie International Edition, 2003, 42(40): 4908-4911. |
| [11] | Somasundaram S, Chenthamarakshan C R N, Tacconi N R, Rajeshwar K. Photocatalytic production of hydrogen from electrodeposited p-Cu2O film and sacrificial electron donors[J]. International Journal of Hydrogen Energy, 2007, 32(18): 4661-4669. |
| [12] | Frame F A, Carroll E C, Larsen D S, Sarahan M, Browning N D, Osterloh F E. First demonstration of CdSe as a photocatalyst for hydrogen evolution from water under UV and visible light[J]. Chemical Communications, 2008, 13(19): 2206-2208. |
| [13] | Chen X, Shen S, Guo L, Mao S. S. Semiconductor-based photocatalytic hydrogen generation[J]. Chemical Reviews, 2010, 110(11): 6503-6570. |
| [14] | Garnett E, Yang P. Light trapping in silicon nanowire solar cells[J]. Nano Letters, 2010, 10(3): 1082 1087. |
| [15] | Kelzenberg M D, Boettcher S W, Petykiewicz J A, Turner-Evans D B, Putnam M C, Warren E L, Spurgeon J M, Briggs R M, Lewis N S, Atwater H A. Enhanced absorption and carrier collection in Si wire arrays for photovoltaic applications[J]. Nature Materials, 2010, 9(3): 239-244. |
| [16] | Kovalev D, Heckler H, Polisski G, Koch F. Optical properties of Si nanocrystals[J]. Physica Status Solidi(b), 1999, 215(2): 871. |
| [17] | Cullis A G., Canham L T, Calcott P D J. The structural and luminescence properties of porous silicon[J]. Journal of Applied Physics, 1997, 82(3): 909. |
| [18] | Fujii M, Nishimura N, Fumon H, Hayashi S, Kovalev D, Diener B G J. Dynamics of photosensitized formation of singlet oxygen by porous silicon in aqueous solution[J]. Journal of Applied Physics, 2006, 100(12): 124302. |
| [19] | Xiao L, Gu L, Howell S B, Sailor M J. Porous silicon nanoparticle photosensitizers for singlet oxygen and their phototoxicity against cancer cells[J]. ACS Nano, 2011, 5(5): 3651-3659. |
| [20] | Shao M, Cheng L, Zhang X, Ma D D D, Lee S T. Excellent photocatalysis of HF-treated silicon nanowires[J]. Journal of the American Chemical Society,2009, 131(49): 17738-17739. |
| [21] | Dasgupta N P, Liu C, Andrews S, Prinz F B, Yang P. Atomic layer deposition of platinum catalysts on nanowire surfaces for photoelectrochemical water reduction[J]. Journal of the American Chemical Society,2013, 135(35): 12932-12935. |
| [22] | Chen Y W, Prange J D, Dühnen S, Park Y, Gunji M, Chidsey C E D, McIntyre P C. Atomic layer-deposited tunnel oxide stabilizes silicon photoanodes for water oxidation[J]. Nature Materials, 2011, 10(7): 539-544. |
| [23] | Peng K Q, Yan Y J, Gao S P, Zhu J. Synthesis of large-area silicon nanowire arrays via self-assembling nanoelectrochemistry[J]. Advanced Materials, 2002, 16(14): 1164. |
| [24] | Fu H, Pan C, Yao W, Zhu Y. Visible-light-induced degradation of rhodamine B by nanosized Bi2WO6[J]. The Journal Physical Chemistry B, 2005, 109(47): 22432-22439. |
| [25] | Schuller J A, Barnard E S, Cai W, Jun Y C, White J S, Brongersma M L. Plasmonics for extreme light concentration and manipulation[J]. Nature Materials, 2010, 9(3): 193-204. |
| [26] | Lee J, Mubeen S, Ji X, Stucky G D, Moskovits M. Plasmonic photoanodes for solar water splitting with visible light[J]. Nano Letters, 2012, 12(9): 5014-5019. |
| [27] | Kirkengen M, Bergli J, Galperin Y M. Direct generation of charge carriers in c-Si solar cells due to embedded nanoparticles[J]. Journal of Applied Physics, 2007, 102(9): 093713. |




