2. 大连大学 辽宁省生物有机化学重点实验室, 辽宁 大连 116622;
3. 大连大学 环境与化学工程学院, 辽宁 大连 116622
2. Liaoning Key Laboratory of Bio-organic Chemistry, Dalian University, Dalian 116622, P. R. China;
3. College of Environmental and Chemical Engineering, Dalian University, Dalian 116622, P. R. China
蛋白质、核酸、多糖等大分子物质在细胞内的浓度很高,使得细胞内的环境是高度拥挤的,大分子在细胞内的浓度可高达80~400 g/L[1],能占细胞总容积的20%~30%[2],由于排斥容积效应,任何可增加可用容积的反应都能被大分子拥挤试剂刺激发生[3,4,5,6]。在生物体内,大多数的生化反应都是在这种高度拥挤的环境中完成的,当蛋白存在于大分子拥挤环境中时,其微环境会发生改变,使得蛋白的结构及稳定性发生变化[2,7],从而使得蛋白的功能表达在拥挤试剂和稀溶液中不同。
生命体的重要组成部分——血红素类蛋白,在生命体中承担着极其重要的功能,例如作为生物催化剂、电子传递蛋白、氧载体和生物传感器等[8]。由于血红素类蛋白含有原卟啉Ⅸ辅基,故其能够吸收特定波长的光,光照通过影响血红素功能的表达而影响蛋白功能。关于光照射血红素类蛋白的研究已有报道,如血红蛋白、肌红蛋白、细胞色素P450、细胞色素C、细胞色素C氧化酶和辣根过氧化物酶等[9,10,11,12,13,14],但是这些研究是在稀溶液中进行的,忽略了生物体细胞内的拥挤环境。目前关于血红素类蛋白在高度拥挤环境下光照的研究还很少。
辣根过氧化物酶(Horseradish Peroxidase,HRP)是以铁卟啉为辅基的血红蛋白,辣根过氧化物酶能利用过氧化氢氧化一些有机和无机化合物,它与植物的呼吸作用、光合作用及生长素的氧化等都紧密相关,而且对氧自由基具有消除作用,减少过氧化物对植物体的毒害作用。辣根过氧化物酶在生物传感器[15]、环境监测、工业应用[16]等方面也发挥了很大的作用,广泛地运用于基因学、生理学及病理学研究中[17,18]。
我们最近研究了紫外-可见光诱导细胞色素C、高铁肌红蛋白[19,20]和HRP的还原及其机制,发现它们的光还原反应机制都是光诱导分子内电子转移。为了进一步了解光诱导血红素蛋白在细胞内环境中的还原过程,本文通过在光照体系中加入大分子拥挤试剂来模拟细胞内环境,研究了该条件下光诱导HRP的还原,利用紫外-可见吸收光谱、同步荧光光谱及圆二色谱等方法对拥挤环境中光照射HRP后其血红素中铁原子价态、蛋白构象及二级结构的变化进行了研究,确定了拥挤环境中HRP的最适光还原条件,分析了光照波长、温度、拥挤试剂浓度等对HRP光还原的影响。
1 实验部分 1.1 试剂与仪器辣根过氧化物酶(Horseradish Peroxidase,HRP)样品购自美国Sigma公司,使用时未经进一步提纯,溶解在0.05 mol/L的Na2HPO4-NaH2PO4 缓冲溶液(pH=7.4)中,配置成浓度为5×10-4 mol/L的蛋白溶液,蛋白溶液冷冻避光保存并尽快应用于实验。
Dextran70和Ficoll70购自上海生工公司,分别将大分子拥挤试剂Dextran70和Ficoll70溶解到pH 7.4的PB缓冲溶液中,使其终浓度达到50 g/L、100 g/L、200 g/L和400 g/L,实验用水为去离子水。
实验仪器主要有UV-Vis分光光度计(V-560,日本Jasco公司),荧光光谱仪(FP-6500,日本Jasco公司)和圆二色光谱仪(J-810,日本Jasco公司),制冷和加热循环器(F-12,德国Julabo公司),实验室pH计(PHSJ-4A,上海雷磁分析仪器厂),实验所用光源为荧光光谱仪的氙灯。
1.2 实验过程 1.2.1 样品处理取20 μL浓度为5×10-4 mol/L的HRP蛋白分别加入到1.98 mL PB缓冲液和已配好的Dextran70、Ficoll70溶液中,得到浓度为5×10-6 mol/L的HRP蛋白溶液,将蛋白样品置于10 mm石英比色池中,密封并持续通入N2,用荧光光谱仪中的氙灯进行光照,然后进行光谱测定。
1.2.2 光谱测定UV-Vis光谱测定:狭缝宽度2 nm,扫描波长范围220~700 nm,扫描速度200 nm/min,响应时间为中等,累计扫描3次。
荧光光谱测定:将拥挤试剂Dextran70和Ficoll70放入10 mm石英比色池中进行荧光光谱 测定,测定条件为:激发波长280 nm,激发和发射狭缝宽度均为5 nm,扫描速度为500 nm/min,响应时间为0.5 s,检测器灵敏度为中等,累计扫描3次。
同步荧光光谱测定:以Δλ=20 nm和Δλ=60 nm测定处理后样品的同步荧光光谱。激发和发 射狭缝均为5 nm,扫描速度为500 nm/min,响应时间为0.5 s,检测器灵敏度为中等,累计扫描3次。
圆二色光谱测定:狭缝宽度1 nm,扫描波长范围190~250 nm,扫描速度50 nm/min,响应时间1 s,累计扫描3次。
2 结果与讨论 2.1 稀溶液/拥挤环境中HRP的紫外-可见与同步荧光光谱在稀溶液中,辣根过氧化物酶在403 nm处的吸光度为0.43,在拥挤试剂Dextran70与Ficoll70中,HRP在403 nm处的吸光度分别为0.48和0.49,与稀溶液中的HRP蛋白在403 nm处的紫外吸收强度相比,拥挤试剂中的HRP蛋白在403 nm处的紫外吸收强度要强。这是由于拥挤试剂对血红素周围的环境有一定的影响,血红素在拥挤试剂中暴露较多,使得吸光度较强。HRP的紫外-可见吸收光谱见图1。
 | 图1 HRP的紫外-可见吸收光谱 The UV-Vis absorption spectra of HRP |
色氨酸残基和酪氨酸残基是蛋白质荧光的主要贡献因素[21]。利用同步荧光光谱可得到酪氨酸和色氨酸残基的特征峰。当选择Δλ=20 nm时显示的是酪氨酸残基的荧光峰,当选择Δλ=60 nm时表现的则是色氨酸残基的荧光峰,并且色氨酸残基的荧光强度和位置对其周围的环境是敏感的[22]。色氨酸残基的最大发射波长红移,表明其所处环境极性增加,疏水性降低,蛋白疏水结构瓦解,肽链伸展程度有所增加;蓝移则表明疏水性增加,分子趋于折叠状态[23]。我们可以根据这些现象来判断蛋白质的构象变化[21]。
在稀溶液中,Δλ=20 nm时(图2A),HRP的酪氨酸残基的荧光峰在305 nm处,Δλ=60 nm(图2B)时,HRP的色氨酸残基的荧光峰在344 nm处。由于拥挤试剂自身能够吸收一定波长的光而发射出荧光(图3),所以在稀溶液中加入拥挤试剂时,使得HRP蛋白溶液的荧光强度急剧增强,酪氨酸和色氨酸残基的荧光峰被掩盖。与相同浓度的Dextran70相比,Ficoll70的荧光强度更强(图3C)。
 | 图2 不同溶液中HRP的同步荧光光谱 Synchronous fluorescence spectra of HRP under different solutions (A)Δλ=20 nm,(B)Δλ=60 nm |
 | 图3 大分子拥挤试剂Dextran70和Ficoll70的同步荧光光谱(A)Δλ=20 nm; (B)Δλ=60 nm; (C)荧光光谱 Fluorescence spectra and synchronous fluorescence spectra of macromolecular crowding reagents |
辣根过氧化物酶在稀溶液与大分子拥挤试剂中采用403 nm单色光照射前后Soret带吸收峰面积变化情况如图4。从图可以看出,403 nm光照 射时,HRP在PB溶液及Dextran70溶液中可以发生光还原反应,而在Ficoll70溶液中没有发生光还原反应。在PB溶液中HRP蛋白随着光照时间的增长被光还原的量增多,而在Dextran70溶液中,光照0.5 h之内HRP蛋白被还原的量较多,随着光照时间的增长HRP蛋白被还原的量有所减少。辣根过氧化物酶在稀溶液与大分子拥挤试剂中,分别采用280 nm单色光照射前后其Soret带吸收峰面积变化情况如图5。从图中可以看出,HRP蛋白在拥挤试剂Dextran70和Ficoll70溶液中有利于光还原反应的发生,并且相同光照时间内,在Ficoll70溶液中HRP蛋白被光还原的量更多。HRP的光还原机理为光诱导的蛋白分子内电子转移,在拥挤条件下HRP蛋白光还原反应易于发生的主要原因是:拥挤试剂Dextran70和Ficoll70自身均能发射荧光,在Dextran70和Ficoll70溶液中HRP蛋白的光还原程度不同,也体现了这两种拥挤试剂光吸收和荧光发射的差异。这种差异是由拥挤试剂结构的不同造成的,Dextran70的持续长度约为0.4 nm,是一种无交联线性的、相对灵活的大分子聚合物,而Ficoll70具有高度交联的结构,是一种刚性共聚体。因此,当Dextran70与Ficoll70浓度相同时,Dextran70可以在溶液中形成准随机螺旋,从而容纳更多的间隙空间,排阻体积效应变小,吸收光能力变弱,使得其荧光发射强度较小,不利于HRP蛋白分子内电荷转移现象的发生。
 | 图4 24 ℃,403 nm光照射不同溶液中HRP其Soret带吸收峰面积的变化 The change of HRP absorption peak area at Soret band by irradiation with 403 nm at 24 ℃ under different solutions |
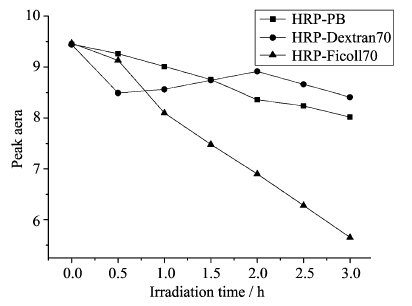 | 图5 24 ℃,280 nm光照射不同溶液中HRP其Soret带吸收峰面积的变化 The change of HRP absorption peak area at Soret band by irradiation with 280 nm at 24 ℃ under different solutions |
不同波长的光能量是不同的,对HRP的光还原情况不同,因此我们考察了拥挤条件下不同定波长光照射HRP溶液的光还原情况,图6A为在拥挤试剂Dextran70溶液中,分别用272、280、403和498 nm波长的光照射HRP蛋白样品后,其Soret带吸收峰面积随光照时间的变化。发现272和498 nm两种波长的光不能使HRP蛋白发生光还原反应。而280和403 nm两种波长的光照射HRP蛋白溶液可以使其发生光还原反应。图6B为在拥挤试剂Ficoll70溶液中,分别用280、403和498 nm波长的光照射HRP蛋白样品后,其Soret带吸收峰面积随光照时间的变化。发现只有280 nm波长的光照射蛋白溶液时能使HRP发生光还原反应。造成这种现象的原因是拥挤试剂Ficoll70在280 nm处有紫外吸收,采用280 nm波长的光照射HRP蛋白溶液,可以激发拥挤试剂Ficoll70发射荧光,从而诱导HRP发生还原。
 | 图6 拥挤条件下不同定波长光照射HRP溶液后其Soret带吸收峰面积的变化 The peak area change of HRP at Soret band after irradiation under different fixed irradiation wavelength in crowded conditions(A) Dextran70,(B) Ficoll70 |
温度的改变可引起HRP蛋白构象发生变化,而HRP蛋白构象的变化会影响其酶活性。为此我们考察了不同温度(4 ℃、24 ℃、44 ℃)对大分子拥挤环境中HRP光还原的影响。
在拥挤试剂Dextran70中(图7A),HRP蛋白溶液在4 ℃、24 ℃、44 ℃三种温度下采用403 nm单色光照射0.5 h后,其Soret带吸收峰面积减小都比较明显。在温度为24 ℃时,随着光照时间的增长,Soret带峰吸收峰面积趋于平缓,在温度为4 ℃和44 ℃时,随着光照时间的增长,Soret带吸 收峰面积越来越小,且4 ℃时Soret带峰面积减少更明显,说明在Dextran70大分子拥挤环境中,403 nm单色光照、 4 ℃时最有利于HRP光还原反应的发生。在拥挤试剂Ficoll70中(图7B),HRP蛋白溶液在4 ℃、24 ℃、44 ℃三种温度下采用280 nm单色光照射,随着光照时间的增加,其Soret带吸收峰面积逐渐减少,在24 ℃,Soret带吸收峰面积减少程度最明显,说明在拥挤试剂Ficoll70中,280 nm单色光照、24 ℃时,最有利于HRP光还原反应的进行。
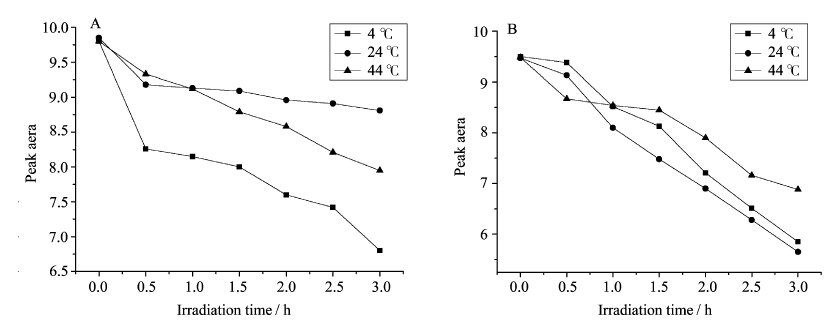 | 图7 不同温度下光照HRP其Soret带吸收峰面积随时间的变化 The change of HRP absorption peak area at Soret band after irradiation under different temperature (A)Dextran70-HRP,(B)Ficoll70-HRP |
图8为不同浓度大分子拥挤试剂中HRP光还原的情况。大分子拥挤试剂Dextran70浓度为100 g/L时,光照后HRP蛋白在Soret带吸收峰面积减少的最多,浓度为400 g/L时Soret带吸收 峰面积反而增加。说明Dextran70浓度为100 g/L 时光照还原HRP的能力最强。可能是Dextran70在较高浓度时使得HRP蛋白的血红素暴露增多,Soret带的吸收峰面积增大,且当Dextran70浓度达到200 g/L时会发生浓度荧光猝灭,其荧光发射强度降低,引起HRP光还原程度降低。在大分子拥挤试剂Ficoll70中,光照后HRP蛋白在Soret带吸收峰面积随着Ficoll70浓度的增大而逐渐减小,Ficoll70浓度为400 g/L时吸收峰面积减少的最多,即浓度为400 g/L时HRP的光还原能力最强。Ficoll70浓度增加其荧光发射强度则会逐渐增强,从而使HRP的光还原程度增大。
 | 图8 光照后不同浓度大分子拥挤试剂中HRP Soret带吸收峰面积的变化 The peak area change of HRP at Soret band after irradiation under different concentration of macromolecular crowded solutions |
某些反应引起的蛋白分子二级结构变化可以通过CD光谱进行检测,因此,我们选用远紫外区CD光谱对拥挤环境中光诱导HRP还原所引起的 蛋白二级结构的变化进行检测,进一步了解拥挤 环境中光诱导HRP蛋白的还原过程。不同光照时间HRP的远紫外CD光谱如图9。由图可知,稀溶液和拥挤试剂中的辣根过氧化物酶在208 nm和222 nm均表现出两个负峰,反映的是α-螺旋结构蛋白的特征谱带,随着光照时间的增加 (0.5 h、1 h、2 h、3 h)HRP在稀溶液与拥挤试剂中208 nm和222 nm的两个负峰未发生变化,说明光照时间内蛋白未变性,光照后蛋白的二级结构未发生改变。
 | 图9 不同溶液中HRP光照后的CD光谱 CD spectra of HRP under different solutions (A)PB-HRP,(B)Dextran70-HRP,(C)Ficoll70-HRP |
本文通过光谱法,对光诱导大分子拥挤环境中辣根过氧化物酶的还原过程进行了研究,结果表明大分子拥挤试剂对光还原HRP的电子传递过程及效率有影响。当采用403 nm单色光照射HRP蛋白溶液时,HRP在拥挤试剂葡聚糖70(Dextran70)中还原程度较好,而在聚蔗糖70(Ficoll70)拥挤环境下HRP不发生光还原反应;采用280 nm单色光照射时,在大分子拥挤试剂葡聚糖70(Dextran70)和聚蔗糖70(Ficoll70)环境中,HRP光还原反应得到促进,且大分子Ficoll70溶液对HRP光还原反应的促进作用更加明显;光诱导HRP还原的最适温度在Dextran70和Ficoll70溶液中分别为4 ℃和24 ℃,定波长280 nm光照射利于HRP还原;HRP在Dextran70溶液中的最适光还原浓度是100 g/L,在 Ficoll70环境中HRP还原程度随着Ficoll70浓度的增加增大;通过CD光谱可知光照射拥挤环境中HRP被还原后,其二级结构基本没有变化。
| [1] | Ellis R. Macromolecular crowding: obvious but underappreciated[J]. Trends in Biochemical Science, 2001, 26: 597-604. |
| [2] | Perham M, Stagg L, Wittung-Stafshede P. Macromolecular crowding increases structural content of folded proteins [J]. Febs Letters, 2007, 581(26): 5065-5069. |
| [3] | Zimmerman S B, Minton A P. Macromolecular crowding: biochemical, biophysical, and physiological consequences [J]. Annual Review of Biophysics and Biomological Structures, 1993, 22: 27-65. |
| [4] | Minton A P. Models for excluded volume interaction between an unfolded protein and rigid macromolecular cosolutes: macromolecular crowding and protein stability revisited[J]. Biophysical Journal, 2005, 88(2): 971-985. |
| [5] | Minton A P. Influence of macromolecular crowding upon the stability and state of association of proteins: predictions and observations [J]. Journal of Pharmaceutical Science, 2005, 94(8): 1668-1675. |
| [6] | Zhou H X. Protein folding and binding in confined spaces and in crowded solutions [J]. Journal of Molecular Recognition, 2004, 17(5):368-375. |
| [7] | Zhu J, He H W, Li S. Macromolecular crowding enhances thermal stability of rabbit muscle creatine kinase [J]. Tsinghua Science and Technology, 2008, 13(4): 454-459. |
| [8] | 林英武, 黄仲贤. 血红蛋白结构及功能相互转换[J]. 世界科技研究与发展, 2006, 28:8. Lin Y W, Huang Z X. Structural and functional conversion between hemoproteins[J]. World Science-Technology R & D, 2006, 28:8. |
| [9] | Pierre J, Bazin M, Debey P, Santus R. One-electron photoreduction of bacterial cytochrome P-450 by ultraviolet light. I. steady-state irradiations [J]. European Journal of Biochemistry, 1982, 124(3): 533-537. |
| [10] | Sakai H, Onuma H, Umeyama M, TAkeoka S, Tsuchida E. Photoreduction of methemoglobin by irradiation in the near-ultraviolet region [J]. Biochemistry, 2000, 39(47): 14595-14602. |
| [11] | Liang X Q, Chen G F, Zhang X, Liu S, Li G X. Study of UVA irradiation on hemoglobin in the presence of NADH [J]. Journal of Photochemistry and Photobiology B, 2008, 90(1): 53-56. |
| [12] | Vorkink W P, Cusanovich M A. Photoreduction of horse heart cytochrome c [J]. Photochemistry and Photobiology, 1974, 19(3): 205-215. |
| [13] | Masuda T, Minemura A, Yamauchi K, Kondo M. A mechanism of direct photoreduction of ferricytochrome c [J]. Journal of Radiation Research, 1980, 21(2): 149-156. |
| [14] | Winterle J S, Einarsdóttir ó. Photoreactions of cytochrome c oxidase [J]. Photochemistry and Photobiology, 2006, 82(3): 711-719. |
| [15] | 李 军, 王柯敏, 肖 丹, 羊小海. 改进溶胶-凝胶法固定酶结构剖析及在苯酚光化学传感器中的应用 [J]. 高等学校化学学报, 2000, 21(7): 1018-1022. Li J, Wang K, Xiao D, Yang X H. The microstructure analysis of enzymes immobilized by sol-gel method and its application in phenol optical chemical sensor[J]. Chemical Journal of Chinese University, 2000, 21(7): 1018-1022. |
| [16] | 周海峰, 杨东杰, 邱学青, 伍晓蕾. 辣根过氧化物酶改性木质素磺酸钠的结构特征及吸附分散性能 [J]. 高等学校化学学报, 2014, 35(4): 895-902. Zhou H F, Yang D J, Qiu X Q, Wu X L. Structural characterization, adsorption and dispersion properties of sodium lignosulfonate by horseradish peroxidase incubation[J]. Chemical Journal of Chinese University, 2014, 35(4): 895-902. |
| [17] | Taraban M B, Anderson M A. Magnetic field dependence of electron transfer and the role of electron spin in heme enzymes: horseradish peroxidase [J]. Journal of the American Chemical Society, 1997, 1199(24): 5768- 5769. |
| [18] | Baek H K, Van Wart H E. Elementary steps in the formation of horseradish peroxidase compound I: direct observation of compound 0, a new intermediate with a hyperporphyrin spectrum[J]. Biochemistry, 1989, 28(14):5714-5719. |
| [19] | 顾晓天, 吴晓红, 周家宏, 魏少华, 刘 颖, 冯玉英. 竹红菌甲素与细胞色素C相互作用的同步荧光光谱研究[J]. 南京师范大学学报, 2005, 28: 70. Gu X T, Wu X H, Zhou J H, Wei S S H, Liu Y, Feng Y Y. Study on the interaction between hypocrellin a and cytochrome c using synchronous fluoresecence of spectra[J]. Journal of Nanjing Normal University, 2005, 28: 70. |
| [20] | 杨昌英, 李 敏, 付 静, 李 昕. 脂质体对细胞色素C结构的稳定作用 [J]. 分析科学学报, 2010, 26: 153. Yang C Y, Li M, Fu J, Li X. Structral stability of cytochrome c in egg phosphatidylcholine liposomes[J]. Journal of Analytical Science, 2010, 26: 153. |
| [21] | Joseph R L. Principles of Fluorescence Spectroscopy[M]. New York: Plenum Press, 1983. 533. |
| [22] | Munk M B, Huvaere K, Bocxlaer J V, Skibsted L H. Mechanism of light-induced oxidation of nitrosylmyoglobin[J]. Food Chemistry, 2010, 121(2):472. |
| [23] | 马 静, 郑学仿, 唐乾,杨彦杰,孙 霞,高大彬. 光谱法研究Cu2+与肌红蛋白的相互作用[J]. 高等学校化学学报, 2008, 29(2): 258-263. Ma J, Zheng X F, Tang Q, Yag Y J, Sun X, Gao D B. Spectroscopic studies on the interaction of Cu2+ with myoglobin[J]. Chemical Journal of Chinese University, 2008, 29(2): 258-263. |




