发展可再生能源是解决人类能源和环境问题的重要途径,太阳能是诸多可再生能源中最理想的能量来源之一,取之不尽,用之不竭,发展将太阳能高效转化为化学能的体系有望从根本上解决人类面临的能源和环境问题。CO2是温室气体的主要组成部分,也是重要的碳源,利用太阳能将CO2还原成可以利用的燃料或者有机物,实现太阳能向化学能的转换,一方面可以大大降低温室气体的排放,减轻环境压力,另一方面也可以实现碳的合理循环和能量可持续利用。
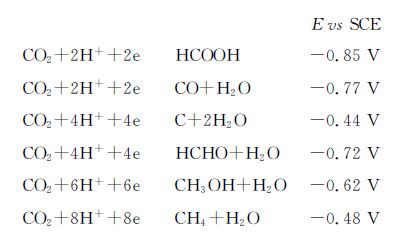
CO2作为碳的最高价化合物具有非常高的稳定性,其还原过程在热力学上是不利过程,如果通过单电子过程将CO2还原为相应的自由基阴离子CO·-2需要很高的能量,相应的还原电势达到了2.14 V(vs SCE),而通过质子偶合的多电子还原过程则能够显著降低其能量需求,质子参与的CO2还原过程及相应还原电势如图 1所示,因此,发展可用于多电子还原反应过程的高效催化体系是目前CO2还原研究工作的重点。
|
图1 质子参与CO2还原过程中的多电子还原电势 CO2 reduction potentials through proton-assisted multiple-electron transfer |
CO2还原方法有许多种,如化学反应还原[1, 2, 3]、光催化还原、电催化还原[4, 5, 6]以及光电催化还原等[7, 8],在这些方法中,光催化还原是最“清洁”的一种方法,它不需要外加电能或热能,直接利用太阳能将CO2还原成可以利用的燃料或者有机物,真正实现能量的可持续利用。光催化还原CO2需要质子耦合参与来降低其还原电势,还原过程通常在溶液体系中进行。根据光催化过程中催化剂的催化方式和状态不同,光催化还原CO2的体系主要分为均相体系和非均相体系。均相光催化还原CO2的体系有两种类型,一种是催化剂和捕光基团为同一组分,该组分既能吸收可见光,又有合适的还原电位,兼具捕光和催化双重功能;另外一种类型是捕光基团和催化剂为两个组分(或基团),分别承担捕光和催化的功能,通过捕光基团吸光和一系列的电子转移过程实现CO2的还原。非均相光催化体系主要是利用具有纳米结构的半导体材料(如二氧化钛)或者金属\\半导体复合材料等为催化剂,通过光照,利用价带跃迁到导带的电子直接(或通过共催化剂)实现CO2的还原。将具有光催化功能的分子通过物理或化学的方法固载到特定固体表面或其它载体,提高催化剂对CO2还原活性、稳定性以及重复利用性是非均相光催化的另外一种方式[9, 10, 11, 12, 13]。最近发表了几篇关于半导体催化方面的综述[14, 15, 16],已经对相关的研究工作进行了全面而详细的总结,本文不再详述。
要实现均相体系中催化剂向CO2的多电子转移过程,需要满足热力学条件,即催化剂(或其激发态)的还原电势绝对值要大于或接近相应耦合半反应的还原电势绝对值,这样催化剂获得电子后才能够有效将电子传递给CO2。另一方面,由于CO2还原是一个多电子还原过程,需要在溶液中进行多次电子转移,这种多电子转移过程从动力学上来看是不利的,这也是为什么均相体系中,还原产物主要都是双电子还原产物CO或HCOOH,更高级的多电子还原产物如甲醇、甲烷则很少有文献报道[17]。均相体系作为光催化还原CO2最早研究的体系[18],对CO2还原的分子机理研究、新型催化剂设计以及体系优化方面具有重要指导意义。
2009年,Fujita等人从分子催化角度对均相体系光催化还原CO2的机理进行了详细阐述[19],在之后的五年中,均相体系光催化还原CO2的研究取得了新的进展,特别在催化机理的研究、高效高选择性催化剂探索和新型催化体系的构建方面,取得了显著进展。均相体系的催化剂以金属配合物为主,这是因为金属配合物容易实现多重氧化还原状态,有效地促进质子耦合的多电子还原过程[20],此外,金属配合物的配体易于进行化学修饰,可以有效调控配合物的氧化还原电势,使其更好地与CO2还原所需的电势相匹配。本文将按配合物催化剂种类分类,结合早期的研究结果,对近五年来均相体系中光催化还原CO2取得的重要研究进展进行综述。
1 贵金属配合物为催化剂的催化体系 1.1 铼(Re)配合物催化剂2,2′-联吡啶三羰基铼氯(溴)化物是最早用于均相体系光催化还原CO2的催化剂之一,也是目前均相光催化体系中研究最广泛、最深入的一类催化剂。1983年,Lehn等人[18]研究了2,2′-联吡啶三羰基铼氯(溴)化物(如图 2a)及其类似物(如图 2b)作为催化剂和光敏剂用于光催化还原CO2的体系,首次证实Re配合物对CO2具有光催化还原活性,虽然其4小时生成CO的催化转换数(TON)只有不到50,但催化得到的产物表现出良好的选择性(CO/H2=97.5/2.5),这一发现为均相体系光催化还原CO2的研究提供一种全新的思路。

|
图2 Lehn等人用于均相光催化还原CO2的铼配合物结构 Structures of Re(L)(CO)3X complexes used as homogeneous photocatalysts by Lehn’s research group |
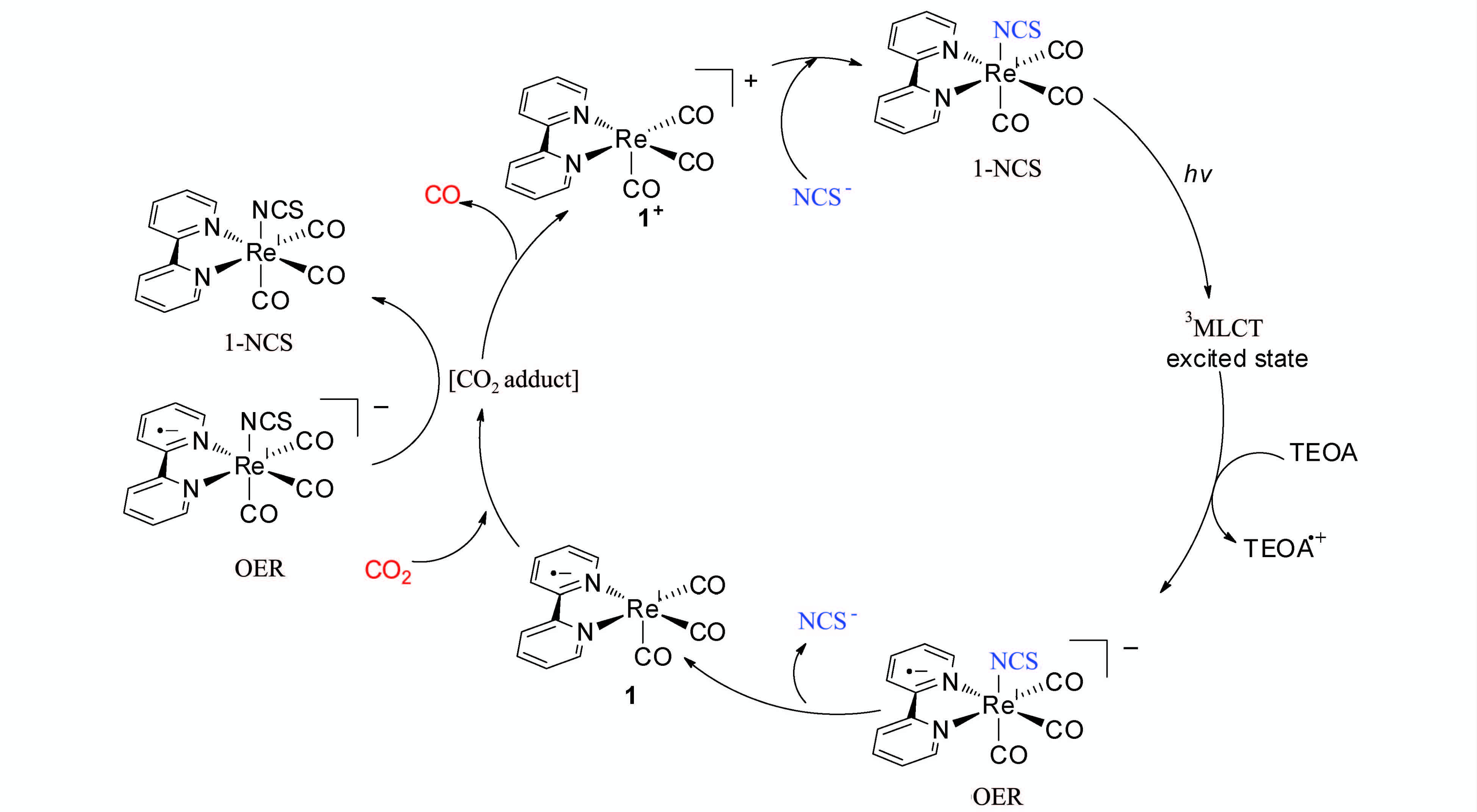
在其后很长一段时间内,对铼配合物催化剂的研究主要集中在不同配位基团(—X)[21, 22]或不同取代的联吡啶有机配体[23]对配合物光催化还原CO2活性的影响,早期的研究结果表明配位基团(—X)和有机配体联吡啶的取代基虽然能影响配合物催化活性,但并没有根本性的提高,单波长照射下的光化学转换量子效率都低于50%,催化转换数都低于100。最近几年,随着检测手段和方法的不断完善,对铼催化还原CO2的机理也进行了深入研究[20]。被广泛认可的催化机理是铼配合物光照后生成激发三重态(3MLCT),激发三重态和 电子牺牲体三乙醇胺(TEOA)发生第一个电子转移过程,生成单电子还原的铼配合物中间体(One-electron reduced species,OER),OER的配位基团(—X)发生离去,然后和CO2通过亲核加成生成CO2加成产物,该加成产物得到第二个电子,将CO2还原成CO并释放出来,铼配合物中间体和配位基团(—X)重新结合,进行下一个催化循环过程。整个催化循环过程中,部分中间体已经通过实验进行了证实,如第一个电子的传递过程(OER的形成)、配位基团(—X)的解离过程等,还有些中间体和过程是通过实验结果进行的推断,缺乏直接的实验证据,如对于CO2的加成产物形成、第二个电子是如何传递等则并不明确。1986年,Lehn等人[24]研究认为铼配合物的催化是以单金属机制(Monometallic Pathway)进行的,即一个催化循环过程中只有一个金属配合物(中间体)参与,第二个电子直接由电子牺牲体提供。2008年,Ishitani等人[25]通过比较不同配位基团的铼配合物(Re-NCS、Re-Cl和Re-CN)催化还原CO2的活性,提出了铼配合物催化存在双金属机制。他们的研究表明这三个铼配合物具有相似的光物理性质,但催化活性却完全不同,通过比较,作者认为以铼配合物为催化剂的体系中,还原过程中第二个电子来自另一个OER(如图 3),即CO2加成物和第二个OER发生第二个电子的转移过程,实现CO2还原成CO的过程。Re-NCS形成的OER具有较长的寿命是其与Re-Cl相比具有更高催化活性的原因,Re-CN几乎没有催化活性,是因为配位基团CN不易解离,无法形成CO2加成产物。他们通过优化催化剂结构和组成,设计具有较长OER寿命的铼配合物,以及带有容易离去配位基团的铼配合物,利用两者混合物可以显著提高体系的催化效率,获得当时最高59%的量子转换效率。
|
图3 铼配合物双金属催化机制示意图 Photocatalytic bimetallic mechanism by Re-NCS |
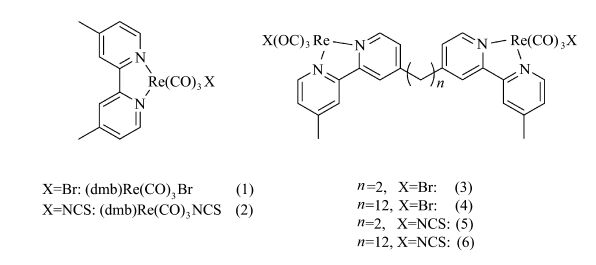
双金属机制需要两个单电子还原中间体OER参与电子转移过程,如果将两个Re催化剂共价连接起来有可能产生协同效应,促进催化还原过程。前期研究结果已经表明NCS配位的铼催化剂(Re-NCS)OER的寿命长,有利于双金属机制,催化效果最好,对于共价连接的双核催化剂效果如何有待实验进一步证实。Rieger等人[26]设计合成了不同配位基团和不同链长连接的Re催化剂(如图 4),他们的研究结果表明:通过共价连接使得两个催化剂相互靠近,无论是NCS还是Br配位,其催化效果相对于单个催化剂都明显增强,但是Re-Br的双催化剂的催化活性优于Re-NCS双催化剂,前者的TOF值是后者的2倍,这主要是因为通过共价连接使得彼此临近的Re-Br一方面可以通过双金属机制促进催化还原,同时Br配位基团和NCS相比更容易离去,有利于OER和CO2加成产物的生成。
|
图4 铼配合物以及通过共价连接双核配合物结构图 Structures of the mononuclear and binuclear Re-catalysts |
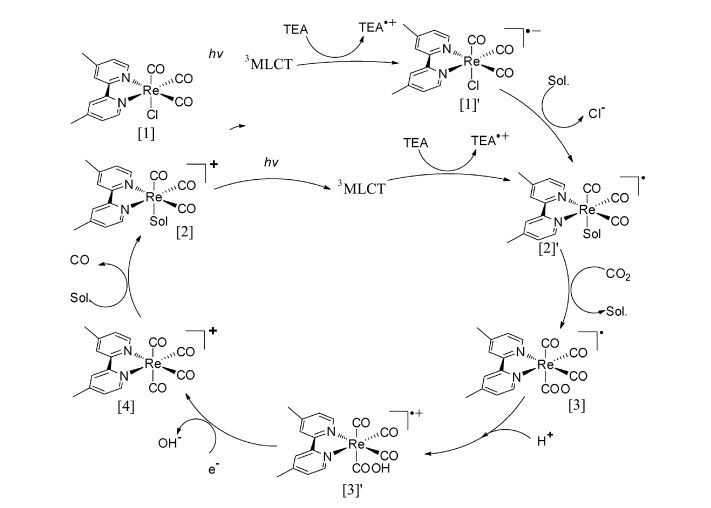
2011年,Muckerman等人[27, 28, 29]通过密度泛函理论,对铼催化剂在CO2还原过程中形成的CO2加成中间体进行了理论计算,从理论上预测催化过程中CO2的加成方式以及中间体对催化过程的影响。2013年,Morimoto等人[30]利用红外光谱,并结合质谱和核磁碳谱证实电子牺牲体三乙醇胺不仅作为电子牺牲体提供电子,而且还参与催化剂和CO2结合过程,随后Inoue等人[31]利用冷喷雾质谱技术(cold-spray ionization mass spectro-metry,CSI-MS),并结合同位素标记的方法第一次在实验中直接观察到了CO2和催化剂加成的中间产物,提出了如图 5所示的催化循环过程,这是迄今为止对Re配合物催化循环过程中形成CO2加成产物这一中间体给出的最有力实验证据。
|
图5 [Re(dmbpy)(CO)3Cl]催化机制示意图 Photochemical CO2 reduction cycle catalyzed by [Re(dmbpy)(CO)3Cl] |
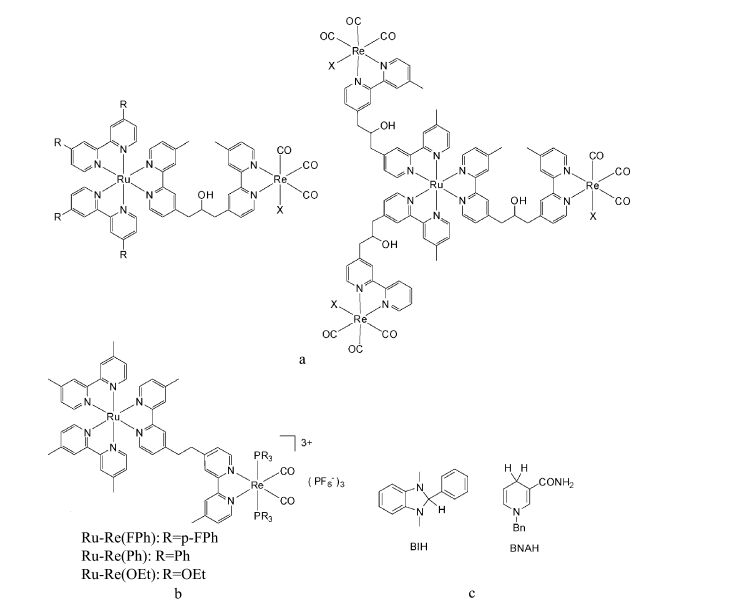
铼配合物本身在可见光区吸收弱,严重影响其对太阳光的利用效率,光敏剂的引入,可以大大提高催化体系的光响应范围。研究表明,通过超分子构建,将光敏剂和铼催化剂共价连接起来是提高其光催化还原效果的有效方法[19]。Ishitani等人[32, 33]在三联吡啶钌光敏剂外围分别共价连接一个或者多个催化剂(如图 6a),光敏剂将吸光范围增加到了更长波长,提高了光捕获效应,体系的最大量子产率达到了0.21,TON值达到了232。催化剂的配位基团对于这种二元体系的催化活性也有显著的影响[34],如图 6b所示,磷原子配位基团上不同取代基团形成的铼催化剂,表现出完全不同的催化活性和催化稳定性,对位氟原子取代的三苯基膦配位基团可以显著提高催化剂的催化活性和稳定性,催化剂的TOF值达到了281 h-1,催化转换数TON达到207,催化的量子效率0.15。利用同样的二元体系,以1,3-二甲基-2苯基-2,3-二氢苯并咪唑(BIH)替换1-苄基-1,4-二氢烟酰胺(BNAH)作为电子牺牲体(如图 6c),体系的催化效率、催化稳定性以及催化速率都得到了明显提高,效率由原来的0.15提高到0.45,TON值由207提高到3029,TOF由4.7 min-1提高到35.7 min-1[35]。
|
图6 共价键连接的光敏剂-催化剂二元体系以及电子牺牲体结构 Structures of photocatalytic-binuclear complexes and the sacrificial electron donors |
光敏剂和催化剂之间的链长以及连接方式也会影响体系的催化效果,Ishitani等人[36]合成了不同链长连接的二元体系(如图 7a所示),研究结果表明两个碳链长度构建的体系催化效果最好,四个和六个碳链长的催化效果没有区别,光物理实验结果证实两个碳链长连接的体系中,光敏剂和催化剂之间存在的弱相互作用促进了光敏剂和电子牺牲体BNAH之间的电子转移,使得两个碳链长度连接的体系具有最佳的催化效果,光敏剂和催化剂之间的电子转移不是整个过程的决速步骤,因此不是导致催化活性差别的主要因素。中科院理化所傅文甫老师课题组[37]通过共轭和非共轭两种方式将光敏剂和铼催化剂连接起来(如图 7b),并对其催化活性进行了比较,研究表明共轭连接的光敏剂和催化剂之间电子离域程度显著增加,但是催化活性和催化转换数却降低了,主要是因为配体之间共轭导致其还原电位升高(-1.73 vs -1.30 V),从而使得生成的单电子组分(OER)还原活性降低。

|
图7 以不同方式连接的光敏剂-催化剂二元体系 Structures of photocatalytic-binuclear complexes covalent connected with different ways |
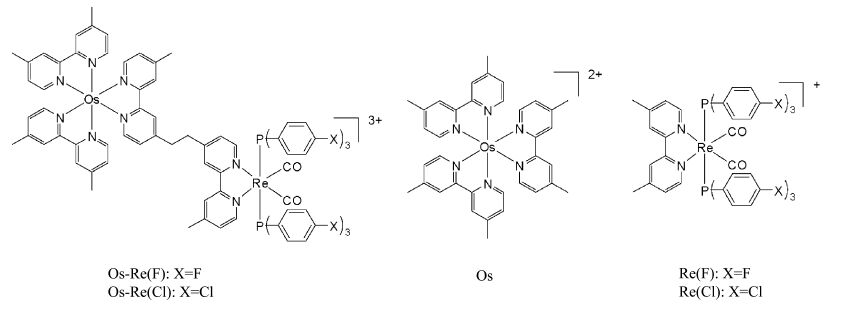
Ishitani研究组[38]利用吸收波长位于红光区域的三联吡啶锇为光敏剂,共价和催化剂铼相连合成得到了如图 8所示的二元体系,他们以1,3-二甲基-2苯基-2,3-二氢苯并咪唑(BIH)为牺牲体,构建了新的CO2催化还原体系,该体系中用大于620 nm的波长光选择性光照三联吡啶锇,实现了CO2的高效还原,体系的催化转换数达到了1138,TOF达到3.3 min-1,催化量子效率0.12。研究表明催化剂膦配位基团对催化活性有明显影响,以对位氟取代的三苯基膦为配位基团的催化剂表现出更优异的催化效果。
|
图8 双核配合物及其相应的模型化合物结构 Structures of photocatalytic-binuclear complexes and model compounds |
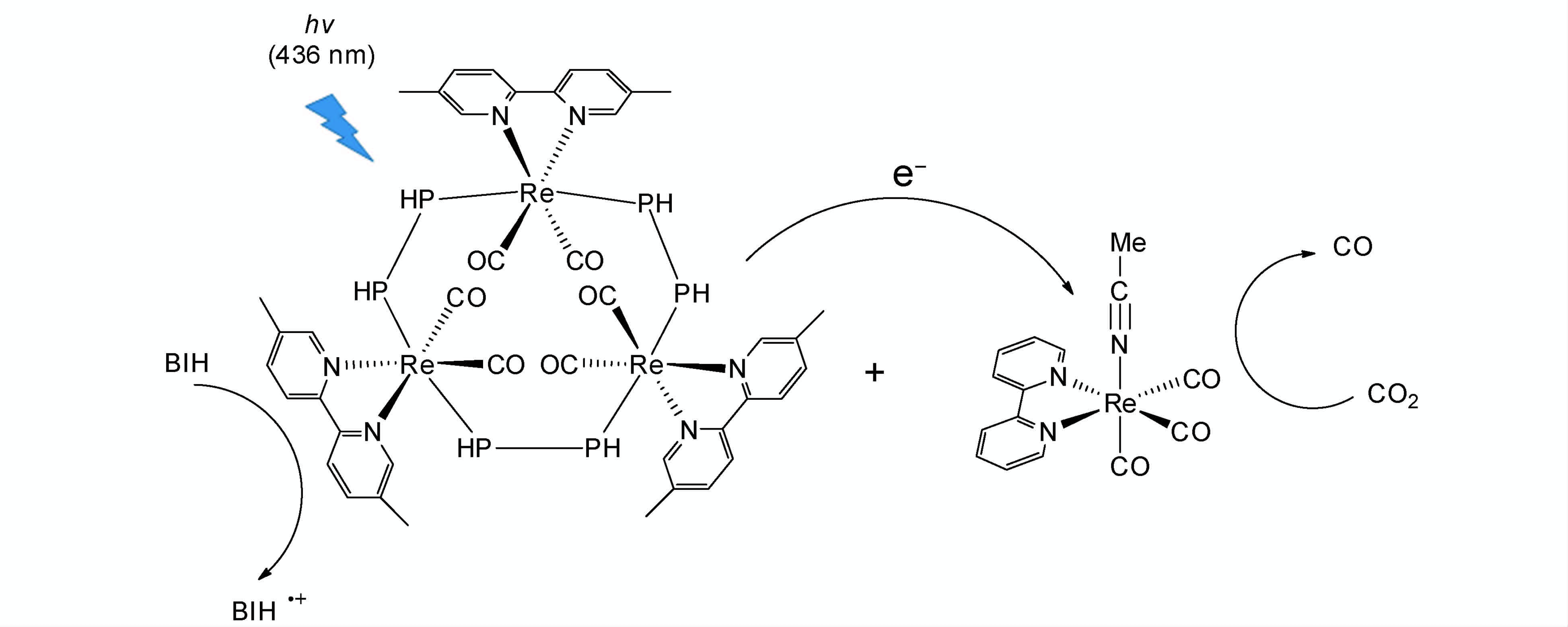
最近,他们研究组[39]又设计合成了一种具有特殊环状多核结构的铼配合物,利用该配合物为光敏剂,BIH为牺牲体,乙腈为配位基的Re配合物为催化剂,构建如图 9所示的催化体系。该体系的催化转换数为526,量子效率达到了82%,是目前国际上报道的最高量子效率。由于类似Re配合物合成分离的难度大,贵金属使用成本高,人们考虑利用廉价的有机染料代替金属配合物为光敏剂来降低成本,Rosenthal等人[40, 41]尝试利用有机染料BODIPY作为光敏剂来代替金属配合物光敏剂对CO2进行催化还原,结果表明,BODIPY染料无论是和Re催化剂共轭相连还是以化学键共价相连,长波激发BODIPY都没有显示出对CO2的催化活性,因此,廉价有机光敏剂的探索也是均相体系面临的一个挑战。
|
图9 环状多核铼配合物为光敏剂的催化体系 Photocatalytic CO2 reduction system composed of a ring-shaped Re(Ⅰ) multinuclear complexes as photosensitizer |
在铼配合物为催化剂的催化体系中,催化效果还受多种其它因素的影响,如溶剂的类型[42]、溶剂中水含量多少[43]等都会对催化效果产生显著影响。因此,对于以铼贵金属配合物为催化剂的体系,不仅要侧重于机理方面的研究,还需要针对不同的体系进行条件优化。
1.2 其它贵金属催化剂铼配合物在CO2还原方面表现出良好的选择性,但在催化的稳定性方面表现的并不很理想,所获得的最佳TON值只有几千,因此人们对其它类型的贵金属催化剂也进行了探索研究。钌配合物是其中研究较早的一类催化剂,研究表明具有催化活性的钌配合物通常是具有CO、Cl或者H配位基团的二联吡啶化合物,结构可表示为Ru(bpy)2(CO)Xn+(X=CO,Cl,H等),其光催化还原CO2的产物以甲酸为主,催化效果更多是表现在电催化方面的催化活性,在光催化方面的效果并不显著[44]。
最近,Ishitani研究组[45]合成了一系列共价键连接的多核联吡啶钌配合物(如图 10),以三联吡啶钌作为光敏剂,二羰基配位的二联吡啶钌为催化剂,BNAH作为电子牺牲体构建了光催化还原体系,体系表现出良好的选择性和稳定性,连接两个光敏剂和一个催化剂的配合物体系表现出最佳的催化效果,催化转换数TON达到了671,TOF值达到11.6 min-1,生成甲酸的量子效率为6.1%。这是均相体系中以钌配合物为催化剂,光催化还原CO2获得的最好结果。

|
图10 用于均相光催化的钌配合物结构 Photocatalytic CO2 reduction system based on Ru multinuclear complexes |
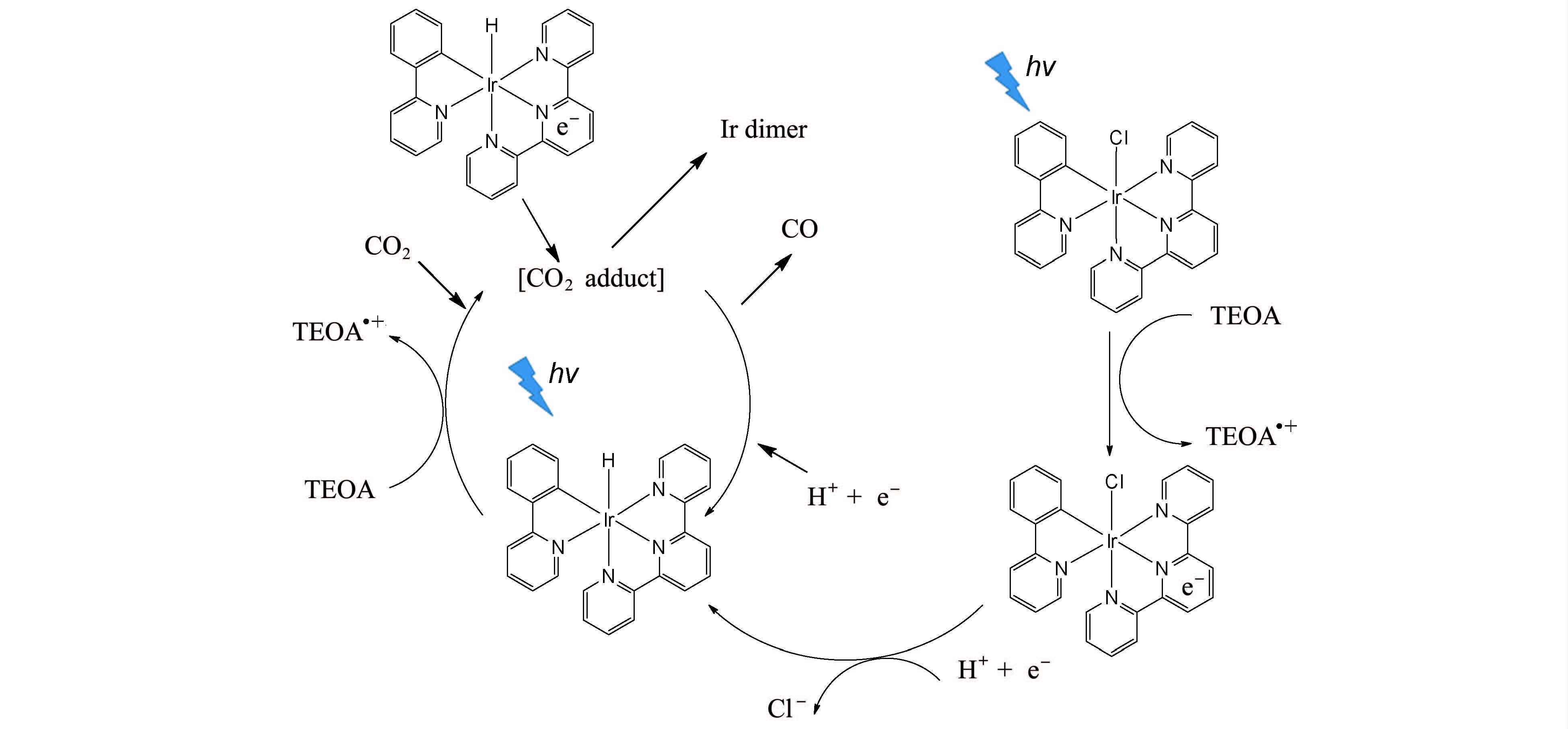
和铼配合物类似,部分铱配合物也表现出对CO2的光催化活性,Ishitani研究组[46]设计合成了一种新型铱配合物(如图 11),该配合物可以同时作为催化剂和光敏剂用于CO2的还原,和铼配合物相比,其吸收光谱位于可见光区,480 nm处的催化量子效率达到21%,是可见光区单核体系获得的最高量子效率,催化转换数比铼配合物略高(TON=38),该催化剂同时表现出良好的选择性,主要还原产物为CO,次要产物(甲酸和H2)含量不到2%。结合核磁和质谱分析,他们认为其循环催化机理和铼配合物类似,即铱配合物经光照到激发态,和电子牺牲体三乙醇胺发生电子转移,然后形成单电子还原中间体Ir(tpy)(ppy)H(OER)以及CO2加成产物,[Ir(tpy)(ppy)H]是催化过程中的关键活性中间体,既能够和CO2加成形成CO2加成物,也能够直接提供电子给CO2加成物发生还原生成CO。
|
图11 基于金属铱配合物的均相光催化体系 Photocatalytic CO2 reduction system based on Ir complexes |
最近,Rieger等人[47]将具有催化活性的铱配合物通过共价烷基链连接,合成了如图 12所示的双核铱配合物催化剂。通过和单核的铱配合物对比,发现双核催化剂的光催化还原的量子效率并没有增加,但是双核催化剂的稳定性却显著增加,不同链长的双核配合物其TON值达到了80~135,是目前报道的铱配合物催化剂最高的结果。研究结果进一步表明,催化剂失活的原因并不是催化过程中催化剂形成二聚体,推测可能是电子牺牲体TEOA的氧化产物导致了催化剂失活。

|
图12 双核铱配合物结构 Structures of photocatalytic binuclear Ir complexes |
从催化的成本和实际应用角度考虑,贵金属由于本身地球储量少,价格昂贵,不适合大规模应用。而且,现实的状况是贵金属配合物催化剂所能达到的催化效率和催化转换数也非常有限,目前,所能达到的最佳TON值不超过2000,虽然单波长的转换效率最大可以达到82%,但是全波段的量子效率还远没有达到实际应用的效果。发展高效的非贵金属配合物催化剂是目前均相光催化还原CO2体系的一个重要研究方向。
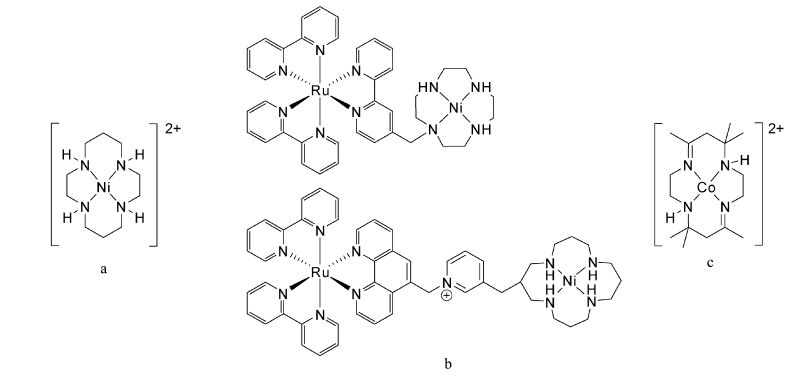
最早利用非贵金属为催化剂并用于均相体系CO2还原的是镍-四氮杂环配合物[48],如图 13a,但催化效果并不理想。Kimura等人[49]通过共价键将光敏剂和催化剂连接起来以提高该催化剂的催化效果(如图 13b),该催化体系生成的产物(CO和H2)选择性较差,得到目标产物CO量少,而且体系中光敏剂仍然采用的贵金属Ru的配合物。随后,又发展了钴-四氮杂环化合物[50, 51],如图 13c,该类配合物在均相体系的光催化还原CO2选择性方面优于相应的镍配合物,但是催化活性并没有显著改进。
|
图13 基于四氮杂环的非贵金属配合物催化剂结构 Structures of [Ni(cyclam)] and [Co(cyclam)] complexes as homogeneous catalysts |
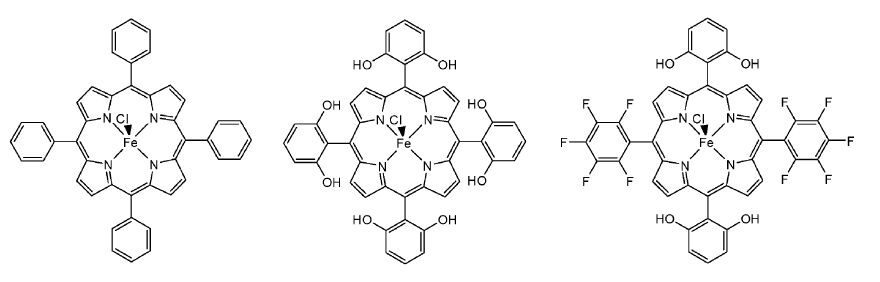
Neta等人[52]最早研究了铁(Ⅲ)卟啉同时作为光敏剂和催化剂用于均相CO2还原的过程,他们利用三乙胺为电子牺牲体,研究了该催化体系的催化还原机理。实验结果表明铁(Ⅲ)卟啉通过多次还原得到电子,生成铁(Ⅱ)卟啉、铁(Ⅰ)卟啉以及铁(0)卟啉。铁(I)卟啉并不具有催化还原CO2的活性,真正具有催化活性的是铁(0)卟啉中间体,体系获得的最高催化转换数为70,作者推测可能是由于CO2还原过程中,卟啉环结构也会被部分还原而发生分解导致催化剂失活。Bonin等人[53]通过对比不同取代基的铁(Ⅲ)卟啉(如图 14)光催化还原CO2的效果,结合光谱技术,进一步证实取代基苯环上的酚羟基有助于CO2还原,他们推测酚羟基和还原中间体(CO2加成产物)形成氢键,一方面可以和催化剂中间体的分解过程进行竞争,降低其分解的几率,提高光催化的稳定性,另一方面也抑制了质子的还原,提高其催化还原CO2的选择性。
|
图14 不同取代基的铁(Ⅲ)卟啉催化剂结构 Structures of Fe(Ⅲ) Porphyrin with different substituents |
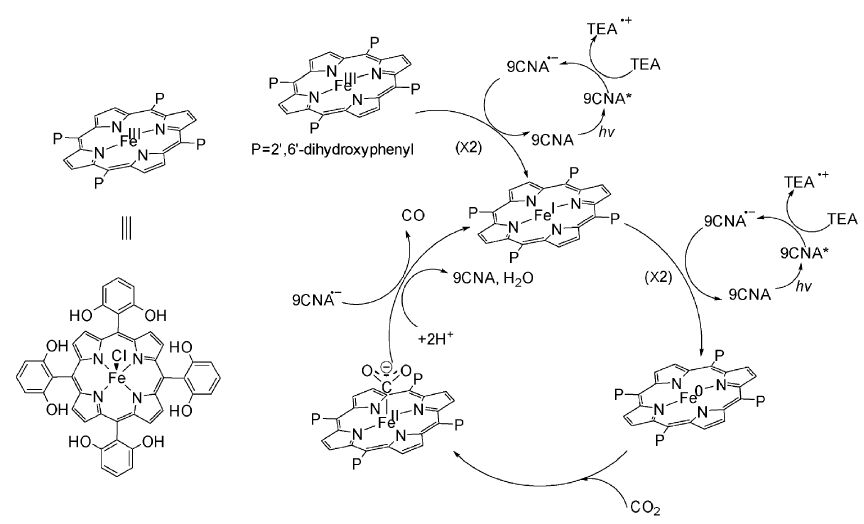
最近,Bonin课题组[54]还是以苯酚取代的三价铁(Ⅲ)卟啉为催化剂,9-氰基蒽(9CNA)为光敏剂,三乙胺(TEA)为牺牲体构建了一个完全没有贵金属组分的CO2还原体系。该催化体系还原CO2过程中专一性获得了CO产物,没有检测到H2,表现出优异的选择性,光照45 h催化转换数达到60以上,而且TON值呈线性增加,证实催化剂具有一定的稳定性。结合实验数据和前期的研究结果,作者提出了如下催化循环机制(如图 15):光照后激发态光敏剂9CNA和电子牺牲体TEA三乙胺发生电子转移,生成光敏剂的阴离子自由基(9CNA·-),然后和铁(Ⅲ)卟啉发生多次电子转移,生成铁(Ⅰ)卟啉和铁(0)卟啉中间体,铁(0)卟啉中间体和CO2结合,在质子参与下从9CNA·-继续获得一个电子,发生还原反应生成CO及铁(Ⅰ)卟啉,铁(Ⅰ)卟啉参与下一个循环,实现整个体系的催化循环过程。整个催化过程涉及到两个双电子转移过程,即铁(Ⅲ)还原成铁(Ⅰ)的过程以及铁(Ⅰ)的催化循环过程,这可能是造成体系的光化学转换的量子效率比较低的原因。
|
图15 铁(Ⅲ)卟啉催化剂结构及光催化还原CO2的机制示意图 Structure of Fe(Ⅲ) Porphyrin and mechanism for the photocatalytic reduction of CO2 to CO |
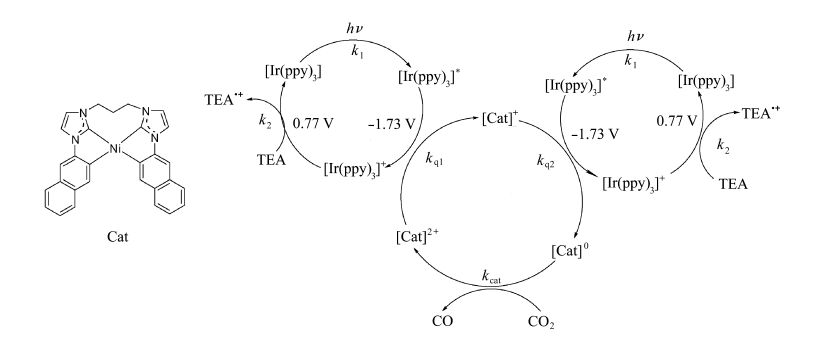
2013年,Chang等人[55]合成了一系列镍-卡宾配合物催化剂,并利用该配合物为催化剂、三联吡啶铱为光敏剂、三乙胺为电子牺牲体构建了一个高效催化体系,其可能的催化循环过程和前面所述的铁(Ⅲ)卟啉相似,如图 16所示,通过两次和还原态光敏剂发生电子转移过程,生成具有催化活性的Ni(0)配合物,催化还原CO2生成CO。在低浓度催化剂条件下,该体系的最大TON值可以达到98000,TOF达到3.9 s-1,是目前报道的均相体系中获得的最高值。体系的不足之处在于光敏剂仍然使用了贵金属铱配合物,光敏剂的漂白作用是影响催化效果的决定因素,通过向体系中补加光敏剂,可以恢复体系催化还原CO2的功能。催化剂所展现出来的高稳定性和高活性具有良好的规模化应用潜能。
|
图16 镍-卡宾配合物结构以及光催化机制示意图 Photocatalytic mechanism by Nickel N-Heterocyclic Carbene-Amine complexes |
以非贵金属完全替代贵金属实现CO2的还原过程虽然取得了一些进展,但还是面临一些亟待解决的问题,如对于利用非贵金属配合物同时作为催化剂和光敏剂的催化体系,如何提高催化剂的稳定性;对于光敏剂和催化剂是不同基团的催化体系,如何选择合适的基团,既要求使用非贵金属配合物或有机物,又要满足光敏剂和催化剂二者之间的电子转移要求,这些都需要进行大量的实验探索,也是下一步发展的重要方向。
3 结论与展望利用太阳能高效的将CO2还原成可以利用的燃料或者有机物,实现太阳能向化学能的转换,可以降低温室气体的排放,减轻由化石燃料引起的环境压力,真正实现化石能源的循环利用。均相光催化还原CO2体系经过近30多年的发展,已经取得一些重要进展,尤其是最近几年在催化机理的研究方面,对一些重要的催化过程和关键中间体证实都取得了一些重要实验证据,机理的研究也为新体系的探索和开发提供了重要基础。另一方面,高效光催化体系的构筑也取得了实质性进展,和最初只有几十的TON相比,体系的最高催化转换数TON达到了98000,这和光催化还原CO2的实际应用(TON~100万)所要求的差距已经显著缩小了。但要真正实现规模化应用还有很多问题需要解决,目前均相体系的发展也面临许多挑战:
1)如何提高催化剂的稳定性和催化活性一直是均相光催化还原CO2体系面临的问题,均相体系中光催化还原CO2所用催化剂以金属配合物为主,为保持配合物催化活性,需要引入相对易于离去的配位基团,这样会增加其不稳定性,既要保持催化活性又要保持稳定性需要根据具体的体系来优化选择,目前,将均相催化剂进行非均相固载是一种有效的方法[10, 13, 56]。
2)发展非贵金属配合物催化剂替代贵金属催化剂是未来发展的重要方向,要实现光敏剂和催化剂完全由非贵金属替代,同时还要满足二者的高效电子转移要求,还需要大量探索性研究。
3)光敏剂在催化体系中起着光捕获和电子传递作用,发展有机染料替代目前常用的金属配合物光敏剂,降低应用成本,同时将光谱范围拓宽到长波长区域也是目前面临的一个挑战。
4)均相体系通常都是采用加入电子牺牲体(如胺类化合物)的氧化实现催化循环过程,如何通过超分子构建,将氧化和还原过程耦合起来,利用醇类或者烯烃这类化工原料为牺牲体代替胺类化合物,在氧化部分实现常用化工原料的选择性氧化,生成目标产物,在还原部分实现CO2的高效还原,这类超分子体系的构建也是未来均相体系催化还原CO2的一个目标。
| [1] | Mikkelsen M, Jorgensen M, Krebs F C. The teraton challenge. A review of fixation and transformation of carbon dioxide[J]. Energy & Environmental Science, 2010, 3(1): 43-81. |
| [2] | Appel A M, Bercaw J E, Bocarsly A B, Dobbek H, DuBois D L, Dupuis M, Ferry J G, Fujita E, Hille R, Kenis P J A, Kerfeld C A, Morris R H, Peden C H F, Portis A R, Ragsdale S W, Rauchfuss T B, Reek J N H, Seefeldt L C, Thauer R K, Waldrop G L. Frontiers, opportunities, and challenges in biochemical and chemical catalysis of CO2 fixation[J]. Chemical Reviews, 2013, 113(8): 6621-6658. |
| [3] | Cokoja M, Bruckmeier C, Rieger B, Herrmann W A, Kuhn F E. Transformation of carbon dioxide with homogeneous transition-metal catalysts: a molecular solution to a global challenge[J]. Angewandte Chemie-International Edition, 2011, 50(37): 8510-8537. |
| [4] | Costentin C, Robert M, Saveant J M. Catalysis of the electrochemical reduction of carbon dioxide[J]. Chemical Society Reviews, 2013, 42(6): 2423-2436. |
| [5] | Qiao J L, Liu Y Y, Hong F, Zhang J J. A review of catalysts for the electroreduction of carbon dioxide to produce low-carbon fuels[J]. Chemical Society Reviews, 2014, 43(2): 631-675. |
| [6] | Benson E E, Kubiak C P, Sathrum A J, Smieja J M. Electrocatalytic and homogeneous approaches to conversion of CO2 to liquid fuels[J]. Chemical Society Reviews, 2009, 38(1): 89-99. |
| [7] | Zhang L H, Zhu D, Nathanson G M, Hamers R J. Selective photoelectrochemical reduction of aqueous CO2 to CO by solvated electrons[J]. Angewandte Chemie-International Edition, 2014, 53(37): 9746-9750. |
| [8] | Kumar B, Llorente M, Froehlich J, Dang T, Sathrum A, Kubiak C P. Photochemical and photoelectrochemical reduction of CO2[J]. Annual Review of Physical Chemi-stry, 2012, 63:541. |
| [9] | Takeda H, Ohashi M, Tani T, Ishitani O, Inagaki S. Enhanced photocatalysis of Rhenium(Ⅰ) complex by light-harvesting periodic mesoporous organosilica[J]. Inorganic Chemistry, 2010, 49(10): 4554-4559. |
| [10] | Wang C, Xie Z G, deKrafft K E, Lin W L. Doping metal-organic frameworks for water oxidation, carbon dioxide reduction, and organic photocatalysis[J]. Journal of the American Chemical Society, 2011, 133(34): 13445-13454. |
| [11] | Dubois K D, Petushkov A, Cardona E G, Larsen S C, Li G H. Adsorption and photochemical properties of a mole-cular CO2 reduction catalyst in hierarchical mesoporous ZSM-5: an in situ FTIR study[J]. Journal of Physical Chemistry Letters, 2012, 3(4): 486-492. |
| [12] | Liu C, Dubois K D, Louis M E, Vorushilov A S, Li G H. Photocatalytic CO2 reduction and surface immobilization of a tricarbonyl Re(Ⅰ) compound modified with amide groups[J]. ACS Catalysis, 2013, 3(4): 655-662. |
| [13] | Windle C D, Pastor E, Reynal A, Whitwood A C, Vaynzof Y, Durrant J R, Perutz R N, Reisner E. Improving the photocatalytic reduction of CO2 to CO through immobilisation of a molecular Re catalyst on TiO2[J]. Chemistry-a European Journal, 2015, 21(9): 3746-3754. |
| [14] | Fan W Q, Zhang Q H, Wang Y. Semiconductor-based nanocomposites for photocatalytic H2 production and CO2 conversion[J]. Physical Chemistry Chemical Physics, 2013, 15(8): 2632-2649. |
| [15] | Habisreutinger S N, Schmidt-Mende L, Stolarczyk J K. Photocatalytic reduction of CO2 on TiO2 and other semiconductors[J]. Angewandte Chemie-International Edition, 2013, 52(29): 7372-7408. |
| [16] | Marszewski M, Cao S W, Yu J G, Jaroniec M. Semiconductor-based photocatalytic CO2 conversion[J]. Materials Horizons, 2015, 2(3): 261-278. |
| [17] | Boston D J, Xu C D, Armstrong D W, MacDonnell F M. Photochemical reduction of carbon dioxide to methanol and formate in a homogeneous system with pyridinium catalysts[J]. Journal of the American Chemical Society, 2013, 135(44): 16252-16255. |
| [18] | Hawecker J, Lehn J M, Ziessel R. Efficient photochemical reduction of CO2 to CO by visible-light irradiation of systems containing Re(Bipy)(Co)3x or Ru(Bipy)2+3-Co2+ combinations as homogeneous catalysts[J]. Journal of the Chemical Society-Chemical Communications, 1983, (9): 536-538. |
| [19] | Morris A J, Meyer G J, Fujita E. Molecular approaches to the photocatalytic reduction of carbon dioxide for solar fuels[J]. Accounts of Chemical Research, 2009, 42(12): 1983-1994. |
| [20] | Takeda H, Ishitani O. Development of efficient photocatalytic systems for CO2 reduction using mononuclear and multinuclear metal complexes based on mechanistic studies[J]. Coordination Chemistry Reviews, 2010, 254(3-4): 346-354. |
| [21] | Ishitani O, George M W, Ibusuki T, Johnson F P A, Koike K, Nozaki K, Pac C J, Turner J J, Westwell J R. Photophysical behavior of a new CO2 reduction catalyst, Re(CO)2(Bpy)(P(OEt)3)2+[J]. Inorganic Chemistry, 1994, 33(21): 4712-4717. |
| [22] | Hori H, Johnson F P A, Koike K, Ishitani O, Ibusuki T. Efficient photocatalytic CO2 reduction using +[J]. Journal of Photochemistry and Photobiology A-Chemistry, 1996, 96(1-3): 171-174. |
| [23] | Kurz P, Probst B, Spingler B, Alberto R. Ligand variations in complexes: effects on photocatalytic CO2 reduction[J]. European Journal of Inorganic Chemistry, 2006, (15): 2966-2974. |
| [24] | Hawecker J, Lehn J M, Ziessel R. Photochemical and electrochemical reduction of carbon-dioxide to carbon-monoxide mediated by (2,2'-Bipyridine)tricarbonylchlororhenium(Ⅰ) and related complexes as homogeneous catalysts[J]. Helvetica Chimica Acta, 1986, 69(8): 1990-2012. |
| [25] | Takeda H, Koike K, Inoue H, Ishitani O. Development of an efficient photocatalytic system for CO2 reduction using rhenium(Ⅰ) complexes based on mechanistic studies[J]. Journal of the American Chemical Society, 2008, 130(6): 2023-2031. |
| [26] | Bruckmeier C, Lehenmeier M W, Reithmeier R, Rieger B, Herranz J, Kavakli C. Binuclear rhenium(Ⅰ) complexes for the photocatalytic reduction of CO2[J]. Dalton Transactions, 2012, 41(16): 5026-5037. |
| [27] | Agarwal J, Fujita E, Schaefer H F, Muckerman J T. Mechanisms for CO production from CO2 using reduced Rhenium tricarbonyl catalysts[J]. Journal of the American Chemical Society, 2012, 134(11): 5180-5186. |
| [28] | Agarwal J, Sanders B C, Fujita E, Schaefer H F, Harrop T C, Muckerman J T. Exploring the intermediates of photochemical CO2 reduction: reaction of Re(dmb)(CO)(3) COOH with CO2[J]. Chemical Communications, 2012, 48(54): 6797-6799. |
| [29] | Agarwal J, Johnson R P, Li G H. Reduction of CO2 on a tricarbonyl Rhenium(Ⅰ) complex: modeling a catalytic cycle[J]. Journal of Physical Chemistry A, 2011, 115(13): 2877-2881. |
| [30] | Morimoto T, Nakajima T, Sawa S, Nakanishi R, Imori D, Ishitani O. CO2 capture by a Rhenium(Ⅰ) complex with the aid of triethanolamine[J]. Journal of the American Chemical Society, 2013, 135(45): 16825-16828. |
| [31] | Kou Y, Nabetani Y, Masui D, Shimoda T, Takagi S, Tachibana H, Inoue H. Direct detection of key reaction intermediates in photochemical CO2 reduction sensitized by a Rhenium bipyridine complex[J]. Journal of the American Chemical Society, 2014, 136(16): 6021-6030. |
| [32] | Gholamkhass B, Mametsuka H, Koike K, Tanabe T, Furue M, Ishitani O. Architecture of supramolecular metal complexes for photocatalytic CO2 reduction: Ruthenium-rhenium bi- and tetranuclear complexes[J]. Inorganic Chemistry, 2005, 44(7): 2326-2336. |
| [33] | Sato S, Koike K, Inoue H, Ishitani O. Highly efficient supramolecular photocatalysts for CO2 reduction using visible light[J]. Photochemical & Photobiological Sciences, 2007, 6(4): 454-461. |
| [34] | Tamaki Y, Watanabe K, Koike K, Inoue H, Morimoto T, Ishitani O. Development of highly efficient supramolecular CO2 reduction photocatalysts with high turnover frequency and durability[J]. Faraday Discussions, 2012, 155: 115-127. |
| [35] | Tamaki Y, Koike K, Morimoto T, Ishitani O. Substantial improvement in the efficiency and durability of a photocatalyst for carbon dioxide reduction using a benzoimidazole derivative as an electron donor[J]. Journal of Catalysis, 2013, 304: 22-28. |
| [36] | Koike K, Naito S, Sato S, Tamaki Y, Ishitani O. Architecture of supramolecular metal complexes for photocatalytic CO2 reduction Ⅲ: effects of length of alkyl chain connecting photosensitizer to catalyst[J]. Journal of Photochemistry and Photobiology A-Chemistry, 2009, 207(1): 109-114. |
| [37] | Bian Z Y, Chi S M, Li L, Fu W F. Conjugation effect of the bridging ligand on the CO2 reduction properties in difunctional photocatalysts[J]. Dalton Transactions, 2010, 39(34): 7884-7887. |
| [38] | Tamaki Y, Koike K, Morimoto T, Yamazaki Y, Ishitani O. Red-light-driven photocatalytic reduction of CO2 using Os(Ⅱ)-Re(Ⅰ) supramolecular complexes[J]. Inorganic Chemistry, 2013, 52(20):11902-11909. |
| [39] | Morimoto T, Nishiura C, Tanaka M, Rohacova J, Nakagawa Y, Funada Y, Koike K, Yamamoto Y, Shishido S, Kojima T, Saeki T, Ozeki T, Ishitani O. Ring-shaped Re(Ⅰ) multinuclear complexes with unique photofunctional properties[J]. Journal of the American Chemical Society, 2013, 135(36): 13266-13269. |
| [40] | Andrade G A, Pistner A J, Yap G P A, Lutterman D A, Rosenthal J. Photocatalytic conversion of CO2 to CO using Rhenium bipyridine platforms containing ancillary phenyl or BODIPY moieties[J]. ACS Catalysis, 2013, 3(8): 1685-1692. |
| [41] | Teesdale J J, Pistner A J, Yap G P A, Ma Y Z, Lutterman D A, Rosenthal J. Reduction of CO2 using a rhenium bipyridine complex containing ancillary BODIPY moieties[J]. Catalysis Today, 2014, 225: 149-157. |
| [42] | Kuramochi Y, Kamiya M, Ishida H. Photocatalytic CO2 reduction in N,N-dimethylacetamide/water as an alternative solvent system[J]. Inorganic Chemistry, 2014, 53(7): 3326-3332. |
| [43] | Nakada A, Koike K, Nakashima T, Morimoto T, Ishitani O. Photocatalytic CO2 reduction to formic acid using a Ru(Ⅱ)-Re(Ⅰ) supramolecular complex in an aqueous solution[J]. Inorganic Chemistry, 2015, 54(4): 1800-1807. |
| [44] | Fujita E. Photochemical carbon dioxide reduction with metal complexes[J]. Coordination Chemistry Reviews, 1999, 185-6: 373-384. |
| [45] | Tamaki Y, Morimoto T, Koike K, Ishitani O. Photocatalytic CO2 reduction with high turnover frequency and selectivity of formic acid formation using Ru(Ⅱ) multinuclear complexes[J]. Proceedings of the National Academy of Sciences of the United States of America, 2012, 109(39): 15673-15678. |
| [46] | Sato S, Morikawa T, Kajino T, Ishitani O. A highly efficient mononuclear Iridium complex photocatalyst for CO2 reduction under visible light[J]. Angewandte Chemie-International Edition, 2013, 52(3): 988-992. |
| [47] | Reithmeier R O, Meister S, Rieger B, Siebel A, Tschurl M, Heiz U, Herdtweck E. Mono- and bimetallic Ir(Ⅲ) based catalysts for the homogeneous photocatalytic reduction of CO2 under visible light irradiation. New insights into catalyst deactivation[J]. Dalton Transactions, 2014, 43(35): 13259-13269. |
| [48] | Grant J L, Goswami K, Spreer L O, Otvos J W, Calvin M. Photochemical reduction of carbon-dioxide to carbon-monoxide in water using a Nickel(Ⅱ) tetra-azamacrocycle complex as catalyst[J]. Journal of the Chemical Society-Dalton Transactions, 1987, (9): 2105-2109. |
| [49] | Kimura E, Bu X H, Shionoya M, Wada S J, Maruyama S. A new Nickel(Ii) cyclam (cyclam=1,4,8,11-tetraazacyclotetradecane) complex covalently attached to Ru(Phen)2+3 (Phen=1,10-phenanthroline)-a new candidate for the catalytic photoreduction of carbon-dioxide[J]. Inorganic Chemistry, 1992, 31(22): 4542-4546. |
| [50] | Matsuoka S, Yamamoto K, Ogata T, Kusaba M, Nakashima N, Fujita E, Yanagida S. Efficient and selective electron mediation of cobalt complexes with cyclam and related macrocycles in the P-terphenyl-catalyzed photoreduction of CO2[J]. Journal of the American Chemical Society, 1993, 115(2): 601-609. |
| [51] | Ogata T, Yamamoto Y, Wada Y, Murakoshi K, Kusaba M, Nakashima N, Ishida A, Takamuku S, Yanagida S. Phenazine-photosensitized reduction of CO2 mediated by a cobalt-cyclam complex through electron and hydrogen-transfer[J]. Journal of Physical Chemistry, 1995, 99(31): 11916-11922. |
| [52] | Grodkowski J, Behar D, Neta P, Hambright P. Iron porphyrin-catalyzed reduction of CO2. Photochemical and radiation chemical studies[J]. Journal of Physical Chemistry A, 1997, 101(3): 248-254. |
| [53] | Bonin J, Chaussemier M, Robert M, Routier M. Homogeneous photocatalytic reduction of CO2 to CO using Iron(0) porphyrin catalysts: mechanism and intrinsic limitations[J]. Chemcatchem, 2014, 6(11): 3200-3207. |
| [54] | Bonin J, Robert M, Routier M. Selective and efficient photocatalytic CO2 reduction to CO using visible light and an Iron-based homogeneous catalyst[J]. Journal of the American Chemical Society, 2014, 136(48): 16768-16771. |
| [55] | Thoi V S, Kornienko N, Margarit C G, Yang P D, Chang C J. Visible-light photoredox catalysis: selective reduction of carbon dioxide to carbon monoxide by a Nickel N-heterocyclic carbene-isoquinoline complex[J]. Journal of the American Chemical Society, 2013, 135(38): 14413-14424. |
| [56] | Ueda Y, Takeda H, Yui T, Koike K, Goto Y, Inagaki S, Ishitani O. A visible-light harvesting system for CO2 reduction using a Ru-Ⅱ-Re-Ⅰ photocatalyst absorbed in mesoporous organosilica[J]. Chemsuschem, 2015, 8(3): 439-442. |




