2. 中国科学院大学, 北京 100049
2. University of Chinese Academy of Sciences, Beijing 100049, P. R. China
半导体TiO2具有独特的光学、电学以及化学性质[1, 2]。由于其化学性质稳定、耐酸碱腐蚀、廉价及光催化活性高等优势,是最理想的光催化材料,因而在光催化降解有机物和光解水方面有广泛的应用[3, 4, 5]。但TiO2是宽禁带半导体(Eg=3.2 eV),只能吸收占太阳光能量不到4%的紫外光,因而对太阳能的利用率很低[6]。近几十年来,人们采用了很多措施对二氧化钛进行改性,提升光催化活性,包括染料敏化[7, 8]、贵金属沉积[9, 10, 11]、离子掺杂[12, 13, 14, 15, 16, 17, 18, 19, 20]和构建异质结等[2, 6, 21, 22, 23, 24]。其中,构建异质结是一种非常有效的途径。当窄带隙半导体与TiO2复合时,既可以扩展吸收光范围,提升太阳能的利用率,同时半导体之间的界面也可以促进光生电子空穴的分离。
CdS是一种典型的窄带隙半导体光催化材料(Eg=2.4 eV),具有很高的可见光催化活性,但是CdS容易发生光腐蚀,影响其使用寿命[25, 26]。通过TiO2/CdS形成复合材料,既能够增强TiO2的可见光活性,也可以减少CdS的光腐蚀[27, 28, 29, 30]。Hsu等人以阳极氧化铝为模板,用液相沉积法制备了CdS@TiO2的同轴电缆阵列[31]。Cao等人用化学还原法制备了TiO2@CdS核壳纳米线,借助TiO2自身为模板,能够在TiO2表面形成完整的CdS外壳[32]。上述方法制备的CdS与TiO2的核壳结构,需要用阳极氧化铝作为模版,或者引入KBH4强还原剂,且生成的CdS形貌很难控制,通常是小颗粒。因此我们想通过简易温和的方法,制备高比表面积的形貌可控CdS与TiO2的核壳结构。
本实验发展了一种CdS超薄片包覆TiO2中空结构的制备方法,同时对其形成过程进行了研究。首先通过静电纺丝的方法,制备了不同钛镉比的纳米纤维。然后在空气中煅烧,获得TiO2/CdO复合纳米纤维,用硫化钠溶液进行水热处理,得到CdS超薄片层包覆TiO2中空结构。随着Ti/Cd的增大,纳米管结构逐渐消失。由此我们推测出复合结构的形成过程:首先,TiO2/CdO复合纳米纤维进行水热硫化处理时,由于CdO的溶解,里面TiO2形成疏松结构,同时外面溶解的CdO与溶液中的硫离子生成CdS,并以超薄片层形貌生长在表面。在Ti/Cd为1∶1和2∶1时,由于更多CdO的溶解,形成CdS超薄片层包覆TiO2纳米管的结构;而Ti/Cd为4∶1和8∶1时,由于溶解的CdO较少,不足以形成TiO2纳米管。当Ti/Cd为1∶1时,TiO2@CdS复合材料具有最好的产氢活性。在300 W氙灯光照条件下和加UVCUT-420 nm滤光片下,50 mg催化剂产氢速率分别为19.7 μmol/h,3.4 μmol/h。
1 实验部分 1.1 主要仪器和试剂JEOL JSM 4800F型扫描电子显微镜;Bruker AXS D8 Focus型X射线衍射仪(XRD)(铜钯,测定波长=0.154056 nm);UV-3600 UV-Vis-NIR型岛津固体紫外分光光度计;中教金源CEL-SPH2N型在线产氢系统和300 W氙灯;GC-2014C型岛津气相色谱仪。
聚乙烯吡咯烷酮(PVP,分析纯,分子量130万,阿拉丁试剂公司);无水乙醇(分析纯,国药集团化学试剂有限公司);冰醋酸(分析纯,国药集团化学试剂有限公司);醋酸镉(分析纯,国药集团化学试剂有限公司);钛酸四丁酯(TBT,分析纯,国药集团化学试剂有限公司);硫化钠(分析纯,国药集团化学试剂有限公司);其他试剂均为普通市售分析纯。
1.2 TiO2@CdS复合材料的制备 1.2.1 TiO2/CdO复合纳米纤维的制备取15 mL无水乙醇,加入0.65 g PVP,待PVP完全溶解后,加入1 mL TBT和1 mL冰醋酸,搅拌30 min。按照元素物质量Ti/Cd为1∶1、2∶1、4∶1和8∶1分别加入一定量的醋酸镉。待醋酸镉完全溶解后,利用静电纺丝制备纳米纤维。其中,电纺丝溶液的流速为0.5 mL/h,控制注射器针尖与收集板锡纸的距离15 cm,电压为15 kV。将所得的电纺丝纳米纤维在450 ℃处理3 h,获得TiO2/CdO复合纳米纤维。
1.2.2 TiO2@CdS中空纤维的合成取上面获得的TiO2/CdO复合纳米纤维50 mg,加入30 mL 1.0 mol/L的硫化钠溶液,转移到50 mL聚四氟乙烯的水热反应釜中120 ℃水热处理6 h,冷却到室温。将水热得到的黄色粉末用去离子水洗3次,离心后70 ℃烘箱烘干,最终得到TiO2@CdS复合材料。
1.3 TiO2@CdS复合材料产氢性能的表征取50 mg TiO2@CdS光催化剂,加入120 mL 25 %(体积分数)的甲醇溶液,光照负载1.0%(质量分数)的Pt纳米粒子。用中教金源CEL-SPH2N型在线产氢系统,在300 W氙灯和UVCUT-420 nm滤光片光照条件下,通过GC-2014C型岛津气相色谱仪来测定产氢量,从而表征TiO2@CdS的光催化产氢性能。
2 结果与讨论 2.1 电纺丝纳米复合纤维煅烧前后形貌分析图 1为电纺丝PVP/TBT-Cd(Ac)2纳米纤维在450 ℃煅烧前后的SEM图片。由图 1可以看出,处理前,纳米纤维表面光滑,直径大约250 nm。高温处理后,纳米纤维由于PVP的除去而变细,直径由原来的~250 nm变为~110 nm,且表面出 现了粗糙结构。这是由于在高温煅烧过程中,TBT和Cd(Ac)2都转化为相应的氧化物TiO2和CdO,形成由TiO2和CdO纳米颗粒堆积的TiO2/CdO纳米纤维(如图 1B中高放大倍数的SEM图片所示)。在相应的XRD图中,我们仅观测到晶态CdO的特征衍射峰。这表明所获得纳米纤维是由无定形的TiO2和晶态的CdO组成。如果提高煅烧温度,则有晶态的CdTiO3生成。

|
图1 Ti/Cd为1∶1(A,B)、2∶1(C,D)、4∶1(E,F)、8∶1(G,H)的电纺丝纳米复合纤维煅烧前后的SEM图 A、C、E、G为煅烧前;B、D、F、H为煅烧后 SEM images of Ti / Cd for 1∶1 (A,B),2∶1 (C,D),4∶1 (E,F),and 8∶1 (G,H) before (A,C,E and G) and after (B,D,F and H) calcination treatment |
为了将CdO转变为CdS,我们将TiO2/CdO纳米纤维放在Na2S的溶液中进行水热处理。水热处理后,样品由原来的白色变为黄色,说明有CdS生成。图 2为水热处理后所生成TiO2@CdS的SEM图片。由图 2可以看出,当Ti/Cd为1∶1和2∶1时,TiO2/CdO纳米纤维转化为由CdS超薄片层包覆的TiO2纳米管状结构(B,D),箭头标记处可以明显看出中空纳米管结构,2B中插图表明纳米薄片厚度在5 nm以下。当Ti/Cd为4∶1和8∶1时,纳米管不是很清晰(F,H),虚线标记为原始纳米纤维的轮廓,可以明显看出纤维内部是小颗粒堆积而成。

|
图2 TiO2@CdS样品的SEM照片 Ti/Cd分别为1∶1(A,B)、2∶1(C,D)、4∶1(E,F)和8∶1(G,H) SEM images of TiO2@CdS nanofibers prepared from the Ti / Cd of 1∶1 (A,B),2∶1 (C,D),4∶1 (E,F) ,and 8∶1 (G,H) |
由TiO2@CdS系列Ti/Cd为1∶1样品的EDAX能谱图(3A)可以看出,水热硫化处理后,Ti/Cd元素比例接近于1∶1,表明样品中的Ti和Cd接近于投料比。Cd/S的元素比也接近于1/1,说明水热硫化后,CdO完全转化为CdS。在EDAX能谱中出现了少量Na元素,表明在经过硫化钠水热处理时,可能有少量钠离子吸附在TiO2@CdS样品的表面。
图 3B为硫化前后以及高温氩气处理后的XRD图。在图 3B中,硫化处理前仅在33.0°、38.3°、55.3°、65.9°处观测到较弱的衍射峰,归属为CdO的特征峰(JCPDS no. 65-2908),所以硫化处理前的纳米纤维由无定形的TiO2和结晶的CdO组成。硫化处理后,在26.5°、30.8°、43.9°、
52.1°、54.5°、64.0°出现的衍射峰归属为立方相CdS的特征峰(JCPDS no. 10-0454);在24.8°和28.2°出现的微弱衍射峰归属为六方相CdS的特征峰(JCPDS no. 41-1049),TiO2的衍射特征峰没有出现。硫化处理后的XRD图说明TiO2@CdS样品,由立方相CdS、无定形的TiO2和少量六方相CdS组成。由于硫化处理后TiO2仍是无定形的不利于光催化性能的提升,所以我们想通过高温氩气下处理,将其转化为结晶的TiO2。高温600 ℃氩气下处理后的XRD图中,在24.8°、26.5°、28.2°、36.6°、43.7°、47.8°出现的衍射峰归属为六方相CdS的特征峰(JCPDS no. 41-1049);而在31.1°、34.2°、38.9°、59.3°出现的衍射峰归属为CdTiO3的特征峰(JCPDS no. 29-0277)。表明高温600 ℃氩气下处理后,CdS由立方相转变成六方相,有少量的钛酸镉生成,但是仍然没有观测到晶态TiO2的出现。

|
图3 (A)TiO2@CdS样品Ti/Cd为1∶1的EDAX能谱图;(B)硫化前后以及高温氩气处理后的XRD图,其中a是硫化前,b是硫化后, c是高温氩气处理硫化后,H-CdS表示六方相CdS,C-CdS表示六方相CdS;(C)氮气等温吸附脱附曲线,插图为孔径分布图 EDAX spectra for Ti / Cd of 1∶1 (A),B are the X-ray diffraction pattern for before (a) and after (b) sulfuration treatment,and high temperature treated sample b under argon atmosphere (c). H-CdS refers to hexagonal phase CdS,C-CdS refers to cubic phase CdS. C is the N2 adsorption-desorption curves,insets are the pore size distribution curves |
图 3C为TiO2@CdS纳米纤维的N2吸附曲线,其BET比表面积可以达到32.8 m2/g。
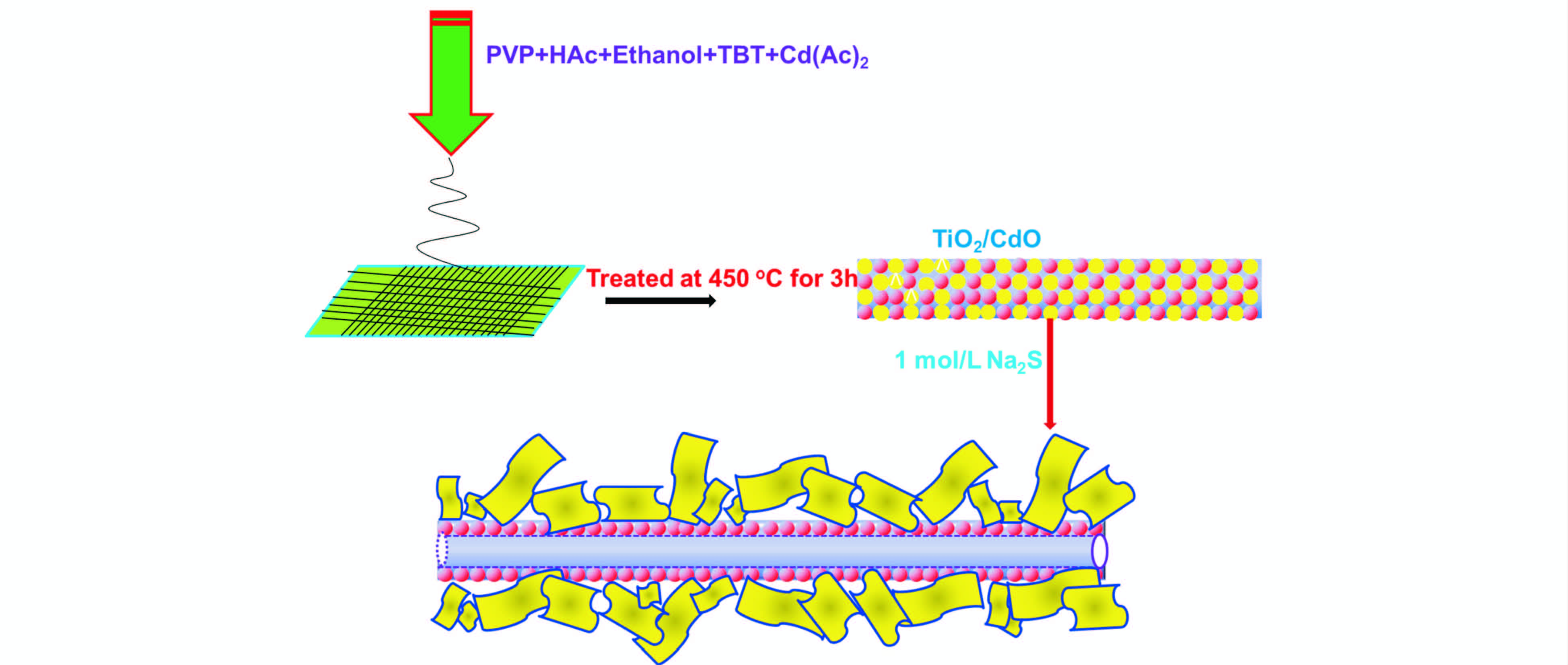
2.4 TiO2@CdS复合结构的形成过程根据TiO2@CdS复合结构的SEM、EDAX和XRD图,我们可以推测出纳米管的形成过程(图 4)。首先,用静电纺丝结合高温煅烧的方法制备了由CdO和TiO2纳米颗粒堆积的纳米纤维,在经过水热硫化处理后,由于纳米纤维中CdO的逐步溶解,导致表面TiO2纳米粒子首先聚集成一层致密的TiO2层,随着反应的进行,里面的CdO逐步溶解,导致里面的TiO2纳米粒子向外层沉积,而CdO溶解所形成的空间造成这种中空结构。同时外面溶解的CdO,与溶液中的硫离子生成更 加稳定的CdS,以超薄片层的结构生长在TiO2的表面。在Ti/Cd为1∶1和2∶1时,由于更多CdO的溶解,形成CdS超薄片层包覆TiO2纳米管的结构;而Ti/Cd为4∶1和8∶1时,由于溶解CdO的量较少,不足以形成TiO2纳米管,生成的CdS纳米片层结构也不能完全包覆TiO2纳米纤维。
|
图4 TiO2@CdS中空复合材料的形成过程 The schematic formation of TiO2@CdS hollow nanofibers composites |
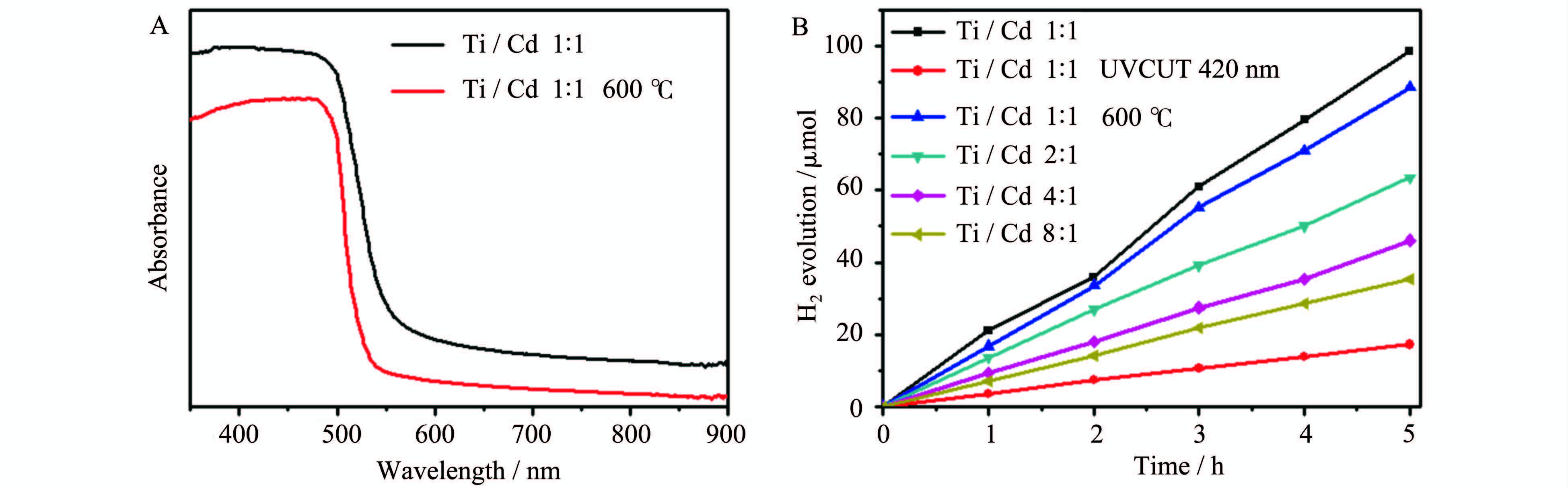
由Ti/Cd为1∶1硫化后和高温600 ℃氩气处理后的固体紫外吸收(图 5A)可以看出,高温600 ℃氩气处理后,固体紫外吸收带边明显的蓝移。这是因为,硫化处理时,生成低温更加稳定的立方相CdS,而高温600 ℃氩气处理后则转变成六方相CdS,从而引起固体紫外吸收的蓝移。TiO2@CdS在300 W氙灯光照下和UVCUT-420 nm滤光片条件下,产氢曲线见图 5B,在全光谱照射下,Ti/Cd为1∶1、2∶1、4∶1和8∶1的TiO2@CdS 50 mg催化剂,产氢速率依次为19.7 μmol/h、12.7 μmol/h、 9.2 μmol/h和7.0 μmol/h。由于硫化处理后TiO2仍是无定形的,不利于光催化的应用,所以我们想通过高温氩气处理,将其转化为结晶的TiO2。高温600 ℃氩气处理后,在全光谱照射下,Ti/Cd为1∶1的TiO2@CdS 50 mg催化剂,产氢速率为17.7 μmol/h。由于TiO2@CdS样品,TiO2没有结晶,产氢活性主要来源于CdS,所以产氢活性随着钛镉比的增加而减少;同时高温600 ℃氩气处理后,TiO2也没有结晶,产氢活性没有增强。当钛镉比为1∶1时,具有最好的产氢活性。Ti/Cd为1∶1的TiO2@CdS 50 mg催化剂,在UVCUT 420滤光片下,产氢速率为3.4 μmol/h。
|
图5 (A)Ti/Cd为1∶1硫化后和高温600 ℃氩气处理后的固体紫外吸收;(B)TiO2@CdS在300 W氙灯和 UVCUT-420 nm滤光片条件下不同样品的产氢曲线 Diffusion reflection UV-Vis spectra for Ti / Cd of 1∶1 nanofibers after sulfuration treatment and heat treatment at 600℃ under argon atmosphere,B is H2 production rate of TiO2@CdS samples under 300 W Xe lamp without and with a UVCUT-420 nm filter |
通过静电纺丝结合高温煅烧的方法,制备了不同钛镉比的纳米纤维。用一步简单的硫化钠溶液水热处理,得到CdS超薄片层包覆TiO2中空结构的复合材料。当Ti/Cd为1∶1和2∶1时,形貌为CdS超薄片层包覆的TiO2纳米管;当Ti/Cd为4∶1和8∶1时,纳米管消失。由此我们提出复合形貌的形成过程:首先,硫化处理前的纳米纤维是由CdO和TiO2纳米颗粒堆积成,水热硫化处理时,由于CdO的溶解,里面TiO2形成中空纳米结构,同时溶解的CdO,与反应液中的S2-生成CdS超薄片层,覆盖在TiO2纳米管的表面。而Ti/Cd为4∶1和8∶1时,由于CdO的含量较少,不足以形成TiO2纳米管,所生成的CdS纳米片层结构也不足以完全包覆TiO2纳米纤维。当Ti/Cd为1∶1时,TiO2@CdS复合材料具有最好的产氢活性。在300 W氙灯下和加UVCUT-420 nm滤光片下,50 mg催化剂产氢速率分别为19.7 μmol/h和3.4 μmol/h。
| [1] | Chen X B, Mao S S. Titanium dioxide nanomaterials:synthesis, properties, modifications, and applications [J]. Chemical Reviews, 2007, 107(7): 2891-2959. |
| [2] | Chen X B, Shen S, Guo L, Mao S S. Semiconductor-based photocatalytic hydrogen generation [J]. Chemical Reviews, 2010, 110(11): 6503-6570. |
| [3] | Acar C, Dincer I, Zamfirescu C. A review on selected heterogeneous photocatalysts for hydrogen production [J]. International Journal of Energy Research, 2014, 38(15): 1903-1920. |
| [4] | Kubacka A, Fernandez-Garcia M, Colon G. Advanced nanoarchitectures for solar photocatalytic applications [J]. Chemical Reviews, 2012, 112(3): 1555-1614. |
| [5] | Ma Y, Wang X, Jia Y, Chen X, Han H, Li C. Titanium dioxide-based nanomaterials for photocatalytic fuel generations [J]. Chemical Reviews, 2014, 114(19): 9987-10043. |
| [6] | Chen C, Cai W, Long M, Zhou B, Wu Y, Wu D, Feng Y. Synthesis of visible-light responsive graphene oxide/TiO2 composites with p/n heterojunction [J]. ACS Nano, 2010, 4(11): 6425-6432. |
| [7] | Bach U, Lupo D, Comte P, Moser J, Weissortel F, Salbeck J, Spreitzer H, Gratzel M. Solid-state dye-sensitized mesoporous TiO2 solar cells with high photon-to-electron conversion efficiencies [J]. Nature, 1998, 395(6702): 583-585. |
| [8] | Charoensirithavorn P, Ogomi Y, Sagawa T, Hayase S, Yoshikawa S. Improvement of dye-sensitized solar cell through TiCl4-treated TiO2 nanotube arrays [J]. Journal of The Electrochemical Society, 2010, 157(3): B354-B356. |
| [9] | Pandikumar A, Murugesan S, Ramaraj R. Functionalized silicate sol-gel-supported TiO2-Au core-shell nanomaterials and their photoelectrocatalytic activity [J]. ACS Applied Materials & Interfaces, 2010, 2(7): 1912-1917. |
| [10] | Subramanian V, Wolf E E, Kamat P V. Influence of metal/metal ion concentration on the photocatalytic activity of TiO2-Au composite nanoparticles [J]. Langmuir, 2003, 19(2): 469-474. |
| [11] | Tom R T, Nair A S, Singh N, Aslam M, Nagendra C, Philip R, Vijayamohanan K, Pradeep T. Freely dispersible Au@ TiO2, Au@ ZrO2, Ag@ TiO2, and Ag@ ZrO2 core-shell nanoparticles: one-step synthesis, characterization, spectroscopy, and optical limiting properties [J]. Langmuir, 2003, 19(8): 3439-3445. |
| [12] | Di Valentin C, Pacchioni G, Selloni A. Reduced and n-type doped TiO2: nature of Ti3+ species [J]. The Journal of Physical Chemistry C, 2009, 113(48): 20543-20552. |
| [13] | Liu M, Qiu X, Miyauchi M, Hashimoto K. Cu (Ⅱ) oxide amorphous nanoclusters grafted Ti3+ self-doped TiO2: an efficient visible light photocatalyst [J]. Chemistry of Materials, 2011, 23(23): 5282-5286. |
| [14] | Liu X, Gao S, Xu H, Lou Z, Wang W, Huang B, Dai Y. Green synthetic approach for Ti3+ self-doped TiO2-x nanoparticles with efficient visible light photocatalytic activity[J]. Nanoscale, 2013, 5(5): 1870-1875. |
| [15] | Park J H, Kim S, Bard A J. Novel carbon-doped TiO2 nanotube arrays with high aspect ratios for efficient solar water splitting [J]. Nano Letters, 2006, 6(1): 24-28. |
| [16] | Serpone N, Lawless D, Disdier J, Herrmann J M. Spectroscopic, photoconductivity, and photocatalytic studies of TiO2 colloids: naked and with the lattice doped with Cr3+, Fe3+, and V5+ cations [J]. Langmuir, 1994, 10(3): 643-652. |
| [17] | Wei H, Wu Y, Lun N, Zhao F. Preparation and photocatalysis of TiO2 nanoparticles co-doped with nitrogen and lanthanum [J]. Journal of Materials Science, 2004, 39(4): 1305-1308. |
| [18] | Zheng Z, Huang B, Meng X, Wang J, Wang S, Lou Z, Wang Z, Qin X, Zhang X, Dai Y. Metallic zinc-assisted synthesis of Ti3+ self-doped TiO2 with tunable phase composition and visible-light photocatalytic activity [J]. Chemical Communications, 2013, 49(9): 868-870. |
| [19] | Zuo F, Wang L, Wu T, Zhang Z, Borchardt D, Feng P. Self-doped Ti3+ enhanced photocatalyst for hydrogen production under visible light [J]. Journal of The American Chemical Society, 2010, 132(34): 11856-11857. |
| [20] | Burda C, Lou Y, Chen X, Samia A C, Stout J, Gole J L. Enhanced nitrogen doping in TiO2 nanoparticles [J]. Nano letters, 2003, 3(8): 1049-1051. |
| [21] | Etgar L, Gao P, Xue Z, Peng Q, Chandiran A K, Liu B, Nazeeruddin M K, Graatzel M. Mesoscopic CH3NH3PbI3/TiO2 heterojunction solar cells [J]. Journal of The American Chemical Society, 2012, 134(42): 17396-17399. |
| [22] | Hou Y, Li X, Zhao Q, Quan X, Chen G. Fabrication of Cu2O/TiO2 nanotube heterojunction arrays and investigation of its photoelectrochemical behavior [J]. Applied Physics Letters, 2009, 95(9): 093108-093108-3. |
| [23] | Huang H, Li D, Lin Q, Zhang W, Shao Y, Chen Y, Sun M, Fu X. Efficient degradation of benzene over LaVO4/TiO2 nanocrystalline heterojunction photocatalyst under visible light irradiation [J]. Environmental Science & Technology, 2009, 43(11): 4164-4168. |
| [24] | Liou F T, Yang C Y, Levine S N. Photoelectrolysis at Fe2O3/TiO2 heterojunction electrode [J]. Journal of the Electrochemical Society, 1982, 129: 342-345. |
| [25] | Lai C Y, Trewyn B G, Jeftinija D M, Jeftinija K, Xu S, Jeftinija S, Lin V S Y. A mesoporous silica nanosphere-based carrier system with chemically removable CdS nanoparticle caps for stimuli-responsive controlled release of neurotransmitters and drug molecules [J]. Journal of the American Chemical Society, 2003, 125(15): 4451-4459. |
| [26] | Li Q, Guo B, Yu J, Ran J, Zhang B, Yan H, Gong J R. Highly efficient visible-light-driven photocatalytic hydrogen production of CdS-cluster-decorated graphene nanosheets [J]. Journal of the American Chemical Society, 2011, 133(28): 10878-10884. |
| [27] | Baker D R, Kamat P V. Photosensitization of TiO2 nanostructures with CdS quantum dots: particulate versus tubular support architectures [J]. Advanced Functional Materials, 2009, 19(5): 805-811. |
| [28] | Das K, De S. Optical properties of the type-II core-shell TiO2@CdS nanorods for photovoltaic applications [J]. The Journal of Physical Chemistry C, 2009, 113(9): 3494-3501. |
| [29] | Fujii H, Inata K, Ohtaki M, Eguchi K, Arai H. Synthesis of TiO2/CdS nanocomposite via TiO2 coating on CdS nano-particles by compartmentalized hydrolysis of Ti alkoxide [J]. Journal of Materials Science, 2001, 36(2): 527-532. |
| [30] | Gao X F, Sun W T, Hu Z D, Ai G, Zhang Y L, Feng S, Li F, Peng L M. An efficient method to form heterojunction CdS/TiO2 photoelectrodes using highly ordered TiO2 nanotube array films [J]. The Journal of Physical Chemistry C, 2009, 113(47): 20481-20485. |
| [31] | Hsu M C, Leu C, Sun Y M, Hon M H. Fabrication of CdS@ TiO2 coaxial composite nanocables arrays by liquid-phase deposition [J]. Journal of Crystal Growth, 2005, 285(4): 642-648. |
| [32] | Cao J, Sun J Z, Li H Y, Hong J, Wang M. A facile room-temperature chemical reduction method to TiO2@CdS core/sheath heterostructure nanowires [J]. Journal of Materials Chemistry, 2004, 14(7): 1203-1206. |




