发展廉价、高效、具有可见光响应的光催化材料是光催化领域的核心课题[1]。经过40余年的研究,在光催化材料研发方面取得了一些标志性的成果,发展了众多的光催化材料体系,但这些材料主要集中于二元及多元金属半导体化合物[2, 3]。最近,石墨相氮化碳(g-C3N4)作为一种不含金属组分的聚合物半导体被确立为一种新型的可见光催化剂,因其具有合适的带隙(2.7 eV)和带边、优异的化学稳定性、价格低廉等诸多优点,引起了人们的广泛关注[4 ,5]。
然而,g-C3N4作为光催化剂还存在一些问题,如:比表面积小(<10 m2·g-1)、产生光生载流子的激子结合能高、光生电子-空穴复合严重、量子效率低和禁带宽度较大而不能高效利用太阳光等[5]。围绕解决这些关键问题,已开展了大量行之有效的改性工作,主要改性手段包括:合成纳米级的g-C3N4、金属/非金属元素掺杂、添加高效助催化剂、染料敏化、形成g-C3N4基复合体系等,采用这些改性手段均可不同程度地提高g-C3N4的光催化活性[6, 7, 8, 9, 10, 11]。
与传统的常见光催化剂相比,g-C3N4不仅有聚合物独特的合成组分易调变优势,而且具有层状结构及层面内存在较活二配位氮原子的特点,这些特性为改性g-C3N4提供了独特的视角。本文正是基于以上理解,提出将碳掺杂与热缩聚过程原位高效的结合以制备碳掺杂的g-C3N4。通过在双氰胺前驱体中加入聚乙二醇制得碳掺杂的含氮空位的g-C3N4,该材料兼具宽的可见光响应范围和高的可见光降解RhB及光催化产氢活性。
1 实验部分 1.1 试剂与仪器双氰胺(纯度99%)和聚乙二醇-4000(分析纯)分别购自Sigma-Aldrich和阿拉丁试剂公司。
采用D/MAX2400X射线衍射仪(XRD)、BrukerTENSOR 27傅立叶变换红外光谱仪(FTIR)、ThermoEsclab250光电子能谱仪(XPS)(单色Al KαX射线,结合能以284.6 eV的C1s峰为内标校正)、JASCO V-550紫外-可见分光光度计、FLSP-920荧光光谱仪对材料结构性能进行表征测试。
1.2 光催化剂制备采用简单常用的固相热缩聚法制备光催化剂[4]。纯g-C3N4参比样品的制备过程为:将3 g双氰胺放入瓷舟中,置于马弗炉内以2.3 ℃/min的升温速率加热至550 ℃保温4 h,自然冷却后研磨得黄色粉末样品。
碳掺杂的g-C3N4制备过程为:分别称取5 mg、10 mg、20 mg、30 mg、50 mg聚乙二醇-4000(PEG)溶解在20 mL去离子水中,再向溶液中加入3 g双氰胺。在搅拌状态下将混合液加热至80 ℃直至将溶剂蒸干。将干的双氰胺-聚乙二醇混合物研磨,采用同制备纯g-C3N4完全一样的温度程序制得掺杂样品,产率约为6%~10%。将所制样品标记为g-C3N4-(X) PEG (X为PEG添加量)。
1.3 光催化活性评价(1) 羟基自由基测试
将5 mg催化剂分散在80 mL浓度为10 mmol/L NaOH、3 mmol/L对苯二酸的溶液中,在暗态下磁力搅拌至吸附平衡后取5 mL初始溶液。之后开光源照射,每隔一定时间取5 mL溶液置于暗处。取样结束后,将溶液以10000 r/min离心5 min,取上层清液,用FLSP-920对其稳态发光信号进行测量。通过检测426 nm处信号峰的强度变化确定催化剂产生羟基自由基的能力。
(2) 光降解罗丹明B (RhB)测试
将20 mg样品分散在100 mL浓度为2×10-5mol/L的罗丹明B溶液中,采用与羟基自由基测试类似的取样离心过程,用分光光度计进行浓度及光吸收谱的测量。浓度标定曲线由标量的不同浓度的罗丹明B在554 nm下的光吸收强度进行标定。
(3) 光催化产氢测试
光解水反应制氢在真空玻璃系统中进行。测试前,将50 mg光催化剂分散到300 mL水溶液(含10%体积比的三乙醇胺)中,并加入3 mL浓度为1 mg/mL的铂助催化剂前驱体氯铂酸溶液。对整个玻璃系统抽真空至20 Pa后开灯光照,通过循环冷却水系统使得光解水反应的温度控制在10~13 ℃。反应产生的气体经过风扇循环平衡后,由氩气作为载气送入气相色谱(日本岛津公司的GC-2014,TCD检测器)进行定量分析。
以上光催化活性测试均采用300 W的氙灯(PLS-SXE-300UV)顶部照射,分别在紫外-可见光和可见光(λ>420 nm)照射下进行。
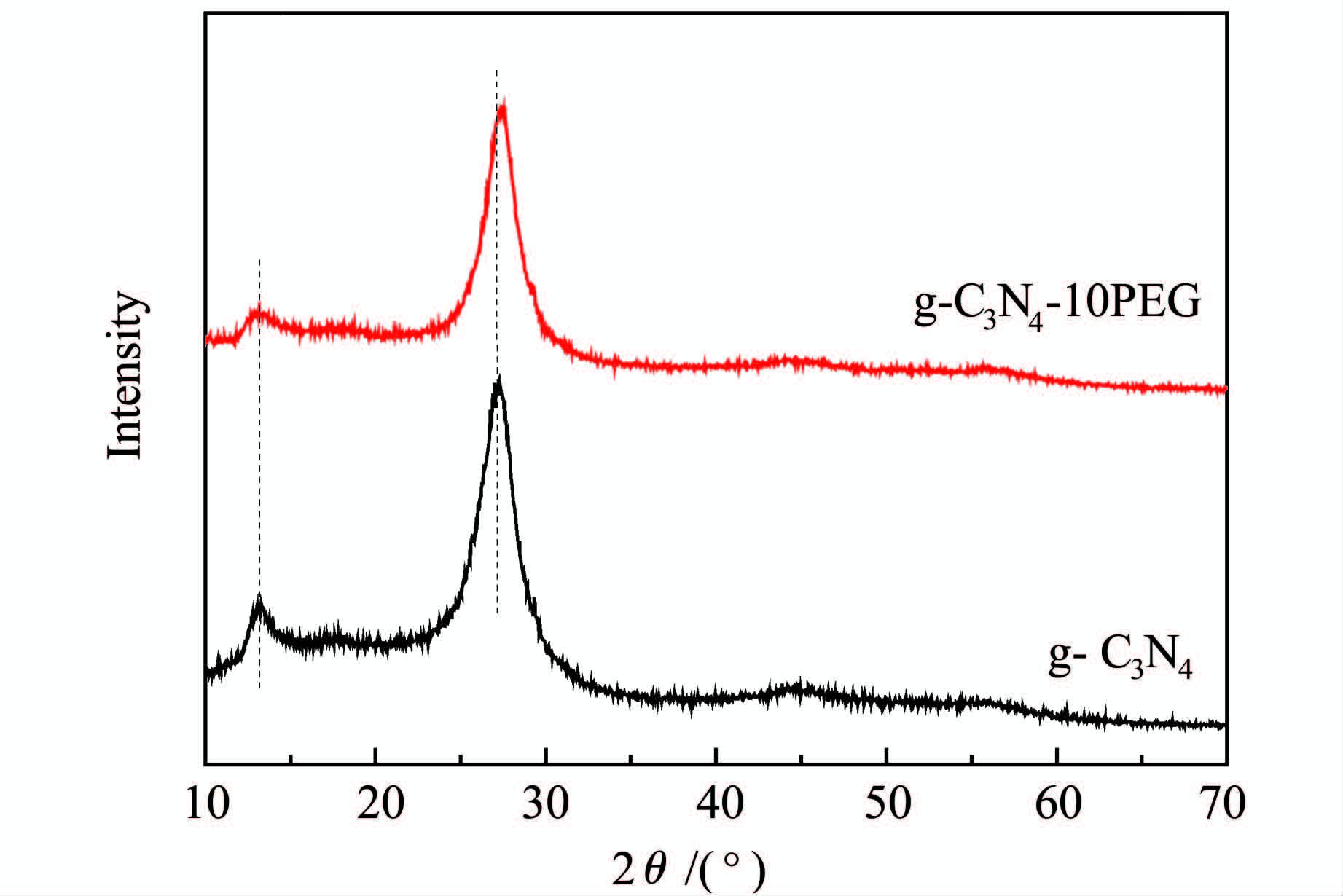
2 结果与讨论 2.1 光催化剂的物相结构表征首先考察了PEG添加量对g-C3N4光催化活性的影响规律,羟基自由基氧化测试结果表明,催化活性随添加量的增加先增加后降低,确定g-C3N4-10PEG样品具有最高的光催化活性,故仅对该样品进行详细的研究。图 1为所制g-C3N4-10PEG及参比样品g-C3N4的XRD图。g-C3N4-10PEG与g-C3N4都具有典型石墨相碳化氮结构的特征衍射峰,其中27.2°峰对应于(002)晶面,表示长程的π共轭平面的周期性堆垛[12],而13.1°峰对应于(100)晶面,表示层内七嗪环结构单元的周期性排列[13]。该结果表明,添加PEG改性样品仍较好地保留了g-C3N4的特征结构。但与纯g-C3N4仔细对比发现,g-C3N4-10PEG样品在27.2°的衍射峰向高角偏移到了27.4°,依据布拉格衍射定理可知样品的层间距离有所减小,表明添加PEG对g-C3N4的层与层之间的堆垛产生了一定的影响。此外,该样品的衍射峰强度有所降低,尤其是位于13.1°的衍射峰强度明显降低,当PEG添加量达6%(质量分数)时该峰则完全消失,这表明添加PEG使g-C3N4的层内增加了一些缺陷,周期性结构受到一定的破坏。
|
图1 样品g-C3N4与g-C3N4-10PEG的XRD衍射图 XRD patterns of g-C3N4 and g-C3N4-10PEG samples |
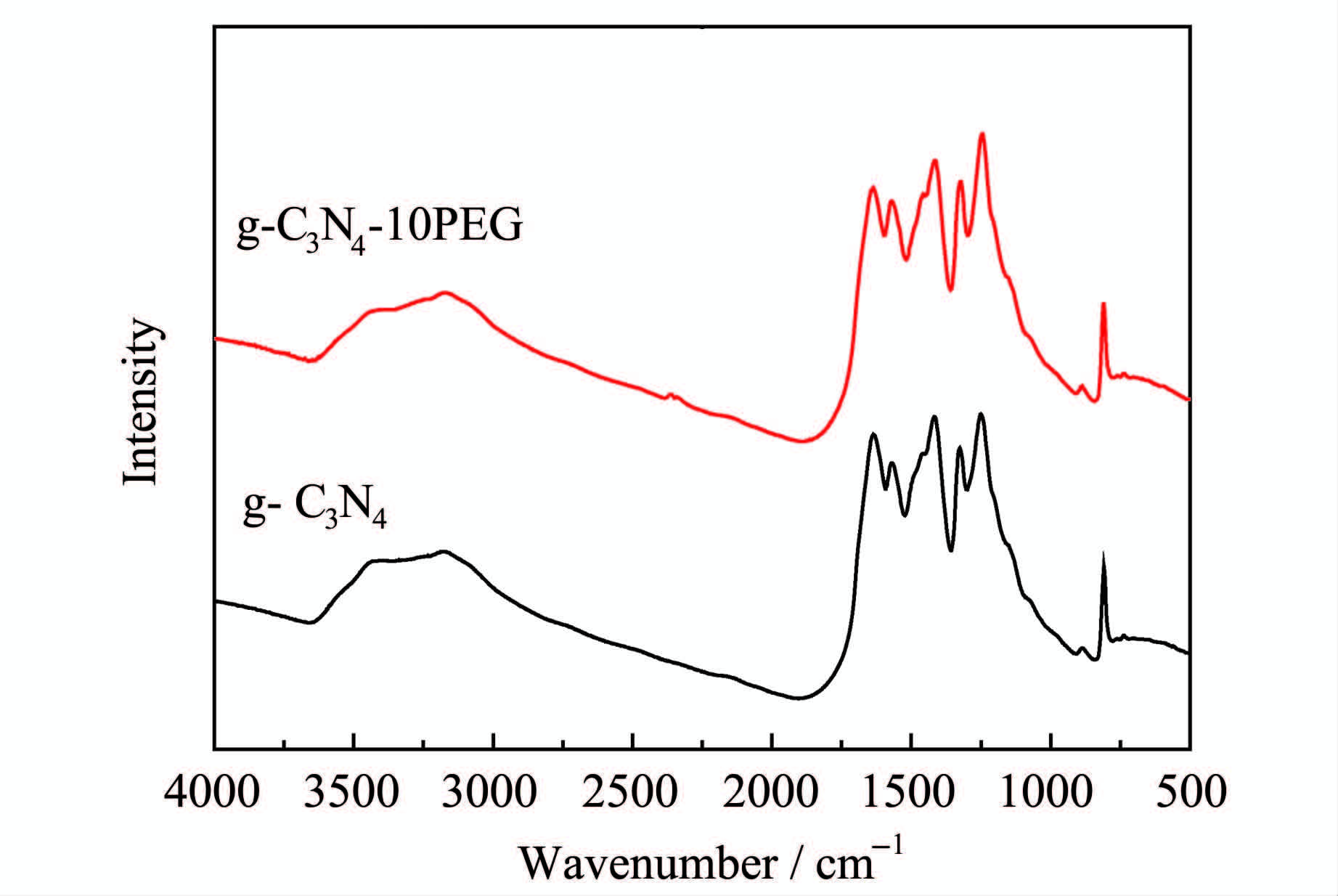
采用傅里叶变换红外光谱表征样品的键价结构,进一步确认添加PEG未明显改变所制样品的晶体结构。从图 2看出,g-C3N4-10PEG样品具有g-C3N4所有典型的红外光谱特征峰:在812 cm-1处的红外吸收对应于“heptazine”的弯曲模式,表明基本“melon”单元未被破坏,在900~1800 cm-1及3000~3500 cm-1区间分别对应于C—N(C)—C或桥接的C—NH—C单元和不完全缩聚的初次及二次氨基的存在,表明两者具有相似的短程有序原子结构[13, 14, 15]。但是与g-C3N4样品相比略有不同的是,g-C3N4-10PEG样品在2000 cm-1下的峰部分向低频有所偏移,且强度有所增加,说明添加PEG对面内微观结构有一定的破坏,这与上述XRD的结果相一致。值得一提的是,这些物相结构变化与我们前期研究在高温下合成含氮空的g-C3N4过程中所观察到的结构变化完全相似[8, 9]。
|
图2 样品g-C3N4与g-C3N4-10PEG的红外吸收光谱 FTIR spectra of the g-C3N4 and g-C3N4-10PEG samples |
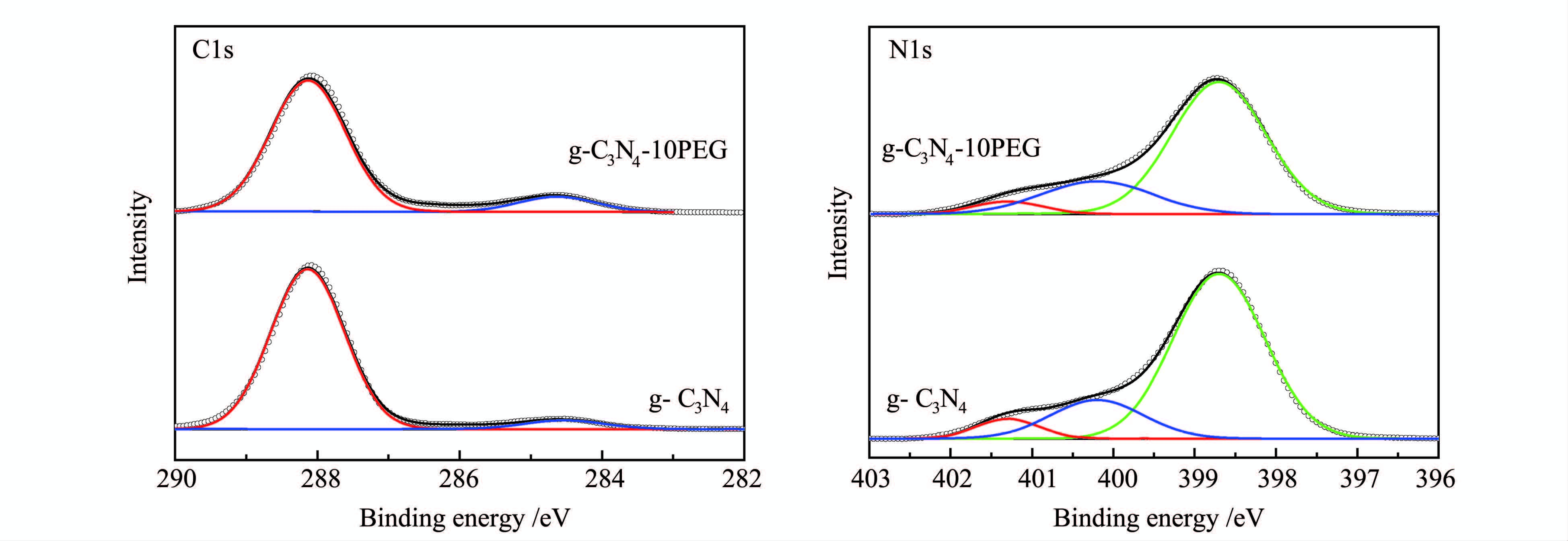
为表征添加PEG所引起g-C3N4-10PEG样品中的缺陷结构及组分变化,对样品进行了XPS元素分析,如图 3所示。从图中可以看出,g-C3N4和g-C3N4-10PEG样品的C1s和N1s内电子的结合能特征峰相似,表明两者具有相似的化学态。两个样品中C1s位于284.6 eV和288.1 eV的特征峰分别来源于石墨碳和g-C3N4平面结构中三配位碳原子C3C[15]。通过分峰处理可明显看出N1s有3个特征峰,峰位大致位于398.6 eV、400.3 eV和401.3 eV,依次对应于g-C3N4平面结构中C—N—C(N2C)、N—(C)3(N3C)和C—N—H中的N原子[12]。虽然两个样品具有相同的N原子配位结构,但是特征峰的比例具有明显的差异。依据峰面积计算表明,样品g-C3N4中表面N2C/N3C的峰面积比为4.1,而样品g-C3N4-10PEG中该比例为3.4,较前者显著降低。相应的样品表面的C/N元素比从参比样品g-C3N4的0.76增加到g-C3N4-10PEG样品的0.84。这些组分变化说明添加PEG使g-C3N4在缩聚过程中表面产生大量的二配位氮空位。究其原因可能源于在缩聚过程中PEG分解生成的外源C通过掺杂增大了g-C3N4中的C/N原子比例从而导致其表面产生大量的氮空位。由于g-C3N4-10PEG样品较好的保持了g-C3N4的类石墨层状结构特征,氮空位的形成应发生在整个材料内。这点可从XPS的表面组分分析结果与体相的XRD物相分析看到平面结构受到一定的破坏相一致得到初步的证实。
|
图3 样品g-C3N4与g-C3N4-10PEG中C1s与N1s的高分辨XPS谱 High resolution XPS spectra of C1s and N1s for g-C3N4 and g-C3N4-10PEG samples |
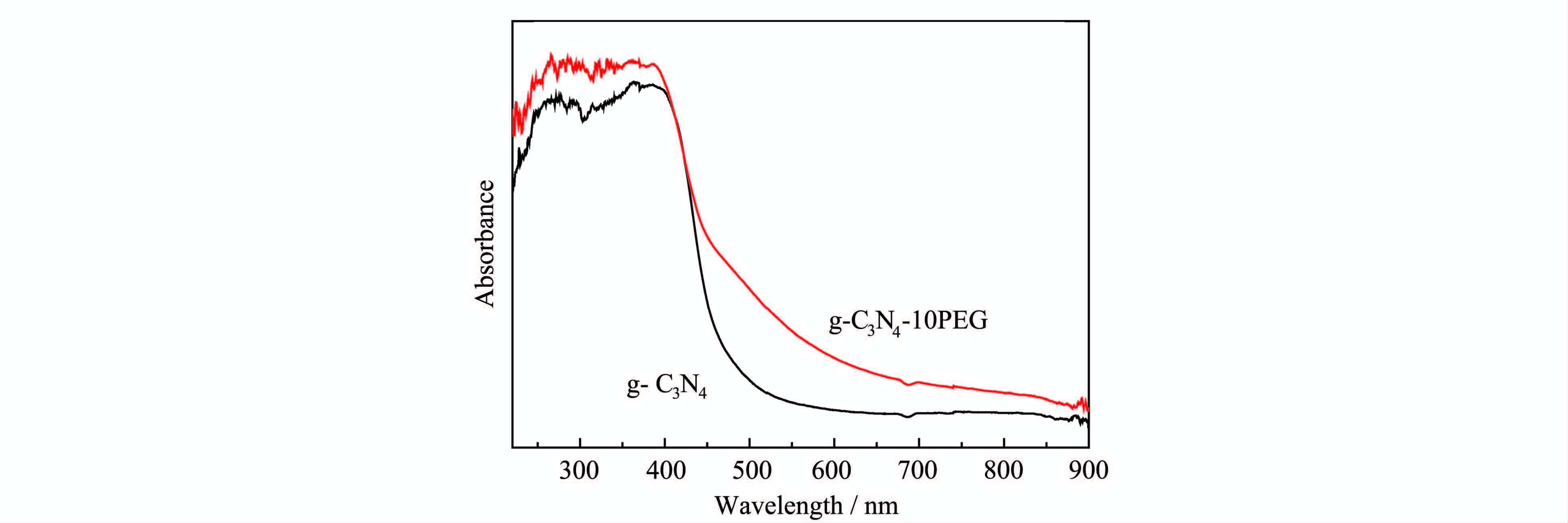
氮空位的形成对g-C3N4的光谱性能产生了显著的影响。从图 4所给出的紫外-可见吸收光谱可以清楚的看出,含氮空位的g-C3N4-10PEG样品的可见光吸收较g-C3N4有明显增加,在450 nm处出现肩膀状吸收并将可见光响应范围拓展至850 nm红外区。与此相一致的是,g-C3N4-10PEG的颜色也从未掺杂g-C3N4的浅黄色变为棕黄色,并且改变幅度随PEG添加量的增加而越发显著。可见光吸收的大幅增加主要源于氮空位缺陷导致在带隙中产生一些局域能级所致。相似的现象在掺杂TiO2等金属半导体光催化材料中也经常可见[14]。
|
图4 样品g-C3N4与g-C3N4-10PEG的紫外-可见吸收光谱 UV-visible light absorption spectra of g-C3N4 and g-C3N4-10PEG samples |
稳态荧光发光光谱进一步研究表明,g-C3N4-10PEG样品中荧光发光峰的强度较纯g-C3N4样品显著降低,如图 5所示。这表明氮空位的生成显著降低了光生电子空穴的发光复合几率,说明空位缺陷可捕获光生载流子,有效抑制载流子的复合。此外,g-C3N4-10PEG样品的发光峰出现少许宽化,这可能与所形成的不均匀局域能级相关。

|
图5 样品g-C3N4与g-C3N4-10PEG的荧光发射光谱(激发波长350 nm) Fluorescence emission spectra of g-C3N4 and g-C3N4-10PEG samples (350 nm excitation) |
为研究引入氮空位对光催化活性的影响,对g-C3N4-10PEG及参比g-C3N4样品进行了光降解RhB,以及三乙醇胺牺牲剂下光催化产氢的测试。图 6给出了紫外-可见光和可见光(λ>420 nm)照射下RhB浓度随时间的变化图。需说明的是,在没有催化剂条件下,RhB即使在长时间光照下几乎没有分解。从图中可看出,不论在紫外-可见光还是可见光照射下,g-C3N4-10PEG较g-C3N4具有更高的光降解RhB活性,尤其是在可见光照射下性能优势更加明显。在紫外-可见光谱照射下,g-C3N4-10PEG可在40 min内将RhB降解完全,而g-C3N4在相同时间内只能降解42%的RhB;在可见光照射下,g-C3N4-10PEG可在50 min内完全降解RhB,而g-C3N4在相同时间内只能降解30%。在紫外-可见光与可见光条件下g-C3N4-10PEG光降解RhB能力分别提高了2.3倍和3.3倍。此外,RhB浓度随光照时间近乎呈线性的降低,表明g-C3N4-10PEG与g-C3N4一样都是较稳定的光催化剂。

|
图6 g-C3N4与g-C3N4-10PEG在不同光照条件下的光降解RhB活性对比 Comparison of photodegradation activity of g-C3N4 and g-C3N4-10PEG samples under UV-visible light and visible light |
光催化产氢结果进一步证实碳掺杂引入氮空位可显著提高光催化活性。图 7给出了在紫外-可见光和可见光下各照射5 h的产氢量对比。在紫外-可见光照射下,g-C3N4的平均产氢速率为48 μmol/h,g-C3N4-10PEG的产氢速率为124 μmol/h,提高了约2.6倍;在可见光(λ>420 nm)照射下,g-C3N4的平均产氢速率为5 μmol/h,g-C3N4-10PEG的产氢速率为34 μmol/h,提高了约6.8倍,显然,在可见光条件下的性能提升更为显著。

|
图7 样品g-C3N4与g-C3N4-10PEG 在不同光照条件下的光催化产氢对比 Comparison of photocatalytic hydrogen evolution of g-C3N4and g-C3N4-10PEG samplesunder UV-visible light and visible light |
本文在双氰胺前驱体中加入聚乙二醇,在热缩聚形成g-C3N4的过程中,成功实现原位碳掺杂制备出含氮空位的g-C3N4。与纯g-C3N4样品相比,含氮空位g-C3N4样品的可见光吸收被拓展至850 nm,在紫外-可见光与可见光照射下光降解RhB以及三乙醇胺作为牺牲剂条件下光催化产氢性能均大幅提高,尤其是在可见光条件下的催化活性提升更为显著。
| [1] | Fujishima A, Honda K. Electrochemical photolysis of water at a semiconductor electrode[J]. Nature (London),1972,238(5358): 37-38. |
| [2] | Kudo A,Miseki Y. Heterogeneous photocatalyst materials for water splitting[J]. Chemical Society Reviews,2009, 38(1): 253-278. |
| [3] | Wen F Y,Yang J H,Zong X,Ma Y,Xu Q,Ma B J,Li C. Photocatalytic hydrogen production utilizing solar energy[J]. Progress in Chemistry,2009,21(11): 2285-2302. |
| [4] | Wang X, Maeda K, Thomas A, Takanabe K, Xin G, Carlsson J M, Domen K,Antonietti M. A metal-free polymeric photocatalyst for hydrogen production from water under visible light[J]. Nature Materials, 2009, 8(1): 76-80. |
| [5] | Zhang J H, Wang B, Wang X C. Carbon nitride polymeric semiconductor for photocatalysis[J]. Progress in Chemistry,2014, 26(1) : 19-29. |
| [6] | Goettmann F, Fischer A, Antonietti M,Thomas A. Metal-free catalysis of sustainable Friedel-Crafts reactions: direct activation of benzene by carbon nitrides to avoid the use of metal chlorides and halogenated compounds[J]. Chemical Communications,2006, (43): 4530-4532. |
| [7] | Goettmann F, Fischer A, Antonietti M,Thomas A. Chemical synthesis of mesoporous carbon nitrides using hard templates and their use as a metal-free catalyst for Friedel-Crafts reaction of benzene[J]. Angewandte Chemie-International Edition, 2006, 45(27): 4467-4471. |
| [8] | Niu P, Liu G, Cheng H M. Nitrogen vacancy-promoted photocatalytic activity of graphitic carbon nitride[J]. The Journal of Physical Chemistry C,2012, 116(20): 11013-11018. |
| [9] | Niu P, Yin L C, Yang Y Q, Liu G, Cheng H M. Increasing the visible light absorption of graphitic carbon nitride (melon) photocatalysts by homogeneous self-modification with nitrogen vacancies[J]. Advanced Materials,2014, 26(47): 8046-8052. |
| [10] | Tong H, Ouyang S, Bi Y, Umezawa N, Oshikiri M,Ye J. Nano-photocatalytic materials: possibilities and challenges[J]. Advanced Materials,2012, 24(2): 229-251. |
| [11] | Ni M, Leung M K H, Leung D Y C,Sumathy K. A review and recent developments in photocatalytic water-splitting using TiO2 for hydrogen production[J]. Renewable and Sustainable Energy Reviews,2007,11(3): 401-425. |
| [12] | Thomas A, Fischer A, Goettmann F, Antonietti M, Müller J O, Schlgl R,Carlsson J M. Graphitic carbon nitride materials: variation of structure and morphology and their use as metal-free catalysts[J]. Journal of Materials Chemistry,2008, 18(41): 4893-4908. |
| [13] | Lotsch B Y, Doeblinger M, Sehnert J, Seyfarth L, Senker J, Oeckler O,Schnick W. Unmasking melon by a complementary approach employing electron diffraction, solid-state NMR spectroscopy, and theoretical calculations-structural characterization of a carbon nitride polymer[J]. Chemistry A Europe Journal,2007, 13(17): 4969-4980. |
| [14] | Bojdys M J, Mueller J O, Antonietti M,Thomas A. Ionothermal synthesis of crystalline, condensed, graphitic carbon nitride[J]. Chemistry A Europe Journal, 2008, 14(27): 8177-8182. |
| [15] | Qiu Y,Gao L. Chemical synthesis of turbostratic carbon nitride, containing C-N crystallites, at atmospheric pressure[J]. Chemical Communications,2003, (18): 2378-2379. |




