2. 华东理工大学 化学与分子工程学院 结构可控先进功能材料及其制备教育部重点实验室, 上海 200237
2. Key Laboratory for Advanced Materials, School of Chemistry and Molecular Engineering, East China University of Science and Technology, Shanghai 200237, P.R. China
在过去几十年里,许多功能化的聚合物胶束在药物传递中应用十分广泛。其中,用于控制药物释放的环境响应型(包括对温度、pH、光等刺激的响应)载体吸引了许多研究者的注意力[1, 2]。而在众多的响应载体中,光响应载体具有“洁净、无创、高效”和“定时、定点、定速”的优点[3]。并且,相对于其他响应,光反应不需要任何特定化学环境的变化[4],只需要开启或关闭光源就可以控制光反应过程。
构建光响应胶束主要有两种策略:(1)光照使光扳机发生可逆的结构变化[5, 6, 7]。常用螺吡喃、偶氮苯等构建此类胶束。这些基团光异构化的可逆性不仅能使胶束解组装,也可使胶束重新组装;(2)光照诱发光扳机不可逆的断裂[8, 9, 10]。构建此类胶束体系的光扳机包括邻硝基苄基类、香豆素类等。光照使得光扳机离去,从而胶束解组装。这两种胶束体系相比,前者对亲疏水平衡改变较弱,光响应动力学慢,每个光照周期,胶束体系很难恢复至初始状态,因此应用受到很大限制。
光响应型胶束的结构通常由一条亲水性主链及连有疏水性的光扳机侧链组成[11]。光照后,疏水段的极性发生变化,从而导致胶束解组装。例如Liu等合成的S-(o-硝基苄酯)-L-半胱氨酸和PEG组成的嵌段共聚物,光照诱发o-硝基苄基断裂,疏水作用减弱,释放药物[12]。除了作为疏水侧链,光扳机也可插入主链重复单元中。光照导致主链断裂,胶束内核快速降解,伴随药物“暴释”。例如Zhao合成的主链疏水段含有硝基苯类重复单元的两亲性三嵌段共聚物PEO-b-PUNB-b-PEO,光照下疏水段快速降解为小分子,胶束疏水核快速瓦解,释放药物[13]。还有一类胶束是以单个光扳机作为胶束壳与核的连接部分,光照使胶束核内疏水链释放出来,疏水链发生聚集并沉淀,胶束解组装释放药物。
光响应胶束的优势在于控制药物释放可以降低药物的泄露,减少不良反应的发生,因此本文制备了一个光响应的聚合物释药载体。作为药物运输载体,光响应胶束必须具有良好的生物相容性和生物可降解性。因此,我们选取了生物相容性好、具有“隐形”作用的PEG作为亲水链,选用了目前研究最为广泛的硝基苯类光扳机。而光扳机种类的不同,以及光扳机在聚合物结构中位置的不同,会直接影响载体瓦解的速率,进而影响药物释放的快慢。所以,与已有报道的o-硝基苄基光响应型共聚物不同,本课题以香草醛(vanilin)为起始原料,通过对光扳机进行结构修饰,在光扳机的苯环上引入甲氧基,使得该光扳机的吸收波长红移,光解量子效率提高,本课题首次将该类型的光扳机作为亲疏水段的连接点,制备快速光响应型的控制释药聚合物胶束,具有潜在的生物医学应用的可能性。
1 实验部分 1.1 主要的试剂与原料香草醛(阿拉丁试剂有限公司)、溴代十二烷(阿拉丁试剂有限公司)、硼氢化钠(上海天莲化工科技有限公司)、4-二甲氨基吡啶(上海萨恩化学技术有限公司)、PEG1000-NH2(嘉兴博美有限公司)、六氟磷酸苯并三唑-1-基-氧基三吡咯烷基磷(PyBop)(上海泰坦化学有限公司)、硝酸、乙酸酐、丁二酸酐、碳酸钾均从上海凌峰化学试剂有限公司购置。
1.2 两亲性嵌段共聚物的制备 1.2.1 光扳机S-(o-硝基-m-甲氧基-p-十二烷氧基苄醇)(VND)的合成VND的合成路线如图1所示。
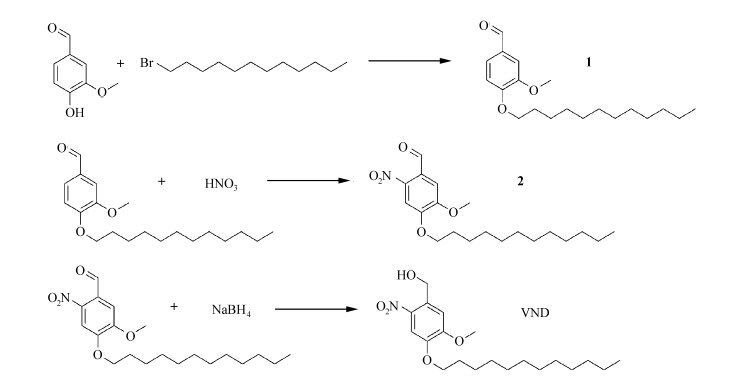 | 图1 光扳机VND的分子结构和合成路线图 The structure and schematic presentation of the synthetic route of phototrigger VND |
(1)化合物1的合成:将香草醛(3.0 g,19.7 mmol)、溴十二烷(9.8 g,39.4 mmol)、碳酸钾(8.2 g,59.1 mmol)、100 mL乙腈一并加入250 mL的单口圆底烧瓶中,混合物在搅拌下加热至70 ℃,TLC监测反应进程直至反应完全。反应结束后,过滤、减压蒸除乙腈、过硅胶柱进行纯化,洗脱剂为石油醚∶二氯甲烷=1∶1,得白色固体,产率为70.6%。
1HNMR(400 MHz,CDCl3):9.84(s,1H),7.44(d,J=7.89 Hz,1H),7.40(s,1H),6.97(d,J=7.89 Hz,1H),4.11(t,J=6.70 Hz,2H),3.92(s,3H),1.91(m,J=6.41 Hz,2H),1.47(m,J=6.51 Hz,2H),1.25~1.34(m,16H),0.89(t,J=8.25 Hz,3H)。
(2)化合物2的合成:在50 mL圆底烧瓶中加入10 mL浓硝酸,磁力搅拌下,于冰浴中缓慢滴加5 mL乙酸酐。滴加完毕后,继续搅拌30 min得A液。在100 mL圆底烧瓶中加入化合物1和5 mL乙酸酐,超声下,固体原料溶解得B液。磁力搅拌下,缓慢滴加A液于B液中,滴加完毕后,室温反应2 h。反应结束后,将上述反应液倾入冰水中,过滤得沉淀并溶于二氯甲烷,以无水硫酸钠干燥后,过滤、减压蒸除溶剂二氯甲烷得粗品。将上述粗品于乙醇中重结晶即得黄色固体产物,产率为82%。
1HNMR(400 MHz,CDCl3):10.44(s,1H),7.59(s,1H),7.41(s,1H),4.14(t,J=7.46 Hz,2H),4.01(s,3H),1.91(m,J=4.61 Hz,2H),1.49(m,J=4.61 Hz,2H),1.25~1.33(m,16H),0.89(t,J=6.47 Hz,3H)。
(3)VND的合成:在100 mL的圆底烧瓶中加入化合物2(3.48 g,9.5 mmol)和200 mL甲醇,超声溶解。缓慢加入硼氢化钠(0.72 g,19.0 mmol),室温反应1 h,TLC监测反应进程。反应结束后,滴加入1 mol/L盐酸溶液中和。减压蒸除溶剂,二氯甲烷萃取所得水溶液,无水硫酸钠干燥有机相。过滤、减压蒸除溶剂二氯甲烷得粗品。粗品以二氯甲烷为洗脱液,经硅胶柱分离纯化后得微黄色固体产物,产率为85.9%。
1HNMR(400 MHz,CDCl3):7.69(s,1H),7.12(s,1H),4.93(s,2H),4.07(t,J=7.71 Hz,2H),3.97(s,3H),1.87(m,J=7.15 Hz,2H),1.47(m,J=6.52 Hz,2H),1.24~1.34(m,16H),0.89(t,J=7.0 1Hz,3H)。
1.2.2 光响应型两亲性嵌段共聚物聚乙二醇-S-(o-硝基-m-甲氧基-p-十二烷氧基苄酯)(PEG-VND)的制备PEG-VND的合成路线见图2。
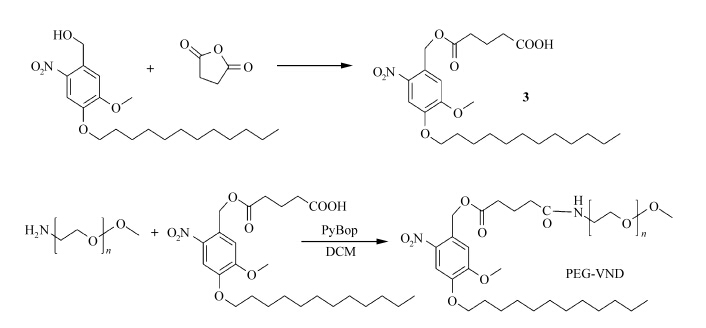 | 图2 PEG-VND的分子结构和合成路线图 The structure and schematic presentation of the synthetic route of PEG-VND |
(1)化合物3的合成:将VND(3.01 g,8.15 mmol)、丁二酸酐(1.63 g,16.3 mmol)、10 mL吡啶和4-二甲氨基吡啶一并加入50 mL圆底烧瓶中,将混合物加热至50 ℃,搅拌下反应24 h。减压蒸除吡啶,以二氯甲烷∶甲醇=100∶1为洗脱液,经硅胶柱分离纯化后得到微黄色固体(2.52 g),产率为54.3%。
1HNMR(400 MHz,CDCl3):12.25(s,1H),7.69(s,1H),7.15(s,1H),5.41(s,2H),4.08(t,J=22.96 Hz,2H),3.93(s,3H),2.63(t,J=6.31 Hz,2H),2.60(t,J=7.58,2H),2.53(m,J=4.60 Hz,2H),1.73(m,J=4.87 Hz,2H),1.40(m,J=7.08 Hz,2H),1.24~1.34(m,16H),0.88(t,J=5.23 Hz,3H)。
(2)PEG-VND的合成:在50 mL的圆底烧瓶中,加入PEG-NH2、化合物3、PyBop和10 mL二氯甲烷,室温搅拌30 min。反应结束后,蒸除二氯甲烷,以二氯甲烷∶甲醇=100∶1为洗脱液,经硅胶柱分离纯化得到微黄色蜡状固体,即为光刺激响应的聚合物PEG-VND。
1.3 结构表征和样品性能表征各产物用CDCl3溶解,1HNMR由Bruker 400 MHz核磁共振仪测试得到。FT-IR是通过KBr压片,由Nexus 670型傅里叶变换红外光谱仪测得。光照通过CHF-XM-500W型氙灯光源,365 nm窄通道滤光片实现。采用马尔文Zetasizer Nano ZS型纳米粒度分析仪测定胶束粒径、PDI、Zeta。胶束形貌用JEOL JEM-1400透射电镜进行观察。Shimadzu UV-2550紫外可见光谱仪测定光照下其吸收光谱的变化。用Varian Cary Eclipses荧光分光光度计测定聚合物胶束的临界胶束浓度以及光控释放尼罗红的性质。
1.4 胶束的制备及载入模型药物尼罗红采用直接法制备空白胶束溶液:称取4 mg PEG-VND溶于2 mL去离子水中,超声,得到浓度为2.0 mg/mL的胶束溶液。用马尔文粒径仪测定聚合物胶束的粒径、PDI和Zeta电位。TEM测空白胶束的形貌。
制备载尼罗红胶束溶液:称取一定量的尼罗红溶于四氢呋喃,配制成浓度为1.0×10-3 mol/L的溶液,取10 μL,在搅拌条件下滴入空白胶束溶液中。蒸除四氢呋喃,即得到载尼罗红的胶束溶液。
1.5 测定临界胶束浓度和光响应行为临界胶束浓度(CMC)的测定:配制一系列浓度(5.0×10-4、1.0×10-3、2.5×10-3、5.0×10-3、1.0×10-2、2.5×10-2、5.0×10-2、0.1、0.25、0.5、1.0 mg/mL)的空白胶束溶液各1 mL,向其中加入10 μL尼罗红的四氢呋喃溶液。超声30 min后,测I633处荧光强度。以I633对LogC作图,采用origin 8.0进行线性模拟,曲线的交界处即为聚合物的临界胶束浓度。
聚合物胶束光响应性质紫外测试:配制聚合物浓度为0.5 mg/mL的二氯甲烷溶液。用365 nm,15 mW/cm2的强度光照,隔一定的时间用紫外分光光度计扫描聚合物溶液的250~500 nm的光谱,跟踪光反应过程。
聚合物胶束包载释放尼罗红测试:配制2.0 mg/mL的空白胶束溶液,按上述方法载入尼罗红。取其中1 mL加入至比色皿中,用365 nm、15 mW/cm2的强度光照,隔一定时间用荧光分光光度计(激发波长530 nm,发射波长633 nm)测荧光强度。
2 结果与讨论 2.1 结构的表征PEG-VND结构如图3所示。1HNMR:PEG-VND(400 MHz,CDCl3):7.71(Ha),7.07(Hb),6.47(Hc),5.54(Hd),4.08(He),4.02(Hf),3.70(Hg),3.38(Hh),3.15(Hi),2.80(Hj),2.58(Hk),1.89(Hl),0.88(Hm)。在化学位移1.2~1.5处为疏水链十二烷基的质子峰。图4清晰表明了所合成的聚合物即为目标产物。
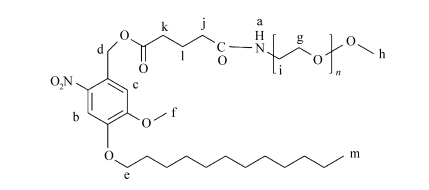 | 图3 PEG-VND的分子结构 The structure of PEG-VND |
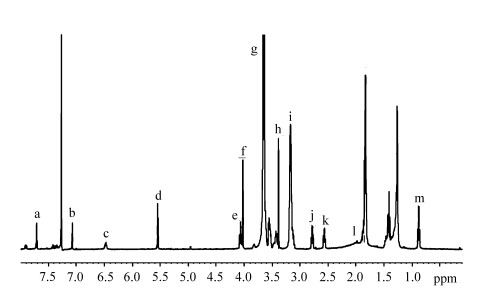 | 图4 PEG-VND的1HNMR谱图 The 1HNMR spectrum of PEG-VND |
图5为PEG-NH2和PEG-VND的FT-IR谱图:1739 cm-1为羰基(CO)的伸缩振动特征峰;1523 cm-1处为苯环的特征吸收峰;921 cm-1处显现出硝基基团的伸缩振动峰。这些数据都证明了PEG-VND的成功制备。
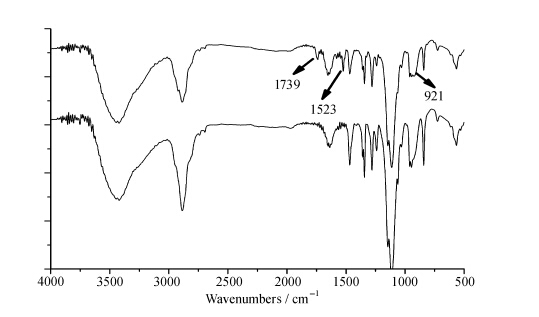 | 图5 PEG-NH2和PEG-VND的FT-IR谱图 The FT-IR spectrum of PEG-NH2 and PEG-VND |
聚合物PEG-VND空白胶束的粒径分布和透射电镜图像如图6所示,PEG-VND在水溶液中能形成分布良好的纳米级胶束,平均粒径为55.7 nm,粒径分布指数为0.144,Zeta为8.7 mV。TEM可清晰的显示胶束为球形,分散良好,粒径约为40 nm。
 | 图6 PEG-VND的胶束粒径分布图和透射电镜图 size distribution and TEM of PEG-VND |
在测临界胶束浓度实验中,以I633对Logc作图,得到两条有交点的直线,如图7所示,此交点即为聚合物胶束的CMC值。CMC值为2.8×10-2 mg/mL。
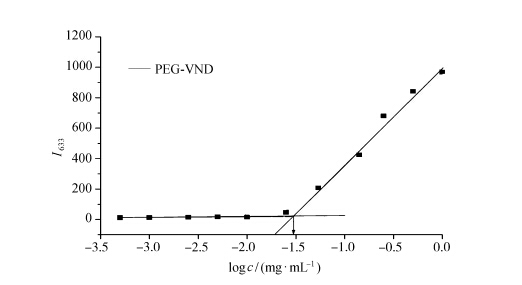 | 图7 PEG-VND的临界胶束浓度图 The CMC of PEG-VND |
我们设计合成了光响应的聚合物胶束载体,该载体最特殊的性能就是具备光响应性。首先,用紫外吸收光谱测试该聚合物在光照条件下的光化学变化。如图8所示,随着光照时间的增加,聚合物在290 nm处的紫外吸收逐渐下降,350 nm处的紫外吸收逐渐红移至380 nm,这说明聚合物在光照下发生了光化学反应。
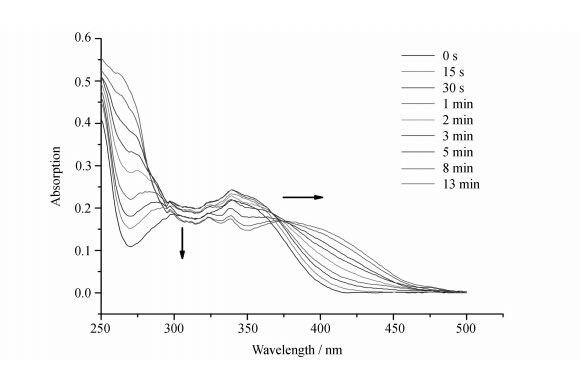 | 图8 365 nm光照(光强15 mW/cm2)PEG-VND的紫外-可见光吸收光谱的变化 Evolution of the UV-Vis absorption spectrum of PEG-VND under irradiation at 365 nm (15 mW/cm2) |
如引言所述,我们合成的是一个光响应药物载体,其通过自组装形成载药纳米胶束,在到达病灶部位后,光照下释放药物。因此,选用了疏水染料尼罗红作为模型药物来研究胶束的光响应释放行为。首先,对载尼罗红胶束的水溶液检测其荧光发射强度。尼罗红自身的疏水结构决定了其在水中没有荧光发射,在疏水环境中才具有荧光发射。因此,用550 nm波长激发时,发现体系有较强的尼罗红荧光发射,说明尼罗红已载入胶束中。然后,对上述体系进行光照,随光照时间的推移,胶束内尼罗红荧光发射强度越来越弱,如图9所示。这是因为聚合物胶束随光照的进行逐渐降解,胶束解组装,尼罗红被释放到水中,从而荧光发射强度逐渐降低。图9a是载尼罗红光响应胶束的荧光发射光谱随光照时间的变化情况。图9a中插图为光照前后载尼罗红光响应胶束水溶液的颜色变化对比,说明尼罗红释放到水溶液中。图9b是光照与非光照条件下,以及光响应胶束(PEG-VND)与非光响应胶束(PEG-PLA)的尼罗红在633 nm处归一化荧光发射强度变化。对比非光响应载尼罗红胶束的荧光变化曲线(图9b红线),说明尼罗红的荧光下降不是光漂白现象,而是光照胶束解组装释放尼罗红的结果。从图9b可以看出,在365 nm,15 mW/cm2的光强下,胶束快速解组装,释放尼罗红,7 min内尼罗红荧光强度下降了约80%。
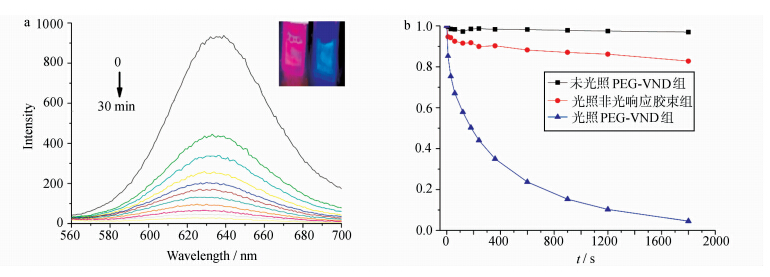 | 图9 (a)载尼罗红光响应胶束的荧光发射光谱随光照时间的变化,插图:载尼罗红光响应胶束在光照前后的荧光成像图; (b)各条件下,尼罗红在633 nm处归一化的荧光发射强度 (a)Evolution of the Fluorescence emission spectrum of PEG-VND with the increased irradiation time, inset:fluorescence photographs before (left) and after (right) irradiation. (b)Normalized fluorescence emission intensity of NR at 633 nm in different conditions |
通过疏水链修饰的硝基苯类光扳机与亲水链PEG高分子的成功键连,我们合成了一个具有光响应性的AB型两亲性嵌段共聚物PEG-VND,在光扳机的苯环上引入甲氧基使得该光扳机的吸收波长红移,光解量子效率提高,将此类光扳机作为亲疏水段的连接点,制备的胶束具有响应迅速、释药可控的前景。该两亲性嵌段共聚物可以在水溶液中自组装成形态均匀、分布良好的聚合物胶束。用马尔文粒径仪和TEM对其粒径和形貌进行了检测。通过紫外可见光照实验说明该聚合物具有光刺激响应性。模型药物尼罗红的成功载入和光照释放进一步证实了PEG-VND在药物光响应释放中的应用潜力。
| [1] | Chaterji S, Kwon I K, Park K. Smart polymeric gels: redefining the limits of biomedical devices[J]. Progress in Polymer Science, 2007, 32(8-9): 1083-1122. |
| [2] | Yamato M, Akiyama Y, Kobayashi J, Yang J, Kikuchi A,Okano T. Temperature-responsive cell culture surfaces for regenerative medicine with cell sheet engineering[J]. Progress in Polymer Science, 2007, 32(8-9): 1123-1133. |
| [3] | Alvarez-Lorenzo C, Bromberg L, Concheiro A. Light-sensitive intelligent drug delivery systems[J]. Photochem Photobiol, 2009, 85(4): 848-860. |
| [4] | Li M H, Keller P. Stimuli-responsive polymer vesicles[J]. Soft Matter, 2009, 5(5): 927-937. |
| [5] | Han D, Tong X, Zhao Y. Block copolymer micelles with a dual-stimuli-responsive core for fast or slow degradation[J]. Langmuir, 2012, 28(5): 2327-2331. |
| [6] | Cabane E, Malinova V, Meier W. Synthesis of photocleavable amphiphilic block copolymers: toward the design of photosensitive nanocarriers[J]. Macromolecular Chemistry and Physics, 2010, 211(17): 1847-1856. |
| [7] | Yang H, Jia L, Wang Z F, Di-Cicco Aurélie, Lévy Daniel, Keller Patrick. Novel photolabile diblock copolymers bearing truxillic acid derivative junctions[J]. Macromolecules, 2011, 44(1): 159-165. |
| [8] | Schumers J M, Gohy J F, Fustin C A. A versatile strategy for the synthesis of block copolymers bearing a photocleavable junction[J]. Polymer Chemistry, 2010, 1(2): 161-163. |
| [9] | Katz J S, Zhong S, Ricart B G, Pochan D J, Hammer D A,Burdick J A. Modular synthesis of biodegradable diblock copolymers for designing functional polymersomes[J]. Journal of the American Chemical Society, 2010, 132(11): 3654-3655. |
| [10] | Cabane E, Malinova V, Menon S, Palivana C G ,Meier W.Photoresponsive polymersomes as smart, triggerable nanocarriers[J]. Soft Matter, 2011, 7(19): 9167-9176. |
| [11] | Zhao Y. Light-responsive block copolymer micelles[J]. Macromolecules, 2012, 45(9): 3647-3657. |
| [12] | Liu G, Dong C M. Photoresponsive poly(S-(o-nitrobenzyl)-L-cysteine)-b-PEO from a L-cysteine N-carboxyanhydride monomer: synthesis, self-assembly, and phototriggered drug release[J]. Biomacromolecules, 2012, 13(5): 1573-1583. |
| [13] | Han D H, Tong X, Zhao Y. Fast photodegradable block copolymer micelles for burst release[J]. Macromolecules, 2011, 44(3): 437-439. |




