以量子点[1]为代表的纳米材料,是20世纪90年代提出的一个新概念,它是在结构上把导带电子、价带空穴和激子在三维方向上束缚住,从而具有量子效应的纳米结构颗粒。这样的结构使得量子点具有很多新奇的性质,在太阳能电池、发光器件、光催化以及生物荧光标记等方面具有广泛的应用前景。但由于量子点大多为Ⅲ-Ⅴ族或者Ⅱ-Ⅵ族元素组成的化合物,其中部分还包含铅、镉、碲等毒性较强且价格较贵的重金属,其环境友好性[2]、工业成本以及苛刻的制作工艺要求是阻碍其规模工业应用的不利因素。
2004年,Xu X Y等在纯化碳纳米管的过程中意外发现了荧光碎片[3], 2006年,美国克莱蒙森大学科学家孙亚平博士首次提出了碳点(碳量子点)的概念[4]。碳点(CDs)的出现是纳米材料领域的一个新的突破,除了具有传统半导体量子点所拥有的优良光学性能和尺寸小等优点外,还具有传统半导体量子点无法比拟的高生物相容性、低细胞毒性、无光闪烁、低制备成本及制作工艺相对简单等优点,在生物学和医学研究领域具有先天优势,因而越来越多地受到科学家的关注。
本文重点概述了荧光碳点的合成方法、显微结构分析、荧光机理以及应用的最新成果,并对当前需要解决的问题以及今后的研究发展方向进行了探讨。
1 荧光碳点的合成方法碳点是准零维纳米结构,一般尺寸不超过10nm,获得碳点的原料多为炭黑、无定形碳、石墨、碳纳米管、碳纤维、石墨烯及各种含碳有机物等。合成方法大致分为两类:自上而下(将宏观尺寸大小的碳经过加工变为纳米级颗粒)的方法和自下而上(将有机碳化合物分子合成为纳米级颗粒)的方法。自上而下的方法一般包括:激光烧蚀法、电化学法、氧化石墨烯法、弧光放电法等,自上而下的方法一般合成效率较低,而且产物大多为混合物,需要一定的分离工序才能把碳点提纯。自下而上的方法一般为:水热法、微波法、热解法、激光化学反应等,自下而上的方法一般产率较高,而且制备工艺简单,实验设备要求低,比较适合大规模制备,是目前采用比较多的一种制备方法。
1.1 自上而下的合成方法激光烧蚀法的原理是将强能量激光照射在碳靶的表面,把碳颗粒从碳靶上剥离出来,形成纳米级的微小碳点。Sun Y P等[4]将碳粉做成碳靶,用氩气作保护气体,在900°的高温、75 kPa水蒸气环境中用Nd:YAG激光 (1064 nm, 10 Hz)照射,制得碳点的前驱体,然后通过浓硝酸来除去杂质,再利用聚乙二醇(PEG)1500 进行表面修饰后获得5 nm左右的荧光碳点 (图 1A),在400 nm波长激发条件下量子产率为4%~10%。Hu S L等[5]同样利用Nd:YAG激光直接在不同的有机溶剂中销蚀石墨粉末,一步法同时完成了碳点的合成和表面修饰,制成量子产率为3.7%~7.8%、粒径在1~8 nm之间的荧光碳点(图 1B),而且通过改变溶剂的种类使碳点的发射波长在一定范围内移动。
电化学法是合成纳米材料常用的一种方法,Zhou J G等[6]使用制成的多壁碳纳米管为电极,乙腈溶液和四丁基高氯酸铵为电解液,构成电解池,得到粒径为3 nm左右的碳点,量子产率为6.4%。利用电化学方法制作的碳点工艺比较繁琐,一般通过将石墨预先制作碳纳米管或者石墨烯等前驱体,再通过电化学反应来进一步解离形成碳点。
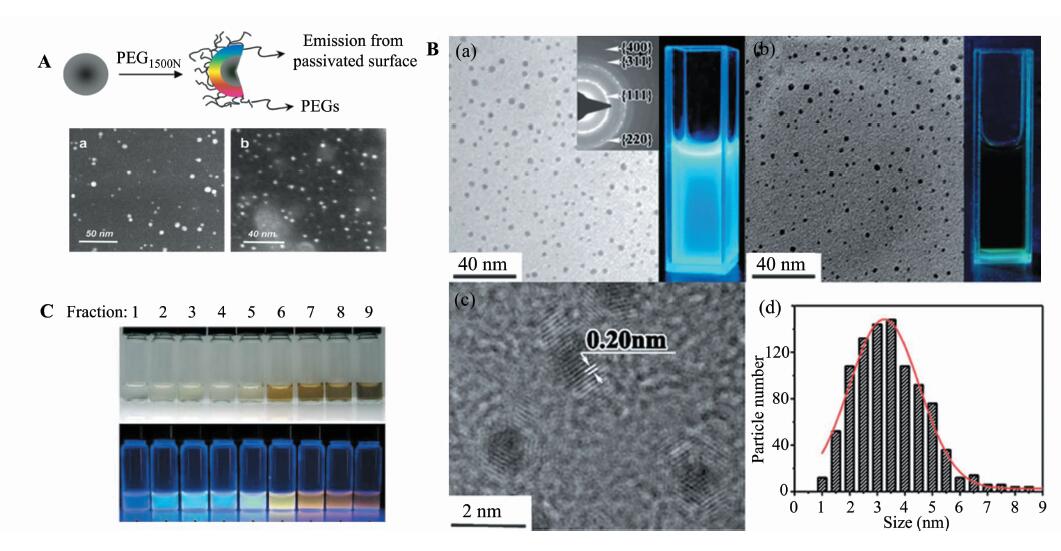 | 图1 自上而下合成法合成的碳点 (A) PEG1500钝化碳点示意图及其STEM图像[4];(B) 样品a和b在365 nm紫外光激发的透射电镜照片(TEM)以及碳点的高分辨TEM像和粒径统计[5];(C) 酸煮法合成的碳点在312 nm紫外光激发下荧光光谱[7]Top-down synthesis of carbon dots (A) STEM and diagram of the carbon dots passivated by PEG1500[4] ;(B) spectra of sample a and b under 365 nm UV TEM,HRTEM images and diameter statistics of carbon dots [5]; (C) spectra of carbon dots synthesized by acid brewing method under 312 nm UV [7] |
2007年,Liu H P等[7]首次利用酸煮蜡烛灰的方法合成碳点,该方法首先收集燃烧不完全的尺寸20~800 nm的蜡烛灰,利用硝酸回流氧化12 h,然后利用电泳方法将产物在聚丙烯酰胺凝胶中分离,制得多色荧光碳点,尺寸在2 nm左右,量子产率很低,仅有0.8%~1.9%(图 1C)。
1.2 自下而上的合成方法就目前碳点的研究进展看,自下而上制备方法是研究人员制备碳点的另一类主要的方法。水热法是制备碳点常用的一种自下而上法,Zhu S J等[8]将柠檬酸和乙二胺溶解到去离子水中,在水热釜中高温(150 ℃、200 ℃、250 ℃)加热5 h,经过冷却、透析后得到粒径2~6 nm的碳点 (图 3A),该产物紫外激发的荧光为亮蓝色,量子产率较高,为58%。Hu S L等[9]用同样的水热方法首次使用乙二醇得到粒径为3.5 nm±0.5 nm的碳点,同时制得了—N、—Cl、—O基团修饰的具有不同特性碳点,但量子产率较低。由此可见,此种水热方法是一种开放性的实验方法,可以使用不同的碳基化合物来制成具有不同性质的碳点。通过研究发现,N元素的修饰能够极大的改变碳点的荧光特性,本课题组利用柠檬酸作为唯一碳源,将一水合氨作为表面N源前驱体,用水热法制备了单分散性好、晶体结构单一、色域宽(图 2B)的高性能荧光碳点,其量子产率最高达40%(图 2A),根据其高分辨透射电镜图像(HRTEM)(图 2C)分析, 制备碳点具有非常良好的石墨2H结构[10]。
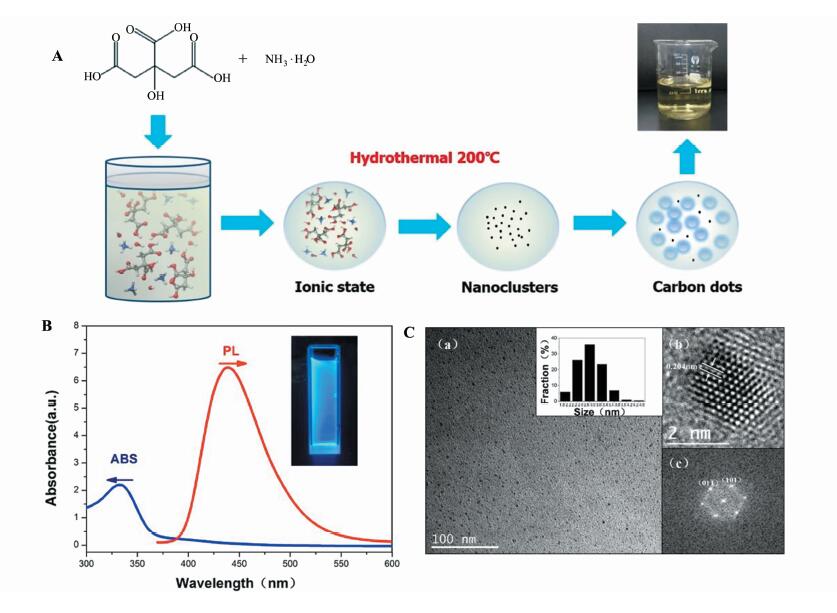 | 图2 水热法合成荧光碳点 (A) 水热法合成碳点流程图;(B) 荧光碳点的紫外-可见吸收光谱(UV-Vis)、荧光光谱(PL)和在365 nm紫外灯照射下样品的发光图像(插图);(C) (a)TEM图片以及碳点粒径统计(插图),(b)高分辨电子衍射二维晶格图像,(c)荧光碳点的快速傅里叶变换(FFT)图像Hydrothermal synthesis of fluorescent carbon dots (A) Synthesis pathway of the fluorescent CDs by hydrothermal method; (B) the ultra-violet (UV) absorption and PL spectra of the CDs, inset is the photograph of the samples under 365 nm UV lamb; (C) (a) TEM image of CDs and the partical size distribution (inset), (b) two-dimension HRTEM and (c) the fast Fourier transform (FFT) image of the signal CD |
热解法是利用高温分解有机碳源制作碳点的一种方法。Dong Y Q等[11]将柠檬酸和聚乙烯亚胺在去离子水中进行混合后,直接加热到200 ℃进行热解3 h,为了防止水分蒸发后反应物被高温烤焦,期间不断添加少量去离子水保持反应物的凝胶状态,待反应物凝胶从浅黄色变成橘黄色,用水溶解后提纯获得荧光碳点(图 3A),紫外荧光量子产率达40%以上。Guo X等[12]首次利用热解环氧聚苯乙烯和甲基丙烯酸缩水甘油酯的二元共聚物交联微球来制备碳点(图 3B),通过控制热解的温度,在没有任何表面修饰工艺的条件下制成粒径大小不同、发光为蓝、橙、白3种颜色且具有较好单分散性的碳点,量子产率在47%以上。
微波法相对于其他自下而上的方法来讲,条件简单,实验时间大大缩短。Wang X H等[13]将碳水化合物和磷酸盐溶液混合,微波加热,制得荧光波长在430 nm(蓝色)到525 nm(绿色)、粒径在2.1 nm±0.7 nm的碳点,而且发射光谱随着激发波长的变化而变化。
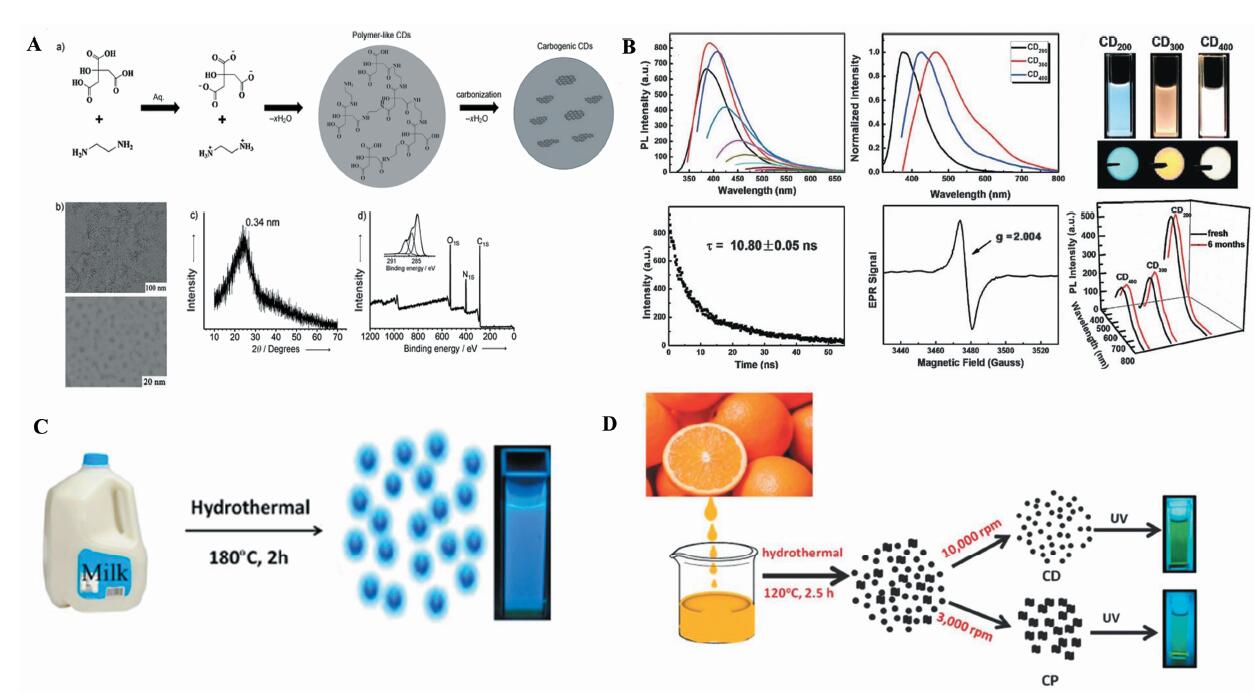 | 图3 自下而上合成碳点 (A) 利用柠檬酸和乙二胺合成碳点原理图以及碳点的TEM、XRD、XPS图谱[8];(B) 热解法合成不同颜色荧光碳点的荧光发射光谱、光衰时间谱以及EPR图谱[12];(C) 利用牛奶合成碳点示意图[16];(D)利用橙汁合成碳点示意图[18]Bottom-up synthesis of carbon dots (A) The TEM、XRD、XPS images of carbon dots synthesized by citric acid and ethylene diamine[8]; (B) PL fluorescence life time and EPR of carbon dots synthesized by pyrolysis method[12]; (C) diagram of carbon dots synthesized by milk[16]; (D) diagram of carbon dots synthesized by orange juice[18] |
最近还发现了大量研究利用人们日常生活中的食品,如蜂花粉[14]、甘蔗渣[15]、牛奶[16](图 3C)、咖啡[17]、橙汁[18](图 3D)等为原料来制备碳点,其合成机理和上述几种方法基本相似,且获得了较好的实验结果。
激光法是一种新近发展的“自下而上”制备量子点的方法,利用激光法照射有机分子来制备碳量子点已成为一种新的探索。
Habiba K[19]等利用激光辐照镍颗粒催化苯分子的方法制备了荧光碳量子点。本课题组发展了激光化学反应法,利用准分子脉冲激光辐照甲苯溶液,在未经催化和表面修饰的情况下,直接制备了荧光碳量子点(图 4A),并在碳量子点的形成机理上作了一些探索。通过第一性原理计算结果表明,248 nm的单光子可以使甲苯分子内的电子从分子最高占据轨道HOMO跃迁到分子最低未占据轨道LUMO(图 4B),而由于准分子脉冲激光下可以发生分子轨道能级的Stark宽化效应,甲苯分子在短时间内将吸收多个光子直至被光解离,制备出了高质量的碳量子点,透射电镜的分析表明,该碳量子点具备石墨晶体结构(图 4C)[20]。
 | 图4 激光解离分子法合成碳点 (A) 在350~400 nm 范围内不同激发波长激发的紫外-可见吸收光谱以及荧光发射光谱; (B) 甲苯分子态密度及其光解离示意图:单光子激发使电子从最高占据轨道(HOMO)到最低未占据轨道(LUMO),多光子激发使甲苯分子发生光解离;(C)高分辨电镜图像:(a) 不同晶向的晶面间距,(b) (a)图的快速傅里叶变换(FFT)图,(c) 石墨2H结构的晶格模拟图像,(d) (c)图的电子衍射模拟图像Synthesis of carbon dots under laser irradiation (A)UV-Vis absorption and PL spectra of the CDs at different excitation wavelength from 350-400 nm; (B) a schematic illustration of photodissociation: Calculated Density of States (DOS) of toluene molecule. Single photon excitation processes for electrons transited from HOMO to LUMO and multiphoton excitation processes for photodissociation; (C)HRTEM images: (a) images observed at direction with different space distance, (b) Fast Fourier transform (FFT) image of (a), (c) simulated HRTEM images of graphite 2H along, (d) simulation of electron diffraction patterns from (c) |
截至目前,碳点的荧光机理还没有一个统一的解释[21, 22]。传统半导体量子点由于受到量子限域效应影响,使得原来费米能级附近的电子能级由连续态变成分立能级,当受到外界光子的激发时,电子从低能级跃迁到高能级,高能级不稳定再向低能级跃迁时释放光子发出荧光,半导体量子点通过控制量子点尺寸的大小来控制荧光的波长[23]。碳点虽然也是具有量子限域效应的纳米颗粒,但一些碳点晶体结构为石墨型,本身是导体而非半导体,碳点的导带和价带重叠,而不是像半导体量子点那样具有禁带而产生带隙发射。所以不同结构的荧光碳点尺寸小到一定程度是否会出现与半导体量子点相似的分裂能级,也是广大研究者讨论的一个热点。
有研究者认为荧光碳点的荧光机理与表面能带相关[24],因为纳米颗粒具有非常大的比表面积,当粒径为2 nm时,表面原子占全部原子比例高达80%[25],会导致纳米颗粒表面原子配位情况较差,通常会有缺陷,同时纳米颗粒为了保持稳定性一般会与其他修饰或者钝化基团连接,起到一种表面修饰的作用。有研究者发现经过表面修饰或者表面钝化的碳点会大大提高荧光量子产率[26],这两种情形使得碳点产生能带,从而发出荧光。
目前,量子产率较高的碳点多用PEG(聚乙二醇)系列物质进行钝化。Zhang S P等[26]利用PEG2000钝化无荧光的碳纳米颗粒后,得到的碳点荧光量子产率高达50% (图 5A)。也有研究者利用N元素修饰合成的碳点前驱体或者直接使用含有N元素的含碳有机物合成,利用紫外波段激发荧光为440~480 nm的蓝光或者蓝绿光[27,28,30]。Yang Y H等[2]利用既含有C骨架又含有N元素的甲壳素原料通过一步水热法直接合成了蓝绿荧光碳点(图 5B)。Li X M等[29]认为碳点发射蓝光或者绿光与其表面氨基的密度有关(图 5C)。与传统的半导体量子点相比,激发和发射波长均短于半导体量子点。虽然它们的制作方法和碳源有所不同,但根据它们性质的相似性可以推断是同一种发光机制产生的受激荧光[27]。
 | 图5 碳点的荧光机理 (A) PEG2000修饰不发光碳点后发出绿色和蓝色荧光[30];(B) 甲壳素一步法合成碳点[2];(C) 碳点表面的氨基密度影响其荧光波长示意图[29];(D) 不同尺寸和表面氧化态的碳点在360 nm激发时不同颜色的荧光[24]Fluorescence mechanism of carbon dots (A) Modified by the PEG2000, carbon dots emit green and blue fluorescence[30]; (B) one-step synthesis of carebon dots with chitin[2];(C) amino density of the carbon surface impacting the fluorescence wavelength[29];(D) carbon dots with different size and surface oxidation states emit different colors of fluorescence under the 360 nm UV[24] |
还有研究者认为碳点荧光的波长不是由颗粒尺寸或者表面态单独来决定的。Bao L等[24]报道,碳点荧光的波长是由量子点尺寸的大小、表面态和尺寸共同决定的,他们通过严格筛选三组分别为<3 kDa、3~10 kDa、10~30 kDa分子量的碳点测试,发现荧光波长分别为430~520 nm、505~570 nm、510~610 nm波长范围(图 5D),同时发现同一组氧化程度高的碳点荧光波长较长,从而提出了碳点尺寸和表面氧化态与荧光波长的影响关系。
3 碳点的应用 3.1 生物成像以及药物运输碳点相对于传统半导体量子点的优势之一就是细胞毒性低,生物相容性好,是生物医学研究中的理想材料[31, 32]。
作为生物荧光探针,碳点已经被广大研究者应用于细胞成像研究[31,33,34],通过单光子或者双光子激发共焦显微镜可观察到碳点在细胞内的分布,与利用传统染料分子和示踪同位素标记方法相比,使用碳点作为荧光探针更加安全快捷,同时灵敏度相当。已经证实CaCo-2细胞、MCF-7细胞、COS-7细胞、小鼠P-19细胞、大肠杆菌等都能够被碳点标记[4,35,36,37]。研究发现,在低于4 ℃的环境温度下,碳点无法进入MCF-7的细胞中,证明碳点进入细胞是需要一定的能量,而不是随机扩散进入(图 6A)[35]。碳点作为荧光探针不仅仅应用于动物细胞研究,Jin X Z等[38]成功地把水热法合成的碳点注入到植物细胞内,利用碳点荧光对pH的敏感性对植物体内pH值进行检测和标定(见图 6B)。
有研究者报道,碳点同样可以进行动物活体成像,经过静脉或者皮下注射等方式,在生物体内碳点依然可以保持强烈的荧光,能够穿透动物组织观察到荧光成像。Yang S T等[39]把碳点皮下注射到小白鼠的体内后,在紫外激发下,可以看到碳点在体内形成的亮斑,同时可以观察到碳点随着淋巴管移动到淋巴结(图 6C)。Parvin N等[40]用果蝇来进行碳点活体成像实验发现,碳点在果蝇体内有效时间长达12h,最后被排出体外。以上实验充分证明了碳点在活体医学检测中的巨大潜力。
碳点不仅应用于生物成像,还可以作为药物传送的载体来运送药物到细胞中。Thakur M等[41]利用水热法制成的碳点和广谱抗生素(盐酸环丙沙星)分子共轭成对,在对酵母菌的实验中,碳点-环丙沙星共轭既可以在酵母菌细胞内成像,又增加了抗生素在细胞内的浓度,表明碳点成功承载环丙沙星进入细菌细胞内部(图 6D)。Zheng M等[42]利用抗癌药物与表面用—NH2修饰的碳点结合,发现碳点具有增强药物疗效的作用。Kong等[43]对碳点进行细胞的渗透性探究,发现不同表面基团修饰的碳点在细胞渗透性方面表现不同,在对海拉癌细胞的渗透实验中,表面基团渗透性排序为—NH2 >—OH>—PEG,同时证明了它们对细胞的渗透不是简单的渗透压平衡,提出了渗透过程可能有细胞内吞作用的参与。
3.2 传感器研究发现,不同基团修饰的碳点除了表现出优异的荧光特性外,对一些金属离子以及生物分子也有敏感特性。因此,可以用来构建新型的纳米传感器[44]。
研究者们发现碳点的荧光特性对一些金属离子非常敏感[45]。Zong J等[46]报道,Cu2+能导致碳点荧光猝灭,最低猝灭极限为2.3×10-8 mol/L。而L-半胱氨酸与Cu2+的亲和力更强,可以与Cu2+反应形成Cu—S键,从而使碳点表面Cu2+脱附,使得荧光猝灭的碳点重新发出荧光,L-半胱氨酸的作用极限达3.4×10-10 mol/L,依据此原理可以制成高灵敏度的传感器来检测Cu2+和L-半胱氨酸。Hu S L等[45]利用水热法合成的碳点与罗丹明B结合可以达到检测Fe3+的目的。Zhai Y L等[47]通过微波法合成碳点制成可以精确探测Hg2+的探测器。此外利用碳点检测的金属还有Be+ [29]、Pb2+[span class="xref">48]等,特别是Pb2+的检测,在铅污染日益严重的现实社会中具有非常大的意义,使得碳点在资源环境保护方面拥有了广阔的应用潜力。
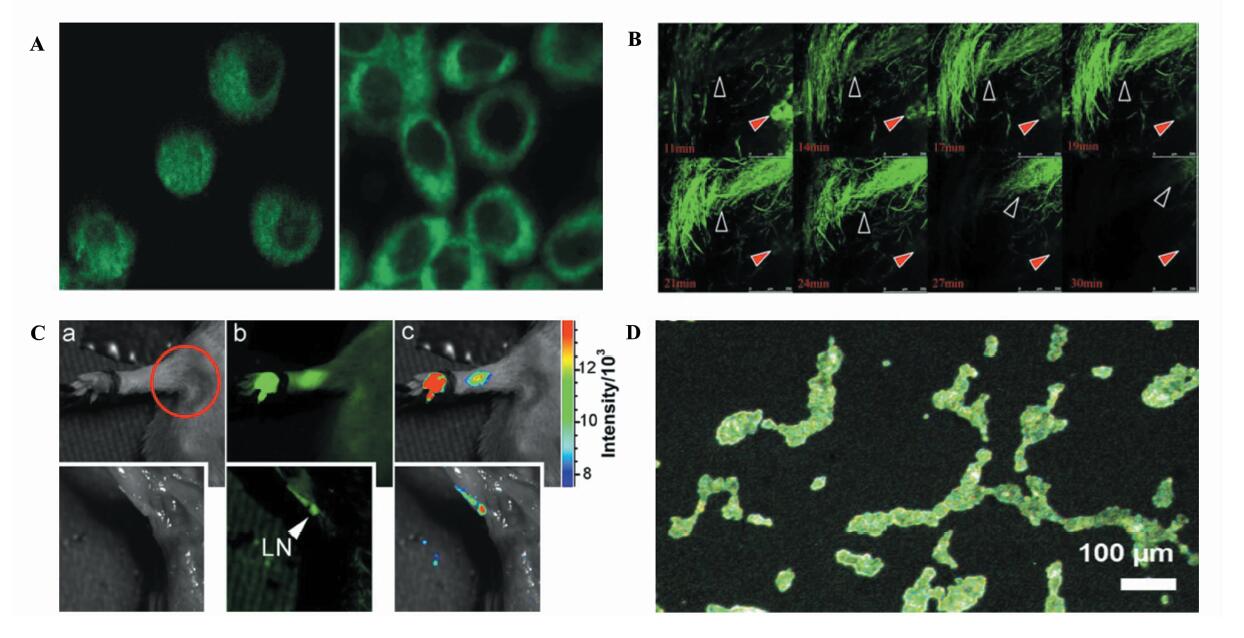 | 图6 生物成像及药物运输 (A) 碳点双光子成像的MCF-7细胞[35];(B) 含有碳点的植物细胞在外部环境pH变化后荧光变化[38];(C) 碳点在活体小白鼠体内沿淋巴管迁移[39];(D) 酵母菌细胞内成像[41]Bio-imaging and drug delivery (A) MCF-7 cells’ images of two-photon fluorescence microscopy by carbon dots[35]; (B) the fluorescence changing with the change of the external pH[38] (C) carbon dots in living mice moving along the lymphatic vessels[39] ; (D) image of the yeast cells[41] |
碳点还可以应用于多种生物分子的检测。Wang Y等[49]利用氧化石墨烯碳点的电化学发光性质来检测谷胱甘肽,此方法具有很高的灵敏度,能够在硫醇物质的影响下准确检测谷胱甘肽和含有谷胱甘肽的药物,而传统的检测方法大多容易受到硫醇物质的影响。Zhang L L等[50]利用碳点制成荧光和电化学两种通道的检测器来检测三硝基甲苯(TNT),TNT为军事上极为常用的烈性炸药,其爆炸威力巨大,在其生产、运输、装配的过程中危险系数较高,Zhang等研制的传感器可以在30 s的时间内检测10 nmol/L~1.5 μmol/L范围的TNT,其军事应用潜力不言而喻。Gao Z等[51]发现赖氨酸修饰的碳点荧光被Fe3+离子猝灭之后,可以使用植酸来恢复,可以利用此原理来制作探测植酸的传感器。Shen P F等[52]以苯基硼酸为原料利用一步法合成的碳点来检测人类血清中的血糖,检测范围在9~900 μmol/L之间 (图 7),且不受血清中其他物质影响,其检测机理颠覆了传统血糖检测中利用的氧化还原反应法,是利用葡萄糖影响碳点自组装程度来对葡萄糖进行检测,其检测精度比传统方法提高几个量级,在血糖快速低成本检测方面具有非常巨大的应用潜力。
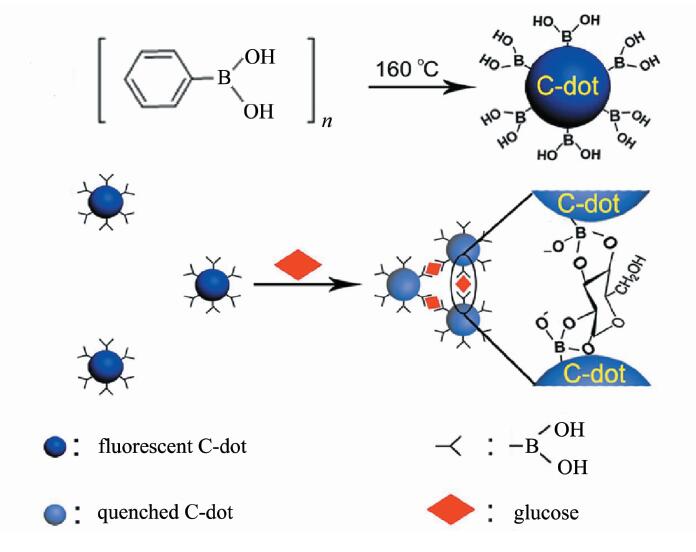 | 图7 一步法合成碳点示意图以及碳点检测葡萄糖原理图[52] One-step synthesis of carbon dots and the mechanism to detect glucose[52] |
光疗包括光动力和光热治疗,该技术被医学界认为是一种继手术、化疗、放疗后最具有发展前途的肿瘤治疗新技术[53]。光诊疗剂就是将在光激发下的荧光成像、光声成像或光热成像等诊断手段和光动力或光热等治疗手段集中在一起,达到同时诊断和治疗的目的。目前,光诊疗剂主要是纳米金、碳纳米管、石墨烯、ICG等有机染料和聚合物纳米材料等[54]。
最近,碳点在光诊疗剂应用研究领域取得了较大的进展。Huang P等[55]将绿光碳点和传统的光敏剂(Ce-6)偶联,碳点发出的荧光通过能量转移机制增强了Ce-6发光,同时产生单线态氧用于杀死肿瘤细胞(图 8A)。Tang J等[56]将蓝光碳点经过聚乙二醇表面修饰后,与阿霉素(Doxorubicin,一种抗癌药物,本身可发595 nm荧光)通过π-π作用和碳点偶联构建C-dots/dox 纳米载药系统 。在这个载药系统中,碳点既是药物载体,又是能量转移的给体(图 8B)。碳点发出的荧光通过能量转移机制激发dox发光。纳米载药体系到达肿瘤处,由于pH发生变化 ,dox脱离载药体系,能量转移消失,只能发出碳点的 498 nm荧光,达到实时监控药物释放的目标。Zheng M等[42]用碳点和顺铂抗癌药物偶联也构建了一种新型的纳米光诊疗剂用于肿瘤的诊断和治疗(图 8C)。但是,在这些工作中,所用碳点的荧光都是蓝绿荧光,碳点起到的只是荧光试剂或能量给体的作用,其本身并没有治疗功能。最近,Ge J C等[57]以功能前驱物聚噻吩季铵盐衍生物为碳源,制备了一系列红色荧光碳点。其中,表面带负电荷的碳点具有集荧光、光声、光热成像和光热治疗四功能于一体(Four-in-One)的特性,可实现光激发下对肿瘤的诊断和治疗,从而拓宽了碳点在纳米生物医学领域中的应用(图 8D)。另一种表面带有正电荷的水溶性近红外发光碳点,在光照下可通过多重态敏化机制高效产生活性氧(1O2)(图 8E)[58]。这种性能独特的碳点不仅能够用于光动力治疗肿瘤、杀灭细菌,而且在可见光催化及光电子等领域也具有重要应用前景。
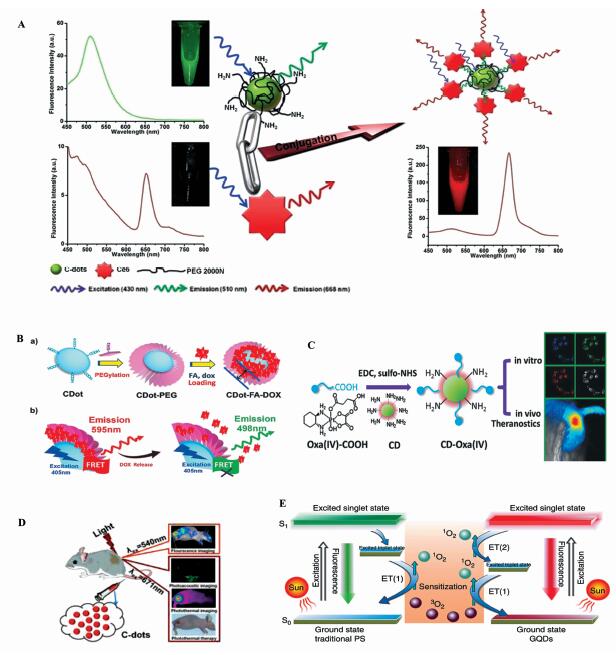 | 图8 碳点在光诊疗剂中的应用 (A) 在C-dots和Ce-6之间的荧光共振能量转移[55];(B) FRET-CDot-DDS 的表面化学耦合机理以及其提出的药物运输过程示意图[56];(C) CD-Oxa在生物成像和诊疗中的应用机理图[42];(D) 碳点的荧光、光声、光热成像和光热治疗四功能于一体(Four-in-One)特性示意图[57];(E) 在含氧溶液中GODs在680 nm激发的荧光机理[58]The applications of the carbon dots in phototheranostics ((A) Fluorescence resonance energy transfer (FRET) process between C-dots and Ce-6[55];(B) the surface coupling chemistry for FRET-CDot-DDS and the proposed mechanism of the FRET-CDot-DDS for drug delivery[56]; (C) synthetic scheme for CD-Oxa and its applications in bioimaging and theranostics[42];(D) the Four-in-One properties of fluorescence,opto-acoustic,opto-thermal imagery and photothermal therapy[57];(E) fluorescence intensity of GQDs at 680 nm versus the O2 concentration in solution[58] |
目前,以LED为主的第四代照明显示光源正在多个领域逐步取代传统照明光源,LED使用的发光材料多为GaN蓝光芯片激发的稀土掺杂发光(Eu、Si、Ce等)以及半导体量子点发光材料(CdS、CdTe、ZnS等)[59]。最近,经过广大科研工作者的广泛研究,一些阻碍碳点在发光显示应用方面的问题逐渐得到解决,碳点正慢慢显示出在发光显示器件方面应用的潜力。
Guo X等[60]利用不同温度下热解环氧富集聚苯乙烯的方法制得蓝色、橙色、白色三种不同颜色荧光的碳点(图 9A),量子产率达47%,同时首次成功把三种不同的碳点封装成紫外激发LED,色坐标分别为蓝(0.19,0.28)、橙(0.45,0.44)、白(0.34,0.37)。虽然此文献中没有提到有关流明效率以及白光显色性的问题,但是较高的量子产率和不同的颜色,使碳点在LED的应用上发展了一大步。一般碳点在蓝绿光波段量子产率较高,一些研究者用蓝光碳点和其他量子点或者发光粉混合制作白光LED。Li C X等[61]利用微波法制成蓝光碳点,使之与绿光(0.34, 0.64)和红光(0.64, 0.36) CdTe量子点(尺寸不同)混合制成红绿蓝三基色紫外激发白光LED,流明效率达30 lm/W,显色指数高达87 (图 9B)。
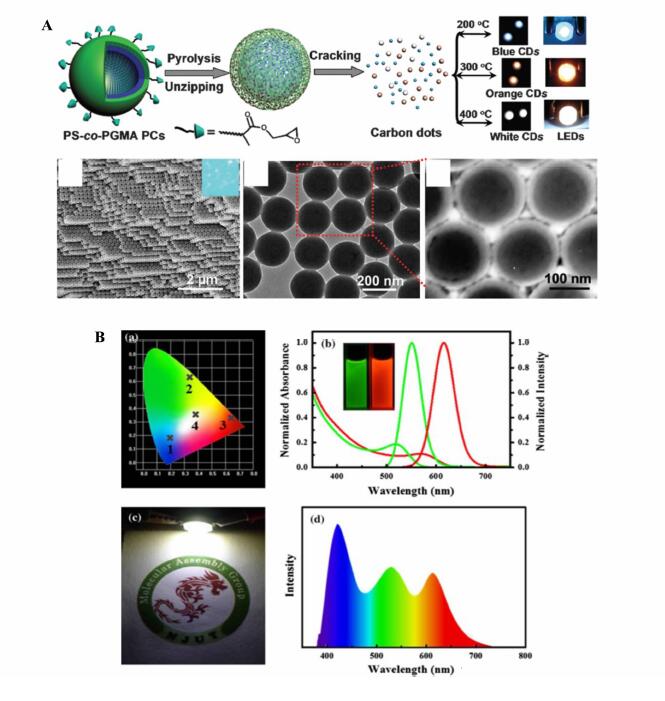 | 图9 LED器件 (A) 蓝、橙、白3种不同颜色荧光碳点封装的LED器件[60];(B) 荧光碳点和CdTe量子点混合混合封装的高显色指数LED器件[61]LED devices (A) The LED devices packaged by blue, orange, white fluorescent carbon dots[60];(B) high CRI LED devices packaged by carbon dots and CdTe quantum dots[61] |
本课题组利用氨调制水热法制备的荧光碳点,用360 nm波段紫外激发芯片封装了具有宽色域的蓝光LED(图 10A)。同时,结合绿色稀土发光材料SrSi2O2N2:Eu粉末(图 10B)与红色稀土发光材料Sr2Si5N8:Eu粉末(图 10C)制备了性能优良的暖白光LED(图 10D),其CIE色坐标为(0.33,0.37)(图 10E),在100 mA电流的驱动下此WLED发出色温5447 K、显色指数高达95.1的明亮白光,完全符合了国际照明委员会规定的用于需要色彩精确对比的场所的光谱连续且频带较宽的光源要求,具有潜在的实际应用价值[10]。
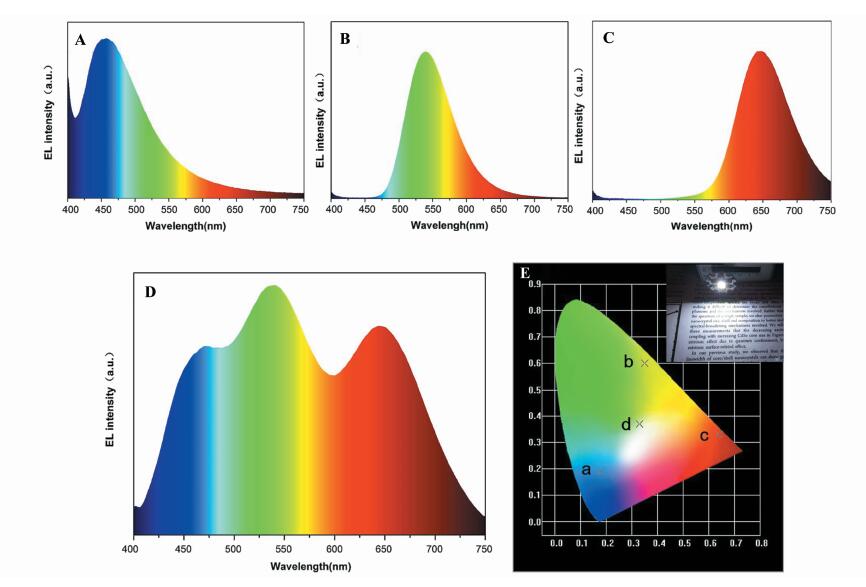 | 图10 氨调制水热法合成的荧光碳点制备LED (A) 氨调制水热法荧光碳点制备蓝光LED光谱; (B) 绿色发光材料SrSi2O2N2:Eu 制备的LED光谱;(C) 红色发光材料Sr2Si5N8:Eu 制备的LED光谱;(D) 以上3种材料制备的WLED光谱;(E) 以上4种LED的CIE 色坐标以及WLED图像The LED prepared with CDs synthesized via ammonia-modified hydrothermal method (A) Spectrum of the blue LED prepared by CDs made via ammonia-modified hydrothermal method;(B) spectrum of the LED fabricated with green-emitting phosphor SrSi2O2N2:Eu; (C) spectrum of the LED fabricated with red-emitting phosphor Sr2Si5N8:Eu; (D) spectrum of the WLED fabricated with the three materials; (E) the CIE color coordinate of the four LEDs and the image of the WLED |
目前,研究和应用最广泛的量子点仍然是由Ⅱ-Ⅵ族或者Ⅲ-Ⅴ族的有潜在毒性的重金属和非金属元素所构成。它们的生产成本较高,工艺相对复杂。碳点作为新一代的量子点材料以其制作成本低、工艺简单、良好的发光性能、优异的生物相容性等优点受到广泛关注。
在生物标记、细胞成像和光诊疗剂等生物医学领域,因其巨大的应用前景受到众多研究者的青睐。到目前为止,有关碳点在制备应用等方面也取得了一定的进展和成果。然而,更高效的制备粒径和形貌均一的高质量碳点的方法还有待开发,碳点的荧光量子产率还有待提高,碳点在生物体内的长期毒性尚需进一步研究,其应用范围也需要拓展。
荧光碳点在LED以及显示器件上的应用尚不成熟,除了量子效率还无法与传统半导体量子点或者稀土掺杂发光材料相比外,荧光波段较窄也很受局限。另外,合成碳点多为水相法,碳点与油相的封装材料相容性较差。因此,在发光显示器件应用方面还有诸多问题需要解决。
| [1] | Shirasaki Y, Supran G J, Bawendi M G, Bulovi V. Emergence of colloidal quantum-dot light-emitting technologies [J]. Nature Photonics, 2013, 7(1): 13-23. |
| [2] | Yang Y H, Cui J H, Zheng M T, Hu C F, Tan S Z, Xiao Y, Yang Q, Liu Yi L. One-step synthesis of amino-functionalized fluorescent carbon nanoparticles by hydrothermal carbonization of chitosan [J]. Chemical Communications, 2012, 48(3): 380-382. |
| [3] | Xu X Y, Robert R, Gu Y L, Ploehn H J, Latha G, Kyle R, Scrivens W A. Electrophoretic analysis and purification of fluorescent single-walled carbon nanotube fragments [J]. Journal of the American Chemical Society, 2004, 126(40): 12736-12737. |
| [4] | Sun Y P, Zhou B, Lin Y, Wang W, Fernando K A , Pankaj P, Mohammed J M, Harruff B A, Wang X, Wang H F. Quantum-sized carbon dots for bright and colorful photoluminescence [J]. Journal of the American Chemical Society, 2006, 128(24): 7756-7757. |
| [5] | Hu S L, Niu K Y, Sun J, Yang J, Zhao N Q, Du X W. One-step synthesis of fluorescent carbon nanoparticles by laser irradiation [J]. Journal of Materials Chemistry, 2009, 19(4): 484-488. |
| [6] | Zhou J G, Christina B, Li R Y, Zhou X T, Sham T K, Sun X L, Ding Z F. An electrochemical avenue to blue luminescent nanocrystals from multiwalled carbon nanotubes(MWCNTs) [J]. Journal of the American Chemical Society, 2007, 129(4): 744-745. |
| [7] | Liu H P, Ye T, Mao C D. Fluorescent carbon nanoparticles derived from candle soot [J]. Angewandte Chemie International Edition, 2007, 46(34): 6473-6475. |
| [8] | Zhu S J, Meng Q N, Wang L, Zhang J H, Song Y B, Jin H, Zhang K, Sun H C, Wang H Y, Yang B. Highly photoluminescent carbon dots for multicolor patterning, sensors, and bioimaging [J]. Angewandte Chemie International Edition, 2013, 125(14): 4045-4049. |
| [9] | Hu S L, Tian R X, Dong Y G, Yang J L, Liu J, Chang Q. Modulation and effects of surface groups on photoluminescence and photocatalytic activity of carbon dots [J]. Nanoscale, 2013, 23(23): 11665-11671. |
| [10] | Wang S D, Zhu Z F, Chang Y J, Wang H ,Yuan N, Li G P, Yu D B, Jiang Y. Ammonium hydroxide-modulated synthesis of high-quality fluorescent carbon dots for white LEDs with excellent color rendering properties[J]. Nanotecnology, 2016. |
| [11] | Dong Y Q, Wang R X, Li G L, Chen C Q, Chi Y W, Chen G N. Polyamine-functionalized carbon quantum dots as fluorescent probes for selective and sensitive detection of copper ions [J]. Analytical Chemistry, 2012, 84(14): 6220-6224. |
| [12] | Guo X, Wang C F, Yu Z Y, Chen L, Chen S. Facile access to versatile fluorescent carbon dots toward light-emitting diodes [J]. Chemical Communications, 2012, 48(21): 2692-2694. |
| [13] | Wang X H, Qu K G, Xu B L, Ren J S, Qu X G. Microwave assisted one-step green synthesis of cell-permeable multicolor photoluminescent carbon dots without surface passivation reagents [J]. Journal of Materials Chemistry, 2011, 8(8): 2445-2450. |
| [14] | Zhang J, Yuan Y, Liang G L, Yu S H. Scale-up synthesis of fragrant nitrogen-doped carbon dots from bee pollens for bioimaging and catalysis [J]. Advanced Science, 2015, 2(4): 1500002. |
| [15] | Du F Y, Zhang M M, Li X F, Li J N, Jiang X Y, Li Z, Hua Y, Shao G H, Jin J, Shao Q X. Economical and green synthesis of bagasse-derived fluorescent carbon dots for biomedical applications [J]. Nanotechnology, 2014, 25(31): 315702. |
| [16] | Wang L, Zhou H S. Green synthesis of luminescent nitrogen-doped carbon dots from milk and its imaging application [J]. Analytical Chemistry, 2014, 86(18): 8902-8905. |
| [17] | Jiang C K, Wu H, Song Xi J, Ma X J, Wang J H, Tan M Q. Presence of photoluminescent carbon dots in nescafes original instant coffee: applications to bioimaging [J]. Talanta, 2014, 127:68-74. |
| [18] | Sahu S, Behera B, Maiti T K, Mohapatra S. Simple one-step synthesis of highly luminescent carbon dots from orange juice: application as excellent bio-imaging agents [J]. Chemical Communications, 2012, 48(70): 8835-8837. |
| [19] | Habiba K, Makarov V I, Avalos J, Guinel M J F, Weiner B R, and Morell G. Luminescent graphene quantum dots fabricated by pulsed laser synthesis [J]. Carbon, 2013, 64(9): 341-350. |
| [20] | Zhu Z F, Wang S D, Chang Y J, Yu D B and Jiang Y. Direct photodissociation of toluene molecules to photoluminescent carbon dots under pulsed laser irradiation[J]. Carbon, 2016. |
| [21] | 胡胜亮, 白培康, 孙 景, 曹士锐. 荧光碳纳米颗粒:新进展和技术挑战 [J]. 化学进展, 2010, 22(2/3): 345-351. Hu S L, Bai P K, Sun J, Cao S R. Fluorescent carbon nanoparticles: recent achievements and technical challenges[J]. Progress in Chemistry, 2010, 22(2/3): 345-351. |
| [22] | Li H T, He X D, Kang Z H, Huang H, Liu Y, Liu J, Lian S Y, Tsang C H A, Yang X B, Lee S T. Water-soluble fluorescent carbon quantum dots and photocatalyst design [J]. Angewandte Chemie International Edition, 2010, 49(26):4430-4434. |
| [23] | Duan H Y, Jiang Y, Zhang Y G, Sun D P, Liu C, Huang J, Lan X Z, Zhou H Y, Chen L. High quantum-yield CdSe<em>xS1-x/ZnS core/shell quantum dots for warm white light-emitting diodes with good color rendering [J]. Nanotechnology, 2013, 24(28): 285201-8(8). |
| [24] | Bao L, Liu C, Zhang Z L, Pang D W. Photoluminescence-tunable carbon nanodots: surface-state energy-gap tuning [J]. Advanced Materials, 2015, 27(10):1663-1667. |
| [25] | 梁大顺. Ⅱ-Ⅵ族核壳结构半导体量子点的制备及其发光特性的物理机制. 东南大学, 2009. Liang D S. Synthesis and photoluminescent physical mechanism of II-VI group core/shell semiconductor quantum dots. Southeast University, 2009. |
| [26] | Zhang S P, Xiong P, Yang X J, Wang X. Novel PEG functionalized graphene nanosheets: enhancement of disper-sibility and thermal stability [J]. Nanoscale, 2011, 3(5): 2169-2174. |
| [27] | Pan D Y, Zhang J C, Li Z, Wu Mi H. Hydrothermal route for cutting graphene sheets into blue-luminescent graphene quantum dots [J]. Advanced Materials, 2010, 22(6): 734-738. |
| [28] | Wang F, Xie Z, Zhang H , Liu C Y, Zhang Y G. Highly luminescent organosilane-functionalized carbon dots [J]. Advanced Functional Materials, 2011, 21(21):1027-1031. |
| [29] | Li X M, Zhang S L, Kulinich S A, Liu Y L, Zeng H B. Engineering surface states of carbon dots to achieve controllable luminescence for solid-luminescent composites and sensitive Be2+ detection [J]. Nature Scientific Reports, 2014, 4(2): 4976. |
| [30] | Zhang J C, Shen W Q, Pan D Y, Zhang Z W, Fang Y G, Wu M H. Controlled synthesis of green and blue luminescent carbon nanoparticles with high yields by the carbonization of sucrose [J]. New Journal of Chemistry, 2010, 11(10):1336-1339. |
| [31] | Luo P G, Sahu S, Yang S T, Sonkar S K, Wang J P, Wang H F, LeCroy G E, Cao L, Sun Y P. Carbon "quantum" dots for optical bioimaging [J]. Journal of Materials Chemistry B, 2013, 1(16):2116-2127. |
| [32] | Liu J H, Yang S T, Chen X X, Wang H F. Fluorescent carbon dots and nanodiamonds for biological imaging: preparation, application, pharmacokinetics and toxicity [J]. Current Drug Metabolism, 2012, 13(8):1046-1056. |
| [33] | Luo P G, Yang F, Yang S T, Sonkar S K, Yang L J, Broglie J J, Liu Y, Sun Y P. Carbon-based quantum dots for fluorescence imaging of cells and tissues [J]. RSC Advances, 2014, 21(21): 10791-10807. |
| [34] | Wang W, Li Y M, Cheng L, Cao Z Q, Liu W G. Water-soluble and phosphorus-containing carbon dots with strong green fluorescence for cell labeling [J]. Journal of Materials Chemistry B, 2014, 2(1): 46-48. |
| [35] | Cao L, Wang X, Meziani M J, Lu F, Wang H, Luo P G, Lin Y, Harruff B A, Veca L M, Murray D, Xie S Y, Sun Y P. Carbon dots for multiphoton bioimaging [J]. Journal of the American Chemical Society, 2007, 129(37):11318-11319. |
| [36] | Liu R L, Wu D Q, Liu S H, Koynov K, Knoll W, Li Q. An aqueous route to multicolor photoluminescent carbon dots using silica spheres as carriers.[J]. Angewandte Chemie International Edition, 2009, 48(25):4598-4601. |
| [37] | Qiao Z A, Wang Y F, Gao Y, Li H W, Dai T Y, Liu Y L. Huo Q S. Commercially activated carbon as the source for producing multicolor photoluminescent carbon dots by chemical oxidation [J]. Chemical Communications, 2010, 46(46):8812-8814. |
| [38] | Jin X Z, Sun X B, Chen G, Ding L X, Li Y H, Liu Z K, Wang Z J, Pan W, Hu C H, Wang J P. PH-sensitive carbon dots for the visualization of regulation of intracellular PH inside living pathogenic fungal cells [J]. Carbon, 2015, 81(1):388-395. |
| [39] | Yang S T, Cao L, Luo P G, Lu F S, Wang X, Wang H F, Meziani M J, Liu Y F, Qi G, Sun Y P. Carbon dots for optical imaging in vivo [J]. Journal of the American Chemical Society, 2009, 131(32): 11308-11309. |
| [40] | Parvin N, Mandal T K, Roy P. Polyelectrolyte carbon quantum-dots: new player as a noninvasive imaging probe in drosophila [J]. Journal of Nanoscience and Nanotech-nology, 2013, 13(10): 6499-6505. |
| [41] | Thakur M, Pandey S, Mewada A, Patil V, Khade M, Goshi E, Sharon M. Antibiotic conjugated fluorescent carbon dots as a theranostic agent for controlled drug release, bioimaging, and enhanced antimicrobial activity [J]. Journal of Drug Delivery, 2014, 2014:282193-282193. |
| [42] | Zheng M, Liu S, Li J, Qu D, Zhao H F, Guan X G, Hu X L, Xie Z G, Jing X B, Sun Z C. Integrating oxaliplatin with highly luminescent carbon dots: an unprecedented theranostic agent for personalized medicine [J]. Advanced Materials, 2014, 26(21): 3554-3560. |
| [43] | Kong W Q, Liu J, Liu R H, Li H, Liu Y, Huang H, Li K Y, Liu J, Lee S T, Kang Z H. Quantitative and real-time effects of carbon quantum dots on single living HeLa cell membrane permeability [J]. Nanoscale, 2014, 6(10): 5116-5120. |
| [44] | Lecroy G E, Sonkar S K, Yang F, Veca L M, Wang P, Tackett K N, Yu J J, Vasile E, Qian H J, Liu Y M, Luo P G, SunY P. Toward structurally defined carbon dots as ultra-compact fluorescent probes [J]. ACS Nano, 2014, 8(5):4522-4529. |
| [45] | Hu S L, Zhao Q, Chang Q, Yang J L, Liu J. Enhanced performance of Fe3+ detection via fluorescence resonance energy transfer between carbon quantum dots and Rhodamine B [J]. RSC Advances, 2014, 4(77):41069-41075. |
| [46] | Zong J, Yang X L, Trinchi A, Hardin S, Cole I, Zhu Y H, Li C Z, Muster T, Wei G. Carbon dots as fluorescent probes for "off-on" detection of Cu2+ and l-cysteine in aqueous solution [J]. Biosensors and Bioelectronics, 2013, 51C:330-335. |
| [47] | Zhai Y L, Zhu Z J, Zhu C Z, Ren J T, Wang E K, Dong S J. Multifunctional water-soluble luminescent carbon dots for imaging and Hg2+ sensing [J]. Journal of Materials Chemistry B, 2014, 2(40):6995-6999. |
| [48] | Jiang Y L, Wang Y X, Meng F D, Wang B X, Cheng Y X, Zhu C J. N-doped carbon dots synthesized by rapid microwave irradiation as highly fluorescent probes for Pb2+ detection [J]. New Journal of Chemistry, 2015, 39(5):3357-3360. |
| [49] | Wang Y, Lu J, Tang L H, Chang H X, Li J H. Graphene oxide amplified electrogenerated chemiluminescence of quantum dots and its selective sensing for glutathione from thiol-containing compounds [J]. Analytical Chemistry, 2009, 81(23): 9710-9715. |
| [50] | Zhang L L, Han Y J, Zhu J B, Zhai Y L, Dong S J. Simple and sensitive fluorescent and electrochemical trinitrotoluene sensors based on aqueous carbon dots [J]. Analytical Chemistry, 2015, 87(4): 2033-2036. |
| [51] | Gao Z, Wang L B, Su R X, Huang R L, Qi W, He Z M. A carbon dot-based "off-on" fluorescent probe for highly selective and sensitive detection of phytic acid [J]. Biosensors and Bioelectronics, 2015, 70:232-238. |
| [52] | Shen P F, Xia Y S. Synthesis-modification integration: one-step fabrication of boronic acid functionalized carbon dots for fluorescent blood sugar sensing[J]. Analytical Chemistry, 2014, 57(5):536-544. |
| [53] | Ge J C, Lan M H, Zhou B J, Liu W M, Guo L, Wang H, Jia Q Y, Niu G L, Huang X, Zhou H Y. A graphene quantum dot photodynamic therapy agent with high singlet oxygen generation [J]. Nature Communications, 2014, 5:4596-4596. |
| [54] | Hu S H, Chen Y W, Hung W T, Chen I W, Chen S Y. Quantum-dot-tagged reduced graphene oxide nanocomposites for bright fluorescence bioimaging and photothermal therapy monitored in situ [J]. Advanced Materials, 2012, 24(13):1748-1754. |
| [55] | Huang P, Lin J, Wang X S, Wang Z, Zhang C L, He M, Wang K, Chen F, Li Z M, Shen G X. Light-triggered theranostics based on photosensitizer-conjugated carbon dots for simultaneous enhanced-fluorescence imaging and photodynamic therapy [J]. Advanced Materials, 2012, 24(37):5104-5110. |
| [56] | Tang J, Kong B, Wu H, Xu M, Wang Y C, Wang Y L, Zhao D Y, Zheng G F. Carbon nanodots featuring efficient FRET for real-time monitoring of drug delivery and two-photon imaging [J]. Advanced Materials, 2013, 25(45):6569-6574. |
| [57] | Ge J C, Jia Q Y, Liu W M, Guo L, Liu Q Y, Lan M H, Zhang H Y, Meng X M, Wang P F. Red-emissive carbon dots for fluorescent, photoacoustic and thermal theranostics in living mice [J]. Advanced Materials, 2015, 27(28):4169-4177. |
| [58] | Ge J C, Lan M H, Zhou B J, Liu W M, Guo L, Wang H. A graphene quantum dot photodynamic therapy agent with high singlet oxygen generation[J]. Nature Communications, 2014, 5: 4596-4596. |
| [59] | Chang Y J, Yao X D, Zhang Z P, Jiang D L, Yu Y L, Mi L F, Wang H, Li G P, Yu D B, Jiang Y. Preparation of highly luminescent BaSO4 protected CdTe quantum dots as conversion materials for excellent color-rendering white LEDs [J]. Journal of Materials Chemistry C, 2015, 3: 2831-2836. |
| [60] | Guo X, Wang C F, Yu Z Y, Chen L, Chen S. Facile access to versatile fluorescent carbon dots toward light-emitting diodes[J]. Chemical Communications, 2012, 48(21): 2692-2694. |
| [61] | Li C X, Yu C, Wang C F, Chen S. Facile plasma-induced fabrication of fluorescent carbon dots toward high-performance white LEDs [J]. Journal of Materials Science, 2013, 48(18): 6307-6311. |




