纳米颗粒材料以其独特的“小尺度效应”,表现出传统体块材料所不具备的物理化学性能,在众多领域中均有着广泛的应用前景[1,2,3,4]。因此,许多研究者都在致力于发掘和探究纳米颗粒材料这些独特而优异的性能。其中,纳米颗粒材料巨大的比表面积,使其成为“天生的”催化材料[5]。纳米颗粒无论是本身作为催化剂,还是作为其他催化剂的载体,都是近期的研究热点。此外,纳米催化剂由于尺度较小,自身不会遮蔽光照,这也是其在光催化方面应用的一大优势[6, 7]。
纳米半导体光催化是近10年来的研究焦点,半导体的光电转化特性使得半导体催化剂能够将光能转化为化学能,外界光波成为化学反应的参与者,更是降低了许多化学反应对反应条件的要求。1976年,Carey J H等人[8]报道了在紫外光照射条件下,纳米TiO2可使难降解的有机化合物多氯联苯脱氯,成为了光催化技术在生态环保领域的研究先导。由于和TiO2具有相近的禁带宽度,ZnO引起了人们越来越多的关注,并且与TiO2相比,ZnO具有直接带隙和高的载流子迁移率[9]。一些研究结果表明,ZnO在处理废水中的一些难降解有机污染物时具有比TiO2更好的光催化效果[10,11]。Suib S L等人[12]通过溶剂热法,以四氢呋喃为溶剂制备的菜花状 ZnO 在紫外光照射下具有很高的光催化活性,光照20 min后对苯酚的降解速率可达到100%。尽管这些ZnO纳米结构的光催化活性很高,但由于其禁带宽度的限制,其吸收光谱绝大部分分布在紫外区,需要紫外光照射才能高效降解有机污染物,这极大地限制了其在实际中的应用[13]。
近来,研究人员发现离子掺杂是一种调节宽带隙半导体能带的有效方法[14,15]。通过将离子掺入到ZnO晶格中,在其带隙内形成缺陷能级或者定域态的杂质能级,并引入丰富的氧空位,能够在拓宽ZnO光响应范围的同时,达到光生载流子有效分离的目的[16,17,18]。本文发展了一种Fe掺杂ZnO纳米催化剂的热蒸发制备方法,通过Fe掺杂在ZnO中引入掺杂能级,拓展了ZnO纳米催化剂的光响应范围,进而得到了良好的催化效率。
1 实验部分 1.1 Fe掺杂ZnO空穴微球的制备取1 g高纯度Zn粉末(纯度99.99%)加入浓度为2 mol/L双氧水溶液中,超声振荡至少10 min直至Zn粉末均匀分散在溶液中。然后,用去离子水与无水乙醇多次离心清洗,自然干燥,得到Zn/ZnO核壳结构粉末。将上述Zn/ZnO核壳结构粉末加入到20 mL浓度为10 mol/L的FeCl2去离子水溶液中,密闭容器,磁力搅拌3 min,溶液中微球会再次团聚,取出再用无水乙醇清洗,并保存于无水乙醇中。粉末表面将附着一层金属Fe,形成Zn/(ZnO/Fe)复合结构(作为对比的未掺杂样品不进行此项操作)。将上述Zn/(ZnO/Fe)复合结构的粉末直接涂在陶瓷片上置于真空管式炉中,室温抽真空至10 Pa以下,保证乙醇挥发干净。随后,在管式炉中通入氧气,调整真空至100 Pa并设置气流流速为20 sccm。将管式炉加热区中心升温到600 ℃,升温速度20 ℃/min,保持1 h后自然冷却至室温,取出样品。
1.2 样品表征采用粉末X射线衍射仪(Bruker D 8 Focus,XRD)、Hitachi S-4800扫描电子显微镜(SEM)观察样品形貌、JEOL-2100F透射电子显微镜(TEM)、能谱仪(EDS)对样品的物相、形貌、结构、成分等进行分析。利用紫外可见光分光光度计Cary 5000及其漫反射组件对Fe掺杂ZnO空心微球以及纯ZnO空心微球的可见光吸收谱进行测量。
1.3 光催化性能测试本实验使用有机染料罗丹明B进行降解性能测试。取0.1 g的Fe掺杂ZnO空心微球,加入到20 mL浓度为1 ml/L的罗丹明B溶液中,搅拌均匀,黑暗中静置1 h。取上述样品若干份,用标准太阳光灯同时照射,每隔15 min取一份样品测量罗丹明B的吸收光谱,所用设备为日本日立公司的F-2100型紫外可见光分光光度计。
2 结果与讨论本文采用离子交换和热蒸发法制备Fe掺杂ZnO空心微球,其生长过程示意图如图 1所示。Zn是一种相对活泼的金属,Zn颗粒暴露在空气中,表面会形成一层超薄的氧化层,即ZnO层。为了使最后的空心球有一定的强度,我们用双氧水预先处理Zn颗粒,用于增加氧化层厚度,形成Zn/ZnO核壳结构。加入FeCl2后,金属Zn能够将Fe2+还原为金属Fe,形成Zn/(ZnO/Fe)的复合核壳结构。在高温条件下,Zn/(ZnO/Fe)核壳结构内部的Zn将会逐渐蒸发,与核壳结构表面的氧气反应生长成为ZnO纳米棒。Fe元素在高温条件下扩散进入ZnO,进一步形成Fe掺杂的ZnO空心微球。
图 2为Fe掺杂ZnO空心微球在制备过程中各个阶段的SEM图片。图 2(a) 是纯金属Zn微球的SEM图片,可以看到微球表面相对光滑。此时Zn颗粒表面有一层很薄的氧化层,如果直接进行热蒸发实验,空心球将极容易破碎,所以我们用高浓度的H2O2进行预氧化,以增加其表面的氧化层厚度。图 2(b)为Zn/(ZnO/Fe)复合结构的SEM图片,在微球表面发现许多微小的Fe颗粒。Fe的常压熔点为1535 ℃,在600 ℃的低真空条件下,会与Zn一起蒸发。但是,Zn比Fe更加活泼,在Zn足量的环境中ZnO更容易形成,Fe不会形成氧化物[见图 3(a)],而以离子的形式掺杂进入ZnO之中。图 2(c)是Fe掺杂ZnO空心微球的SEM照片,从中可以看到微球表面长满了较短的ZnO纳米棒。相对于球形颗粒而言,ZnO纳米棒极大地增加了微球的比表面积,同时又不会因纳米棒过长而导致微球互相穿插在一起。图 2(d)是一个开口的Fe掺杂ZnO微球,说明合成的球体内部是空心的。空心球的优势主要有两点,(1)其表面积至少是同直径球体的两倍;(2)空心结构使样品能够更好地分散于溶液中。
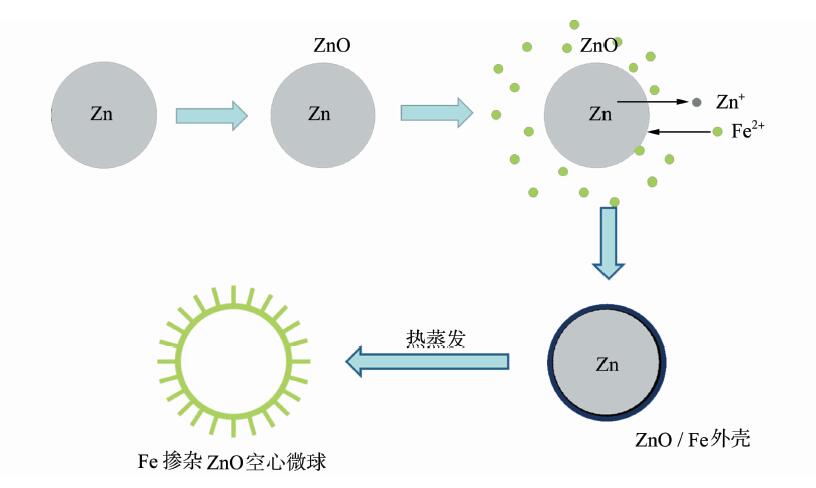 | 图1 Fe掺杂ZnO空心微球的生长机理图 Schematic growth mechanism of Fe doped ZnO hollow microsphere |
 | 图2 (a) Zn空心微球的SEM图片;(b) ZnO/Fe 复合微球的SEM图片;(c) Fe掺杂ZnO空心微球SEM照片;(d) 一个开口的Fe掺杂ZnO微球 (a) SEM image of ZnO hollow microsphere; (b) SEM image of ZnO/Fe hollow microsphere; (c) SEM image of Fe doped ZnO hollow microsphere; (d) SEM image of Fe doped ZnO hollow microsphere with a small hole |
图 3(a)为产物的XRD衍射图谱,从图谱中可以看到多个尖锐的衍射峰,说明制备的样品具有较高的结晶性。另外,可以发现XRD图谱中的衍射峰与XRD标准图谱(PDF NO:36-1451)吻合较好,且没有其它衍射峰,表明获得的产物为六方相ZnO。图 3(b)为Fe掺杂ZnO空心微球的TEM照片,可以看到空心球外表面有向外伸展的ZnO纳米棒,直径与长度都约为100多纳米。图3(c)是ZnO纳米棒的高分辨TEM(HRTEM)图片,图中标注的条纹间距约为0.26 nm,与六方相ZnO的(002)晶面间距相对应。HRTEM图片的傅立叶变换展示于图 3(c)之中,可以看到一套完整规则的电子衍射点,表明此纳米棒为单晶,其中,临近点和次临近点分别对应与六方相ZnO的(002)和(-1-10)晶面。图 3(a)为Fe掺杂ZnO空心微球的EDX图谱,可以看到,除了来自电镜载网的Cu和C两种元素以外,能谱中只含有O、Zn和Fe 三种元素的信号,这证明Fe元素在反应过程中成功进入到ZnO空心微球之中。
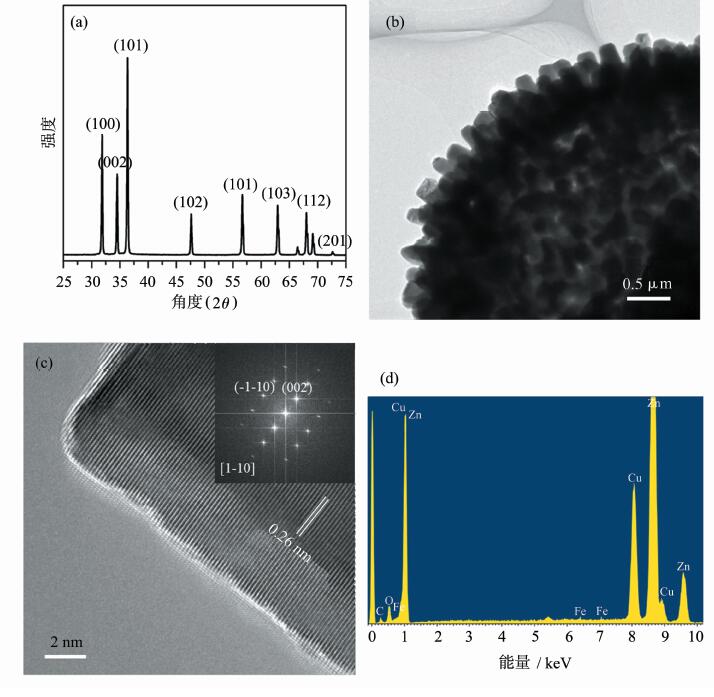 | 图3 (a)Fe掺杂ZnO空心微球粉末的XRD照片;(b)Fe掺杂ZnO空心微球的TEM照片;(c)生长在Fe掺杂ZnO空心微球表面的ZnO纳米棒的HRTEM照片及其傅里叶变换;(d) Fe掺杂ZnO空心微球的EDS照片 (a) XRD pattern of the Fe doped ZnO hollow microspheres; (b) TEM image of a Fe doped ZnO hollow microsphere;(c) HRTEM image of a ZnO nanorod grown on a Fe doped ZnO hollow microsphere and the corresponding Fourier transform image; (d) EDX spectrum of the Fe doped ZnO hollow microsphere |
图 4为Fe掺杂ZnO空心微球与纯ZnO样品的光漫反射吸收光谱,从中可知纯ZnO的禁带宽度约为3.3 eV,对应于375 nm的吸收边。另外,还可以看出纯ZnO样品几乎不吸收波长超过375 nm的光,而Fe掺杂ZnO空心微球因为掺杂了Fe元素,引入了杂质能级,没有表现出一个明显的吸收边,电子可在杂质能级间跃迁,实现了对波长375~600 nm的光波的吸收。以上结果表明在Fe掺杂的ZnO催化剂中,杂质能级吸收的可见光光波能量足够产生空穴电子对,分解催化剂表面吸附的氢氧自由基,提供活性氧离子,从而降解溶液中的污染物。
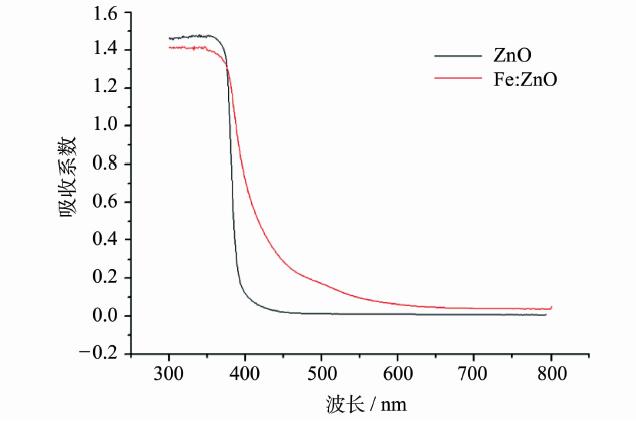 | 图4 Fe掺杂ZnO空心微球与纯ZnO微球的漫反射吸收光谱 Diffuse reflectance spectrum of the Fe doped ZnO hollow microspheres and the pure ZnO hollow microspheres |
光吸收光谱证明Fe掺杂ZnO空心微球能够实现对波长375~600 nm的光波的吸收,表明可以将Fe掺杂ZnO空心微球用于可见光光降解。接下来,我们利用合成的样品作为催化剂,进行罗丹明B的光降解测试,实验结果如图 5所示。从图中可以看到,随着光照时间的延长,罗丹明B的紫外可见光吸收光谱的吸收逐渐降低,表明罗丹明B的浓度随着时间的延长而降低。另外,可以看到,光照时间达到90 min时,罗丹明B的降解率就超过了90%,说明本实验中合成的Fe掺杂ZnO空心微球不仅能够在可见光下降解有机染料,还是一种相当高效的光催化剂。
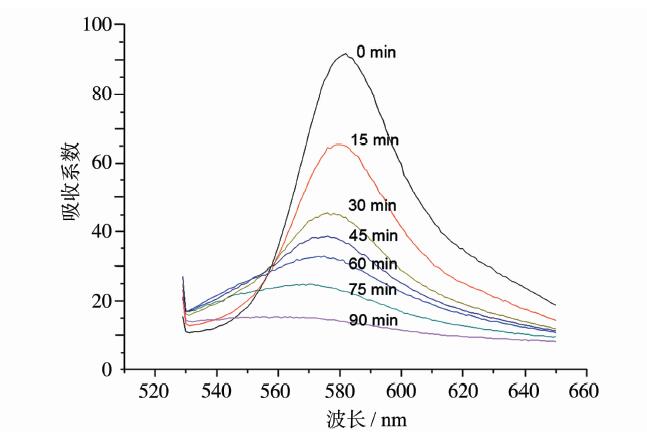 | 图5 利用Fe掺杂ZnO空心微球作为催化剂在不同光照时间条件下罗丹明B的紫外可见光吸收光谱 UV-Vis absorbance spectra of Rh B solution after different irradiation time in the presence of Fe doped ZnO hollow microspheres |
本文中,我们通过离子交换和热蒸发法合成了Fe掺杂的ZnO空心微球。SEM表征表明合成的Fe掺杂ZnO空心微球表面有大量毛刺状的ZnO纳米棒,XRD和TEM表征证明合成的空心微球为Fe掺杂ZnO,不含其它杂质,而漫反射吸收光谱测试表明Fe掺杂ZnO空心微球可以实现对波长375~600 nm光波的吸收。另外,光降解实验证明合成的Fe掺杂ZnO空心微球具有优异的光降解能力,可以作为光催化剂用于光降解有机废物。
| [1] | Gleiter H. Nanocrystalline materials[J]. Progress in Materials Science, 1989, 33(4): 223-315. |
| [2] | Andres R P, Averback R S, Brown W L, Brus L E, Goddard W A, Kaldor A, Louie S G, Moscovits M, Peercy P S, Riley S J, Siegel R W, Spaepen F, Wang Y. Research opportunities on clusters and cluster-assembled materials-a department of energy, council on materials science panel report[J]. Journal of Materials Research, 1989, 4(3): 704-736. |
| [3] | McHenry M E, Willard M A, Laughlin D E. Amorphous and nanocrystalline materials for applications as soft magnets[J]. Progress in Materials Science, 1999, 44(4): 291-433. |
| [4] | Oelerich W, Klassen T, Bormann R. Metal oxides as catalysts for improved hydrogen sorption in nanocrystalline Mg-based materials[J]. Journal of Alloys and Compounds, 2001, 315(1-2): 237-242. |
| [5] | Fujishima A, Honda K. Electrochemical photolysis of water at a semiconductor electrode[J].Nature, 1972, 238(5358): 37. |
| [6] | Bahnemann D. Photocatalytic water treatment: solar energy applications[J]. Solar Energy, 2004, 77(5): 445-459. |
| [7] | Malato S, Blanco J, Vidal A, Richter C. Photocatalysis with solar energy at a pilot-plant scale: an overview[J]. Applied Catalysis B-Environmental, 2002, 37(1): 1-15. |
| [8] | Carey J H, Lawrence J, Tosine H M. Photo-dechlorination of pcbs in presence of titanium-dioxide in aqueous suspensions [J]. Bulletin of Environmental Contamination and Toxicology, 1976, 16(6): 697-701. |
| [9] | Mapa M, Gopinath C S. Combustion synthesis of triangular and multifunctional ZnO1-xNx (x<= 0.15) materials[J]. Chemistry of Materials, 2009, 21(2): 351-359. |
| [10] | Tian C, Zhang Q, Wu A, Jiang M, Liang Z, Jiang B, Fu H. Cost-effective large-scale synthesis of ZnO photocatalyst with excellent performance for dye photodegradation[J]. Chemical Communications, 2012, 48(23): 2858-2860. |
| [11] | Duan X, Wang G, Wang H, Wang Y, Shen C, Cai W. Orientable pore-size-distribution of ZnO nanostructures and their superior photocatalytic activity[J]. Crystengcomm, 2010, 12(10): 2821-2825. |
| [12] | Xu L, Hu Y L, Pelligra C, Chen C H, Jin L, Huang H, Sithambaram S, Aindow M, Joesten R, Suib S L. ZnO with different morphologies synthesized by solvothermal methods for enhanced photocatalytic activity[J]. Chemistry of Materials, 2009, 21(13): 2875-2885. |
| [13] | Tong H, Ouyang S, Bi Y, Umezawa N, Oshikiri M, Ye J. Nano-photocatalytic materials: possibilities and challenges[J]. Advanced Materials, 2012, 24(2): 229-251. |
| [14] | Xiao Q, Zhang J, Xiao C, Tan X. Photocatalytic decolorization of methylene blue over Zn1-xCoxO under visible light irradiation[J]. Materials Science and Engineering B-Solid State Materials for Advanced Technology, 2007, 142(2-3): 121-125. |
| [15] | Jia T, Wang W, Long F, Fu Z, Wang H, Zhang Q. Fabrication, characterization and photocatalytic activity of La-doped ZnO nanowires[J]. Journal of Alloys and Compounds, 2009, 484(1-2): 410-415. |
| [16] | Wang C Y, Bottcher C, Bahnemann D W, Dohrmann J K. A comparative study of nanometer sized Fe(Ⅲ)-doped TiO2 photocatalysts: synthesis, characterization and activity[J]. Journal of Materials Chemistry, 2003, 13(9): 2322-2329. |
| [17] | Mahmood M A, Baruah S, Dutta J. Enhanced visible light photocatalysis by manganese doping or rapid crystallization with ZnO nanoparticles[J]. Materials Chemistry and Physics, 2011, 130(1-2): 531-535. |
| [18] | Lu Y, Lin Y, Xie T, Shi S, Fan H, Wang D. Enhancement of visible-light-driven photoresponse of Mn/ZnO system: photogenerated charge transfer properties and photocatalytic activity[J]. Nanoscale, 2012, 4(20): 6393-6400. |




