2. 贵州大学 农学院, 贵州 贵阳 550025;
3. 中国科学院 理化技术研究所, 北京 100190;
4. 贵州师范学院 化学与生命科学学院, 贵州 贵阳 550018
2. College of Agriculture, Guizhou University, Guiyang 550025, Guizhou, P.R.China;
3. Technical Institute of Physics and Chemisry, Chinese Academy of Sciences, Beijing 100190, P.R.China;
4. School of Chemical and Biological Science, Guizhou Normal College, Guiyang 550018, Guizhou, P.R.China
阳离子表面活性剂常用作消毒剂、胶体稳定剂、织物柔软剂及矿物捕收剂等。它易吸附于固体表面,从而可以显著改变物体的表面性能。但是阳离子表面活性剂一般在自然界中不易生物降解,易造成环境污染。为了提高它的生物降解性,人们在表面活性剂的分子结构中常引入酯基、酰胺基团等官能团,生物降解性从而可以得到极大改善[1,2]。这些官能团对表面活性剂性能的影响成为目前关注的焦点。
Bordes等[3]研究了酰胺基团对羧酸盐型表面活性剂性质的作用,发现它对表面活性剂的疏水相互作用具有显著影响。他们还发现酰胺基团对双羧酸盐型表面活性剂的临界胶团浓度影响较小[4]。Stjerndahl等[5]发现酰胺基团能增强表面活性剂的水合作用。目前相关的报道主要集中于传统表面活性剂,这方面研究还有待进一步深化。
Gemini表面活性剂是一类具有两个亲水基、两条疏水长链及连接基团的新型表面活性剂。与传统表面活性剂相比,Gemini表面活性剂一般具有更高的表面活性[1]。本文合成了含有酰胺基团和不含酰胺基团的两类Gemini阳离子表面活性剂,利用荧光探针法等测定了它们的物化参数,探讨了酰胺基团对表面活性剂的性能和聚集行为的影响。
1 实验部分 1.1 试剂和仪器芘(Py)为Sigma公司产品,5-doxyl stearic acid (5-DSA)为Sigma公司产品,使用前未进一步提纯。二苯甲酮:分析纯,北京化学试剂公司,使用前用甲醇重结晶。所测样品均用二次蒸馏水配制。表面活性剂g1、g2、g3和g4为自制,它们的krafft 点都小于10 ℃。
表面张力测量仪,K100型,德国克吕士有限公司。荧光光谱仪,HITACHI F4500型,日本日立株式会社。
1.2 实验方法 1.2.1 表面活性剂的合成式1为两类Gemini阳离子表面活性剂的分子结构。表面活性剂g1和g2按文献[6, 7]合成,表面活性剂g3和g4按文献[8]合成。图 1(a、b、c、d)为表面活性剂的核磁图谱。
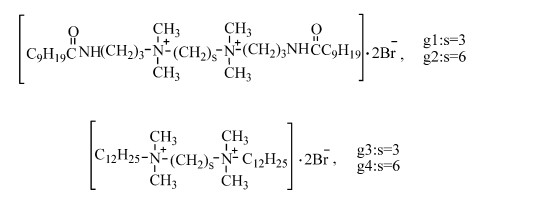 | 式1 两类Gemini表面活性剂的分子结构 Molecular structures of the Gemini surfactants |
 | 图1 (a) 表面活性剂g1核磁图,(b) 表面活性剂g2核磁图,(c) 表面活性剂g3核磁图,(d) 表面活性剂g4核磁图 1HNMR spectra of g1, g2, g3 and g4 |
表面活性剂的结构表征如下:
(1) 表面活性剂g1:1HNMR(D2O):0.65(m,6H,CH3),1.07(m,24H,CH3(CH2)6),1.40(m,4H,CH3(CH2)6CH2),1.86(m,4H,N+CH2CH2),2.11(m,4H,CH3(CH2)6CH2CH2),2.14(m,2H,N+CH2CH2CH2),3.03(s,12H,N+CH3),3.14(m,4H,CONHCH2),3.31(m,8H,N+CH2);
(2) 表面活性剂g2:1HNMR(D2O):0.75(m,6H,CH3),1.18(m,24H,CH3(CH2)6),1.35(m,4H,NHCH2CH2),1.48(m,4H,N+CH2CH2),1.67(m,4H,N+CH2CH2CH2),1.89(m,4H,CH3(CH2)6CH2),2.16(m,4H,CH3(CH2)6CH2-CH2),3.00(s,12H,N+CH3),3.14(m,4H,CONHCH2),3.23(m,8H,N+CH2);
(3) 表面活性剂g3:1HNMR(D2O):0.70(m,6H,CH3),1.12~1.30(m,36H,CH3(CH2)9),1.60(m,4H,CH3(CH2)9CH2),2.11(m,2H,N+CH2CH2),3.02(s,12H,N+CH3),3.32(m,8H,N+CH2);
(4) 表面活性剂g4:1HNMR(D2O):0.80(m,6H,CH3),1.15~1.21(m,36H,CH3(CH2)9),1.31(m,4H,CH3(CH2)9CH2),1.38(m,4H,N+CH2CH2CH2),1.66(m,4H,N+CH2CH2),3.05(s,12H,N+CH3),3.26(m,8H,N+CH2)。
1.2.2 物化参数的测定表面张力的测定:用二次蒸馏水分别配制一系列不同浓度的Gemini表面活性剂的水溶液,25 ℃下用Wilhelmy吊片法测定表面活性剂溶液的表面张力。
胶团聚集数的测定:在50 mL容量瓶中加入250 μL芘的甲醇溶液(5.00×10-6mol/L),用N2除去溶剂,加入10倍cmc的表面活性剂溶液50 mL,用超声波分散2 h。在另一系列5 mL容量瓶中准确移入不同体积二苯甲酮的甲醇溶液(1.00×10-3 mol/L),用N2除去溶剂,加入上述制配的芘的表面活性剂溶液5 mL,用超声波分散2 h。测定芘在λ=372 nm时的荧光强度I。激发波长335 nm,狭缝宽度:Ex:2.5 nm,Em:1.0 nm,激发电压:700 V。
荧光强度I与胶团聚集数Nagg有如下关系[1]:
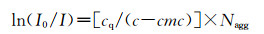
图 2为Gemini表面活性剂的表面张力曲线。
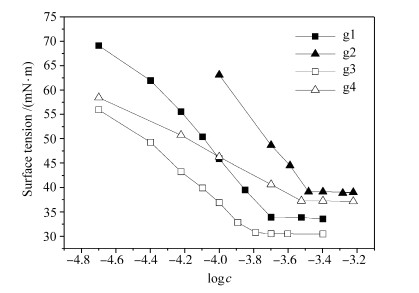 | 图2 Gemini表面活性剂的表面张力曲线(25 ℃) γ-logc curves of the Gemini surfactants(25 ℃) |
表 1为Gemini表面活性剂的表面活性数据。比较g1与g2、g3与g4,无论是否存在酰胺基团,连接基团从3个亚甲基增至6个亚甲基,Gemini表面活性剂的临界胶团浓度(cmc)都增大。当连接基团增长时,Gemini表面活性剂在溶液中自发聚集形成胶团的能力降低。因为连接基团增长(连接基团碳原子数≤6),疏水链的间距增大,表面活性剂的疏水相互作用减弱,所以表面活性剂的cmc增大。
| 表1 Gemini表面活性剂的表面活性数据(25 ℃) Surface activity of the Gemini surfactants (25 ℃) |
比较g1与g3,含酰胺基团的g1的cmc大于不含酰胺基团的g3的cmc。比较g2与g4也可得到相同结论,即酰胺基团提高了Gemini表面活性剂的临界胶团浓度。这类似于传统非离子表面活性剂中酰胺基团的作用[9]。Paulo等人[10]利用核磁共振的方法,发现传统季铵盐性阳离子表面活性剂的酰胺基因不位于胶团内部,而位于胶团与溶液的界面。因此只有羰基外侧的疏水链参与胶团的形成,含酰胺基团的Gemini表面活性剂只能在更高的表面活性剂浓度时形成胶团,所以cmc较大。
2.2 饱和吸附量和最小分子横截面积比较g1与g2,连接基团从3个亚甲基增至6个亚甲基,含酰胺基团的Gemini表面活性剂的饱和吸附量(Гmax)略有增大,这可能是由于较长的连接基团更有利于分子间氢键的形成。比较不含酰胺基团的g3与g4,连接基团从3个亚甲基增至6个亚甲基,Gemini表面活性剂的饱和吸附量(Гmax)降低,这是由于疏水链间疏水相互作用减弱的结果。
从表 1还可知,将酰胺基团引入表面活性剂后,g1的饱和吸附量(Гmax)明显大于g3的Гmax,g1的最小分子横截面积(Amin)则比g3的更小。比较g2与g4,也可得到相同结论,即酰胺基团提高了Gemini阳离子表面活性剂在溶液表面的饱和吸附量,降低了最小分子横截面积。Ge A等人[11]利用频振动光谱证实了季铵盐型阳离子表面活性剂疏水链上的酰胺基团可以形成分子间氢键。因此,g1疏水链上酰胺基团的羰基与H—N易形成分子间氢键,利于Gemini阳离子表面活性剂在溶液表面的吸附,因此Гmax增大,Amin减少。而g3的疏水链上无酰胺基团,不能形成氢键。因此与g3相比,g1的Гmax更大,Amin更小。
图 3为这两类表面活性剂在溶液表面饱和吸附的情况。
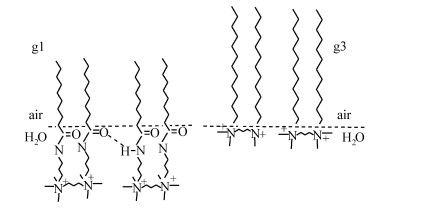 | 图3 Gemini表面活性剂(g1、g3)在溶液表面的吸附情况 Absorption of the Gemini surfactants at the surface of the solution (g1, g3) |
图 4示出芘的荧光强度与不同猝灭剂溶液体积(Vq)的关系图。
 | 图4 在Gemini表面活性剂g2溶液中芘的荧光光谱 VPy: (1) 0 μL, (2) 50 μL, (3) 100 μL, (4) 150 μL, (5) 200 μL, (6) 250 μL Fluorescence spectra of Py in the solutions of g2 |
图 5示出芘的lnI0/I与不同猝灭剂浓度(cq)的关系。从图 5可知,芘的lnI0/I值与cq成正比。计算各表面活性剂的胶团聚集数(Nagg),如表 2所示。从表 2可知,引入酰胺基团后,Gemini阳离子表面活性剂的Nagg明显减小,即酰胺基团降低了Gemini阳离子表面活性剂的胶团聚集数。文献[1]报道了传统季铵盐型阳离子表面活性剂(疏水基有12个碳原子)的聚集数Nagg为50,而Paulo等[10]测定了引入酰胺基团后对应的表面活性剂Nagg为43,聚集数降低。因此对这几类表面活性剂而言,酰胺基团都降低了胶团聚集数。
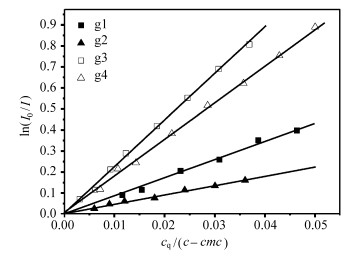 | 图5 ln(I0/I)值与猝灭剂浓度的关系(25 ℃) ln(I0/I) value vs quencher concentration(25 ℃) |
芘的荧光光谱具有特征的五峰结构,第1峰(λ=372 nm)与第3峰(λ=385 nm)的荧光强度的比值取决于所处胶团微环境的极性[12]。表 2示出了两种表面活性剂在10倍cmc时芘的I1/I3值。从表 2可知,当存在酰胺基团时,芘的I1/I3值增大,胶团微极性增加,表面活性剂分子在胶团中排列较为疏松。
| 表2 Gemini表面活性剂的胶团聚集数和I1/I3(25 ℃) Nagg and I1/I3 of the Gemini surfactants(25 ℃) |
酰胺基团对Gemini阳离子表面活性剂的表面活性和聚集行为都具有重要影响。当分子中引入酰胺基团后,Gemini阳离子表面活性剂的临界胶团浓度增加,饱和吸附量增大,胶团聚集数减少,胶团的微极性增强。
| [1] | Zana R.Surfactant Solutions: New Methods of Investigation[M].New York: Marcel Dekker, Inc., 1987. |
| [2] | Ghosh S, Dey J. Binding of fatty acid amide amphiphiles to bovine serum albumin: role of amide hydrogen bonding[J]. Journal of Physical Chemistry B, 2015, 119(5):7804-7815. |
| [2] | Fan Y, Hou Y, Xiang J Y, Yu D F, Wu CY, Tian M Z. Synthesis and aggregation behavior of a hexameric quaternary ammonium surfactant[J]. Langmuir, 2011, 27:10570-10579. |
| [3] | Bordes R, Holmberg K. Amino acid-based surfactants-do they deserve more attention[J]. Advances in Colloid and Interface Science, 2015, 222: 79-91. |
| [4] | Bordes R, Holmberg K. Physical chemical characteristics of dicarboxylic amino acid-based surfactants[J]. Colloids and Surfaces A, 2011, 391: 32-41. |
| [5] | Stjerndahl M, Lundberg D, Zhang H, Menger F M. NMR Studies of aggregation and hydration of surfactants containing amide bonds[J]. Journal of Physical Chemistry B, 2007, 111:2008-2014. |
| [6] | 姜小明, 宋磊, 赵濉.新型易降解的季铵盐型Gemini表面活性剂的合成[J]. 合成化学, 2012, 20(1): 49-51. Jiang X M, Song L, Zhao S. Synthesis of Gemini cationic surfactants easily degraded[J]. Chinese Journal of Synthetic Chemistry, 2012, 20(1): 49-51. |
| [7] | 旷爱忠,陈晓阁,姜小明.荧光探针法研究新型Gemini表面活性剂在水溶液中的聚集行为[J].影像科学与光化学,2010, 28(6): 425-432. Kuang A Z , Chen X G, Jiang X M. Study of aggregation properties of anionic Gemini surfactants in aqueous solution by fluorescence method[J]. Imaging Science and Photochemistry, 2010, 28(6): 425-432. |
| [8] | Wang G T, Kang Y T, Tang B, Zhang X. Tuning the surface activity of Gemini amphiphile by the host-guest interaction of cucurbit[7] uril[J]. Langmuir, 2015, 31: 120-124. |
| [9] | Mikael U R, Claesson P M, Linse P. Surface properties of tetra(ethylene oxide) dodecyl amide compared with poly(ethylene oxide) surfactants.1.Effect of the headgroup on adsorption[J]. Langmuir, 2002, 18:6745-6753. |
| [10] | Paulo A R, Pires O A. Surfactants with an amide group "spacer": synthesis of 3-(acylaminopropyl)trimethylammonium chlorides and their aggregation in aqueous solutions[J]. Journal of Colloid and Interface Science, 2006, 304: 474-85. |
| [11] | Ge A, Peng Q L, Wu H L, Liu H J, Tong Y J, Nishida T, Yoshida N, Suzuki K, Sakai T, Osawa M, Ye S. Effect of functional group on the monolayer structures of biodegradable quaternary ammonium surfactants[J]. Langmuir, 2013, 29: 14411-14420. |
| [12] | Zhang Y L, Romsted L S. Simultaneous determination of interfacial molarities of amide bonds, carboxylate groups, and water by chemical trapping in micelles of amphiphiles containing peptide bond models[J]. Langmuir, 2013, 29:534-544. |




