2. 复旦大学 化学系, 上海 200433
2. Department of Chemistry, Fudan University, Shanghai 200433, P. R. China
次氯酸 (HClO) 是一种弱酸性的活性氧化物,在生理pH条件下可解离为次氯酸根 (ClO-)[1]。作为强氧化剂,HClO和ClO-被广泛应用于漂白纸浆和纺织物、饮用水的消毒和净化等工作。但是,它会破坏细胞膜表面的蛋白质分子,对人体造成一定损害[2]。通常它的工作浓度为10-5~10-2 mol/L[3]。因此,研究日常生活中HClO浓度的便捷监测方法具有重要意义。
可用于HClO检测的方法有碘量滴定法、库仑法、极谱法和辐解法等,但这些方法都依赖于仪器测量[4-6],可视化检测由于不需要检测仪器辅助,更容易推广到日常生活中应用[7, 8]。相比于荧光方法,色度法是最直观的可视化检测方法[9]。近年来,陆续有不少HClO色度探针的报道,选用的体系有BODIPY、罗丹明、荧光素、花菁、对甲氧基苯酚、香豆素和金属配合物等[9-14],但这些次氯酸探针大部分水溶性较差,需要有机溶剂助溶,并且容易被光漂白,因而使其应用受到了限制。
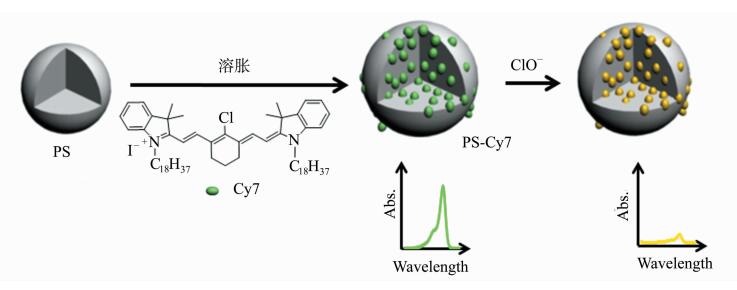
为解决有机染料类探针的水溶性差和易被光漂白的问题,本论文发展了一类通用策略 (见图 1),以水溶性聚苯乙烯微球 (PS) 为载体,负载有机染料为响应探针,构建水溶、光稳定的色度纳米探针。选择花菁染料 (Cy7) 为ClO-响应基团,设计合成了Cy7花菁染料负载的PS球纳米探针PS-Cy7。所合成的纳米探针对次氯酸具有专一的选择性响应,而不受其它活性氧物种的干扰。而且,该策略还改善了花菁染料的水溶性和光稳定性。
|
图 1 有机染料负载PS球的合成过程和与ClO-反应前后的光谱变化示意图 Fig.1 Schematic illustration of synthetic route and absorption change in dye-loading polystyrene interacted with ClO- |
乙酸钠、乙酸酐、无水乙醇、乙二醇等均为国产分析纯或化学纯试剂,未加说明均为未经过任何处理直接应用;NaClO、叔丁基过氧化氢 (tBHP)、2, 2′-偶氮 (2-脒基丙烷) 二氯化氢盐酸盐 (ROO)、KO2购自Sigma-Aldrich公司;OtBu由高氯酸亚铁水溶液和tBHP混合稀释制得;HO·由Fe2+和H2O2混合稀释制得;(2-氯-3-羟基)-环己烯-1-甲醛 (化合物1) 参考文献方法[14]合成;2, 3, 3-三甲基-1-十八基吲哚 (化合物2) 参考文献方法[15]合成,单分散聚苯乙烯 (PS) 纳米粒子参考文献方法[16],通过乳液聚合法合成;实验用水均为去离子水。
聚苯乙烯纳米粒子 (PS) 和纳米探针PS-Cy7的形貌和尺寸通过场发射扫描电子显微镜 (FESEM)(FEI, 5 kV,Ultra 55) 观察;紫外-可见吸收光谱在Shimadzu 2550型吸收光谱仪器上测得,扫描范围为400~900 nm;动态光散射 (DLS) 测量在马尔文Zetasizer Nano ZS90上进行。1HNMR谱测量在Bruker Mercuryplus 400 MHz核磁共振谱仪上完成,用TMS为内标。
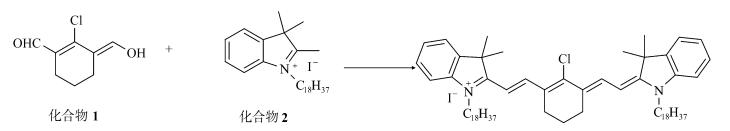
1.2 有机染料Cy7的合成有机染料Cy7参考文献[14]中方法合成,但以长碳链的2, 3, 3-三甲基-1-十八基吲哚 (化合物2为原料,其合成路线如图 2所示。将 (2-氯-3-羟基)-环己烯-1-甲醛 (化合物1,924 mg,1.714 mmol)、2, 3, 3-三甲基-1-十八基吲哚 (化合物2,147.4 mg,0.857 mmol)、乙酸钠 (210 mg,2.571 mmol) 和10 mL的乙酸酐加入50 mL反应瓶中,60 ℃反应4 h,析出大量沉淀,过滤并用甲醇重结晶,得到化合物Cy7,产率53%。
|
图 2 染料Cy7的合成路线 Fig.2 Synthetic route of the dye Cy7 |
1HNMR (400 MHz, CDCl3):8.37(d, J=10.8 Hz, 2H),7.42(m, 4H),7.27(d, J= 6.0 Hz, 2H),7.19(d, J= 6.0 Hz, 2H),6.28(d, J=10.5 Hz, 2H),4.24(t, J= 5.4 Hz, 4H),2.78(t, J= 4.5 Hz, 4H),1.89(m, 4H),1.74(s, 12H),1.62(m, 2H),1.48(m, 4H),1.40(m, 4H),1.27(m, 52H),0.91(t, J=5.1 Hz, 6H)。
1.3 纳米探针PS-Cy7的合成将2.2 mg花菁染料Cy7和50 mg聚苯乙烯纳米球分散在4 mL水和丙二醇的混合液 (V/V =1/3) 中,在室温下用摇床摇晃4 h,然后用透析方法除去混合溶液里的有机溶剂和部分未被包裹的染料分子,得到蓝色的负载Cy7的聚苯乙烯纳米探针。
1.4 Cy7和PS-Cy7的次氯酸滴定以及活性氧滴定Cy7和PS-Cy7的次氯酸滴定以及其它活性氧物质 (H2O2、NO、O2-、ROO、OtBu、tBHP和HO·) 滴定实验在1 cm × 1 cm石英比色皿中完成。PS-Cy7水溶液的浓度为20 μmol/L。次氯酸的滴定实验:每隔5 min向PS-Cy7水溶液 (或Cy7丙酮溶液) 滴加5 μmol/L NaClO溶液,充分反应测定样品的吸光度值。为了考察PS-Cy7的选择性,在相同条件下,向PS-Cy7水溶液 (或Cy7丙酮溶液) 中分别滴加浓度为62.5 μmol/L的不同活性氧物种 (ROS),测试其吸收光谱的变化。各种ROS均现用现配置。
1.5 光稳定性测试将浓度为30 μmol/L的PS-Cy7水溶液置于比色皿中,密封。用功率密度为100 mW/cm2的760 nm激光器照射样品,每隔5 min在紫外可见分光光度仪上测定样品的吸光度值,根据吸光度值随光照时间的变化来评估样品的光稳定性。染料Cy7用丙酮和水 (V/V=9/1) 配成相同浓度在同样光照条件下考察其光稳定性。
2 结果与讨论 2.1 PS-Cy7纳米探针的合成与表征本文采用溶胀法使聚苯乙烯聚合物纳米球在有机溶剂中溶胀,从而物理吸附长链花菁染料Cy7,实现有机染料的负载。图 3a和3b分别给出了PS纳米粒子和PS-Cy7纳米探针的场发射扫描电子显微镜 (FESEM) 图。从图 3可知,相比于纯PS球而言,负载Cy染料后粒子的形貌依然规整,分布均一。高分辨FESEM图片 (图 3b插图) 显示PS-Cy7纳米探针的表面依然是光滑,呈现出大小均一。但PS-Cy7的粒径与PS纳米粒子球的粒径略微增大。动态光散射测试数据显示:PS和PS-Cy7纳米粒子的水合粒径分别为75 nm和78 nm,分散系数 (PDI) 分别为0.007和0.012,表明PS和PS-Cy7纳米粒子都有良好的单分散性。

|
图 3 聚苯乙烯 (PS) 纳米粒子 (a) 和PS-Cy7纳米探针 (b) 的FESEM图,插图为PS-Cy7的高分辨FESEM图 Fig.3 FESEM images of PS nanosphere (a) and PS-Cy7 nanoprobe (b), inset: High FESEM image of PS-Cy7 |
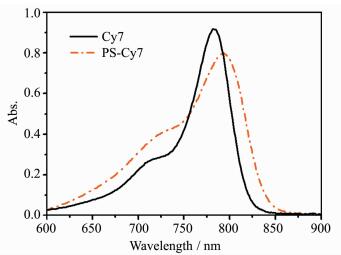
考察了PS-Cy7的光物理性质。图 4是PS-Cy7水分散液稀释50倍后的吸收光谱。与染料Cy7的吸收光谱相比,PS-Cy7纳米粒子的吸收带明显展宽,中心吸收波长位于793 nm,比Cy7染料的吸收峰红移了28 nm,表明Cy7染料成功地负载到PS纳米粒子中,而且Cy7染料分子发生了明显的聚集且存在J-聚集体[16]。通过与不同浓度的Cy7丙酮溶液的吸光度值相比较,计算出PS纳米粒子中负载Cy染料的浓度是27 μmol/L,表明Cy7是一种优良的负载染料。
|
图 4 染料Cy7丙酮溶液和PS-Cy7水溶液的吸收光谱图 Fig.4 Absorption spectra of Cy7 in acetone solution and PS-Cy7 nanoprobe dispersed in water |
运用紫外-可见吸收光谱研究PS-Cy7纳米探针中Cy7染料的泄漏行为。分散在水中的PS-Cy7纳米探针储存1个月后,离心分离所得的上清液在793 nm处的吸光度值低于仪器的检查限,表明Cy7染料没有从PS纳米粒子中泄漏出来,即PS-Cy7探针具有非常低的染料泄漏率。
2.2 PS-Cy7纳米探针的光稳定性花菁类染料特别是大共轭体系Cy7的光稳定性差是制约其广泛应用的重要因素,因此,改善Cy7染料的光稳定性具有十分重要的现实意义。图 5给出了含相同浓度Cy7(30 μmol/L) 的PS-Cy7水溶液和Cy7丙酮溶液的光漂白实验结果。如图所示,在功率密度为100 mW/cm2的760 nm激光持续照射下,丙酮溶液中46%染料Cy7被光漂白了,而在相同的光照条件下,PS负载体系的吸光度只下降了8%,表明PS-Cy7纳米粒子中Cy7的光稳定性得到了明显的改善,这是因为Cy7染料处于PS球内部,被聚苯乙烯长链缠绕保护,有效地避免了光氧化反应的发生。

|
图 5 经功率密度为100 mW/cm2的760 nm激光照射1 h的PS-Cy7水溶液 (30 μmol/L) 和Cy7丙酮溶液 (30 μmol/L) 的吸光度变化 Fig.5 Change in absorbance of PS-Cy7 in water (30 μmol/L) and Cy7 in acetone solution (30 μmol/L) under irradiation with 760 nm laser (power density of 100 mW/cm2) for 1 hour |
通过紫外-可见吸收光谱方法考察了PS-Cy7纳米粒子对ClO-的响应行为。如图 6所示,随着NaClO的加入,PS-Cy7在600~850 nm范围吸光度逐渐下降,下降趋势先快后慢,并伴随着其溶液颜色逐渐褪色,表明PS-Cy7纳米粒子中Cy7染料与NaClO之间发生了反应。由于ClO-有较强的氧化能力,当加入的ClO-通过渗透作用进入PS球后,与染料Cy7反应,破坏Cy7染料的共轭结构,导致染料在793 nm处的吸收峰下降。最低检出限可用吸收光谱滴定实验数据,按照3σ/k计算得到,在本实验条件下对HClO的检测限为0.22 μmol/L,表明PS-Cy7对HClO检测具有较高的灵敏度。

|
图 6 PS-Cy7水溶液 (20 μmol/L) 与不同浓度 (0~60 μmol/L) ClO-反应后的吸收光谱变化,插图:PS-Cy7水溶液加入ClO-前后的颜色变化 Fig.6 Change in absorption spectra of PS-Cy7 nanoprobe in water (20 μmol/L) under addition of ClO- with different concentration (0-60 μmol/L), inset: photographs of PS-Cy7 dispersed in water in the absence and presence of ClO- |
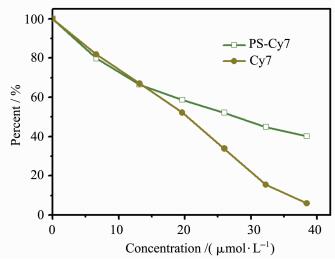
此外,比较了PS-Cy7纳米探针和染料Cy7与ClO-的响应速度。从图 7可知,染料Cy7与不同浓度ClO-(0~38 μmol/L) 的响应速度几乎不变,但加入不同浓度ClO-后的PS-Cy7纳米探针的吸光度下降速度是先快后慢。当加入的ClO-处于较低浓度 (13 μmol/L) 时,PS-Cy7的吸光度下降速度与Cy7没有差别,但当加入的ClO-再增加后,PS-Cy7的吸光度下降速度比Cy7慢,表明PS-Cy7对ClO-响应速度随加入的ClO-浓度不同而不同。由此可以推测:由于PS的包覆作用,加入的ClO-优先接触PS纳米粒子外层的Cy7染料,当外层Cy7染料与ClO-反应后,内层的Cy7才与陆续扩散进入的ClO-反应,导致高浓度ClO-反应速度下降。
|
图 7 PS-Cy7水溶液和Cy7染料与不同浓度ClO-应后的吸收度的变化 Fig.7 Change in absorbance of Cy7 and PS-Cy7 under addition of different concentrations of ClO- |
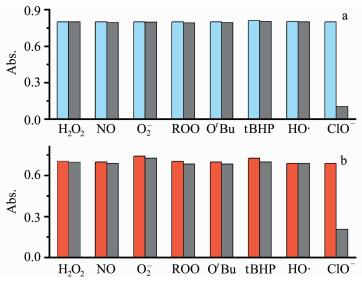
性能优异的探针分子应该只与被检测物有良好的响应,而其它具有相似性质的物种对其检测不造成干扰。为评估Cy7对ClO-选择响应能力,首先研究了Cy7染料对其它各类活性氧物质ROS (H2O2、NO、O2-、ROO、OtBu、tBHP、HO·) 的响应行为。如图 8a所示,在相同条件下, 添加其它过量的ROS (浓度均为60 μmol/L) 后基本不影响染料Cy7的吸收光谱。对比之下,在NaClO存在下,Cy7在765 nm处的吸收度急剧下降。研究表明:Cy7对ClO-响应具有良好的选择性。进一步考察了PS-Cy7纳米探针对ClO-响应的选择性。在相同条件下,向PS-Cy7水溶液 (20 μmol/L) 中分别滴加浓度为3当量 (60 μmol/L) 的不同反应性活性氧物质,测试紫外-可见吸收光谱的变化。如图 8所示,探针PS/ Cy7对次氯酸的响应较好,而其它的活性氧 (H2O2、NO、O2-、ROO、OtBu、tBHP、HO·) 对次氯酸的检测不造成干扰。因此,纳米探针PS-Cy7对次氯酸具有优异的选择性响应。
|
图 8 浓度为20 μmol/L的染料Cy溶液 (a, λabs=765 nm) 和PS-Cy7溶液 (b, λabs=793 nm) 加入60 μmol/L不同活性氧物质 (H2O2、NO、O2-、ROO、OtBu、tBHP、HO·、ClO-) 前后的吸光度值变化 Fig.8 Change in absorbance of Cy7 solution (a, λabs=765 nm) and PS-Cy7 solution (b, λabs=793 nm) in the presence of ClO- and other ROS (H2O2, NO, O2-, ROO, OtBu, tBHP, HO·) with the concentration of 60 μmol/L |
本文发展了一种新的色度探针制备策略,即通过溶胀分散法将花菁染料Cy7载入到聚苯乙烯纳米球,制备出对次氯酸具有选择性响应的色度纳米探针PS-Cy7。相比于染料Cy7,PS-Cy7的光稳定性和水溶性均有明显改善,且只对次氯酸选择性响应,最低检测限为0.22 μmol/L。综上所述,所制备的色度探针PS-Cy7对次氯酸根的检测具有简单、快速和高灵敏度等特点,在次氯酸根检测应用中具有重要的潜在应用价值。
致谢 感谢国家自然科学基金委 (21231004和21375024) 的资助| [1] | Chapman A L P, Hampton M B, Senthilmohan R, Winterbourn C C, Kettle A J. Chlorination of bacterial and neutrophil proteins during phagocytosis and killing of staphylococcus aureus[J]. Journal of Biological Chemistry, 2002, 277(12): 9757–9762. DOI:10.1074/jbc.M106134200 |
| [2] | Adam L C, Gordon G. Direct and sequential potentiometric determination of hypochlorite chlorite, and chlorate ions when hypochlorite ion is present in large excess[J]. Analy-tical Chemistry, 1995, 67: 535–540. DOI:10.1021/ac00099a009 |
| [3] | Aoki T, Munemori M. Continucus flow determination of free chlorine in water[J]. Analytical Chemistry, 1983, 55: 209–212. DOI:10.1021/ac00253a010 |
| [4] | Ballesta-Claver J, Valencia-Mirón M C, Capitán-Vallvey L F. Determination of hypochlorite in water using a chemiluminescent test strip[J]. Analytica Chimica Acta, 2004, 522: 267–273. DOI:10.1016/j.aca.2004.06.051 |
| [5] | Soldatkin A P, Gorchkov D V, Martelet C, Jaffrezic-Renault N. New enzyme potentiometric sensor for hypochlorite species detection[J]. Sensor Actuators B, 1997, 43: 99–104. DOI:10.1016/S0925-4005(97)00144-5 |
| [6] | Watanabe T, Idehara T, Yoshimura Y, Nakazawa H. Simultaneous determination of chlorine dioxide and hypochlorite in water by high-performance liquid chromatography[J]. Journal of Chromatography A, 1998, 796: 397–400. DOI:10.1016/S0021-9673(97)01009-1 |
| [7] | Lou B, Chen Z Q, Bian Z Q, Huang C H. Multisignaling detection of cyanide anions based on an Iridium (Ⅲ) complex: remarkable enhancement of sensitivity by coordination effect[J]. New Journal of Chemistry, 2010, 34: 132–136. DOI:10.1039/B9NJ00442D |
| [8] | Tang Y, Yang H R, Sun H B, Liu S J, Wang J X, Zhao Q, Liu X M, Xu W J, Li S B, Huang W. Rational design of an "OFF-ON" phosphorescent chemodosimeter based on an Iridium (Ⅲ) complex and its application for time-resolved luminescent detection and bioimaging of cysteine and homocysteine[J]. Chemistry-A European Journal, 2013, 19: 1311–1319. DOI:10.1002/chem.201203137 |
| [9] | Yang Y M, Zhao Q, Feng W, Li F Y. Luminescent chemodosimeters for bioimaging[J]. Chemical Reviews, 2013, 113: 192–270. DOI:10.1021/cr2004103 |
| [10] | Chen X Q, Wang F, Hyun J Y, Wei T W, Qiang J, Ren X T, Shin I, Yoon J Y. Recent progress in the development of fluorescent, luminescent and colorimetric probes for detection of reactive oxygen and nitrogen species[J]. Chemical Society Reviews, 2016, 45: 2976–3016. DOI:10.1039/C6CS00192K |
| [11] | Yue Y K, Huo F J, Yin C X, Escobedoc J O, Strongin R M. Recent progress in chromogenic and fluorogenic chemosensors for hypochlorous acid[J]. Analyst, 2016, 141: 1859–1873. DOI:10.1039/C6AN00158K |
| [12] | Zhao C C, An J C, Zhou L, Fei Q, Wang F Y, Tan J, Shi B, Wang R, Guo Z Q, Zhu W H. Transforming the recognition site of 4-hydroxyaniline into 4-methoxyaniline grafted onto a BODIPY core switches the selective detection of peroxynitrite to hypochlorous acid[J]. Chemical Communications, 2016, 52: 2075–2078. DOI:10.1039/C5CC08936K |
| [13] | Cui K, Zhang D, Zhang G, Zhu D. A highly selective naked-eye probe for hypochlorite with the p-methoxyphenol-substituted aniline compound[J]. Tetrahedron Letters, 2010, 51(46): 6052–6055. DOI:10.1016/j.tetlet.2010.09.041 |
| [14] | Li Y H, Sun Y, Li J C, Su Q Q, Yuan W, Dai Y, Han C M, Wang Q H, Feng W, Li F Y. Ultrasensitive near-infrared fluorescence-enhanced probe for in vivo nitrore-ductase imaging[J]. Journal of the American Chemical Society, 2015, 137: 6407–6416. DOI:10.1021/jacs.5b04097 |
| [15] | Matsui M, Yamamoto T, Kubota Y, Funabiki K. Survey, fluorescence spectra, and solubility of liquid cyanine dyes[J]. New Journal of Chemistry, 2016, 40: 10187–10196. DOI:10.1039/C6NJ02160C |
| [16] | Mooney W F, Brown P E, Russell J C, Costa S B, Pedersen L G, Whitten D G. Photochemistry and photophysics of surfactant trans-stilbenes in supported multilayers and films at the air-water interface[J]. Journal of the American Chemical Society, 1984, 106(19): 5659–5667. DOI:10.1021/ja00331a041 |
| [17] | Yang L, Ke Y. Synthesis of polystyrene nanolatexes via emulsion polymerization using sodium dodecyl sulfonate as the emulsifier[J]. High Performance Polymers, 2014, 26(8): 900–905. DOI:10.1177/0954008314533979 |




