2. 南洋模范中学, 上海 200032
2. Nanyang Model School, Shanghai 200032, P.R. China
随着食品科技日新月异的发展和变化,人们在享受更多美食的同时,相伴着对食品安全问题的焦虑和担忧。糖精钠是食品工业中常用的合成甜味剂,具有潜在的致癌性,过量食用会对肝脏和神经系统造成危害。最新版的国家标准《食品添加剂使用标准》(GB2760-2014) 于2015年5月24日实施[1],对食品添加剂糖精钠的使用有严格的限制标准。因此,快速准确地检测食品中是否含有过量的糖精钠,对维护食品安全和人们的身心健康有重要意义。
荧光分子探针分析法因其具有灵敏度高、选择性强、取样量少和操作简便等优点,在环境化学、生命科学以及药物分析测定方面得到了广泛的应用[2]。荧光分子探针检测是利用探针分子与底物作用后荧光光谱改变,实现对底物的检测[3],涉及的识别机理主要包括光诱导电子转移 (PET)[4]、分子内电荷转移 (ICT)[5]、荧光共振能量转移 (FRET)[6]、聚集诱导发光 (AIE)[7]等。常见的荧光染料主要有罗丹明类荧光染料[8]、氟硼吡咯 (BODIPY) 类荧光染料[9]、香豆素类荧光染料[10]。此外,冠醚和金属阳离子的相互作用也广泛应用于荧光分子探针的开发,其识别基础是分子识别、大环效应和协同作用,这些基本概念是现代超分子化学研究和发展的基础。近年来,超分子化学作为一门新兴的学科发展迅速,尤其在2016年,诺贝尔化学奖授予了化学家Jean-Pierre Sauvage、J.Fraser Stoddart和Bernard L.Feringa,以表彰他们在发明行动可控、给予能源后可执行任务的分子机器方面做出的卓越贡献。这是超分子化学领域获得1987年诺贝尔化学奖之后再次获得世界最高奖项,这项荣誉对于超分子化学这个前景无限的新兴领域,无疑是最好的鼓励,同时也把超分子化学这门学科带入了一个全新的发展高度,应用前景广阔[11]。
超分子化学研究的对象是多个物种以非共价键弱相互作用 (如范德华力、疏水相互作用和氢键)[12]形成的复杂有序且具有特定功能的分子聚集体。冠醚作为第一代主体化合物,由于其螯合和大环效应,对于金属和有机阳离子以及中性分子有很好的选择性络合作用[13],而氮杂冠醚作为冠醚化学中一个重要分支,由于氮原子相对的软碱性质,使其与金属离子的配位能力和选择性更强[14]。
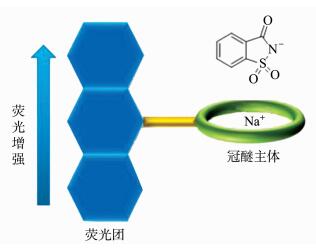
随着时代的发展,食品检测、环境化学和临床检验诊断面临的挑战层出不穷,需要我们与时俱进地开发新的方法来应对这些挑战,而荧光探针分子的高灵敏度成为传统检测手段的一种很好的补充。基于冠醚与金属阳离子的相互作用在荧光分子探针方面的广泛应用,本文设计并合成了一种含蒽荧光团的氮杂15-冠-5化合物R,利用分子识别的原理,15-冠-5作为功能性基团能够特异性识别溶液中的糖精钠,通过糖精钠和氮杂15-冠-5的相互作用使蒽荧光团荧光强度显著增强,溶液的荧光强度发生可视变化 (二者的作用示意图如图 1所示),进而检测出食品中是否含有糖精钠,这为检测食品中的糖精钠提供了一种简便可行的手段。
|
图 1 探针分子与糖精钠的作用示意图 Fig.1 Schematic representation of the interaction between fluorescence molecular probe and saccharin sodium |
核磁共振氢谱由Bruker-400核磁共振仪测定 (内标:TMS,溶剂:CDCl3);高分辨质谱由LCT Premier XE测定;紫外-可见光谱由Varian Cary-100型分光光度计测定;荧光光谱由Varian Cary Eclipse荧光光谱仪测定。
9-蒽醇和糖精钠购于上海泰坦科技股份有限公司;氮杂-15-冠醚-5购于梯希爱 (上海) 化成工业发展有限公司;三溴化磷购于上海阿拉丁生化科技股份有限公司;甲苯、乙腈、碳酸钠、氯化钠、碳酸氢钠、硫酸钠均由上海凌峰化学试剂有限公司提供;实验中所用试剂除特别说明外均为分析纯。
1.2 氮杂15-冠-5化合物R的合成合成路线见图 2。

|
图 2 目标化合物的合成路线 Fig.2 The synthetic route of target compound |
9-蒽醇 (100 mg,0.48 mmol) 置于25 mL Schlenk反应管中,向其中注入4 mL的无水甲苯,抽氩气保护,冰浴条件下搅拌,用注射器向反应管中注入1.0 mL溶有PBr3 (0.26 g, 0.96 mmol) 的甲苯溶液,冰浴条件下反应1 h,然后撤去冰浴,常温搅拌反应过夜。混合物中加入5.0 mL饱和Na2CO3溶液猝灭反应,去离子水洗涤,用CH2Cl2萃取,合并有机层,有机层用无水硫酸钠干燥,抽滤,有机相真空旋干,得到黄色固体135 mg (不提纯直接下一步)。
将得到的黄色固体135 mg、氮杂-15-冠醚-5(109 mg,0.50 mmol) 和K2CO3 (137 mg, 1.0 mmol) 溶于10 mL的无水乙腈中,氩气保护,加热条件下回流过夜,混合物用去离子水洗涤,CH2Cl2萃取,有机层用无水硫酸钠干燥,抽滤,有机相真空旋干,固体混合物柱层析提纯 (CH2Cl2/MeOH=100/1) 得到黄色固体产物R150 mg, 产率76.3 %。
1HNMR (400 MHz, CDCl3): 8.54 (d, J=8.8 Hz, 2H), 8.40(s, 1H), 7.98(d, J=8.4 Hz, 2H), 7.51(t, J=8.4 Hz, 2H), 7.45 (t, J=7.6 Hz, 2H), 4.62(s, 2H), 3.68~3.56(m, 16H), 3.03~2.80(m, 4H)。HRMS (ESI) (m/z): [M+H]+理论值C25H32NO4, 410.2326,实测值410.2333。
1.3 光谱测定配制一定浓度 (1.0×10-5 mol/L) 探针分子的乙腈溶液,分别加入不同量的糖精钠的水溶液,分别测定其吸收和荧光光谱变化。为证明合成的探针分子只对糖精钠具有特异性识别作用,分别向其中加入10当量的NaCl、Na2CO3、NaHCO3、Na2SO4和糖精钠水溶液,测试其荧光光谱变化。
1.4 Job’s plot的测定将探针分子和糖精钠的总浓度保持为1.0×10-5 mol/L,连续变化糖精钠的含量,荧光强度随着探针分子与糖精钠的摩尔比变化而发生变化,以摩尔比为横坐标,荧光强度为纵坐标,荧光强度最大的点所对应的横坐标的值即为探针分子与糖精钠的络合比例。
2 结果与讨论 2.1 探针分子的合成PBr3极易水解,为了保证反应的顺利进行,必须在无水无氧的条件下进行反应,得到的苄溴中间体化合物不稳定,直接用于下一步的反应,最后得到的混合物直接使用柱层析色谱法提纯。通过1HNMR和高分辨质谱HRMS (ESI) 对目标化合物进行表征,结果分析如下:δ位于8.59~7.40的峰是蒽荧光团上的H,4.62处的峰是蒽荧光团和氮杂-15-冠-5之间亚甲基上的H,3.68~2.80的峰是氮杂-15-冠-5上的H,三处的峰面积积分比正好是9:2:20,与目标分子三个位置的H数目相符合。目标化合物高分辨质谱的实测值为[M+H]+: 410.2333,与精确分子量理论值[M+H]+:410.2326相吻合,证明得到的目标化合物是正确的。
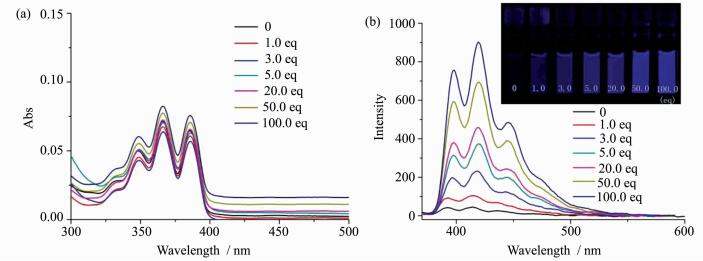
2.2 探针分子的光学性能从图 3a可以看出,随着糖精钠量的增加,探针分子溶液吸收光谱基本没有变化,但其荧光强度逐渐增加 (图 3b),这说明糖精钠和探针分子的共同作用对其吸收光谱没有影响,但会导致其荧光强度增加。其机理可以解释为:目标分子为典型的Photoinduced Electron Transfer (PET) 型荧光探针,体系中氮杂冠醚为电子供体 (donor),蒽荧光团为电子受体 (acceptor)。初始状态,由于电子供体和电子受体之间存在较强的PET过程,此时分子荧光处于“OFF”状态。当加入金属阳离子溶液后,氮杂冠醚与金属离子络合,导致氮原子的孤电子对与金属离子结合降低了它的供电子能力,此时探针分子的荧光处于“ON”状态,随着阳离子浓度的增加,氮杂冠醚与金属阳离子结合数目增加,导致氮杂冠醚与蒽荧光团之间的PET过程越来越弱,体系的荧光强度逐渐加强,当阳离子数目增加到一定浓度时,溶液的荧光强度不再增加,达到荧光饱和状态。这种荧光变化能够肉眼识别,并且能够检出微量的糖精钠,说明探针分子能够用于检测食品中微量糖精钠的存在,具有现实可行性。
|
图 3 不同量的糖精钠在乙腈中对探针分子 (1.0×10-5 mol/L) 吸收 (a) 和荧光 (b) 光谱影响,激发波长348 nm Fig.3 Absorption spectra (a) and fluorescence spectra (b) of probe molecular (1.0×10-5 mol/L) responding to different equivlent saccharin sodium salt in CH3CN, the excitation wavelength was 348 nm |
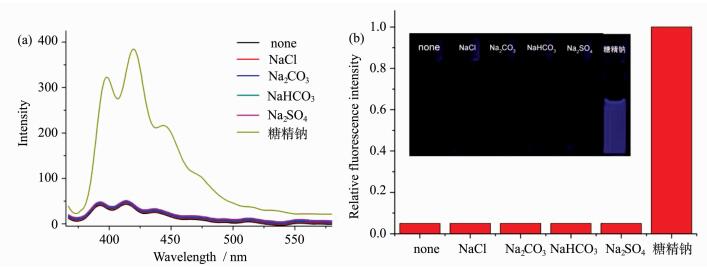
从图 4a可以看出,当向含有目标化合物的乙腈溶液中分别加入10 eq的NaCl、Na2CO3、NaHCO3、Na2SO4的水溶液时,荧光强度基本没有变化,当向其中加入糖精钠水溶液时其荧光强度发生明显的变化,并且其荧光强度对比非常明显 (图 4b),表明该探针分子可以选择性识别糖精钠盐,而对其他钠盐基本没有选择性,因此,该探针分子可用于检测糖精钠的存在。推测其作用机理是:探针分子与金属离子的选择性结合是由于氮杂冠醚环对不同钠盐的键合能力不同引起的,而这种能力受空腔尺寸匹配作用和阴离子偶极共同作用影响,溶液中阴离子的存在对氮杂冠醚识别金属阳离子具有协同作用,氮杂冠醚可选择性地与糖精钠形成一种弱的分子间作用力。糖精钠分子式中阳离子和阴离子对识别目标分子的氮杂冠醚空腔具有协同作用,在二者的共同作用下,目标分子中氮杂冠醚与蒽荧光团的PET过程减弱,导致体系的荧光增强,探针荧光信号的变化主要是对上述结合过程的响应。
|
图 4 不同的钠盐 (10 eq) 在乙腈中对探针分子 (1.0×10-5 mol/L) 荧光 (a) 光谱影响和相对荧光强度的对比示意图 (b),激发波长348 nm Fig.4 Fluorescence spectra (a) and schematic representation of relative fluorescence intensity (b) of probe molecular (1.0×10-5 mol/L) responding to different sodium salt (10 eq) in CH3CN, the excitation wavelength was 348 nm |
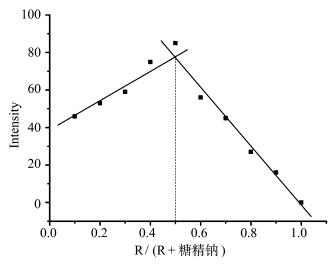
探针分子R与糖精钠存在良好的络合作用,为进一步确定二者的络合比,作了Job’s plot曲线,结果如图 5所示。当糖精钠摩尔分数为0.5时,探针分子与糖精钠的络合物在发射波长 (410 nm) 处出现最大的荧光强度,表明探针分子与糖精钠之间是以1:1的比例络合。
|
图 5 荧光探针分子R与糖精钠作用的Job-plot曲线 Fig.5 Job's plots for fluorescence molecular probe and saccharin sodium |
荧光分子探针由于其对金属离子识别具有选择性好、灵敏度高、操作简单、响应时间短等诸多优点,近年来发展迅速。本文设计合成的含蒽荧光团的氮杂15-冠-5探针分子,能够特异性识别溶液中的糖精钠,具有肉眼可见、易于识别的特点,可实现对糖精钠的快速检测,有望成为一种检测食品中糖精钠的新方法,为今后发展一种简便、响应迅速、肉眼可辨的糖精钠试纸奠定了基础。
| [1] |
GB 2760-2014, 食品添加剂使用标准.
GB 2760-2014, Standard for the Use of Food Additives. |
| [2] | Yang Y M, Zhao Q, Wei F, Li F Y. Luminescent chemodosimeters for bioimaging[J]. Chemical Reviews, 2013, 113(1): 192–270. DOI:10.1021/cr2004103 |
| [3] | Fan J L, Hu M M, Zhan P, Peng X J. Energy transfer cassettes based on organic fluorophores: construction and applications in ratiometric sensing[J]. Chemical Society Reviews, 2013, 42(1): 29–43. DOI:10.1039/C2CS35273G |
| [4] | Zhu H, Fan J L, Wang J Y, Mu H Y, Peng X J. An "enhanced PET"-based fluorescent probe with ultrasensitivity for imaging basal and elesclomol-induced HClO in cancer cells[J]. Journal of the American Chemical Society, 2014, 136(37): 12820–12823. DOI:10.1021/ja505988g |
| [5] | Liu C, Shen Y M, Yin P, Li L D, Liu M L, Zhang Y Y, Li H T, Yao S Z. Sensitive detection of acetylcholine based on a novel boronate intramolecular charge transfer fluorescence probe[J]. Analytical Biochemistry, 2014, 465: 172–178. DOI:10.1016/j.ab.2014.08.003 |
| [6] | Wei C, Wei L, Xi Z, Yi L. A FRET-based fluorescent probe for imaging H2S in living cells[J]. Tetrahedron Letters, 2013, 54(50): 6937–6939. DOI:10.1016/j.tetlet.2013.10.049 |
| [7] | Hong Y, Lam J W Y, Tang B Z. Aggregation-induced emission[J]. Chemical Society Reviews, 2011, 40(11): 5361–538. DOI:10.1039/c1cs15113d |
| [8] |
龚毅君. 新型罗丹明和芘的衍生物荧光探针的设计合成及其性能研究[D]. 长沙: 湖南大学, 2013.
Gong Y J. The optimized design, synthesis of novel rhodamine, pyrene derivatives and their application in fluorescent probes[D]. Changsha: Hunan University, 2013. |
| [9] | Boens N, Leen V, Dehaen W. Fluorescent indicators based on BODIPY[J]. Chemical Society Reviews, 2012, 41(3): 1130–1172. DOI:10.1039/C1CS15132K |
| [10] | Singh B, Parshad R, Khajuria R K, Gurud S K, Pathania A S, Sharma R, Chibe R, Aravinda S, Guptag V K, Khan I A, Bhushan S, Bharate S B, Vishwakarma R A. A new cytotoxic methylated isocoumarin from Saccharomonospora azurea[J]. Tetrahedron Letters, 2013, 54(49): 6695–6699. DOI:10.1016/j.tetlet.2013.09.060 |
| [11] | Balzani V, Credi A, Venturi M. Molecular Devices and Machines: Concepts and Perspectives for the Nanoworld[M]. 2nd edition. Weinheim: Wiley-VCH, 2008. |
| [12] | Steed J W, Atwood J L. Supramolecular Chemistry[B]. 2nd edition.John Wiley & Sons, Ltd., 2009. |
| [13] |
吴寿昌.
冠醚化学[M]. 北京: 科学出版社, 1992.
Wu S C. Crown Ether Chemistry[M]. Beijing: Science Press, 1992. |
| [14] | Maruyama T, Fujie Y, Oya N, Hosaka E, Kanazawa A, Tanaka D, Hattori Y, Motoyoshiya J. Control of peroxyoxalate chemiluminescence by nitrogen-containing ligand quenching: turning off and on by ligandemetal ion hosteguest interactions[J]. Tetrahedron, 2011, 67(36): 6627–6633. |




