维生素D3是动物体内天然存在的一种脂溶性维生素,与生命健康密切相关。目前在人类的30多种细胞和组织中都发现了维生素D3受体的表达[1]。在人体中,维生素D3最基本的作用是通过其代谢活性物种25-羟基维生素D3和1, 25-二羟基维生素D3维持血液中的钙磷平衡[2]。维生素D3缺乏时,人体会出现佝偻病的症状,儿童表现为低血钙、牙齿发育迟缓、骨骼变软变弯等;成人则表现为骨质软化、骨质疏松等。随着人们对维生素D3认识的加深和研究工作的开展,其在肿瘤[3]、心血管疾病[4]、糖尿病[5]的治疗方面也发挥出积极的作用。为促进禽畜健康快速地成长,维生素D3更是饲料中不可或缺的添加剂。
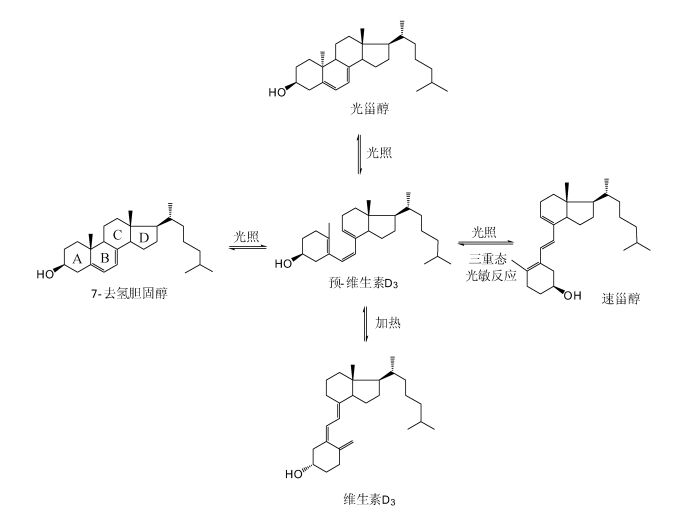
生产维生素D3最关键技术是7-去氢胆固醇光照开环合成预维生素D3(图 1),该技术长期被国外大公司垄断,长久以来我国维生素D3生产几近空白。2002年,中国科学院理化技术研究所曹怡、张宝文团队成功发明了光化学合成维生素D3新技术[6],并通过浙江花园集团将该技术实现产业化,填补了我国维生素D3生产空白,使我国一跃成为世界上掌握维生素D3最先进生产技术的国家,维生素D3产量世界第一。虽然该技术达到了世界领先水平,但反应中使用的传统釜式(Batch)光反应器制约了光异构化反应过程中的传质效率,即靠近光源部分的光反应液被过度光照,而远离光源部分的光反应液又光照不充分,致使7-去氢胆固醇的转化率必需严格控制在30%以下,即便如此,仍无法避免副产物生成。同时,70%以上未反应的原料需要经过-20 ℃的低温冷冻进行分离,工业生产中必需依赖大型冷冻设备。从原料的光照反应到后期浓缩、冷冻、过滤、洗涤等分离处理,整个工艺流程需要经历一周的时间才能最终获得树脂状维生素D3产品。树脂状维生素D3可直接用作家禽家畜的饲料添加剂,或者通过重结晶获得临床药用维生素D3。如何提高原料转化率、免除原料与产物的分离操作,以及缩短生产周期成为进一步提升树脂状维生素D3工业生产效率和降低生产成本的关键。
|
图 1 7-去氢胆固醇光化学反应合成维生素D3的路线 Fig.1 Synthetic routes of vitamin D3 |
近年来,微流技术为有机光化学合成开辟了一片崭新天地[7]。与传统的釜式光反应器相比,微流光反应器具有得天独厚的优势:微流光反应器的主体是由内径十微米到几毫米的微通道构成,反应器比表面积高达10000~50000 m2·m-3,如此高的比表面积决定了微流反应器具有极高的传质传热效率,能够克服传统光反应器中因光程过大导致的光照不均匀所引起的原料转化率低和副产物多等一系列问题;由于微流反应器是一个流动的开放体系,通过简单延长反应时间即可实现反应的放量。2001年,Jensen等[8]首次利用微流光反应器实现苯频哪醇的合成。此后,寡聚酰胺-胺[9]、糖复合物[10]、青蒿素[11]等化合物的微流光化学合成也相继被报道。
针对由7-去氢胆固醇光异构化制备树脂状维生素D3所面临的原料转化率低、产物提纯难度大、生产周期长等问题,我们利用微流光反应器开展了光化学合成树脂状维生素D3的研究。
1 实验部分 1.1 仪器和试剂高压液相色谱仪,日立L-2000,天美(中国)科学仪器有限公司;蠕动泵,B704F-YZ1515,北京信康亿达科技发展有限公司;高压汞灯,GGZ1000-1,北京电光源研究所。
7-去氢胆固醇,分析纯,北京维迪思通化学品技术有限公司产品;2-甲基四氢呋喃、乙酸乙酯、石油醚、乙醇、正己烷、甲醇均为化学纯,百灵威科技有限公司。
1.2 实验方法 1.2.1 微流光反应器中制备预维生素D3将0.96 g 7-去氢胆固醇溶入100 mL 4:1的正己烷/甲醇混合溶液中,配制成摩尔浓度为0.13 mol/L的光反应液。向光反应液中通入N2 30 min,接通冷凝水,开启500 W高压汞灯,在N2保护下借助蠕动泵,以3.5 mL/min的流速向微流反应器中泵入光反应液。反应过程中保持光反应液的温度为23 ℃~28 ℃。从微流管的出口处收集反应生成的预维生素D3。
1.2.2 釜式光反应器中制备预维生素D3将0.96 g 7-去氢胆固醇溶入100 mL 4:1的正己烷/甲醇混合溶液中,配制成摩尔浓度为0.13 mol/L的光反应液,并将光反应液全部倾倒入釜式光反应器中。向光反应液中通入N2 30 min,接通冷凝水,开启500 W高压汞灯,在N2保护下进行光照反应。反应过程中保持光反应液的温度为23 ℃~28 ℃。30 min后关闭高压汞灯,结束光照反应,从釜式光反应器中倾倒出光照产物。
1.2.3 热反应异构化制备维生素D3在N2保护的条件下,将从微流光反应器中收集的预维生素D3溶液浓缩,加热到65 ℃保持4 h。然后,将反应液缓慢降温到35 ℃,保持10 h。用旋转蒸发仪旋蒸,除去溶剂,得到树脂状维生素D3。
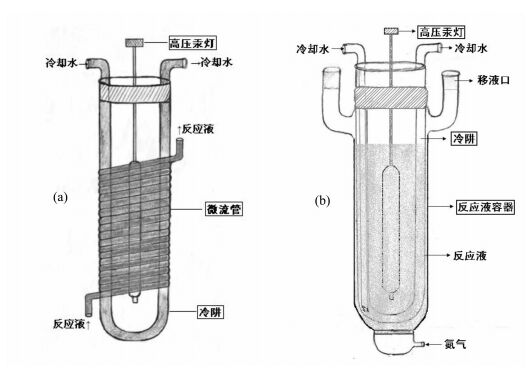
2 结果与讨论 2.1 光反应器图 2(a)是微流光反应器示意图。微流光反应器由冷阱、微流管、光源三部分组成。冷阱的材质为石英玻璃,可以透过300 nm以下的紫外光;微流管为内径2 mm的聚四氟乙烯管,缠绕在石英冷阱的外侧,其有效光照体积为33 mL;光源为500 W的高压汞灯,放置在冷阱内。光反应液从微流管的下端入口由蠕动泵泵入管中,经光照后由微流管的上端出口流出。冷阱上端左侧是冷凝水的入口,右侧是冷凝水的出口,冷凝水流经冷阱时带走高压汞灯产生的热量,保证光反应在23 ℃~28 ℃左右的条件下发生。
|
图 2 微流(a)和釜式(b)光反应器示意图 Fig.2 Schematic diagrams of micro-flow (a) and batch (b) photo-reactors |
在300 nm以下的光照条件下,7-去氢胆固醇B环断裂生成预维生素D3(图 1)。由于微流光反应的光程只有2 mm,加之整个反应系统是一个开放流动的体系,光反应产物预维生素D3生成后立即移出体系,因此,利用微流光反应器不仅可以使微通道内的各个部位的反应液都能有效发生光反应,还可以抑制光反应产物继续被光照而发生一系列副反应。此外,通过控制光反应液流速,可以非常方便地优化光反应底物的转化率。
图 2(b)是釜式光反应器的示意图。釜式光反应器由冷阱、反应液容器、光源三部分组成。冷阱同样是石英玻璃,在冷阱外面套有一个玻璃反应液容器,光反应液盛放于冷阱与反应液容器的夹层之间,反应液的有效体积为100 mL。光源为500 W的高压汞灯,放置在冷阱内。釜式光反应器冷阱的作用与微流光反应器相似。
2.2 反应介质对微流光反应的影响选择2-甲基四氢呋喃、乙酸乙酯,以及不同的极性溶剂与非极性溶剂的混合溶剂石油醚/乙醇、正己烷/甲醇作为光反应介质,开展7-去氢胆固醇的微流光反应研究。
反应介质对光反应的影响见表 1。从表 1中可以看出,在同样的流速情况下,石油醚/乙醇介质中7-去氢胆固醇转化率,以及预维生素D3和维生素D3的收率均偏低,而正己烷/甲醇介质中7-去氢胆固醇转化率,以及预维生素D3和维生素D3的收率最佳,分别达到95.9%和73.5%。对于混合溶剂来说,溶剂之间的混溶度和7-去氢胆固醇在介质中的溶解度,与光反应息息相关。一般来讲,溶剂间的混溶度越高,7-去氢胆固醇在介质中的溶解度越好,其转化率就越高。当正己烷与甲醇的比例为4:1时,这两种溶剂能够完全混溶,7-去氢胆固醇在该介质中的溶解性最好,摩尔消光系数最大。因此,在4:1的正己烷/甲醇溶剂中,微流光照反应的效率最高。2-甲基四氢呋喃与乙酸乙酯属于绿色环保溶剂,从环保的角度考虑,工业生产中这两种溶剂是最佳选择。
| 表 1 反应介质对光反应的影响 Table 1 Influence of solvents on the micro-flow photoreaction of 7-dehydrocholesterol |
以介质正己烷/甲醇(4:1) 为例,我们进一步研究了7-去氢胆固醇光反应液在微流光反应器中存留时间(即流速)对光反应的影响,结果列入表 2。
| 表 2 光反应液在微流光反应器中存留时间对光反应的影响 Table 2 Influence of residence time on the micro-flow photoreaction of 7-dehydrocholesterol |
存留时间是指7-去氢胆固醇原料的光反应液从泵入光反应器的入口到从出口流出的时间。从表 2可知,当存留时间为10 min(流速3.3 mL/min)时原料的转化率和产物的收率都达到了峰值。当存留时间缩短为6 min(流速5.5 mL/min)或者延长为15 min(流速2.2 mL/min)时,7-去氢胆固醇的转化率和预维生素D3的收率都明显降低。缩短存留时间,7-去氢胆固醇光照时间不充分,只有一部分原料吸收了光子发生反应,因此产物的收率降低;延长存留时间,虽然原料能够充分吸收光子进行反应,但产物却被过度光照,导致副产物光甾醇、速甾醇,以及其它高效液相色谱(HPLC)检测不到的复杂副产物的生成,并使部分预维生素D3逆向转化为7-去氢胆固醇,也使原料的转化率与产物的收率大打折扣。
通过上述实验,最终确定微流光反应器中7-去氢胆固醇光照生成预维生素D3的最优化反应条件为:正己烷/甲醇为反应介质,7-去氢胆固醇的浓度为0.13 mol/L,在通入氮气的条件下,用蠕动泵将反应液泵入微流光反应器中,光照波长为小于300 nm的紫外光。调整蠕动泵的流速,将存留时间控制在10 min。在此优化条件下,反应物7-去氢胆固醇的转化率高达95.9%,产物预维生素D3与维生素D3的收率加和达到73.5%(表 2)。
2.4 热异构化反应合成树脂状维生素D3最终目标产物维生素D3是通过预维生素D3(图 1)的热异构化反应获得。氮气保护下,预维生素D3溶液浓缩,加热到65 ℃,保持4 h,然后缓慢降温到35 ℃,保持10 h;用旋转蒸发仪旋蒸除去溶剂,得到含有树脂状维生素D3,其HPLC收率可达到81.2%。
2.5 微流光反应技术与釜式光反应技术对比我们利用传统的釜式光反应器制备了预维生素D3,通过光反应液的高压液相色谱数据,比较了微流光化学反应技术与釜式光化学反应技术在制备树脂状维生素D3方面的差异(图 3)。
|
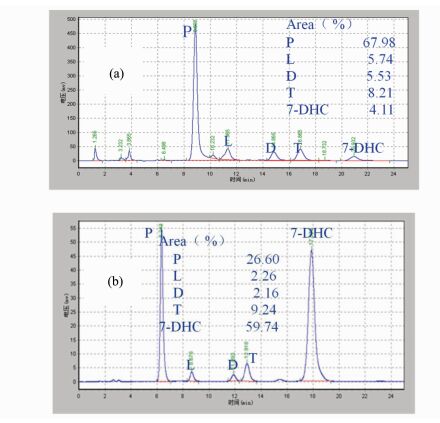
图 3 7-去氢胆固醇光化学反应后的HPLC谱图 (a)微流光化学反应技术,溶剂为正己烷/甲醇(4:1);(b)釜式光化学反应技术,溶剂为正己烷/甲醇(4:1) P为预维生素D3,L为光甾醇,D为维生素D3,T为速甾醇,7-DHC为7-去氢胆固醇 Fig.3 HPLC data of the photoreaction product of 7-dehydrocholesterol in micro-flow (a) or batch (b) photoreactors P, L, D, T, and 7-DHC represent pre-vitamin D3, lumisterol, vitamin D3, toxisterol, and 7-dehydrocholesterol, respectively |
图 3(a)为7-去氢胆固醇微流光化学反应后的HPLC谱图。从图中可以看出,7-去氢胆固醇的含量仅为4.11%,95%以上的原料已发生光异构化反应。其中生成的预维生素D3和维生素D3的总量为73.51%,可以直接进行热异构化反应,得到树脂状维生素D3。图 3(b)为7-去氢胆固醇釜式光化学反应后的HPLC谱图。从图中可以看出,7-去氢胆固醇的含量高达60%。原料含量如此之高,需要对原料进行回收。回收过程需要经过-20 ℃低温冷冻,再经过过滤、洗涤等, 才能够将未反应的原料与产物分离,整个分离过程需持续4天的时间。
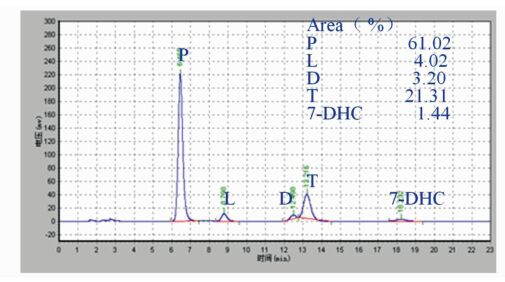
图 4是釜式光化学反应后的产物经冷冻、过滤、洗涤,除去原料7-去氢胆固醇后得到滤液的HPLC谱图。此时,7-去氢胆固醇HPLC含量为1.44%,预维生素D3和维生素D3的总量为64.22%,可用于进行热异构化反应,获取目标产物维生素D3。图 4与图 3(a)对比,其产物分布基本相当,但图 3(a)中预维生素D3和维生素D3的总量为73.51%,图 4中预维生素D3和维生素D3的总量为64.22%,也就是说,微流光反应技术直接得到的反应液比釜式光反应技术经4天处理得到的滤液,其产物含量还要高出9个百分点。
|
图 4 釜式光化学反应回收7-去氢胆固醇后滤液的HPLC谱图 P为预维生素D3,L为光甾醇,D为维生素D3,T为速甾醇,7-DHC为7-去氢胆固醇 Fig.4 HPLC data of the photoreaction product of 7-dehydrocholesterol in a batch photoreactor after removal of unreacted 7-dehydrocholesterol P, L, D, T, and 7-DHC represent pre-vitamin D3, lumisterol, vitamin D3, toxisterol, and 7-dehydrocholesterol, respectively |
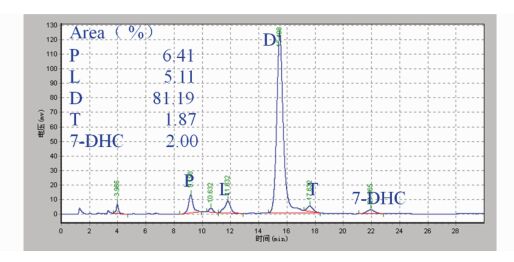
利用微流光反应技术,100 mL光反应液以最佳流速3.3 mL/min在微流光反应器中进行光反应,0.5 h后光反应结束,然后,浓缩光反应液,进行热异构化反应,最后,热异构化反应产物经低温过夜过滤,获得维生素D3的树脂状产物0.77 g。从光照反应到获得最终产品,总时间在24 h以内。而利用釜式光化学反应技术,从光照反应到获得最终产品需要历时4天,获得树脂状产物0.31 g。图 5为微流光反应后,进行热异构化反应得到的最终产物树脂状维生素D3的HPLC图谱,从图 5可知,维生素D3的收率高达81.2%。
|
图 5 微流光化学反应热异构反应后树脂状维生素D3HPLC谱图 P为预维生素D3,L为光甾醇,D为维生素D3,T为速甾醇,7-DHC为7-去氢胆固醇 Fig.5 HPLC data of the resin-like vitamin D3 obtained from micro-flow photoreaction of 7-dehydrocholesterol followed by thermal isomerization reaction P, L, D, T, and 7-DHC represent pre-vitamin D3, lumisterol, vitamin D3, toxisterol, and 7-dehydrocholesterol, respectively |
与釜式光反应技术相比,微流光反应技术将原料转化率从低于30%提高到95%;光反应产物无需提纯,可直接投入热异构化反应;生产周期从4天缩短到24 h以内。由此可见,微流光反应技术解决了目前釜式光反应技术所面临诸多困境。
3 结论我们将微流光反应技术引入到树脂状维生素D3的制备中。将原料7-去氢胆固醇的转化率从低于30%提高到95%,树脂状维生素D3的HPLC收率达到了80%以上。利用微流光反应技术制备维生素D3省去了原料回收工艺,简化了树脂状维生素D3的生产过程,为进一步提高维生素D3生产效率和降低生产成本奠定了基础。
| [1] | Tian J, Liu Y, Williarns L A, de Zeeuw D. Potential role of active vitamin D inretarding the progression of chronic kidney is easing[J]. Nephrology Dialysis Transplantation, 2007, 22: 321–328. |
| [2] | Adams T H, Noman A W. Studies on the mechanism of action of calciferol[J]. Journal of Biological Chemistry, 1970, 245: 4421–4431. |
| [3] | Prüfer K, Racz A, Lin G C, Barsony J. Dimerization with retinoid X receptors promotes nuclear localization and subnuclear targeting of vitamin D receptors[J]. Journal of Biological Chemistry, 2000, 275: 41114–41123. DOI:10.1074/jbc.M003791200 |
| [4] | Wang T J, Pencina M J, Booth S L, Jacques P F, Ingelsson E, Lanier K, Benjamin E J, D'Agostino R B, Wolf M, Vasan R S. Vitamin D deficiency and risk of cardiovascular disease[J]. Circulation, 2008, 117: 503–511. DOI:10.1161/CIRCULATIONAHA.107.706127 |
| [5] | Mietinen M E, Reinert L, Kinnunen L, Harjutsalo V, Koskela P, Surcel H M, Lamberg-Allardt C, Tuomilehto J. Serum 25-hydroxyvitamin D level during early pregnancy and type Idiabetes risk in the offspring[J]. Diabetologia, 2012, 55: 1291–1294. DOI:10.1007/s00125-012-2458-8 |
| [6] |
张宝文, 程学新, 刘颙颙, 王雪松, 曹怡. 光化学合成VD3的方法[P]. 中国专利, ZL02104444. 9. 2002-03-18.
Zhang B W, Cheng X X, Liu R R, Wang X S, Cao Y. The synthesis method of VD3 by photochemistry[P].Chinese patent, ZL02104444.9.2002-03-18. |
| [7] | Sumino S, Uno M, Fukuyama T, Ryu I, Matsuura M, Yamamoto A, Kishikawa Y. Photoredox-catalyzed hydro-difluoroalkylation of alkenes using difluorohaloalkyl compounds and a hantzsch ester[J]. Journal of Organic Chemi-stry, 2017, 82: 5469–5474. DOI:10.1021/acs.joc.7b00609 |
| [8] | Lu H, Schmidt M A, Jensen K F. Photochemical reactions and on-line UV detection in microfabricated reactors[J]. Lab on a Chip, 2001, 1: 22–28. DOI:10.1039/b104037p |
| [9] | Wojcik F, O'Brien A G, G tze S, Seeberger P H. Hartmann L, Synthesis of carbohydrate-functionalized sequence-defined Oligo(amidoanine)s by photochemical thiol-ene coupling in a continuous flow reactor[J]. Chemistry-A European Journal, 2013, 19: 3090–3098. DOI:10.1002/chem.201203927 |
| [10] | Andrews R S, Becker J J, Gagné M R. A photoflow reactor for the continuous photoredox-mediated synthesis of C-glycoamino acids and C-glycolipids[J]. Angewandte Chemie International Edition, 2012, 51: 4140–4143. DOI:10.1002/anie.201200593 |
| [11] | Kopetzki D, Lévesque F, Seeberger P H. A continuous-flow process for the synthesis of artemisinin[J]. Chemistry-A European Journal, 2013, 19: 5450–5456. DOI:10.1002/chem.201204558 |




