当前人们使用的能源主要来自于化石,然而有限的化石能源预计将在50~100年内耗尽[1],同时大量使用化石能源也造成了诸多环境问题,例如温室效应、雾霾等[2]。因此,寻求可替代的清洁能源成为了人们关注的热点问题。可再生能源包括太阳能、核能、地热能、风能、潮汐能、生物质能等,其中太阳能被认为是最可行、最有前景替代传统化石能源的可再生能源[3]。当前,科学家们主要将太阳能以化学键的形式实现能量储存。光解水产氢是实现清洁能源转化的一种环境友好路径[4]。但要实现此过程,催化剂的选择起着至关重要的作用。目前,大部分水分解反应由铂、钌、铱、铑等贵金属催化剂来实现[5],但由于地壳中贵金属含量稀少、价格昂贵,限制了其实际使用,因此对非贵金属催化剂(铁、镍、铜、钴、钼等)的研究势在必行[6, 7]。其中,因为铁、镍在诸多非贵金属中丰度最高,价格相对最便宜,所以镍、铁基催化剂成为了催化剂最理想的、最经济的选择。
自然界中,铁镍氢化酶因具有良好的催化性能成为科学家竞相模拟的对象[8, 9],镍基催化剂的研究正是在这样的大背景下展开。由于受水溶性的限制,大部分的镍催化剂都是在有机相中使用有机或无机酸实现催化质子还原产氢的。如近年来报道的镍催化剂主要有镍的N4大环配合物[10]、二亚胺-二肟配合物[11]、吡啶二亚胺配合物[12]、二硫纶配合物[13]、硫醇类配合物[14]、卟啉类[15]及2-硫基吡啶-N-氧配体[16]等。其中含有1, 4, 8, 11-四取代四氮杂环十四烷[10]、6, 6′-二-1, 4, 8, 11-四取代四氮杂环十四烷[10]、2-硫基吡啶-N-氧[16]以及三吡啶二胺配体基的镍配合物1~4在中性水溶液中具有产氢活性[17]。对于本文中配体的设计,考虑到抗衡离子对电催化活性可能存在的影响,我们设计了中性配体与正二价镍金属配位得到中性配合物。本文通过简单的曼尼希(Mannich)反应合成配体L,通过与简单镍盐配位,得到了较高产率的镍基配合物NiL。且NiL在水溶液中具有一定溶解度,电化学测试表明配合物NiL可实现在中性缓冲溶液中电化学催化质子还原产氢,这为进一步研究电催化产氢体系提供了一种新思路。
1 实验部分 1.1 试剂与仪器所用试剂均为分析纯试剂,邻甲酚、2-氨甲基吡啶、甲醛、磷酸二氢钠、磷酸氢二钠、乙腈溶剂在反应前均需除氧,以保证配位反应在无氧条件下进行。
采用Bruker公司的400 Hz核磁共振仪、Apex Ⅳ FTMS高分辨质谱仪对合成化合物进行表征;采用日立U-3900H紫外-可见吸收光谱仪对催化剂稳定性进行测试;采用上海辰华CHI660E电化学工作站对催化活性进行测试。
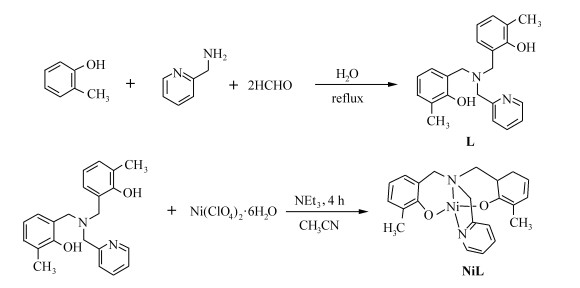
1.2 化合物的合成和表征[N2O2]型配体L的合成步骤参照文献[18],通过简单的曼尼希反应,一锅煮得到粗品,层析分离和重结晶得到纯净的配体,具体合成路线如式1所示。邻甲酚(2 g, 18.45 mmol)、2-氨甲基吡啶(0.92 mL,9.25 mmol)、甲醛(1.38 mL,18.45 mmol)均溶解在50 mL蒸馏水中,回流16 h后, 有固体析出,过滤、层析分离得到纯净的配体(乙酸乙酯:二氯甲烷= 1:30)。
|
式1 配合物NiL的合成路径 Scheme1 Synthetic route of the target compound NiL |
1HNMR(400 MHz, CDCl3): 10.70(br s, 2H), 8.73(d, J = 3.1 Hz, 1H), 7.74(td, J=1.8, 7.7, 15.4 Hz, 1H), 7.31~7.22 (m, 1H), 7.15(d, J=7.8 Hz, 1H), 7.08(d, J=7.6 Hz, 2H), 6.94(d, J = 8.0 Hz, 2H), 6.73(t, J = 7.4 Hz, 2H), 3.88(s, 2H), 3.83(s, 4H), 2.27(s, 6H)。13CNMR(400 MHz, CDCl3): 153.3,148.4,137.2,131.3,128.6,127.4,125.4,123.6,122.6,120.5,56.7,55.4,16.3。EIS(m/z): Calcd for [L+H]+:349.1916;Found:349.1911。
NiL配合物的合成通过简单的配位反应实现:控制配体与金属盐的比例为1.5:1,将金属盐溶于除气的高氯酸镍乙腈溶液中,回流状态下加入配体及少量三乙胺,回流4 h,旋蒸除去溶剂,重结晶(大量乙醚和少许乙腈)得到目标配合物。通过高分辨质谱表征配合物,EIS(m/z): Calcd for [M+H]+:405.1113;Found:405.1119,同时根据高分辨质谱推测了配合物的结构式(见式1)。利用德国Elementar Vario EL Ⅲ元素分析仪测试CHN含量,其中理论CHN含量:C,65.06;H,5.71;N,6.90;实际CHN含量:C,64.98;H,5.73;N,6.86。
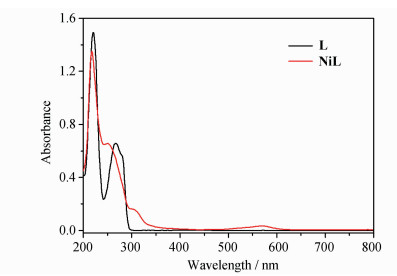
2 结果与讨论 2.1 合成配体L可以与多种金属盐相配位,得到具有特定功能的配合物。2015年,展树中课题组合成了一种基于配体L的双核铁基配合物,在DMF和水中具有一定催化产氢活性[19];2016年,他们又将配体L与CoCl2配位合成了一种既能光催化产氢又能电催化产氢的钴配合物[20]。最近,我们小组以高氯酸铜与该配体配位合成了一种单核配合物,通过电沉积方法,得到了一种超薄材料,在中性条件下能实现高效产氢(待发表)。本文通过在乙腈或甲醇溶剂中加入三乙胺拔氢,回流即可得到对应的镍配合物,合成产率为45%。通过比较配体和配合物在乙腈中的紫外-可见吸收光谱(图 2),可见配位后原来配体出峰的位置发生了偏移,并伴随有新峰出现,这提示有新物质镍配合物的生成。因为同一化合物在不同的溶剂中会因为溶质与溶剂分子间相互作用使紫外-可见吸收光谱存在一定差异,所以影响了NiL配合物的吸收峰强度和形状。
|
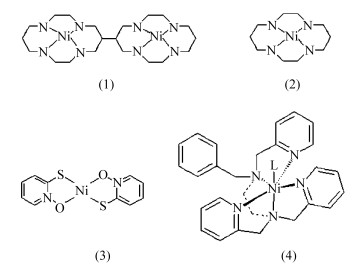
图 1 已报道的几种在水溶液中产氢的镍分子催化剂[10, 16, 17] Fig.1 Some hydrogen production reports of nickle-based molecular catalysts in aqueous solution[10, 16, 17] |
|
图 2 配体L和配合物NiL的紫外-可见光谱图 Fig.2 UV-Vis spectra of the ligand and the NiL complex in CH3CN |
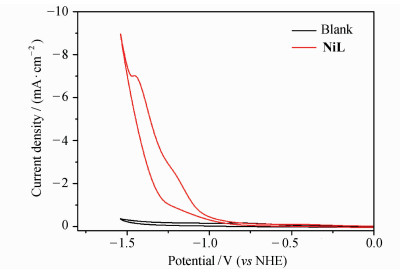
以玻碳电极为工作电极,Ag/AgCl为参比电极,铂丝为对电极,在0.1 mol/L中性磷酸缓冲溶液中对NiL配合物的电化学性质进行了初步研究,如图 3所示。在pH=7的0.1 mol/L磷酸缓冲溶液中,催化剂浓度为25 μmol/L,相对于标准氢电极起峰电位为-0.63 V,起峰过电势为217 mV,其中电压为-1.26 V处属于Ni2+/Ni+峰,-1.43 V峰归属于催化峰[10]。当催化剂浓度为25 μmol/L时,催化产氢电流密度达到9 mA/cm2, 然而在没有加入催化剂的体系中,电流密度几乎为零,说明该催化剂在中性条件下具有良好的产氢性质。
|
图 3 25 μmol/L NiL催化剂在中性磷酸缓冲溶液中的循环伏安曲线图 Fig.3 CVs of 25 μmol/L NiL obtained in a 0.1 mol/L phosphate buffer, pH=7 |
将催化剂溶于缓冲溶液中,通过检测分别电解24 h和43 h时催化剂的紫外-可见吸收光谱的变化,来观察催化剂在体系中的稳定性。如图 4所示,电解24 h后吸光度下降了0.01,在误差范围内,电解43 h后,催化剂在中性磷酸缓冲液中的紫外吸收未发生明显变化,基本可以认为该催化剂在电解过程中是稳定存在的。

|
图 4 25 μmol/L NiL催化剂置于中性磷酸缓冲溶液中0 h、24 h、43 h后的紫外可见光谱图 Fig.4 UV-Vis spectra of NiL (2.5×10-5 mol/L) in 0.1 mol/L phosphate buffer after electrolysis for 0 h, 24 h, 43 h, pH=7 |
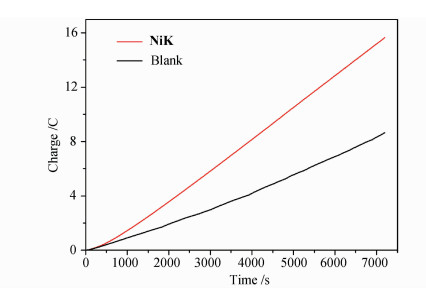
通过恒电压电解,我们对NiL配合物的电催化产氢性能进行了进一步的研究(图 5)。在-1.5 V(vs NHE)电压下,加入0.1 mol/L NaClO4来维持离子强度,电解2 h, 扣除空白后,流过电路的电荷量为8 C, 同时在电解过程中可明显观察到气泡的产生。采用以甲烷作为内标的气相色谱来检测氢气的产生。根据公式TOF =ΔC/(F*n1*n2* t), 其中ΔC表示扣除空白后的电量,F表示法拉第常数96480 C/mol,n1指1 mol氢气所需的电子数,n2指催化剂的物质的量,单位为mol, t表示电解时间,TOF指每摩尔催化剂每小时产生的氢气量,单位为h-1。由此可计算出催化剂的TOF值等于83 h-1。
|
图 5 加入NiL催化剂和不加催化剂在-1.5 V电解2 h的电荷量-时间图 Fig.5 Charge buildup vs time from electrolysis of NiL in 0.1 mol/L phosphate buffer with NaClO4 to sustain ion intensity under -1.5 V (vs NHE), pH 7 |
通过一锅煮法合成了[N2O2]型配体,与高氯酸镍通过简单的配位反应合成了一种镍基配合物NiL,研究了其在中性磷酸缓冲溶液下的产氢性能。结果表明该配合物具有良好的催化产氢活性。同时,紫外-可见光谱监测显示该催化剂在催化过程中稳定性较好。在中性磷酸缓冲液中以-1.5 V恒电压电解,其TOF值可达83 h-1(pH = 7)。
| [1] | Lewis N S, Nocera D G. Powering the planet:chemical challenges in solar energy utilization[J]. Proceedings of the National Academy of Sciences, 2006, 103(43): 15729–15735. DOI:10.1073/pnas.0603395103 |
| [2] | Climate Change 2007:Mitigation of Climate Change, IPC=C Working Group Ⅲ Fourth Assessment Report[R]. Inter-governmental Panel on Climate Change:Geneva, 2007. |
| [3] | Armaroli N, Balzani V. The future of energy supply:challenges and opportunities[J]. Angewandte Chemie International Edition, 2007, 46(1-2): 52–66. DOI:10.1002/(ISSN)1521-3773 |
| [4] | Gratzel M. Solar energy conversion by dye-sensitized photovoltaic cells[J]. Inorganic Chemistry, 2005, 44(20): 6841–6851. DOI:10.1021/ic0508371 |
| [5] | Vesborg P C K, Jaramillo T F. Addressing the terawatt challenge:scalability in the supply of chemical elements for renewable energy[J]. RSC Advances, 2012, 29(21): 7933–7947. |
| [6] | Artero V, Fontecave M. Some general principles for designing electrocatalysts with hydrogenase activity[J]. Coordination Chemistry Reviews, 2005, 249(15-16): 1518–1535. DOI:10.1016/j.ccr.2005.01.014 |
| [7] | Zou X, Zhang Y. Noble metal-free hydrogen evolution catalysts for water splitting[J]. Chemical Society Reviews, 2015, 44(15): 5148–5180. DOI:10.1039/C4CS00448E |
| [8] | Cracknell J A, Vincent K A, Armstrong F A. Enzymes as working or inspirational electrocatalysts for fuel cells and electrolysis[J]. Chemical Reviews, 2008, 108(7): 2439–2461. DOI:10.1021/cr0680639 |
| [9] | Wright J A, Turrell P J, Pickett C J. The Third Hydrogenase:more natural organometallics[J]. Organometallics, 2010, 29(23): 6146–6156. DOI:10.1021/om1008567 |
| [10] | Collin J P, Jouaiti A, Sauvage J P. Electrocatalytic properties of Ni(cyclam)2+ and Ni2(biscyclam)4+ with respect to Co2 and H2O reduction[J]. Inorganic Chemistry, 1988, 27(11): 1986–1990. DOI:10.1021/ic00284a030 |
| [11] | Pantani O, Anxolabehere-Mallart E, Aukauloo A, Millet P. Electroactivity of cobalt and nickel glyoximes with regard to the electro-reduction of protons into molecular hydrogen in acidic media[J]. Electrochemistry Communications, 2007, 9(1): 54–58. DOI:10.1016/j.elecom.2006.08.036 |
| [12] | Luca O R, Konezny S J, Blakemore J D, Colosi D M, Saha S, Brudvig G W, Batista V S, Crabtree R H. A tridentate Ni pincer for aqueous electrocatalytic hydrogen production[J]. New Journal of Chemistry, 2012, 36(5): 1149–1152. DOI:10.1039/c2nj20912h |
| [13] | Quentel F, Passard G, Gloaguen F. Electrochemical hydrogen production in aqueous micellar solution by a diiron benzenedithiolate complex relevant to FeFe hydrogenases[J]. Energy & Environmental Science, 2012, 5(7): 7757–7761. |
| [14] | Han Z, Shen L, Brennessel W W, Holland P L, Eisenberg R. Nickel pyridinethiolate complexes as catalysts for the light-driven production of hydrogen from aqueous solutions in noble-metal-free systems[J]. Journal of the American Chemical Society, 2013, 135(39): 14659–14669. DOI:10.1021/ja405257s |
| [15] | Han Y, Fang H, Jing H, Sun H, Lei H, Lai W, Cao R. Singly versus doubly reduced nickel porphyrins for proton reduction:experimental and theoretical evidence for a homolytic hydrogen-evolution reaction[J]. Angewandte Chemie International Edition, 2016, 55(18): 5457–5462. DOI:10.1002/anie.201510001 |
| [16] | Das A, Han Z, Brennessel W W, Holland P L, Eisenberg R. Nickel complexes for robust light-driven and electroca-talytic hydrogen production from water[J]. ACS Catalysis, 2015, 5(3): 1397–1406. DOI:10.1021/acscatal.5b00045 |
| [17] | Zhang P, Wang M, Yang Y, Zheng D, Han K, Sun L. Highly efficient molecular nickel catalysts for electrochemical hydrogen production from neutral water[J]. Chemical Communications, 2014, 50(91): 14153–14156. DOI:10.1039/C4CC05511J |
| [18] | Kerton F M, Whitwood A C, Willans C E. A high-throughput approach to lanthanide complexes and their ra-pid screening in the ring opening polymerisation of caprolactone[J]. Dalton Transactions, 2004(15): 2237–2244. DOI:10.1039/b406841f |
| [19] | Fu L Z, Zhou L L, Tang L Z, Zhang Y X, Zhan S Z. A molecular iron(Ⅲ) electrocatalyst supported by amine-bis(phenolate) ligand for water reduction[J]. International Journal of Hydrogen Energy, 2015, 40(28): 8688–8694. DOI:10.1016/j.ijhydene.2015.05.026 |
| [20] | Fu L Z, Zhou L L, Liang Q N, Fang C, Zhan S Z. Synthesis and electro-and photo-catalytic properties of a dinuclear cobalt(Ⅲ) complex supported by 2-pyridylamino-N, N-bis(2-methylene-4, 6-bimethyl)phenol[J]. Polyhedron, 2016, 107: 83–88. DOI:10.1016/j.poly.2015.11.019 |




