自Chandrasekhar[1]在1977年首次报道盘状液晶分子的合成与表征,此后有大量的工作集中于各种结构盘状液晶分子的合成与表征,到目前为止已有数千种的化合物被合成并研究其液晶性能。盘状液晶分子是一种具有平面盘状结构且能在一定条件下有序排列形成液晶态的分子,一般是由平面型或类似于平面型的刚性中心核和围绕刚性核的多条柔性侧链共同组成的。刚性中心核的种类很多,但主要为多(稠)环芳烃,它们通过平面分子间的π-π相互作用实现一维方向上的有序排列;柔性部分则多为脂肪族长链,其作用在于向刚性体系中引入扰动因素,并增加化合物的溶解性,从而在适当的条件下调节这些平面分子的堆积方式,促使其液晶态的出现[2]。
盘状液晶分子可以形成独特的柱状相结构。在柱状相中,分子排列在垂直于盘状平面的方向上,具有一维有序性,当盘状液晶基元本身具有π-电子共轭性,沿柱状排列的主轴方向即发生π-轨道交叠,形成了准一维的共轭性电子云分布。这些结构特征使盘状液晶作为光电材料具有很好的应用前景[3-6]。此外,与具有类似柱状堆积的晶体相比,由于柔性链扰动和一定分子流动性所带来的自修复功能在很大程度上减少了盘状液晶体系当中的缺陷,盘状液晶分子又体现出作为半导体材料在载流子传输上的独特优势。
盘状液晶材料作为光电和半导体材料,决定其实用性的关键因素包括高度有序性和良好的电荷传输性能、稳定的六方柱状液晶相以及宽介晶温度范围。通过分子结构的改变可以调节盘状化合物的相态、相转变温度以及相态的稳定性来达到上述要求。盘状液晶的结构修饰,在中心核确定以后, 其性能还依赖于核周围柔性链的变化[7],如改变柔性链与核的连接方式或改变柔性链长度, 在柔性链中引入官能团、盘状液晶齐聚物[8]或聚合物[9, 10]等。例如,闻建勋等[11]将不饱和基团炔基引入液晶分子,得到低熔点、介晶相温度范围较宽、介晶相稳定的液晶化合物;Rego[12]将炔基直接引入到苯并菲刚性核上,化合物出现了较好的液晶性。本文主要介绍含炔基结构的盘状液晶以及不同盘状中心核和二聚体引入炔基修饰后的介晶性和半导体性质的显著变化,以及聚炔类盘状液晶聚合物的研究进展。
1 盘状液晶分子 1.1 含炔基结构的盘状液晶 1.1.1 苯环衍生物苯环结构是芳香化合物的基本单元,由单个苯环衍生的化合物自然成为较早研究的对象。自从1977年首次发现六取代含酯基的苯衍生物,各式各样的苯衍生物盘状液晶层出不穷。
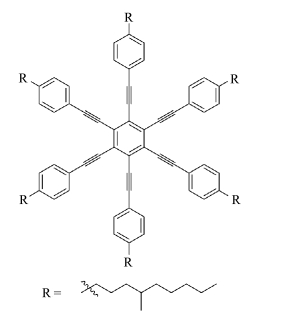
Kumar等[13]利用Wolff-Kishner还原和钯催化的偶联反应等步骤制备了支链烷基取代的六乙炔基苯衍生物(图 1),该化合物在室温下即可呈现向列盘状液晶相[13, 14],拓宽了液晶显示的视角。进一步的研究表明,此类分子的液晶行为随取代基链长和连接原子的变化而改变。通过引入电子受体,使分子产生电荷转移效应,也可调控该类分子的液晶行为[15]。
|
图 1 六乙炔基苯衍生物 Fig.1 Hexaalkynylbenzene derivative |
Varshney等[16]研究了放射型聚炔基苯系物结构与性能的关系,观察到非手性的烷基支链形成的是柱状相(columnar phase, Col),正常的烷氧基支链形成盘状向列相(nematic-discotic phase, ND),至于手性烷氧基支链则形成手性盘状向列相(chiralnematic-discoticphase, ND*)。通过“分子对称性效应”成功降低相转变温度至环境温度,电荷转移复合物与2, 4, 7-三硝基芴-9-酮(TNF)形成的是单变的六方柱状相(hexagonal columnar phase, Colh)。Lee等[17]进一步利用这些化合物的分子旋转性来高效地传递电荷。Hennrich等[18]研究高度可极化性C3-对称性1, 3, 5-三炔基苯系物,发现这些化合物不仅显示出四方柱状相(rectangular columnar phase, Colr)、Colh和ND相,且具有强荧光性,量子效率高达42%,具有明显的斯托克斯位移,但是光电导性一般。Ruy等[19]通过链接反应用三乙炔基苯获得星形1, 3, 5-三炔基苯衍生物,在环境温度时观察到Col相和垂直排列趋势。
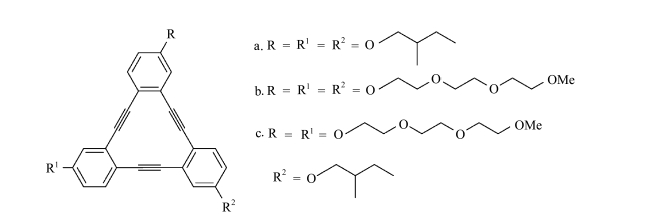
1.1.2 苯撑乙炔大环类化合物第一个大环化合物由Fischer等[20]在1994年合成。大环化合物是由在边缘位置的芳香性或反芳香性基团和作为连接桥的刚性炔烃或低炔单元共同组成。通常的大环化合物是三角形或六角形状。Seo等[21]合成出最小的大环化合物(图 2),并验证了侧链对介晶性的影响。化合物2a侧链是短的戊烷基支链,结果形成Colr相,化合物2b环内侧链是亲水性三甘醇,结果形成了Colh相,不对称的化合物2c有两个不同的侧链导致了ND相的形成。
|
图 2 三角形苯撑乙炔大环 Fig.2 Triangular macrocycles |
Zhao[22]和Höger[23]的团队分别利用Sonogashira-Hagihara和氧化Glaser偶合反应合成得到图 3中的大三角形(1) 和六角形(2) 化合物。由于亚苯基间距和边缘单元的芳基存在,环状三聚体(1) 检测到Colr、Colh和ND相。相比之下,六角形大环化合物(2) a液晶性表现更为传统,自组装成Colh和Colr相。

|
图 3 大三角形和六角形化合物 Fig.3 Large triangular and hexagonal macrocycles |
Luo等[24]研究三角形化合物的光电性能,三角形化合物不仅能提供nA-型光电流,开/关比也达到103,是组成光电开关的优良材料。Kato等[25]报道四烷氧基-菲-混合脱氢[n]轮烯,即菲在三角形(或四边形)的边缘组成的形状稳定的大环化合物。某些轮烯是发冷光的,而相应反芳香性的轮烯却没有检测到有荧光性质。轮烯为[12]和[18]的化合物的HOMO和LUMO差距分别为1.94 eV和2.33 eV。
Höger的团队研究大环化合物环内侧链对性能的影响[26, 27],通过Sonogashira-Hagihara偶合反应合成出图 4所示化合物(1),其自组装成Colr相,而对应的环内无侧链的类似物却显示ND相,但是两者的相转变温度相近。

|
图 4 六角形大环化合物(1) 和(2) Fig.4 Hexagonal macrocycles (1) and (2) |
Lee等合成了图 4中所示2种环内含侧链的化合物(2)。化合物(2) a有2个环内柔性链,有形成ND相的明显趋势,化合物(2) b有6个环内柔性链,只形成晶态[28]。
1.2 含炔基官能团的盘状液晶 1.2.1 苯并菲类盘状液晶苯并菲类盘状分子具有易合成、易加工的优点,同时其熔点较低,因而已成为研究较多的盘状液晶材料之一。此类液晶分子的构成包括刚性平面的苯并菲核心和围绕刚性核的多条柔性链。具有此种结构的苯并菲分子易于形成柱状液晶相,并沿柱轴方向有较高的电荷和激子传输性能。从应用角度来说,扩大液晶相的温度范围、降低熔点,是盘状液晶材料实用化首要解决的问题,这主要可以通过改变分子结构来实现。
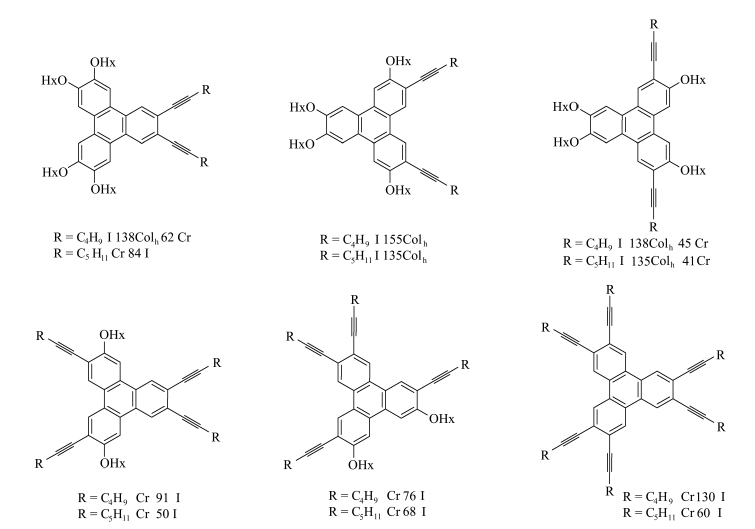
Andrew等[29]合成了一系列取代基为炔烃和烷氧基组合的多取代苯并菲(图 5),旨在研究结构性因素对盘状苯并菲中间相形成、类型和稳定性的影响。结果表明,当苯并菲含2个炔烃时确实可以提升柱状中间相行为;但当含有4个或6个炔烃时,中间相行为被完全的抑制了。
|
图 5 一系列取代基为炔烃和烷氧基组合的多取代苯并菲 Fig.5 A series of mixed alkynyl-alkoxy-triphenylenes |
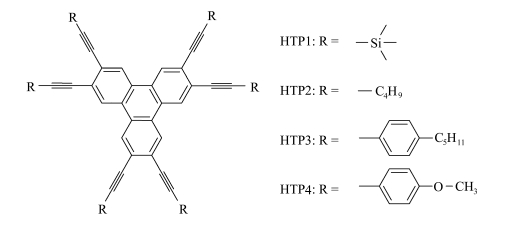
Wang等[30]由六溴苯并菲合成一系列6个对称取代基苯并菲衍生物(图 6)。6个对称取代基不仅可以增加苯并菲长π-型共轭范围,而且增加了化合物的溶解度。通过比较它们的性能,研究结构性能之间的关系,证明了盘状分子的不同取代基会影响电子性质和中间相。通过比较这些纯化合物的吸收及光致发光光谱,证明苯并菲衍生物受到扩展的π-共轭长度的影响,随着π-共轭长度的增加,吸收波长的光致发光光谱显示出明显的红移。这些化合物的电化学性质表明,化合物HTP3和HTP4的LUMO能级低于HTP1和HTP2,这可能是由于添加的苯基团增长了共轭长度,从而增强了π-电子离域。
|
图 6 盘状对称六取代基苯并菲衍生物HTP1~HTP4 Fig.6 Disk-shaped symmetric hexa-substituted triphenylene HTP1-HTP4 |
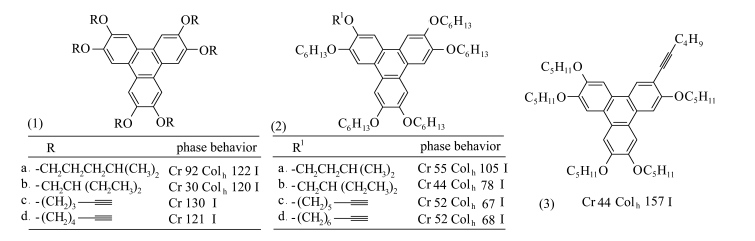
结构-性能关系和对称性对介晶性作用的研究多见报道。例如,Stackhouse和Hird[31]系统地研究了两个支链为烷氧基链系列的苯并菲(图 7)。他们研究了含乙炔基外围链的苯并菲衍生物,发现图 7中苯并菲(1) c和d是对称取代,在快速冷却时表现出单变性的中间相[32]。图 7中不对称苯并菲衍生物(2) c和d的末端是炔基单元,柱状相宽度与各自相对应的烷氧基苯并菲相比是减少的,然而化合物(3) 内含炔烃却增加了柱状相宽度。由刚性的丁二炔连接的两个戊烷氧基苯并菲形成的双生碟型二聚体形成了ND相,然而Varshney[33]和Cammidge[34]报道氢化作用对于刚性的丁基桥来说会导致化合物介晶性的损失。
|
图 7 两个支链为烷氧基链系列的苯并菲和单炔基取代的戊烷氧基苯并菲 Fig.7 Two series of branched alkoxy chain triphenylenes and alkynyl-substituted pentaalkoxytriphenylenes |
赵可清课题组[35]将含有不饱和基团的柔链引入苯并菲周围, 研究柔链对相态、相转变温度以及相态稳定性的影响。结果显示目标化合物都呈现有序的六方柱状介晶相,端炔基链化合物系列熔点最高,端烯基柔链化合物系列比端炔基柔链化合物系列的熔点低, 清亮点稍高,液晶相宽。乙烯氧基柔链化合物系列有最高的清亮点和最宽的介晶性温度范围,且随着不饱和醚链数的增多,清亮点明显升高。
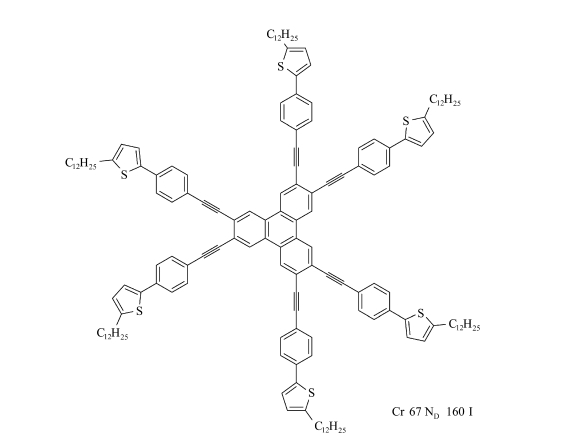
六(苯乙炔基)苯并菲自组成ND相在盘状液晶中是很少见的,然而这类化合物的宽带隙能量不利于它们应用在有机电子学方面。为了抵消这种影响,通过Suzuki和Sonogashira交叉偶合反应在外围引入噻吩单元(如图 8所示),结果显示苯并菲衍生物不仅显示出ND相,还有相对较低的带隙能量2.53 eV[36]。
|
图 8 六(苯乙炔基)苯并菲 Fig.8 Hexakis(phenylethynyl)triphenylenes |
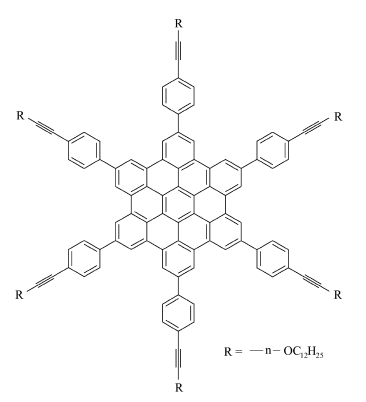
六苯并蔻(HBC)由42个碳原子通过共价键组成直径为0.15 nm的大环芳香族化合物, 其衍生物,即周围取代侧基后易形成柱状相。Müllen小组[37]利用过渡金属催化的环化反应合成了具有手性基团和外消旋基团的HBC衍生物,发现该化合物的溶解性能和加工性能得到改善,且晶相向柱状相转变的温度降低。该化合物在低于室温的温度即可进入柱状相区间,一直保持到400 ℃没有发现清亮点。而结构类似的对十二烷基苯乙炔取代的HBC (图 9)在15 ℃和80 ℃时有相应的相转变,这表明作为连接臂的乙炔基的引入影响了化合物的相转变温度。
|
图 9 含乙炔侧基的六苯并蔻衍生物 Fig.9 Acetylene-substitued hexabenzocorene derivative |
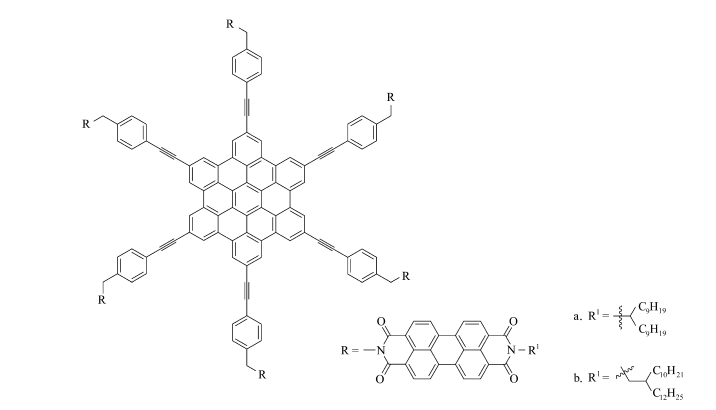
Dössel等[38]合成了共价连接的六-六苯并蒄/苝二酰亚胺二联体(图 10)作为研究能量和电子转移过程的基本模型。化合物自组装成的柱状聚合物是不稳定的,但表现出光致发光性[39]。二联体的链接部分是非共轭的,是为了抑制直接的电荷复合。这类星形二联体沿着柱向通道传输空穴和电子,可能是存在一种同轴线作用于晶体场效应,因为没有发现给体和受体间存在电子间相互作用。
|
图 10 六-六苯并蒄/苝二酰亚胺二联体 Fig.10 Hexa-peri-hexabenzocoronene/perylene bisimide dimers |
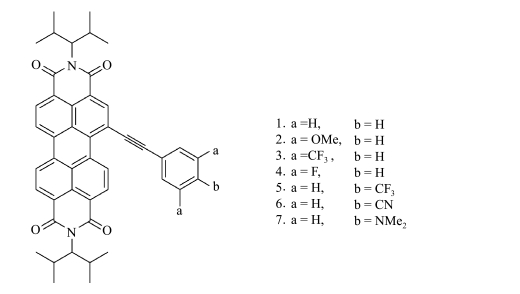
苝酰亚胺类化合物所具有的稠环共轭体系和分子平面性,使分子之间大π键相互作用增强,晶格能增大,导致大多数苝酰亚胺类化合物在常见有机溶剂中的溶解度较差。为改善此类化合物的溶解性,可以引入不同官能团。苝酰亚胺(PBI)在湾位为苯炔取代基的衍生物[40]已经通过Sonogashira偶合反应合成(图 11)。合成的二联体通过检测吸收峰和急剧的电子振动进程显示出明显的红移。富电子取代基促使电荷高效地从取代基到缺电子的PBI核转移。光谱特征表明PBI的乙炔基(二甲氨基苯基)取代基有较强的供电性。
|
图 11 湾位苯炔取代的苝酰亚胺衍生物 Fig.11 Mono-bay alkynyl-phenyl substituted perylene bisimides |
Belviso等[41]和Kayal等[42]报道了对称的八(硫代烷烃)含氮卟啉(图 12)末端分别为叠氮化物和乙炔基团,可以通过“点击”反应(CuAAC)交联成Langmuir膜或热激活叠氮化物-炔烃环加成作用形成Colh相。令人惊奇的是,中间相受交联的影响很小。

|
图 12 八(硫代烷烃)含氮卟啉 Fig.12 Octa-(thioalkyl)azaporphyrins |
液晶二聚体(liquid crystal dimers)是由两个相同或不同的刚性介晶基元通过桥链连接构成。其物理性能有别于传统的小分子液晶,不仅具有丰富的介晶相态,而且有些液晶二聚体化合物还表现出高分子性能,如在相变过程中出现玻璃化转变,提高了盘状液晶作为有机半导体材料的实用性。通过桥链将两个苯并菲盘状分子介晶基元相连,得到苯并菲二聚体化合物,是除对苯并菲介晶基元周边柔链进行修饰获得稳定柱状相方法外的另一新途径。
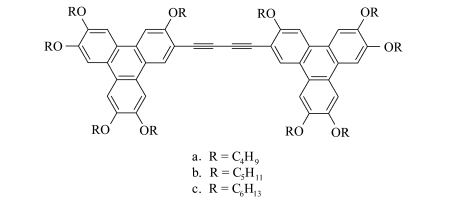
Kumar等[43]在Cu/Pd催化下将单炔化苯并菲衍生物进行自身偶联,得到了含共轭炔结构的二聚体化合物(图 13)。经过POM和DSC测试,发现3种化合物a~c都能观察到典型的纹影织构,呈盘状向列相,而单体化合物能形成有序柱状相,这说明过短的刚性桥可能会造成局部重叠或交错,空间位阻增大,刚性核平面性降低,π-π作用力相应减弱,造成刚性核还能保持一维轴向有序,但是失去平面二维有序特性,形成ND相。
|
图 13 盘状液晶二聚体 Fig.13 Discotic liquid crystal dimers |
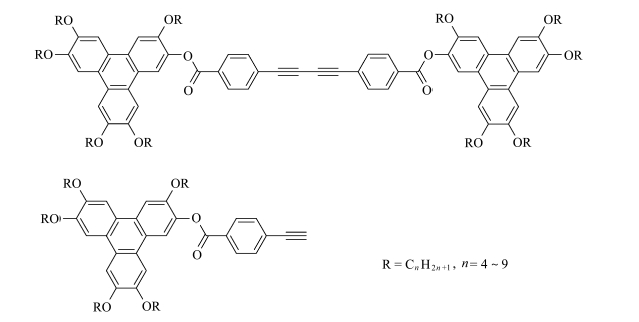
赵可清课题组[44]合成了一系列官能化的盘状液晶单体,通过Pd催化端炔自身偶联反应合成了二苯基丁二炔桥连的苯并菲盘状液晶二聚体(图 14)。热失重分析(TGA)结果显示其有良好的热稳定性,在370 ℃才开始分解。通过偏光显微镜和差示扫描量热法检测, 显示出所有单体及二聚体化合物均为柱状相液晶,在室温都处于液晶相。图 14所示盘状二聚体,其化合物刚性介于Kumar报道的化合物[43]与1, 3-丁二炔柔链桥连衍生物[45]之间,分子有非常稳定的柱状堆积和高清亮点及宽介晶相范围。证实了通过半刚性桥链将两个盘状介晶基元相连,可以在一定程度上稳定柱状相。通过文献对比发现,中心桥链的刚性对苯并菲盘状液晶二聚体介晶性有重要影响,刚性较强的二苯基丁二炔中心桥链有利于分子的有序堆积,得到了稳定的Col相。
|
图 14 苯并菲单体和苯并菲盘状液晶二聚体 Fig.14 Triphenylene monomers and discotic liquid crystal dimers |
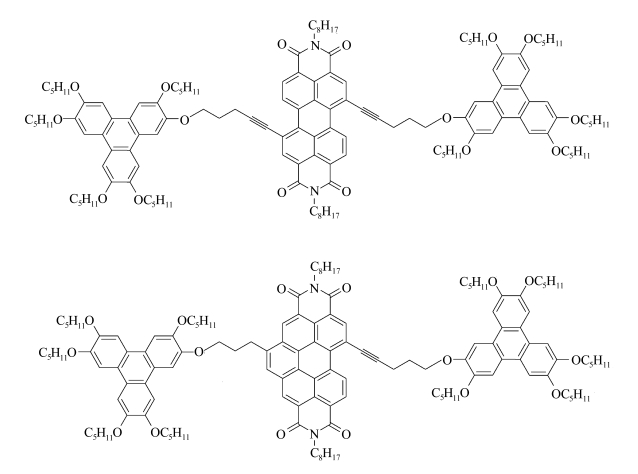
赵可清等还通过Sonogashira偶合和环合反应合成了一系列的苯并菲为电子给体,苝二酰亚胺为电子受体的(D-A-D)三聚体(图 15)[46]。所有的三聚体会自组装形成层形柱状倾斜相,由于有效的分子自主排序,能形成高度分离的给体-受体(D-A)异质结结构。第一次通过富电子的苯并菲作为空穴瞬态通路和六苯并苯二酰亚胺堆叠形成电子传输通道,在分子水平上实现和证明所谓的p-n异质结。
|
图 15 苯并菲-苝二酰亚胺三聚体 Fig.15 Triphenylene-perylene bisimide triads |
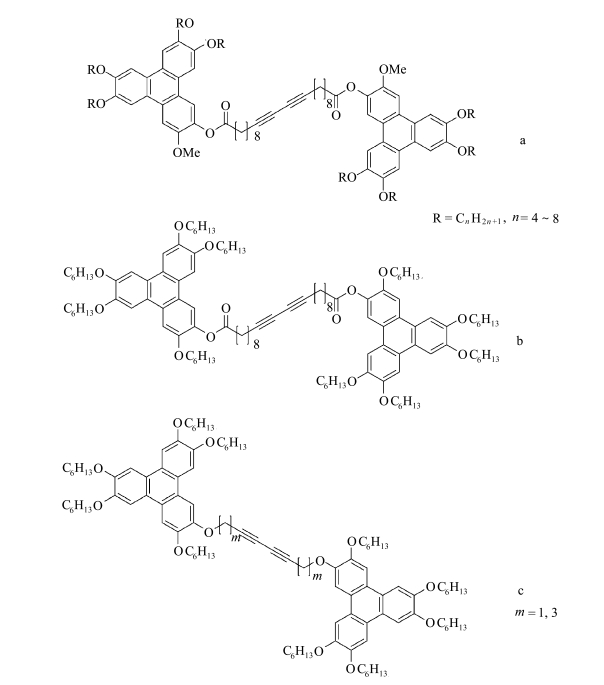
冀虹等[47]通过铜盐催化Eglinton偶联反应合成了二乙炔桥连的苯并菲盘状液晶二聚体化合物(图 16)。差示扫描量热法(DSC)和热台偏光显微镜(POM)对其介晶性进行研究发现,图 16所示二聚体a在结构上与柔性链接的二聚体的差别仅在于,前者中心桥链含有刚性的二乙炔基, 碳碳叁键具有更大的电子云密度和可极化性,从而增强了分子间π-π相互作用和偶极相互作用,有利于分子的柱状有序堆积。图 16所示二聚体化合物b中苯并菲介晶基元是直接通过丁二炔基相连,桥链是全刚性的共轭二炔结构,分子形状可以近似为“哑铃型”,而非“盘状”, 不利于分子的有序堆积,出现有序度低的向列相。而图 16中二聚体c的苯并菲介晶基元是通过醚键连接基与碳碳叁键相连,适当降低了桥链刚性,有利于分子芳核的有序堆积和柱内运动,具有更稳定的柱状相。
|
图 16 二乙炔桥连的苯并菲盘状液晶二聚体化合物 Fig.16 Acetylene connective triphenylene discotic liquid crystal dimers |
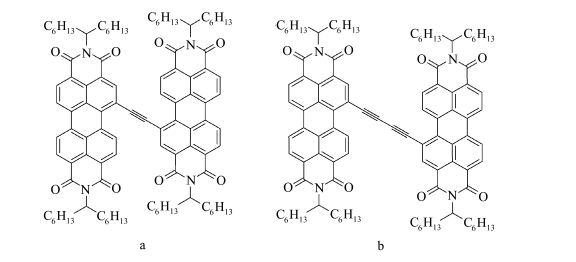
Myshkostupov等[48]合成了如图 17中2个具有代表性的阶梯式的乙炔桥苝二酰亚胺(PDI)二聚体化合物。为了增加二聚体溶解性,在酰亚胺氮位引入了1-己丁基为增溶基团。在此基础上Jumper等[49]对图 17中化合物a的光学性质和分子内能量转移机制进行了深入的研究。发现较短的分子间距离使得其吸收光谱与单体相比较出现了显著的蓝移,且荧光量子产率急剧降低,表明在单体之间存在激子耦合。
|
图 17 乙炔桥苝二酰亚胺二聚体 Fig.17 Acetylene connective perylene bisimide dimers |
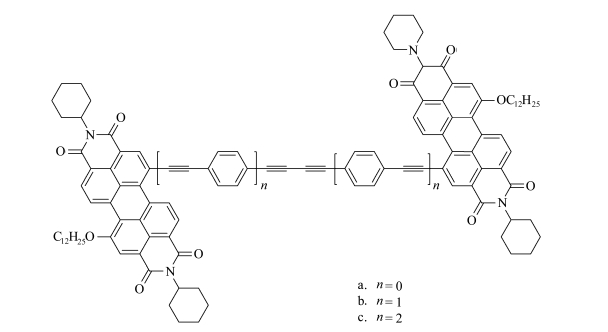
Shi等[50]合成了如图 18所示的苯-炔刚性桥链接的苝二酰亚胺二聚体化合物,发现共轭连接的二聚体a的吸收峰(λmax=534 nm)发生了显著的蓝移,而拥有更长共轭桥链的化合物b和c吸收峰未发生蓝移,因此可知,在化合物b和c的单体间并没有产生联系,因此表现出了与苝二酰亚胺(PBI)单体相似的吸收光谱。此外,化合物a的荧光量子产率急剧降低,化合物b和c则显示出较高值。
|
图 18 苯-炔刚性桥链接的苝二酰亚胺二聚体化合物 Fig.18 Benzene-acetylene rigid connective perylene bisimide dimers |
高分子液晶是将液晶基元通过化学键连接而形成的高分子,兼有液晶的光电性和高分子的稳定性的优点。单取代侧链液晶聚炔由于含有功能性侧链,在电学、光学等领域具有广阔的应用前景[51]。
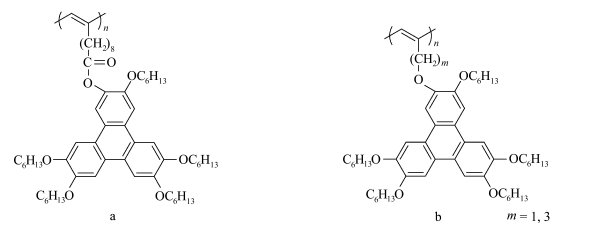
唐本忠课题组[52]通过调节间隔基到聚炔主链上的键长度,利用Rh(nbd)2Cl2/Et3N催化体系在四氢呋喃溶液中成功地将单体聚合,得到图 19所示聚合物分子a,易溶于常规的有机溶剂、分子量很高,产率能高达84%。所有的聚合物均具有非常高的热分解温度,加热到300 ℃无任何的分解。含4个碳的尾链型的苯并菲呈现的是六方柱状相,而间隔基长度为5个碳的亚甲基时聚合物的X射线衍射峰最为尖锐,相应的形成了混合的柱状液晶相。研究发现烷基链的长度对苯并菲类聚合物的结构和液晶基元的堆砌有重要的影响。
|
图 19 单取代侧链盘状液晶聚炔 Fig.19 Monosubstituted side-chain liquid crystalline polyacetylenes |
Yu等[53]研究了图 19中所示类似结构的分子b,单体通过催化剂[Rh(nbd)Cl]2聚合,聚合后的分子热稳定和结构稳定性均增强,热分解温度高达340 ℃以上,这么高的分解温度可能是因为侧链苯并菲介晶基元体积较大,能够在刚性的主链周围形成“甲壳效应”,单体和聚合物自组装成六方柱状相。
4 总结与展望本文主要介绍含炔基结构的盘状液晶及各类中心核和二聚体引入炔基修饰后盘状液晶分子的介晶性和半导体性质的显著变化,以及聚炔类盘状液晶聚合物的研究进展。虽然距发现盘状液晶已经40多年,已报道的化合物数千种,但含有炔基的盘状液晶仍是一个新兴领域。目前盘状液晶材料领域存在的主要问题包括如何提升盘状液晶柱状相的有序度、改善盘状液晶的成膜性能等。本文综述了含炔基的盘状液晶分子的性质特点,为解决目前盘状液晶分子存在的问题, 也为今后盘状液晶分子设计的新思路提供了参考。
| [1] | Chandrasekhar S, Sadashiva B K, Suresh K A. Liquid crystals of disc-like molecules[J]. Pramana, 1977, 9(5): 471–480. DOI:10.1007/BF02846252 |
| [2] | Brédas J L, Beljonne D, Coropceanu V, Cornil J. Charge-transfer and energy-transfer processes in π-conjugated oligomers and polymers:a molecular picture[J]. Chemical Reviews, 2004, 104(11): 4971–5001. DOI:10.1021/cr040084k |
| [3] | Geelhaar T, Griesar K, Reckmann B. 125 Years of liquid crystals-a scientific revolution in the home[J]. Angewandte Chemie International Edition, 2013, 52(34): 8798–8809. DOI:10.1002/anie.201301457 |
| [4] | Bremer M, Kirsch P, Klasen-Memmer M, Tarumi K. The TV in your pocket:development of liquid-crystal materials for the new millennium[J]. Angewandte Chemie International Edition, 2013, 52(34): 8880–8896. DOI:10.1002/anie.201300903 |
| [5] | Kumar S. Design concepts and synthesis of discotic liquid crystals[J]. Handbook of Liquid Crystals, 2014, 26(4): 467–520. |
| [6] | Bushby R J, Boden N. Responses of discotic liquid crystals to mechanical, magnetic, and electrical fields[J]. Handbook of Liquid Crystals, 2014, 26(5): 569–602. |
| [7] |
陈树森, 李田, 赵达慧. 盘状液晶材料的研究进展[J]. 物理化学学报, 2010, 26(4): 1124–1134.
Chen S S, Li T, Zhao D H. Progress in discotic liquid crystalline materials[J]. Acta Physico-Chimica Sinica, 2010, 26(4): 1124–1134. |
| [8] | Monika G, Santanu K P. Triphenylene-based room-tempe-rature discotic liquid crystals:a new class of blue-light-emitting materials with long-range columnar self-assembly[J]. Langmuir, 2016, 32(4): 1120–1126. DOI:10.1021/acs.langmuir.5b03353 |
| [9] | Yu Z Q, Lam J W Y, Zhao K Q, Zhu C Z, Yang S, Lin J S, Li B S, Liu J H, Chen E Q, Tang B Z. Mesogen jacketed liquid crystalline polyacetylene containing triphenylene discogen:synthesis and phase structure[J]. Polymer Chemistry, 2013, 4(4): 996–1005. DOI:10.1039/C2PY20535A |
| [10] | Yang H, Lü Y J, Xu M, Wang J, Lin B P, Guo L X, Chen E Q. Poly(vinyl benzoate)-backbone mesogen-jacketed liquid crystalline polymers[J]. Polymer Chemistry, 2016, 37(6): 6709–6719. |
| [11] |
李衡峰, 刘克刚, 王侃, 闻建勋. 含1, 3, 2-二氧硼杂环的二苯乙炔类液晶的合成与相变研究[J]. 液晶与显示, 2001, 16(3): 176–180.
Li H F, Liu K G, Wang K, Wen J X. Synthesis and mesomorphic properties of tolane-type liquid crystals containing a 1, 3, 2-dioxaborinane ring[J]. Chinese Journal of Liquid Crystals and Displays, 2001, 16(3): 176–180. |
| [12] | Rego J A, Kumar S, Ringsdorf H. Synthesis and characterization of fluorescent, low-symmetry triphenylene discotic liquid crystals:Tailoring of mesomorphic and optical properties[J]. Chemistry of Materials, 1996, 8(7): 1402–1409. DOI:10.1021/cm950582x |
| [13] | Kumar S, Varshney S K, Chauhan D. A room-temperature discotic nematic liquid crystal[J]. Molecular Crystals and Liquid Crystals, 2003, 396(1): 241–250. DOI:10.1080/15421400390213573 |
| [14] | Kouwer P H J, Jager W F, Mijs W J, Picken S J. Specific interactions in discotic liquid crystals[J]. Journal of Materials Chemistry, 2003, 13(3): 458–469. DOI:10.1039/b208923h |
| [15] | Grafe A, Janietz D, Frese T, Wendorff J H. Star-shaped discotic oligomesogens based on radial pentakisphenylethynylbenzene moieties[J]. Chemistry of Materials, 2005, 17(20): 4979–4985. DOI:10.1021/cm051042v |
| [16] | Varshney S K, Takezoe H, Rao D S. Discotic liquid crystals:synthesis and characterization of radial polyalkynylbenzene derivatives[J]. Bulletin of the Chemical Society of Japan, 2008, 81(1): 163–167. DOI:10.1246/bcsj.81.163 |
| [17] | Lee S L, Lin H A, Lin Y H, Chen H H, Liao C T, Lin T L, Chu Y C, Hsu H F, Chen C, Lee J J. Gearing of molecular swirls:columnar packing of nematogenic hexakis(4-alkoxyphenyl-ethynyl)benzene derivatives[J]. Chemistry-A European Journal, 2011, 17(3): 792–799. DOI:10.1002/chem.v17.3 |
| [18] | Hennrich G, Cavero E, Barbera J, Gomez L B, Hanes R E, Talarico M, Golemme A, Serrano J L. Optoelectronic devices based on mesomorphic, highly polarizable 1, 3, 5-trisalkynyl benzenes[J]. Chemistry of Materials, 2007, 19(25): 6068–6070. DOI:10.1021/cm702617v |
| [19] | Ryu M H, Choi J W, Cho B K. Design synthesis and self-assembly behavior of C3-symmetry discotic molecules via click chemistry[J]. Journal of Materials Chemistry, 2010, 20(9): 1806–1810. DOI:10.1039/b921685e |
| [20] | Fischer M, Lieser G, Rapp A, Schnell I, Mamdouh W, Feyter S, Schryver F C, Höger S. Shape-persistent macrocycles with intraannular polar groups:synthesis, liquid crystallinity, and 2D organization[J]. Journal of the American Chemical Society, 2004, 126(1): 214–222. DOI:10.1021/ja038484x |
| [21] | Seo S H, Jones T V, Seyler H, Peters J O, Kim T H, Chang J Y, Tew G N. Liquid crystalline order from orthophenylene ethynylene macrocycles[J]. Journal of the American Chemical Society, 2006, 128(29): 9264–9265. DOI:10.1021/ja060354b |
| [22] | Li T, Yue K, Yan Q, Huang H, Wu H, Zhu N, Zhao D. Triangular arylene ethynylene macrocycles:syntheses, optical, and thermotropic liquid crystalline properties[J]. Soft Materials, 2012, 8(8): 2405–2415. DOI:10.1039/c2sm06144a |
| [23] | Fritzsche M, Bohle A, Dudenko D, Baumeister U, Sebastiani D, Richardt G, Spiess H W, Hansen M R, Höger S. Empty helical nanochannels with adjustable order from low symmetry macrocycles[J]. Angewandte Chemie International Edition, 2011, 50(13): 3030–3033. DOI:10.1002/anie.201007437 |
| [24] | Luo J, Yan Q, Zhou Y, Li T, Zhu N, Bai C, Cao Y, Wang J, Pei J, Zhao D. A photoswitch based on self-assembled single microwire of a phenyleneethynylene macrocycle[J]. Chemical Communications, 2010, 46(31): 5725–5727. DOI:10.1039/c0cc00739k |
| [25] | Kato S, Takahashi N, Tanaka H, Kobayashi A, Yoshihara T, Tobita S, Yamanobe T, Uehara H, Nakamura Y. Tetraalkoxyphenanthrene-fused dehydroannulenes:synthesis, self-assembly, and electronic, optical, and electrochemical properties[J]. Chemistry-A European Journal, 2013, 19(36): 12138–12151. DOI:10.1002/chem.201301262 |
| [26] | Vollmeyer J, Baumeister U, Höger S. The influence of intraannular templates on the liquid crystallinity of shape-persistent macrocycles[J]. Beilstein Journal of Organic Chemistry, 2014, 10(1): 910–920. |
| [27] | Höger S, Weber J, Leppert A, Enkelmann V. Shape persistent macrocycle with intraannular alkyl groups:some structural limits of discotic liquid crystals with an inverted structure[J]. Beilstein Journal of Organic Chemistry, 2008, 4(1): 1–8. |
| [28] | Li Q, Huang R, Xiong S, Xie X. Synthesis, mesophase behaviour and design principles for discotic liquid crystals of phenyl ethynylene macrocycles with intraannular flexible chains[J]. Liquid Crystals, 2012, 39(2): 249–258. DOI:10.1080/02678292.2011.636843 |
| [29] | Andrew N C, Hemant G. Synthesis and liquid crystal properties of mixed alkynyl-alkoxy-triphenylenes[J]. Liquid Crystals, 2009, 36(8): 809–816. DOI:10.1080/02678290903063000 |
| [30] | Wang D, Mi Y S, Tang J K, Liang P X, Jin Z K, Yang Z, Yang H. Disk-shaped symmetric hexa-substituted triphenylene derivatives:synthesis, physical properties and self-assembly[J]. Chemical Research in Chinese Universities, 2013, 29(3): 495–499. DOI:10.1007/s40242-013-2288-3 |
| [31] | Stackhouse P J, Hird M. Influence of branched chains on the mesomorphic properties of symmetrical and unsymmetrical triphenylene discotic liquid crystals[J]. Liquid Crystals, 2008, 35(5): 597–607. DOI:10.1080/02678290802040026 |
| [32] | Stackhouse P J, Hird M. Influence of acetylene-containing peripheral chains on the mesomorphic properties of triphenylene based liquid crystals[J]. Liquid Crystals, 2009, 36(9): 953–965. DOI:10.1080/02678290903165490 |
| [33] | Varshney S K, Takezoe H, Prasad V, Rao D S S. π-Conjugated triphenylene twins exhibiting polymesomorphism including the nematic phase[J]. Molecular Crystals and Liquid Crystals, 2009, 515(1): 16–38. DOI:10.1080/15421400902987677 |
| [34] | Cammidge A N, Gopee H. Synthesis and liquid crystal properties of mixed alkynyl-alkoxy-triphenylenes[J]. Liquid Crystals, 2009, 36(8): 809–816. DOI:10.1080/02678290903063000 |
| [35] |
赵可清, 周慧, 余文浩, 胡平, 汪必琴, 物部浩达, 清水洋. 官能化苯并菲盘状液晶的合成及不饱柔链对介晶性的影响[J]. 中国科学B辑:化学, 2011, 41(10): 1565–1574.
Zhao K Q, Zhou H, Yu W H, Hu P, Wang B Q, Monobe Hirosato, Shimizu Yo. Synthesis of functionalized triphenylene discotic liquid crystals and the influence of unsaturated periphery on mesomorphism[J]. Science in China(Series B), 2011, 41(10): 1565–1574. |
| [36] | Hoang M H, Cho M J, Kim K H, Lee T W, Jin J I, Choi D H. Semiconducting 2, 3, 6, 7, 10, 11-hexakis{[4-(5-dodecylthiophen-2-Yl)phenyl]ethynyl}triphenylene and its discotic liquid crystalline properties[J]. Chemistry Letters, 2010, 39(4): 396–397. DOI:10.1246/cl.2010.396 |
| [37] | Fechtenktter A, Tchebotareva N, Watson M, Müllen K. Discotic liquid crystalline hexabenzocoronenes carrying chiral and racemic branched alkyl chains:supramolecular engineering and improved synthetic methods[J]. Tetrahedron, 2001, 57(17): 3769–3774. DOI:10.1016/S0040-4020(01)00252-6 |
| [38] | Dössel L F, Kamm V, Howard I A, Laquai F, Pisula W, Feng X, Li C, Takase M, Kudernac T, Feyter S. Synthesis and controlled self-assembly of covalently linked hexaperi-hexabenzo-coronene/perylene diimide dyads as models to study fundamental energy and electron transfer processes[J]. Journal of the American Chemical Society, 2012, 134(13): 5876–5886. DOI:10.1021/ja211504a |
| [39] | Mativetsky J M, Kastler M, Savage R C, Gentilini D, Palma M, Pisula W, Müllen K, Samorì P. Self-assembly of a donor-acceptor dyad across multiple length scales:functional architectures for organic electronics[J]. Advanced Functional Materials, 2009, 19(15): 2486–2494. DOI:10.1002/adfm.v19:15 |
| [40] | Ruchika M, Jong M L, Minjung S, Piyush P. Tuning the electronic nature of mono-bay alkynyl-phenyl substituted perylene bisimides:synthesis, structure, and photophysical properties[J]. Chemistry-A European Journal, 2014, 20(19): 5776–5786. DOI:10.1002/chem.201400099 |
| [41] | Belviso S, Amati M, Rossano R, Crispini A, Lelj F. Non symmetrical aryl-and arylethynyl-substituted thioalkyl-porphyrazines for optoelectronic materials:synthesis, properties, and computational studies[J]. Dalton Transactions, 2015, 44(5): 2191–2207. DOI:10.1039/C4DT03317E |
| [42] | Kayal H, Ahmida M, Dufour S, Taing H, Eichhorn S H. Cross-linking of discotic tetraazaporphyrin dyes in 2 and 3 dimensions by "click" chemistry[J]. Journal of Materials Chemistry C, 2013, 1(42): 7064–7072. DOI:10.1039/c3tc31588f |
| [43] | Kumar S, Varshney S K. Design and synthesis of discotic nematic liquid crystals[J]. Organic Letters, 2002, 4(2): 157–159. DOI:10.1021/ol010200v |
| [44] |
赵可清, 周慧, 余文浩, 汪必琴.钯催化偶联反应合成刚性桥连的苯并菲盘状液晶二聚体[J].化学学报, 2011, 69(16):1895-1902.
Zhao K Q, Zhou H, Yu W H, Wang B Q, Hu P. Palladium catalyzed homo-coupling reaction for the synthesis of rigid-spacer connected discotic liquid crystal dimers with triphenylene mesogens[J]. Acta Chimica Sinaca, 2011, 69(16):1895-1902. http://kns.cnki.net/KCMS/detail/detail.aspx?filename=hxxb201116009&dbname=CJFD&dbcode=CJFQ |
| [45] | Ji H, Zhao K, Yu W, Wang B, Hu P. Synthesis and mesomorphism of diacetylene-bridged triphenylene discotic liquid crystal dimers[J]. Science in China Series B-Chemistry, 2009, 52(7): 975–985. DOI:10.1007/s11426-009-0003-5 |
| [46] | Zhao K Q, An L L, Zhang X B, Yu W H, Hu P, Wang B Q, Xu J, Zeng Q D, Hirosato M, Yo S, Beno H, Bertrand D. Highly segregated lamello-columnar mesophase organizations and fast charge carrier mobility in new discotic donor-acceptor triads[J]. Chemistry-A European Journal, 2015, 21(8): 10379–10390. |
| [47] |
冀虹, 赵可清, 余文浩. 二乙炔桥连苯并菲盘状液晶二聚体的合成及其介晶性[J]. 中国科学B辑:化学, 2008, 38(12): 1088–1099.
Yi H, Zhao K Q, Yu W H. Link the two acetylene benzene and thin disk synthesis and crystal of liquid crystal dimers[J]. Science in China(Series B), 2008, 38(12): 1088–1099. |
| [48] | Myahkostupov M, Prusakova V, Oblinsky D G. Structural refinement of ladder-type perylenediimide dimers:a classical tale of conformational dynamics[J]. The Journal of Organic Chemistry, 2013, 78(17): 8634–8644. DOI:10.1021/jo401348w |
| [49] | Jumper C C, Anna J M, Stradomska A. Intramolecular radiationless transitions dominate exciyion relaxation dynamics[J]. Chemical Physics Letters, 2014, 599(4): 23–33. |
| [50] | Shi Y, Wu H, Xue L, et al. Synthesis and properties of perylenetetracarboxylic diimide dimers linked at the bay position with conjugated chain of different length[J]. Journal of Colloid and Interface Science, 2012, 365(1): 172–177. DOI:10.1016/j.jcis.2011.09.036 |
| [51] | Liu K P, Zhen Q Y, Liu J H, Chen E Q. Molecular shapes of monosubstituted poly-acetylenes in their liquid crystalline phases macromol[J]. Chemical Physics, 2009, 210(4): 707–716. |
| [52] | Xing C M, Jacky W Y L, Zhao K Q, Tang B Z. Synthesis and liquid crystalline properties of poly (1-alkyne)s carrying triphenylene discogens[J]. Polymer Chemistry, 2008, 46(9): 2960–2974. DOI:10.1002/(ISSN)1099-0518 |
| [53] | Yu Z Q, Jacky W Y L, Zhao K Q, Zhu C Z, Yang S, Lin J S, Li B S, Liu J H, Chen E Q, Tang B Z. Mesogen jacketed liquid crystalline polyacetylene containing triphenylene discogen:synthesis and phase structure[J]. Polymer Chemistry, 2013, 4(4): 996–1005. DOI:10.1039/C2PY20535A |




