碳量子点(carbon quantum dots,CQDs)是一种新型的碳纳米材料,也称为碳点、碳纳米点、碳纳米晶,是尺寸大小在10 nm以下的、单分散的、几何形状近乎准球型的一种新兴碳纳米功能材料。它与其它碳纳米材料(如富勒烯、碳纳米管和石墨烯[1]等)一样备受研究者关注。传统的半导体量子点和有机染料缺点明显:制备方法繁琐、价格昂贵、环境不友好、易发生光漂白等。而荧光碳量子点价格低廉、容易制备、粒径小、水溶性好、化学惰性高、易于功能化、耐光漂白、低毒性,并且在修饰后有一定的生物相容性;尤其是CQDs具有吸收光子能量低于发射光子能量的上转换发光特性,使其在荧光探针成像、生物荧光标记和防伪等领域有着广阔的应用前景。
2004年,Scrivens小组[2]进行纯化单壁碳纳米管的电泳实验过程中,意外得到了这种具有荧光性质的产物,即荧光碳量子点。2006年,Xu等[3]利用激光消融的方法制备了粒子尺寸很小的纳米粒子,然后用聚合物PEG1500N进行钝化,得到了可见光区域可调的荧光物质。之后的众多研究者利用不同的方法和不同的原料制备了结构、组成相似或有差异的一系列的CQDs,并对其进行了修饰,例如结合金属粒子、金属化合物、有机聚合物、元素沉积和包覆等,丰富了CQDs在生物科学、化学科学和物理科学方向的新应用。在本文中,我们总结了在CQDs领域的研究进展,重点对其上转换发光机理、影响因素(合成方法、尺寸控制、表面功能化和掺杂)和应用进行了深入的探讨。1性能和发光机理
1 性能和发光机理 1.1 光学性质 1.1.1 光稳定性绝大部分有机荧光染料随光照时间的增加其荧光发光强度会逐渐减弱。而碳量子点具有良好的光稳定性,Zhao等[4]发现,碳量子点在激光持续照射数小时后,其荧光强度基本不发生变化,也不会发生光漂白和光眨眼等。
1.1.2 上转换发光(Up Conversion Photoluminescence, UCPL)上转换发光是指在长波长激发光的激发下,体系发出短波长光子的现象,即辐射光子能量大于所吸收的光子能量,这属于反斯托克斯现象。上转换荧光性质使CQDs的很多应用都得到了开发和保障。Jia等[5]通过一步法合成了具有上转换荧光性质的CQDs,并解释CQDs的上转换荧光性质可能来源于多光子过程,即同时吸收2个或多个光子。Li等[6]对碱辅助电化学氧化石墨得到的CQDs进行光学性质研究,得到了波长500~1000 nm激发的CQDs荧光光谱(如图 1)。发射峰位置从325 nm红移到425 nm,表现出了明显的上转换荧光性质。他们认为CQDs的这种具有上转换荧光的性质是多光子活性过程,这与上边报道的一致。其他的一些研究团队也通过不同的方法制备了一系列的具有上转换荧光的CQDs,他们也基本认同这是多光子的活性过程。
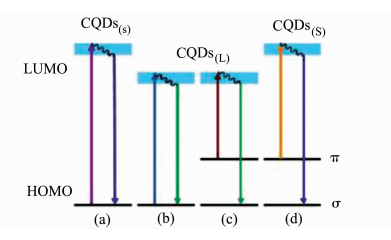
Shen等[7]则认为多光子的活性过程不足以解释CQDs的上转换荧光性质。他们制备的石墨烯量子点在激发波长为600~800 nm时,发射波长为390~468 nm。他们注意到上转换激发波长和发射波长所对应的能量差为1.1 eV。图 2为石墨烯各种典型电子跃迁过程示意图。作者假设碳量子点中有两个基态轨道,为π和δ轨道。当受到光的激发时,π轨道上的电子跃迁到最低未占据轨道(LUMO),然后电子再跃迁回低能级轨道,若跃迁回δ轨道(最高占据轨道HOMO),则发生上转换荧光现象。如果δ轨道上的电子受到激发,那么电子会跃迁回δ轨道,则会产生下转换荧光现象。这就可以解释上转换荧光发射中激发波长和发射波长的能量差为一个常数的原因。
|
图 2 参考文献[7]中石墨烯量子点的电子转移机理图:石墨烯小尺寸(a)和大尺寸(b)的正常发光机制;石墨烯大尺寸(c)和小尺寸(d)的上转换发光机制 Fig.2 A schematic illustration of various typical electronic transitions processes of CQDs in reference [7]: normal PL mechanisms in CQDs for small size(a) and large size(b); UCPL mechanisms in CQDs for large size(c)and small size(d) |
同时也有研究报道CQDs的上转换发光来自于正常的光致发光,它是由荧光分光光度计中单色仪的二次衍射波激发而产生的。通过在荧光分光光度计的激发路径上添加一个合适的长通滤波器就可以消除CQDs的上转换现象。所以,当研究CQDs的上转换发光特性时,需要排除正常荧光的干扰。CQDs的上转换荧光特性使其在能源领域的光催化设计、生物成像以及防伪油墨方面有良好的应用。
1.1.3 电致发光电化学发光主要取决于表面态的跃迁,而光致发光依赖于核的状态。Zheng等[8]发现CQDs在330 nm波长激发下,光致发光的CQDs发射峰在455 nm,而电化学发光的CQDs的发射峰位置在535 nm处,发生了红移现象。若CQDs表面不存在缺陷,则表面发光应与核的发光一样,电化学发光应与光致发光类似,而Zheng等制备的CQDs的电化学发光和光致发光的发射峰的位置不同,说明实验合成的CQDs的表面存在缺陷。
1.2 发光机制由于制备方法和材料不同等原因,影响CQDs荧光性质的因素是多种多样的,有尺寸、表面缺陷、激发波长、温度、pH等。碳量子点上转换发光有常见的两种机制:反斯托克斯光致发光和多光子机制[9, 10]。也可以分为发射波长依赖激发波长和不依赖激发波长两种。其中前者CQDs与其他荧光体的区别在于其发射波长由激发波长决定;后者的独立激发荧光行为表明CQDs的荧光特性主要依赖CQDs的表面状态[11]。如Zhou等[12]用激光刻蚀MWCNTs制备了碳量子点,其荧光激发行为由激发波长决定;而刻蚀石墨制备的碳量子点,其荧光激发行为却不随激发波长变化。这说明CQDs有多个发光中心,这些发光中心可能来自于CQDs自身的结构,也可能是由制备过程中引入的表面官能团促使产生的。研究CQDs的发光机理有助于我们优化CQDs的合成条件、制备出性能最优的CQDs,同时对于荧光CQDs应用的研究也有重要的理论指导意义。
2 影响上转换发光的因素根据上转换碳量子点的发光机制,对于激发波长依赖的CQDs,激发波长的改变将使发射波长峰值改变,如发生红移。对于发射波长不受激发波长影响的CQDs,其制备方法和后处理将会直接影响上转换荧光现象。
2.1 碳量子点的制备方法在过去十年中已经提出了许多制备CQDs的方法,大致可以分为自上而下和自下而上的方法,它们可以在制备或后处理过程中被修改。自上而下的合成法由于含碳前体很难被完全剥离和切割,所以产率不高。自下而上的合成法是碳化一些小分子的含碳前体(如柠檬酸、葡萄糖、丙三醇等)来合成CQDs,如微波法、化学氧化法、模板合成法等,这类制备方法产率较高。章燕清[13]采用一锅合成法,以CCl4作为碳源、NaNH2作为脱氯剂和N源制备的N掺杂荧光碳量子点,在700~900 nm的激发光下有明显的上转换荧光现象,由于N含量不同,发射光峰值随之变化。N掺杂碳量子点的这种上转换发光性质最适合用多光子机制来解释。何玉珩等[14]采用一步水热法,以葡萄糖为碳源制备出了同时具有上下转换荧光现象的水溶性碳量子点,在激发波长为757~775 nm时,CQDs的最大发射峰基本都在440 nm左右,说明其不受激发光影响,这可能与制备过程的温度和反应物浓度有关。
2.2 尺寸控制CQDs并不是大小确定的,而是分布在某一范围内的小于10 nm的准球型粒子。根据文献报道[15, 16],由于量子限域效应,较大尺寸碳量子点的荧光发射波长较长。因此,为研究特定的应用和机理,通过控制CQDs的大小以获得均匀的性质十分重要。近年来已经提出了许多方法来得到均匀的CQDs。如Kwon等[17]利用反胶束团作为纳米反应器制备了高荧光性的石墨化的CQDs,其尺寸大小由胶团的大小决定。Bao等[18]利用电化学刻蚀碳纤维制备了CQDs,通过控制电位,不需要进一步的分离或者钝化即得到了发蓝光的CQDs。电压越高,电解过程中碳纤维表面越粗糙,所得CQDs的尺寸越小。根据不同的合成方法,影响CQDs尺寸的因素也不同,如碳源、反应条件、后处理等。
3 功能化采用水热法等方法制备的CQDs一般无荧光或荧光量子产率较低(大部分都不高于10%),不能满足应用(如用于荧光标记或生物成像)所需条件,所以提高CQDs的荧光产率以及光学稳定性成为许多学者研究的重点。
3.1 表面修饰表面修饰是一种可靠的方法,修饰原理为:在CQDs表面引入一些特定基团、分子或贵金属,填补CQDs表面的缺陷或使CQDs表面产生能量势阱,使荧光发射更稳定,从而提高荧光产率。此外,一般情况下合成的CQDs表面存在羧基,故可引入氨基或巯基等基团以增加CQDs水溶性,从而更好地应用于生物学研究。CQDs的表面修饰主要包括含氧基团的修饰、含氮基团的修饰、含硫基团的修饰、有机分子的修饰以及贵金属的修饰。
3.1.1 基团的修饰CQDs表面经含氧基团的修饰后,其表面态发生了变化,导致电子空穴对的辐射复合和表面发射势肼,进而影响CQDs的性能,同时增强了CQDs的亲水性,可以更好地应用于生物检测、分析[19]等方面。Zheng等[20]将制得的CQDs用硼氢化钠进行还原,使其表面的羰基还原为羟基。经过修饰后的CQDs粒径不变,但荧光量子产率从2%提高到24%,最大吸收波长从520 nm移至450 nm。
CQDs表面经含氮基团的修饰,能够使发光颜色发生改变,且荧光强度也会增强,有利于提高荧光量子产率,进而使其得到更广泛的应用。Barman等[21]以柠檬酸和EDTA为碳源,在170 ℃下加热1 h,水热法合成表面含氮基团修饰的CQDs,其荧光量子产率高达64%,CQDs表面含氮基团的存在对反应起到加快的催化作用。该CQDs有望应用于太阳能电池或者光电设备。
CQDs表面经过含硫基团的修饰后,其荧光量子产率会得到提高,并且荧光最大吸收峰的位置会发生红移。Sun等[22]以头发为碳源与浓硫酸混合后,经超声、搅拌提纯制备出表面有含硫基团的CQDs,硫的含量与反应湿度在一定程度上成正比例关系,且含硫量高的CQDs其荧光光谱的最大吸收峰较普通CQDs出现在长波长处。
3.1.2 分子的修饰学者们研究发现,CQDs表面经有机分子或聚合物修饰后,表面态发生变化形成一个新的能级,能够导致激发电子势阱增加,电子和空穴进行复合的机会变大,可能弥补了CQDs的表面缺陷,进而导致荧光量子产率和荧光强度的增加。
Wang等[23]以无水柠檬酸为碳源,长链氨基硅烷为修饰剂合成了硅烷功能化的CQDs,其量子产率高达47%。Xu等[3]通过激光法制备的CQDs本身不具有荧光性,但是经过PEG1500N在CQDs表面的修饰后具有了高强度的荧光。
3.1.3 贵金属的修饰金属修饰CQDs的原理是:金属离子与CQDs表面的羧基等基团发生作用,通过加入还原剂将金属离子还原成金属原子,从而使金属包裹在CQDs表面。经修饰的CQDs具有更强的荧光性能,广泛应用于光催化剂等领域,但是由于修饰后的CQDs粒径普遍偏大,不适用于生物等方面的应用。
Tian等[24]将CQDs与金属离子溶液混合后加入柠檬酸,制得了铜、银、铅修饰的CQDs,与修饰前的CQDs相比具有更高的荧光量子产率。Cao等[25]将金属金和铂包覆在CQDs表面,用作光催化剂,已成功将二氧化碳还原为甲酸、甲醛和甲醇等,并可以将水氧化为氧气,为解决二氧化碳升高的问题提供了新的思路。
综上所述,对于CQDs的修饰,我们可以根据CQDs的应用需要来选择,如将CQDs作为荧光剂制备荧光防伪油墨,主要要增加荧光量子产率和加大吸收波范围,所以采用含氮修饰是不错的选择。
3.2 表面改性表面改性是一种为了特定的应用而调整材料表面性能的有效方法。CQDs通过表面化学或交互的方法实现表面功能化有很多方法,如共价键、溶剂协调、π-π键相互作用、溶胶凝胶技术。大多数的CQDs含氧基团丰富,表面钝化剂通过含胺共价键结合是提高CQDs发光的常用方法,这表明表面改性对CQDs性能的重要影响。除了共价键结合到CQDs,加入协调溶剂是另一个有用的改性方法。Wang等[26]报道了在1 min内用有机硅烷作为一个协调溶剂合成高发光(量子点产率为47%)的非晶碳量子点的方法。
3.3 掺杂掺杂是一种广泛用以调节光致发光材料的发光性能的方法。如已报道的用N、S、P来调整CQDs的性质。N掺杂是较常用的通过诱导在导带中的费米能级和电子的上移来提高CQDs发射的方法。它表明氮碳键确实能提高CQDs发光。N-CQDs证实氮含量依赖PL强度多色和双光子上转换特性。Li等[27]研究了Mg/N共掺杂的方法制备量子点产率为83%的高发光量子点。P和N掺杂的CQDs是通过在磷酸存在下微波辐射的方法合成的。这些量子点具有良好的光致发光特性与较高的氧还原反应的电催化活性。
4 应用 4.1 生物医学碳量子点上转换发光特性的发现,突破了其在生物成像领域的限制,极大地扩展了碳量子点的应用范围。CQDs已应用于多种细胞的转染成像,Gong等[28]制备的CQDs己成功应用于人体乳腺癌细胞BCap-37以及正常乳腺细胞化Hs-578的成像。Goh等[29]制备的PEG钝化的CQDs结合玻璃尿酸(HA)形成HA-Cdot进行活体生物成像。同时,Sun研究小组[30]也完成了将CQDs的生物成像做到活体内的实验。其他研究者利用CQDs优良的发光性质进行了不同细胞的成像实验[31-35]。同时利用CQDs的上转换荧光效应进行生物成像的案例也并不鲜见,因为使用近红外光激发(800~900 nm)实现碳点的双光子细胞成像,有助于消除细胞自体荧光的干扰[36]。如Cao等[37]采用激光刻蚀法合成了具有上转换荧光性质的CQDs,并利用其上转换荧光对人体乳腺癌细胞进行成像分析;Yang等[38]在880 nm激光的激发下获得了绿色荧光成像图。Zhang等[39]使用C3N4纳米点实现了细胞核的双光子成像。Kong等[36]制备了PH敏感碳点纳米传感器,利用碳点的双光子荧光实现了活细胞和组织成像。双光子激发模式可避免紫外光对细胞核等其他生物组织的损伤。
除了生物成像,具有上转换荧光性能的CQDs在生物医学方面的应用还有很多,如生物传感器、生物医药配送系统等。CQDs传感器可用于葡萄糖、细胞内铜、磷酸盐、铁、钾、pH和核酸的视觉监控。Kim等[40]将功能化的CQDs及与其他分子的复合体作为载体在细胞间实现转染。
4.2 荧光油墨由于CQDs的激发波长改变时,荧光发射波长也会发生改变,这些特点使其成为一种有潜力的新型荧光油墨,有望取代那些传统的油墨用于隐形墨水、信息识别和防伪等。现有的防伪墨水一般为下转换发荧光,利用CQDs的下转换机制制备紫外防伪墨水已经有了很大进展。如Wang的研究组[41]报道了一种水溶性的碳量子点荧光油墨,适合用于纸质基底。Zhu等[42]报道了一种高荧光量子产率的CQDs,并利用这种CQDs水溶液在纸上直接喷墨打印了图案,图案在紫外灯下显示出蓝色,初步证明了这类水溶性CQDs可以用于喷墨打印。因此有理由相信利用有上转换荧光的CQDs来制备近红外防伪墨水是可行的,这将极大丰富防伪墨水的种类,但现有对上转换CQDs的研究还远远不够,今后应在这一方面进行更多的研究。
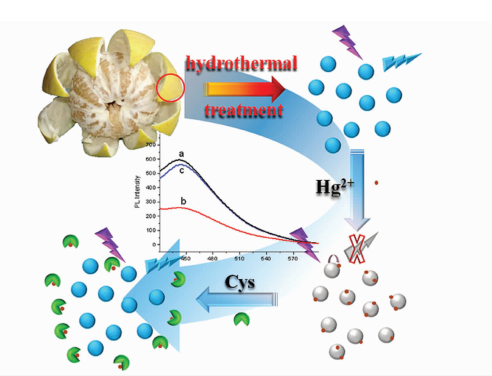
4.3 化学传感器目前,使用CQDs作为荧光探针,基于其下转换荧光实现了对DNA、凝血酶、亚硝酸盐、葡萄糖、pH、Fe3+[43]、Hg2+[44]、Cu2+[45]等的分析检测。随着对CQDs的深入了解,将其上转换荧光特性应用于荧光探针已经有了更多的进展,如Salinas-Castillo等[46]在使用CQDs检测Cu2+过程中充分利用CQDs的上转换突光特性避免了Fe3+的干扰, 增强了其检测的灵敏度,并且显示出低细胞毒性,适合于细胞内传感。
|
图 3 柚子皮为碳源合成碳量子点被Hg2+猝灭以及恢复过程示意图[44] Fig.3 The Hg2+ quenching and recovery process of the CQDs synthesized by the grapefruit peel[44] |
CQDs具有光电荷转移特性以及良好的光稳定性和低的生物毒性,相比其他光催化剂(如TiO2、Fe2O3),CQDs具有明显的上转换光学特性,可以吸收利用可见光和红外光提高光催化效率,很好地降解有机物或高效地产生氢气。Li等[47]将CQDs与传统的光催化剂TiO2结合。TiO2的能带比较大,只有用紫外光才能让其激发,因此对太阳光利用率较低,而由于CQDs的上转换特性,可以更好地利用可见光和红外光部分。利用CQDs催化剂还可以分解一些有机染料(如甲基蓝)。Cao等[25]则提出用金纳米颗粒包裹CQDs,并将它作为一种有效的光催化剂来分解CO2。
4.5 上转换发光碳量子点的其他应用CQDs在光电学领域也有很好的应用,CQDs优异的光稳定性和无毒无害的特性使得它们在染料敏化太阳能电池上显示出极大的应用潜力,目前已有一些研究将CQDs应用于该类电池中。同时CQDs的量子产率也较高,因此可以作为光转化材料用于制造发光器件。
5 总结与展望本文阐述了CQDs领域的最新研究进展,关注了其上转换发光的机理及其应用。通过选择合适的碳源和制备条件来制备具有上转换荧光效应的CQDs,同时通过控制CQDs的尺寸来控制其荧光现象;表面修饰和改性,以及制备方法的恰当选择都是提高量子产率的好方法,如用含氮基团对CQDs进行修饰或者采用有机分子或聚合物等与CQDs掺杂。根据CQDs的上转换性质,其可应用于生物医学、荧光油墨、光催化和化学传感器等领域。如CQDs的上转换特性可以在检测Cu2+时避免Fe3+的干扰,也可以在作光催化剂时增大对太阳光的利用率等。我们期待在不久的将来,可以制备出量子产率更高和尺寸更加均匀的具有上转换荧光现象的CQDs,使其在生产和生活中得到更广泛的应用。
| [1] |
罗妍, 周奕华, 钱俊. 基于喷墨打印石墨烯透明导电薄膜研究进展[J]. 影像科学与光化学, 2016, 31(5): 482–490.
Luo Y, Zhou Y H, Qian J. Development of transparent conductive films based on inkjet-printed graphene[J]. Imaging Science and Photochemistry, 2016, 31(5): 482–490. DOI:10.7517/j.issn.1674-0475.2016.05.482 |
| [2] | Xu X, Ray R, Gu Y, Ploehn H J, Gearheart L, Raker K, Scrivens W A. Electrophoretic analysis and purification of fluorescent single-walled carbon nanotube fragments[J]. Journal of the American Chemical Society, 2004, 126(40): 12736–12737. DOI:10.1021/ja040082h |
| [3] | Xu J, Sahu S, Cao L, Christopher E B, Peng G, Liu Y, Shiral K A, Wang P, Elena A. G, Mohammed J M, Qian H, Sun Y P. Efficient fluorescence quenching in carbon dots by surface-doped metals-disruption of excited state redox processes and mechanistic implications[J]. Langmuir the ACS Journal of Surfaces & Colloids, 2012, 28(46): 16141–7. |
| [4] | Zhao Q L, Zhang Z L, Huang B H, Peng L, Zhang M, Pang D W. Facile preparation of low cytotoxicity fluorescent carbon nanocrystals by electrooxidation of graphite[J]. Chemical Communications, 2008, 41(41): 5116. |
| [5] | Jia X, Li J, Wang E. One-pot green synthesis of optically pH-sensitive carbon dots with upconversion luminescence[J]. Nanoscale, 2012, 4(18): 5572–5575. DOI:10.1039/c2nr31319g |
| [6] | Li H, He X, Kang Z, Huang H, Liu Y, Liu J, Lian S, Tsang C H, Yang X, Lee S. Water-soluble fluorescent carbon quantum dots and photocatalyst design[J]. Angewan-dte Chemie International Edition, 2010, 49(26): 4430–4434. DOI:10.1002/anie.200906154 |
| [7] | Shen J H, Zhu Y H, Chen C, Yang X, Li C. Facile preparation and upconversion luminescenceof grapheme quantum dots[J]. Chemical Communications, 2011, 47(9): 2580–2582. DOI:10.1039/C0CC04812G |
| [8] | Zheng L, Chi Y, Dong Y, Lin J, Wang B. Electrochemiluminescence of water-soluble carbonnanocrystals released electrochemically from graphite[J]. Journal of the American Chemical Society, 2009, 131(13): 4564–4565. DOI:10.1021/ja809073f |
| [9] | Cao L, Wang X, Meziani M J, Lu F, Wang H, Luo P G, Lin Y, Harruff B A, Veca L M, Murray D, Xie S Y, Sun Y P. Carbon dots for multiphoton bioimaging[J]. Journal of the American Chemical Society, 2007, 129(37): 11318–11319. DOI:10.1021/ja073527l |
| [10] | Shen J, Zhu Y, Chen C, Yang X, Li C. Facile preparation and upconversion luminescence of graphene quantum dots[J]. Chemical Communications, 2011, 47(9): 2580. DOI:10.1039/C0CC04812G |
| [11] | Ge J, Jia Q, Liu W, Guo L, Liu Q, Lan M, Zhang H, Meng X, Wang P. Red-emissive carbon dots for fluorescent, photoacoustic, and thermal theranostics in living mice[J]. Advanced Materials, 2015, 27(28): 4169. DOI:10.1002/adma.v27.28 |
| [12] | Zhou J, Booker C, Li R, Zhou X, Sham T K, Sun X, Ding Z. An electrochemical avenue to blue luminescent nanocrystals from multiwalled carbon nanotubes (MWCNTs)[J]. Journal of the American Chemical Society, 2007, 129(4): 744–745. DOI:10.1021/ja0669070 |
| [13] |
章燕清. 碳量子点的性能调控与应用[D]. 温州: 温州大学, 2013.
Zhang Y Q. Properties adjustment and applications of carbon quantum dots[D].Wenzhou:Wenzhou University, 2013. http://cdmd.cnki.com.cn/Article/CDMD-10351-1013352377.htm |
| [14] |
何玉珩, 冯晓婷, 张漪, 杨永珍, 刘旭光, 许并社. 水溶性碳量子点的制备及荧光性能[J]. 太原理工大学学报, 2014, 45(3): 279–284.
He Y H, Feng X T, Zhang Y, Yang Y Z, Liu X G, Xu A S. Synthesis and fluorescence property of water-soluble carbon dots[J]. Journal of Taiyuan University of Technology, 2014, 45(3): 279–284. |
| [15] | Liu H, Ye T, Mao C. Fluorescent carbon nanoparticles derived from candle Soot[J]. Angewandte Chemie International Edition, 2007, 46(34): 6473–6475. DOI:10.1002/(ISSN)1521-3773 |
| [16] | Li H, He X, Kang Z, Huang H, Liu Y, Liu J, Lian S Y, Chi H A T, Yang X B, Shuit-Tong L. Water-soluble fluorescent carbon quantum dots and photocatalyst design[J]. Angewandte Chemie International Edition, 2010, 49(26): 4430–4434. DOI:10.1002/anie.200906154 |
| [17] | Kwon W S, Rhee S W. Facile synthesis of graphitic carbon quantum dots with size tunability and uniformity using reverse micelles[J]. Chemical Communications, 2012, 48(43): 5256–5258. DOI:10.1039/c2cc31687k |
| [18] | Bao L, Zhang Z L, Tian Z Q, Zhang L, Liu C, Lin Y, Qi B, Pang D W. Electrochemical tuning of luminescent carbonnanodots:from preparation to luminescence mechanisme[J]. Advanced Materials, 2011, 23(48): 5801–5806. DOI:10.1002/adma.v23.48 |
| [19] | Baker S N, Baker G A. Luminescent carbon nanodots:emergent nanolights[J]. Angewandte Chemie International Edition, 2010, 49(38): 6726–6744. DOI:10.1002/anie.200906623 |
| [20] | Zheng H, Wang Q, Long Y, Zhang H, Huang X, Zhu R. Enhancing the luminescence of carbon dots with a reduction pathway[J]. Chemical Communications, 2011, 47(38): 10650. DOI:10.1039/c1cc14741b |
| [21] | Barman M K, Jana B, Bhattacharyya S, Patra A. Photophysical properties of doped carbon dots (N, P, and B) and their influence on electron/hole transfer in carbon dots-Nickel (Ⅱ) phthalocyanine conjugates[J]. Journal of Physical Chemistry C, 2014, 118(34): 20034–20041. DOI:10.1021/jp507080c |
| [22] | Sun D, Ban R, Zhang P H, Wu G H, Zhang J R, Zhu J J. Hair fiber as a precursor for synthesizing of sulfur-and nitrogen-co-doped carbon dots with tunable luminescence properties[J]. Carbon, 2013, 64(11): 424–434. |
| [23] | Wang F, Xie Z, Zhang H, Liu C Y, Zhang Y G. Highly luminescent organosilane-functionalized carbon dots[J]. Advanced Functional Materials, 2011, 21(21): 1027–1031. |
| [24] | Tian L, Ghosh D, Chen W, Pradhan S, Chang X J, Chen S W. Nanosized carbon particales from natural gas soot[J]. Chemistry of Materials, 2009, 21(13): 2803–2809. DOI:10.1021/cm900709w |
| [25] | Cao L, Sahu S, Anilkumar P, Bunker C E, Xu J, Shiral K A, Wang P, Guliants E A, Tackettll K N, Sun Y P. Carbon nanoparticles as visible-light photocatalysts for efficient CO2 conversion and beyond[J]. Journal of the American Chemical Society, 2011, 133(13): 4754–4757. DOI:10.1021/ja200804h |
| [26] | Wang F, Xie Z, Zhang H, Liu C Y, Zhang Y G. Highly luminescent organosilane-functionalized carbon dots[J]. Advanced Functional Materials, 2011, 21(21): 1027–1031. |
| [27] | Li F, Liu C J, Yang J, Wang Z, Liu W G, Tian F. Mg/N double doping strategy to fabricate extremely high luminescent carbon dots for bioimaging[J]. RSC Advances, 2014, 4(7): 3201. DOI:10.1039/C3RA43826K |
| [28] | Gong J, An X, Yan X. A novel rapid and green synthesis of highly luminescent carbon dots with good biocompatibility for cell imaging[J]. New Journal of Chemistry, 2014, 38(4): 1376–1379. DOI:10.1039/C3NJ01320K |
| [29] | Goh E J, Kim K S, Kim Y R, Jung H S, Beack S, Kong W H, Scarcelli G, Yum S H, Hahn S K. Bioimaging of hyaluronic acid derivatives using nanosized carbon dots[J]. Biomacromolecules, 2012, 13(8): 2554–2561. DOI:10.1021/bm300796q |
| [30] | Yang S T, Wang X, Wang H, Lu F, Luo P G, Cao L, Meziani M J, Liu J H, Liu Y, Chen M, Huang Y, Sun Y P. Carbon dots as nontoxic and high-performance fluorescence imaging agents[J]. Journal of Physical Chemistry C, 2009, 113(42): 18110. DOI:10.1021/jp9085969 |
| [31] | Liu L Q, Li Y F, Zhan L, Liu Y, Huang C Z. One-step synthesis of fluorescent hydroxyls-coated carbon dots with hydrothermal reaction and its application to optical sensing of metalions[J]. Science China Chemistry, 2011, 54(8): 1342–1347. DOI:10.1007/s11426-011-4351-6 |
| [32] | Zhu S, Zhang J, Qiao C, Tang S, Li Y, Yuan W, Li B, Tian L, Liu F, Hu R, Gao H, Wei H, Zhang H, Sun H, Yang B. Strongly green-photoluminescent graphene quantum dots for bioimaging applications[J]. Chemical Communications, 2011, 47(24): 6858–6860. DOI:10.1039/c1cc11122a |
| [33] | Li Q, Ohulchanskyy T Y, Liu R, Koynov K, Wu D Q, Andreas B, Rajiv K, Adela B, Paras N P. Photoluminescent carbon dots as biocompatible nanoprobes for targeting cancer cells in vitro[J]. Journal of Physical Chemistry C, 2010, 114(28): 12062–12068. DOI:10.1021/jp911539r |
| [34] | Neugart F, Zappe A, Jelezko F, Tietz C, Boudou J P, Krueger A, Wrachtrup J. Dynamics of diamond nanoparticles in solution and cells[J]. Nano Letters, 2007, 7(12): 3588–3591. DOI:10.1021/nl0716303 |
| [35] | Luo P G, Sahu S, Yang S T, Sumit K S, Wang J, Wang H, Gregory E L, Cao L, Sun Y P. Carbon "quantum" dots for optical bioimaging[J]. Journal of Materials Chemistry B, 2013, 1(16): 2116–2127. DOI:10.1039/c3tb00018d |
| [36] | Kong B, Zhu A, Ding C, Zhao X, Li B, Tian Y. Carbon dot-based inorganic-organic nanosystem for two-photon imaging and biosensing of pH variation in living cells and tissues[J]. Advanced Materials, 2012, 24(43): 5844. DOI:10.1002/adma.201202599 |
| [37] | Cao L, Wang X, Meziani M J, Lu F, Wang H, Luo P G, Lin Y, Harruff B A, Veca L M, Murray D, Xie S Y, Sun Y P. Carbon dots for multiphoton bioimaging[J]. Journal of the American Chemical Society, 2007, 129(37): 11318–11319. DOI:10.1021/ja073527l |
| [38] | Yang S T, Wang X, Wang H, Lu F, Luo P G, Cao L, Meziani M J, Liu J H, Liu Y, Chen M, Huang Y, Sun Y P. Carbon dots as nontoxic and high-performance fluorescence imaging agents[J]. Journal of Physical Chemistry C Nanomaterials & Interfaces, 2016, 113(42): 18110. |
| [39] | Zhang X, Wang H, Wang H, Zhang Q, Xie J, Tian Y, Wang J, Xie Y. Single-layered graphitic-C(3) N(4) quantum dots for two-photon fluorescence imaging of cellular nucleus[J]. Advanced Materials, 2014, 26(26): 4438–43. DOI:10.1002/adma.v26.26 |
| [40] | Kim J, Park J, Kim H, Singha K, Kim W J. Transfection and intracellular trafficking properties of carbon dot-gold nanoparticle molecular assembly conjugated with PEI-pDNA[J]. Biomaterials, 2013, 34(29): 7168–7180. DOI:10.1016/j.biomaterials.2013.05.072 |
| [41] | Qu S, Wang X, Lu Q, Liu X, Wang L. A biocompatible fluorescent ink based on water-soluble luminescent carbon nanodots[J]. Angewandte Chemie International Edition, 2012, 51(49): 12215–12218. DOI:10.1002/anie.v51.49 |
| [42] | Zhu S, Meng Q, Wang L, Zhang J, Song Y, Jin H, Zhang K, Sun H, Wang H, Yang B. Highly photoluminescent carbon dots for multicolor patterning, sensors, and bioimaging[J]. Angewandte Chemie International Edition, 2013, 52(14): 3953–3957. DOI:10.1002/anie.v52.14 |
| [43] | Qu K, Wang J, Ren J, Qu X. Carbon dots prepared by hydrothermal treatment of dopamine as an effective fluorescent sensing platform for the label-free detection of Iron(Ⅲ) ions and dopamine[J]. Chemistry-A European Journal, 2013, 19(22): 7243–7249. DOI:10.1002/chem.v19.22 |
| [44] | Lu W, Qin X, Liu S, Chang G, Zhang Y, Luo Y, Asiri A M, Al-Youbi A O, Sun X. Economical, green synthesis of fluorescent carbon nanoparticles and their use as probes for sensitive and selective detection of mercury(Ⅱ) ions[J]. Analytical Chemistry, 2012, 84(12): 5351. DOI:10.1021/ac3007939 |
| [45] | Dong Y, Wang R, Liu G, Chen C, Chi Y, Chen G. Polyamine-functionalized carbon quantum dots as fluorescent probes for selective and sensitive detection of copperions[J]. Analytical Chemistry, 2012, 84(14): 6220–6224. DOI:10.1021/ac3012126 |
| [46] | Salinas-Castillo A, Ariza-Avidad M, Pritz C, Camprubí-Robles M, Fernández B, Ruedas-Rama M J, Megia-Fernández A, Lapresta-Fernández A, Santoyo-Gonzalez F, Schrott-Fischer A, Capitan-Vallvey L F. Carbon dots for copper detection with down and upconversion fluorescent properties as excitation sources[J]. Chemical Communications, 2013, 49(11): 1103. DOI:10.1039/c2cc36450f |
| [47] | Li H, He X, Kang Z, Huang H, Liu Y, Liu J, Lian S, Chi Him A T, Yang X, Lee S T. Water-soluble fluorescent carbon quantum dots and photocatalyst design[J]. Angewandte Chemie International Edition, 2010, 49(26): 4430–4434. DOI:10.1002/anie.200906154 |





