乙炔基功能化聚合物可以通过巯-炔点击反应以及Cu(Ⅰ)催化的1, 3偶极环加成点击反应(CuAAC)等方法对其进行后功能化,因而被广泛应用于药物释放、光电子器件、聚合物刷等领域;同时,也可以通过热或光引发的乙炔基交联反应提高材料的耐热性和力学性能[1-7]。因此,探索乙炔基功能化聚合物的新合成方法,对理论研究和实际应用都具有极大的价值。
利用传统自由基聚合直接制备乙炔基功能化聚合物存在极大的难度,因为乙炔基的化学活性高,容易与增长自由基反应而导致聚合物分子链支化,甚至凝胶化。例如,用丙烯酸甲酯(MA)与丙烯酸丙炔酯(PA)进行光引发自由基聚合,当PA单含量超过8 mol%时,在聚合反应低转化率阶段就会发生凝胶化[8]。因此,很难直接通过含乙炔基的丙烯酸酯的自由基聚合反应一步得到乙炔基功能化的聚合物。合成含乙炔基官能团的丙烯酸酯聚合物,目前主要有两种方法:一种方法先将PA的乙炔基用三甲基硅烷进行保护,聚合完成后再进行脱保护复原出乙炔基[9];另一种方法则是先合成含有羟基基团的聚合物,再经过丙炔酸与羟基的酯化反应来制备[10]。前一方法需要多步反应,纯化过程复杂;后者因为大分子官能团活性较低,基团转化率低,同时长时间的反应还可能会因为炔基的热交联而导致凝胶化。活性聚合如原子转移自由基聚合(ATRP)、可逆加成断裂链转移自由基聚合(RAFT)、活性阴离子聚合以及基团转移聚合也被应用于合成乙炔基功能化聚合物[2, 11],但这些方法都有相应的缺点,例如ATRP与基团转移聚合引入了金属离子,RAFT聚合使产物带有颜色,而活性阴离子聚合反应条件苛刻,不便实施。
在PA研究的基础上,我们设计了用叔炔丙基的丙烯酸酯制备乙炔基功能化聚合物的路线,如图 1所示。主要思路是:1-乙炔基环己基丙烯酯(ECA)结构中,叔碳的空间位阻降低了三键的活性,加大了三键与C=C的活性差;而且PA中炔丙基H原子对自由基有转移作用,而ECA没有可转移的H原子,避免了增长自由基向H原子转移而导致的支化和交联副反应。我们按图 1的路线合成了ECA,研究了ECA的自由基聚合特性,发现ECA的乙炔基在丙烯酸酯的常规自由基聚合中可以保留下来,得到了可溶性、甚至线性的乙炔基功能化聚合物,而且聚合物链上的乙炔基还可以进行“巯-炔”快速光点击反应。该结果对功能高分子材料的设计和改性都具有极大的参考价值,本文将报道这种简单、直接地制备乙炔基功能化聚合物的方法和乙炔基功能聚合物的一些特性。

|
图 1 乙炔基功能化丙烯酸酯聚合物的合成和光催化的巯-炔“点击”反应 Fig.1 Synthesis and photoinitiated thiol-yne "click" reaction of acetylene-functionalized polyacrylates |
1-乙炔基-1环己醇(ECL):98%,阿拉丁试剂;丙烯酰氯,自制,用前蒸馏;丙烯酸酯甲酯(MA):99%,天津迪博化工,用前蒸馏;三羟甲基丙烷三(3巯基丙酸酯)(TMTP)为日本KSK商品,直接使用;2-羟基-2-甲基苯丙酮(光引发剂1173):天津久日新材料股份有限公司商品,直接使用;其他原料和试剂均为市售原料,直接使用。
核磁共振谱仪(AVⅡ-400 MHz, Bruker公司);傅里叶变换红外光谱仪(Nicolet IS10,Thermo Scientific公司);紫外光源(PowerArc UV100, 500 W,蓝天特灯发展有限公司);凝胶渗透色谱仪(HLC-8320,日本东曹株式会社);差示扫描量热仪(TG209F1,TA仪器公司)。
1.2 1-乙炔基1-环己基丙烯酸酯(ECA)的合成将20 g(0.16 mol) 1-乙炔基-1-环己醇(ECL)、21.15 g(0.21 mol)三乙胺和110 mL氯仿(CHCl3)加入250 mL圆底烧瓶,置于冰浴中,在电磁搅拌下缓慢将17.5 g(0.193 mol)新制的丙烯酰氯滴加到圆底烧瓶中,2 h滴完,室温反应12 h后升温到40 ℃继续反应3 h。抽滤除去三乙胺盐,旋蒸除去氯仿,用环己烷将浓缩后的产物稀释5倍,分别用饱和碳酸氢钠水溶液洗3次,5%的NaCl水溶液洗3次。有机相用无水Na2SO4干燥过夜,抽滤除去Na2SO4,旋蒸除去环己烷。将浓缩后的产物减压蒸馏得到目标产物,产率54%。1HNMR(from TMS): 6.30(CH2=CH—, 1H), 5.70(CH2=CH—, 1H), 6.00(CH2=CH—, 1H),2.50(CH=C—, 1H),1.00~2.30(—C6H10, 10H)。
1.3 ECA的自由基聚合将1 g(5.62×10-3 mol)ECA、1 g乙酸乙酯、0.006 g(0.6%,质量分数)AIBN,加入到5 mL的圆底烧瓶中,用橡胶塞封口,通氮气30 min后升温至70 ℃,电磁搅拌反应8 h。产物用正己烷洗涤沉淀2次后,置于真空干燥箱中40 ℃干燥6 h,得到白色粉末状均聚物PECA 0.38 g,产率38%。
将1 g(5.62×10-3 mol) ECA、4 g(4.65×10-2 mol)丙烯酸甲酯(MA)、5 g乙酸乙酯、0.03 g (1.83×10-4 mol) AIBN加入到20 mL圆底烧瓶,用橡胶塞封口,通氮气30 min后升温至70 ℃,电磁搅拌反应8 h。产物用正己烷洗涤沉淀2次后,于真空干燥箱中30 ℃干燥6 h,得到白色有粘性的共聚物PMA-co-PECA 3.1 g,产率62%。
1.4 光催化的巯-炔光交联反应以及凝胶分数的测定取0.5 g PMA-co-PECA共聚物、0.17 g TMTP、0.5 g乙酸乙酯、0.0067 g(1%,质量分数)光引发剂1173,置于3 mL圆底玻璃瓶中,翻口橡胶塞密封后通氮气10 min,用500 W的紫外灯辐照5 min,得到凝胶状产物。
用实时红外跟踪共聚物与MTP的光交联反应:取上述反应前的溶液适量,涂抹于溴化钾盐片上,烘干溶剂后,盖上另外一片溴化钾盐片,500 W紫外点光源照射,同时用实时红外跟踪反应过程。
凝胶分数的测定:将烘干至衡重的凝胶块称重,放入烧杯中加入乙酸乙酯浸泡,4 h换一次溶剂,直至凝胶块重量不再变化,取出称量后放入40 ℃的真空干燥箱中烘干至恒重。浸泡后的重量与浸泡前的重量之比即为凝胶分数。取3次测量的平均值,凝胶分数为92%。
1.5 测试与表征核磁共振氢谱(1HNMR):用氘代氯仿(CDCl3)为溶剂,四甲基硅氧烷(TMS)为内标,用Bruker公司400M超导傅里叶数字化核磁共振谱仪测定聚合物的1HNMR图。红外吸收光谱(FTIR)用Nicolet IS10傅里叶变换红外吸收光谱仪测试,采用压片法制备溴化钾压片(将样品溶解于适当溶剂中,涂抹在溴化钾压片上,经红外灯烤后溶剂挥发)。聚合物分子量及分子量分布用日本东曹株式会社公司的HLC-8320GPC型凝胶渗透色谱(GPC)进行测定,色谱柱为TSK gelsuper HZM-M 6.0*150 mm和TSK gelsuper HZ3000 6.0*150 mm串联使用,使用示差折光检测器,以THF作为溶剂,流速为0.6 mL/min,单分散聚苯乙烯为标样,温度40 ℃,根据流出时间的不同得到聚合物的分子量及分布。差示扫描量热仪(DSC)测试用TA仪器公司的TG209F1:氮气下二次升温消除热历史,升温速度为10 ℃/min,测试温度范围0 ℃~150 ℃。
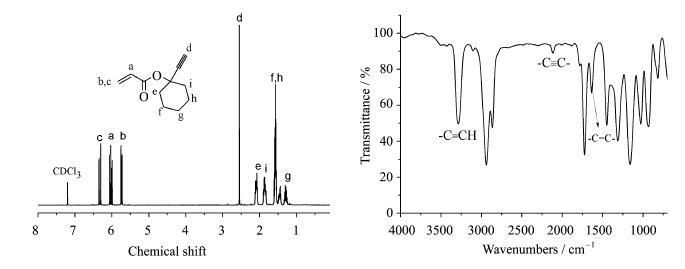
2 结果与讨论 2.1 1-乙炔基1-环己基丙烯酸酯(ECA)的合成和表征ECA单体通过炔基叔碳醇与丙烯酰氯反应得到(丙烯酰氯为新制得并经蒸馏后立即使用),通过减压蒸馏提纯后的产物收率不高(约低于60%)。ECA的结构用1HNMR和FT-IR进行了表征(图 2)。在1HNMR谱图中,端炔基氢的特征化学位移峰在2.5, 其余各质子的归属在图 2上已标示,各峰的积分面积与质子数成正比,并且没有杂峰,表明所合成ECA的纯度很高。在FT-IR图谱中,ECA中乙炔基的特征C—H振动特征吸收峰在3300 cm-1左右,C≡C的振动吸收峰在2150 cm-1左右,羰基的特征振动吸收在1720 cm-1左右。
|
图 2 ECA单体的核磁共振氢谱图和红外图 Fig.2 1HNMR and FT-IR of ECA monomer |
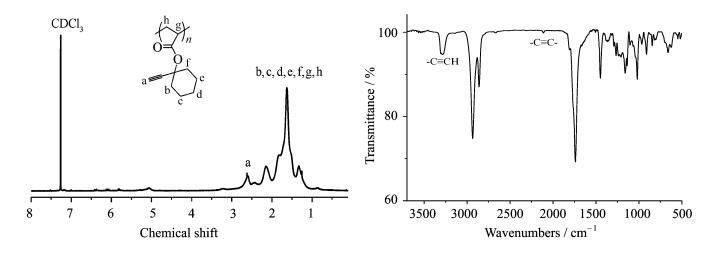
ECA在乙酸乙酯溶剂中,用AIBN作为引发剂的常规自由基聚合进行得较顺利,没有任何凝胶现象出现。产物用环己烷进行沉淀和洗涤,以去除未反应的单体。对PECA进行了1HNMR以及IR表征(图 3)。从核磁图中可以看到乙炔基末端氢在2.5~2.6处的特征化学位移,在红外谱图上,3300 cm-1左右有—C≡C—H的伸缩振动吸收峰,在2150 cm-1处有C≡C的伸缩振动吸收峰,表明均聚物中保留了乙炔基,并且1HNMR上乙炔基质子峰面积与其余质子峰的积分面积比大致符合聚合物中的比例。PECA的GPC测试结果显示,数均分子量达到1.4×104, 分子量分布指数PDI(即Mw/Mn)小于2,见表 1。根据自由基聚合反应动力学,该分布指数表明所得到的聚合物的分子量分布符合统计分布,聚合物为线性结构,即在ECA的自由基聚合过程中没有发生明显的支化反应,这可能是大体积基团的位阻降低了乙炔基的反应活性所致。与丙烯酸丙炔酯(PA)相比,不需要对ECA的乙炔基进行保护和脱保护或借助于RAFT试剂,就可以通过一步反应得到乙炔基功能化的聚合物,大大简化了合成过程。
|
图 3 均聚物PECA的核磁共振氢谱和红外图 Fig.3 1HNMR and FT-IR of homopolymer PECA |
| 表 1 乙炔基功能化聚合物的分子量和Tg Table 1 The molecular weight and Tg of the acetylene functionalized polymer |
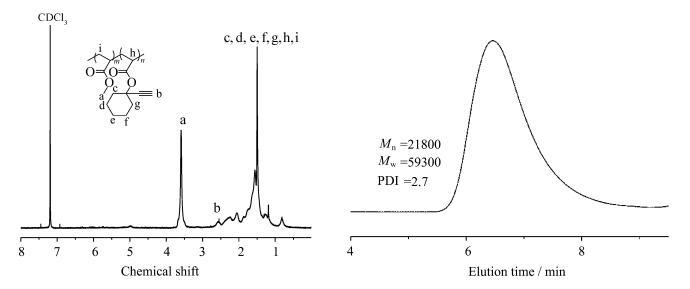
MA与ECA按质量比4:1(摩尔比约8:1)的常规自由基共聚合反应进行正常,聚合过程中始终溶液均匀,共聚产物在溶剂中充分溶解。产物用环己烷沉淀和洗涤,以去除未反应的单体,真空干燥后用1HNMR、GPC以及红外表征。从图 4的1HNMR谱上可以看到MA单元的甲基质子峰位于3.6处,ECA单元的乙炔基质子峰在2.5处,两单元的摩尔比约为MA:ECA=5:1(换算成质量比为7:3);共聚物PMA-co-PECA的数均分子量达到2.18×104,GPC曲线为较为对称的单峰,说明在聚合过程中没有发生明显的支化反应。在红外吸收光谱中(共聚物红外与均聚物类似,在此未列出)有位于2150 cm-1左右的碳碳三键伸缩振动峰和3300 cm-1左右的乙炔基碳氢伸缩振动峰。这些数据都说明共聚物中乙炔基得到了保留。
|
图 4 共聚物PMA-co-PECA的核磁共振氢谱和GPC曲线 Fig.4 1HNMR and GPC spectra of copolymer PMA-co-PECA |
均聚物PECA和共聚物PMA-co-PECA的分子量以及玻璃化转变温度如表 1所示,测得均聚物PECA的温度为110 ℃,共聚物P(MA-co-ECA)的玻璃化转变温度为30 ℃,且DSC曲线上共聚物只有一个玻璃化转变温度,表明该产物是共聚物而非两种单体的均聚物的混合物。根据共聚物组成比约为MA:ECA=7:3(质量比),由Fox公式计算的共聚物的理论玻璃化温度大约为33 ℃,实验值与理论值接近。
考察了均聚物PECA和共聚物P(MA-co-ECA)的溶解性能,发现均聚物以及共聚物在常用溶剂如氯仿、丙酮、DMF、四氢呋喃中都具有较好的溶解性。
2.4 乙炔基功能化聚合物的光巯-炔“点击”反应我们用光引发自由基的巯-炔“点击”反应来检查所合成的乙炔基功能化聚合物中乙炔基的点击反应活性。
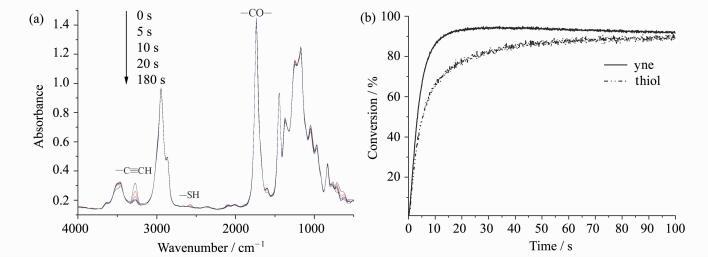
为此,将共聚物PECA-co-PMA与三官能巯基化合物TMTP按照thiol:yne=2:1(摩尔比)混合,加入质量分数为2%的光引发剂1173后,用紫外灯点光源照射,同时用红外光谱仪对反应过程进行实时跟踪。RT-FTIR跟踪的结果以及数据转换出的乙炔基和—SH官能团转化率随光照时间的变化过程如图 5所示。随着光照时间增加,位于3300 cm-1左右的—C≡CH的伸缩振动峰与位于2600 cm-1左右的—SH的特征吸收峰强度逐渐减弱,而1750 cm-1羰基的吸收峰强度以及2900 cm-1左右的饱和碳氢振动吸收峰的吸收强度几乎不变,表明乙炔基以及—SH的吸收强度减弱是发生了巯-炔加成反应导致官能团消失所致。以羰基吸收峰为内标,可以从RT-FTIR结果转换出乙炔基以及巯基的转化率随光照时间的变化。可以看出,光照约20 s后,乙炔基的转化率超过90%,巯基最终的转化也很显著。因此,聚合物分子链上的乙炔基可以进行巯-炔加成反应。我们还用浸泡法大致检查了光巯-炔加成反应后的交联产物的凝胶率,3次测量取平均值,测得凝胶分数可达92%。
|
图 5 共聚物PMA-co-PECA与TMTP的光交联反应实时红外图(a)和巯基与乙炔基的转化率-时间曲线(b) Fig.5 (a) Real-time IR traces of thiol-yne reaction between PMA-co-PECA; (b) TMTP and plot of conversion of —SH and the triple bonds |
本文通过1-乙炔基环己醇与丙烯酰氯的酯化反应制备了叔炔基丙烯酸酯功能单体ECA。ECA可以用常规自由基聚合,一步合成反应得到可溶的乙炔基功能化均聚物和共聚物。ECA的自由基聚合是高度区域选择性的,无需对乙炔基进行保护或借助于RAFT试剂,乙炔基便可在自由基聚合中得以保留,所得到的乙炔基功能化聚合物可以通过硫醇-炔点击反应进行快速光交联和功能化。本方法为反应性聚合物的设计以及新材料改性提供了新思路。
致谢 本工作得到高分子材料工程国家重点实验室自主项目经费以及江苏博益鑫成高分子材料公司的支持和帮助,在此一并致谢。| [1] | Lowe A B, Hoyle C E, Bowman C N. Thiol-yne click che-mistry:a powerful and versatile methodology for materials synthesis[J]. Journal of Materials Chemistry, 2010, 20(23): 4745–4750. DOI:10.1039/b917102a |
| [2] | Sanchez-Sanchez A, Asenjo-Sanz I, Buruaga L, Pomposo J A. Naked and self-clickable propargylic-decorated single-chain nanoparticle precursors via redox-initiated RAFT polymerization[J]. Macromolecular Rapid Communications, 2012, 33(15): 1262–1267. DOI:10.1002/marc.v33.15 |
| [3] | Wu J T, Huang C H, Liang W C, Wu Y L, Yu J, Chen H Y. Reactive polymer coatings:ageneral route to thiol-ene and thiol-yne click reactions[J]. Macromolecular Rapid Communications, 2012, 33(10): 922–927. DOI:10.1002/marc.201200011 |
| [4] | Wang H, Jiang P, Zhang M, Dong X. Synthesis of a novel restricted access chiral stationary phase based on atom transfer radical polymerization and click chemistry for the analysis of chiral drugs in biological matrices[J]. Journal of Chromatography A, 2011, 1218(9): 1310–1313. DOI:10.1016/j.chroma.2011.01.005 |
| [5] | Rahane S B, Hensarling R M, Sparks B J, Stafford C M, Patton D L. Synthesis of multifunctional polymer brush surfaces via sequential and orthogonal thiol-click reactions[J]. Journal of Materials Chemistry, 2012, 22(3): 932–943. DOI:10.1039/C1JM14762E |
| [6] | Badarau C, Wang Z Y. Photoinitiated cross-linking of acetylene-containing polymers in the presence of tungsten hexacarbonyl[J]. Macromolecules, 2003, 36(19): 6959–6961. DOI:10.1021/ma034657r |
| [7] | Liras M, García-García J M, Quijada-Garrido I, Gallardo A, París R. Thermo-responsive allyl-functionalized 2-(2-methoxyethoxy) ethyl methacrylate-based polymers as versatile precursors for smart polymer conjugates and conetworks[J]. Macromolecules, 2011, 44(10): 3739–3745. DOI:10.1021/ma200456c |
| [8] | Ciftci M, Kahveci M U, Yagci Y, Allonas X, Ley C, Tar H. A simple route to synthesis of branched and cross-linked polymers with clickable moieties by photopolymerization[J]. Chemical Communications, 2012, 48(82): 10252–10254. DOI:10.1039/c2cc35607d |
| [9] | Prasher A, Loynd C M, Tuten B T, Frank P G, Chao D, Berda E B. Efficient fabrication of polymer nanoparticles via sonogashira cross-linking of linear polymers in dilute solution[J]. Journal of Polymer Science Part A:Polymer Chemistry, 2016, 54(1): 209–217. DOI:10.1002/pola.27942 |
| [10] | Huynh V T, Chen G, Souza P D, Stenzel M H. Thiol-yne and Thiol-ene "click" chemistry as a tool for a variety of platinum drug delivery carriers, from statistical copolymers to crosslinked micelles[J]. Biomacromolecules, 2011, 12(5): 1738–1751. DOI:10.1021/bm200135e |
| [11] | Ghasdian N, Ward M A, Georgiou T K. Well-defined "clickable" copolymers prepared via one-pot synthesis[J]. Chemical Communications, 2014, 50(54): 7114–7116. DOI:10.1039/C4CC02660H |




