如何应对环境污染和能源短缺一直是人们所关注的热点。利用纳米材料进行光催化降解有机污染是净化水体的一种重要方法,它可以快速且完全矿化污染物,不留下任何有害残余物[1]。在众多半导体纳米光催化材料中,TiO2纳米材料具有化学性质稳定、价格低廉、无毒以及易于制备等优点[2-4]。目前,利用阳极氧化法制备的TiO2纳米管阵列具有独特的优势,相对于其它TiO2纳米材料而言,TiO2纳米管垂直生长在钛片上,拥有较大的界面面积以及良好的电子渗透路径,同时也更容易回收重复利用。然而,大多数研究是以金属钛片为载体,得到二维(2D)结构的TiO2纳米管阵列。而以钛网为基底,得到三维(3D)结构TiO2纳米管阵列报道并不多。与钛片相比,钛网具有更好的韧性及透光度,可以更有效地吸收太阳光的散射光和折射光,大大地增强了对太阳光的吸收能力[5]。但是,TiO2的禁带宽度较大,光诱导产生的电子-空穴对又会迅速复合,这极大地降低了TiO2纳米管阵列的光催化效果[6]。为了提高TiO2对太阳光的利用率和光催化性能,就需要拓宽TiO2在可见光区的吸收范围,增强对可见光的吸收利用,这些可通过对TiO2催化剂进行改性,抑制光生电子与空穴的复合,延长载流子的寿命而实现。
对二氧化钛的改性主要通过以下几种方法:贵金属沉积[7]、掺杂金属[8]和非金属离子[9]、窄禁带半导体复合修饰[10]等。其中,利用带隙合适的半导体纳米材料对TiO2纳米管阵列进行修饰是一种有效的方法。由于两种半导体之间导带和价带存在能级差,可以促进光生电子和空穴的分离,从而延长了载流子的寿命。CdS是一种窄带隙的半导体,其禁带宽度为2.4 eV。当CdS修饰到TiO2上时,二者会形成异质结。在可见光的照射下,CdS能够有效地吸收可见光,产生光生电子和空穴对。由于CdS的导带比TiO2导带更负(约0.5 eV),CdS受激发产生的光生电子会从CdS的导带转移到TiO2的导带,从而有效了抑制了光生电子和空穴的复合[10]。
本文首先采用阳极氧化法在水、乙二醇以及氟化氨的有机体系中制备出TiO2纳米网,然后通过连续离子层吸附法对TiO2纳米网进行CdS沉积,得到CdS/TiO2复合纳米材料,进行了表征并分析其光电性能。最后,在模拟太阳光的照射下,将CdS/TiO2复合纳米材料应用于光催化降解有机染料亚甲基蓝(MB), 研究其光催化性能。
1 实验方法 1.1 试剂与仪器实验试剂:无水乙醇(分析纯,天津市德恩化学试剂有限公司)、丙酮(分析纯,天津市德恩化学试剂有限公司)、氟化氨(分析纯,天津市科密欧化学试剂有限公司)、乙二醇(分析纯,天津市风船化学试剂科技有限公司)、硫化钠(分析纯,天津市大茂化学试剂厂)、硝酸镉(分析纯,天津市科密欧化学试剂有限公司)、钛网(河北安平县盛卓钛网制品有限公司),实验用水为去离子水。
实验仪器:稳压直流电源(台湾Array公司)、电化学工作站(CHI 660D,上海辰华仪器有限公司)、300 W氙气灯(PLS-SXE300,北京泊菲莱)、扫描电子显微镜(Quanta 250,捷克FEI公司)、X射线衍射仪(D8 ADVANCE,德国Bruker公司)、紫外可见近红外分光光度计(UV-3600,日本Shimadzu公司)、荧光分光光度计(Cary Eclipse,澳大利亚Agilent公司)。
1.2 TiO2纳米网的制备首先,用丙酮和乙醇对钛网进行超声波清洗,然后将清洗后的钛网在室温条件下进行阳极氧化,电解液为氟化铵的乙二醇水溶液。该过程在双电极体系下进行,其中铂片是阴极,钛网为阳极。阳极氧化后,将样品置于马弗炉中,500 ℃下煅烧3 h,将无定形态转化为锐态矿。TiO2样品的有效面积是1 cm×4 cm,阳极和阴极之间的距离为2 cm。
1.3 CdS/TiO2纳米网的制备本实验采用连续离子层吸附反应法制备CdS/TiO2复合纳米材料。首先,将TiO2纳米网在0.5 mol/L的Cd(NO3)2溶液中浸润1 min,取出用蒸馏水冲洗,吹风机吹干。然后,在0.2 mol/L的Na2S水溶液中浸润1 min,取出用蒸馏水冲洗,吹风机吹干。上述步骤重复若干个循环,目的是使适量的CdS纳米颗粒沉积到TiO2纳米网上。最后,将制备好的复合材料在管式炉中300 ℃下煅烧1 h,得到晶型良好的CdS/TiO2复合纳米材料。
1.4 测试方法 1.4.1 样品表征对制备的TiO2纳米网和CdS/TiO2复合纳米材料进行一系列的表征。本实验用扫描电子显微镜(Scanning Electron Microscope,SEM)、X射线能量色谱仪(Energy Dispersive X-Ray Spectrascopy,EDX)、X射线衍射仪(X-Ray Diffraction Phase Analysis,XRD)等仪器对光催化剂进行微观形貌、表面的元素化学组成与价态以及晶体结构的表征,以证实该纳米复合材料的成功制备;使用紫外-可见漫反射光谱仪(Ultra Violet Visible Diffuse Reflection Spectrum,UV-Vis DRS)、荧光光谱仪对其光电性能进行测试,以证明该纳米复合材料拓宽了二氧化钛的可见光响应范围,复合材料的光生电子空穴对的复合能力低于钛网,促进了光生电子和空穴的分离能力。
1.4.2 光电化学测试光电化学测试是在电化学工作站CHI 660D上进行,实验采用的是三电极体系:CdS/TiO2复合纳米材料为工作电极,Pt片为对电极,甘汞电极为参比电极。光电流实验在模拟太阳光的300 W高压氙气灯下进行,光照射密度是100 mW·cm-2,其电解液为0.2 mol/L的Na2S溶液。阻抗的电解液为5×10-3 mol/L的Fe(CN)63-/4-和0.2 mol/L的KCl溶液,扫描速率为50 mV/s,信号振幅为5 V。所用容器均为实验室提供的玻璃仪器且实验条件要求不高。
1.4.3 CdS/TiO2复合纳米材料光催化降解MB通过测定水溶液中的MB降解速度来反映光催化剂的催化性能。光催化剂为TiO2纳米网和CdS/TiO2复合纳米材料,有效电极面积为4 cm×3 cm,竖直立于石英烧杯中。将20 mg/L的MB倒入石英烧杯中,在磁力搅拌的条件下吸附30 min以达到吸附平衡。然后,以300 W氙弧光灯为太阳光模拟光源,光照密度是100 mW·cm-2,氙灯和石英杯之间的距离为8 cm,进行光催化降解MB的实验。降解过程中MB的实时浓度变化通过紫外-可见分光光度计测定其特征峰处的吸光度进行计算,每隔20 min取一个样记录吸光度值,每个数据平行测定3次,以未修饰的TiO2纳米网为光催化剂降解MB作为对照实验。
2 结果与讨论 2.1 CdS/TiO2纳米网的形貌、晶型表征制备材料的形貌如图 1所示。图 1(a)、(b)所示为未修饰的TiO2纳米网的SEM图,可以看出TiO2纳米管垂直生长在钛丝上,钛丝之间相互交织形成网状结构。从图 1(c)中可以看出,用本文方法制备出来的TiO2纳米网具有整齐向上开口的管状结构,孔径大小均匀。图 1(d)所示为TiO2纳米网的侧面图,纳米网排列有序,高度大约为4.2 μm。图 1(e)、(f)所示是CdS/TiO2复合纳米材料阵列的表面形貌图,可以看出,CdS成功沉积在纳米管的顶端和侧面,并没有堆积堵塞管口。由于CdS的修饰作用,使得复合纳米材料的表面变得更加粗糙,暴露出了更多的活性位点。

|
图 1 样品的SEM图 (a)低倍数下的TiO2纳米网落结构的电镜图;(b~c)不同放大倍数下TiO2/Ti纳米网的电镜图;(d) TiO2纳米网的侧面电镜图;(e) CdS/TiO2的电镜图;(f) CdS/TiO2的侧面电镜图 Fig.1 SEM images of the samples (a) The low magnification of TiO2 nanomesh; (b-c) different magnification of TiO2/Ti nanomesh; (d) cross section of TiO2 nanomesh; (e) CdS/TiO2 nanomesh; (f) cross section of CdS/TiO2 nanomesh |
为了确定样品的晶相,对样品进行了XRD衍射分析, 谱图如图 2所示。曲线(1)展示了经过500 ℃高温煅烧的TiO2纳米网的XRD谱图,图中可见TiO2的锐钛矿特征衍射峰。与TiO2纳米网的XRD谱图相比,曲线(2)CdS/TiO2纳米网展现出了一些新的特征峰,在26.5°、43.9°、52.1°处显示的特征峰是CdS,这些特征峰2θ角对应的晶格间距为3.366、2.060和1.755。以上结果证明CdS纳米粒子成功地沉积在TiO2纳米网上。

|
图 2 TiO2和CdS/TiO2的XRD图 Fig.2 XRD patterns of TiO2 and CdS/TiO2 |
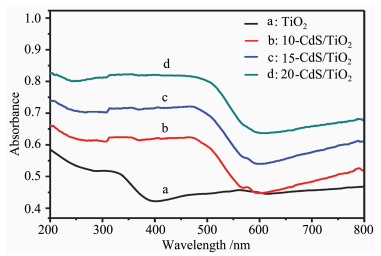
图 3给出了未修饰的TiO2纳米网和沉积不同圈数的CdS/TiO2纳米网的紫外-可见漫反射光谱图。相较于未修饰的TiO2纳米网,CdS/TiO2纳米网复合材料在紫外光区和可见光区的吸收峰明显增强,并且最高吸收峰的位置从紫外光区红移至可见光区。这是由于窄带隙CdS的引入使二氧化钛的禁带宽度减小,带隙结构发生变化,拓宽了TiO2纳米网对可见光区域的响应范围,增强了材料对可见光的吸收能力[11]。如图 3所示,随着沉积圈数的增多,材料对光的吸收能力愈强,由此可知,修饰CdS后的复合纳米材料具有更好的可见光吸收能力。
|
图 3 样品的固体紫外-可见漫反射图谱 Fig.3 UV-Visible diffuse reflectance spectra of different samples |
光电流表明了材料的载流子传输和光生电子-空穴的分离率[12]。图 4为TiO2纳米网以及沉积不同圈数CdS的CdS/TiO2纳米网的光电流响应图。由图 4中可以看出,在无太阳光照射时,样品的光电流可以忽略不计,说明样品在黑暗环境中没有被激发出光生电子和电子空穴。在模拟太阳光照射的条件下,样品的光电流都明显提高。TiO2的光电流约为0.09 mA·cm-2,沉积了10、15、20圈的CdS/TiO2复合纳米材料样品的光电流分别增大到约为0.25 mA·cm-2、0.35 mA·cm-2和0.30 mA·cm-2。实验结果表明,随着CdS沉积圈数的增多,光电流呈先增大后减少的趋势,沉积了15圈CdS的样品光电流最大。该结果说明沉积了15圈的CdS/TiO2纳米网在光照下更有利于载流子的传输和空穴电子对的分离,有利于更快、更好地降解有机污染物。沉积了20圈CdS纳米颗粒的CdS/TiO2纳米网的光电流反而降低,可能是因为过多的CdS纳米粒子成了空穴和电子的复合中心。

|
图 4 样品的时间-电流曲线图(a) TiO2;(b) 10圈CdS/TiO2;(c) 15圈CdS/TiO2;(d) 20圈CdS/TiO2 Fig.4 Transient photocurrent response of (a) TiO2, (b) 10 cycles CdS/TiO2, (c) 15 cycles CdS/TiO2 and (d) 20 cycles CdS/TiO2 |
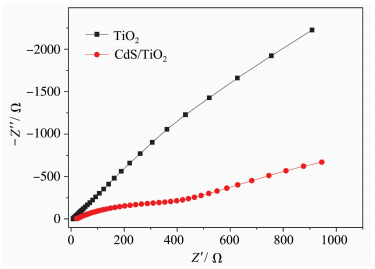
通过奈奎斯特图(Nyquist plot, 电化学阻抗谱图)的小圆弧大小能够反映材料的载流子转移能力,半圆的半径越大,对应材料的阻抗越大,载流子的转移能力越低[13]。图 5为TiO2纳米网、CdS/TiO2纳米网的电化学阻抗谱图,测试条件是以含有5 mmol/L Fe(CN)63-/4-活性探针的0.2 mol/L KCl为电解质溶液,扫描速率50 mV/s,信号振幅5 mV。可以明显看到,曲线半圆的半径大小顺序为:CdS/TiO2纳米网 < TiO2纳米网,即CdS/TiO2纳米网的载流子转移能力比TiO2纳米网强。因此,CdS修饰的TiO2纳米网可能会具有更好的光催化活性。
|
图 5 样品的电化学阻抗谱图 Fig.5 Electrochemical impedance spectroscopy of different samples |
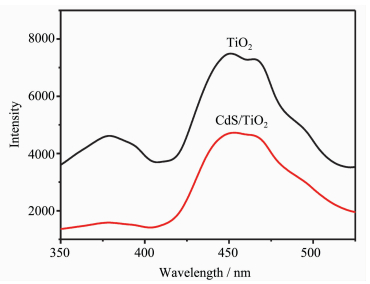
半导体材料受到光的激发后,会产生电子空穴对,一部分电子和空穴会参与氧化过程,形成活性物质,从而降解目标污染物;另一部分会发生复合而发射出光子,导致光致发光。因此,光致发光强度越高,意味着更高的空穴和电子复合率,即更短的光生载流子的寿命,所以我们可以从光致发光的强度来判断材料对光生载流子的捕获和转移能力[14]。由图 6可知,两种材料的荧光强度大小为TiO2纳米网>CdS/TiO2纳米网。这说明修饰过CdS纳米颗粒后,复合材料的发光强度有所降低,有效的抑制了空穴和电子对的复合,提高了空穴电子对的分离效率。因此,CdS/TiO2复合材料表现出更高的光电流强度。
|
图 6 TiO2和CdS/TiO2的荧光光谱图 Fig.6 PL spectra of TiO2 and CdS/TiO2 |
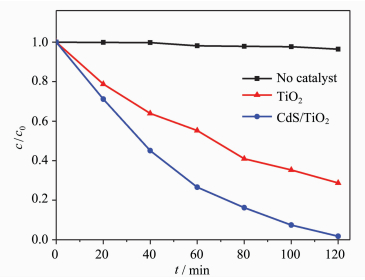
通过在模拟太阳光下光催化降解MB来评价催化剂的催化性能,其中MB的初始浓度为20 mg/L,所选催化剂为未修饰的TiO2纳米网以及沉积了15圈的CdS/TiO2纳米网复合材料。首先,在黑暗条件下,将样品放在50 mL的MB溶液中30 min,以达到吸附-解吸平衡。然后,打开光源,在模拟太阳光下进行光催化降解MB的实验。降解过程中每隔20 min取一个样,并使用紫外-分光光度计来实时监测降解过程中溶液的浓度变化。由图 7可以看出,在没有加入催化剂时,MB几乎没有降解。当打开光源后,TiO2纳米网以及CdS/TiO2纳米网复合材料均能够降解MB。但是,相比于没有修饰的TiO2纳米网,CdS/TiO2纳米网复合材料具有更高的光催化降解MB的能力。120 min以后,CdS/TiO2纳米网复合材料对MB的移除效率为98.3%,远高于未修饰的TiO2纳米网的降解效率(71.3%)。
|
图 7 不同催化剂的光催化降解MB效果分析 Fig.7 Photodegradation efficiency of MB in different samples |
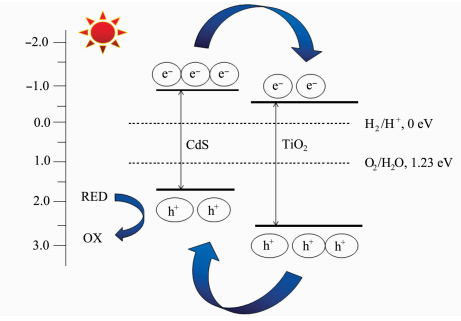
图 8为CdS/TiO2纳米网复合材料在光照下光生电子和空穴转移分离的过程。由图 8可知,CdS的价带和导带都高于TiO2,当材料受到光照射时,TiO2和CdS都会产生光生电子和空穴,由于它们两者的能带结构不同,所以光生电子从CdS的导带上转移到TiO2的导带上,而TiO2价带上的空穴则转移到较低价带的CdS上,这样就加快了光生电子和空穴的分离。在光催化降解实验的进程中,储存在TiO2上的电子与溶解的氧气分子发生一系列反应生成羟基自由基。而羟基自由基是一种很强的氧化剂,可以直接矿化有机污染物,与此同时,CdS上的空穴也能够与水分子反应生成羟基自由基,进而分解有机污染物MB,生成水和二氧化碳[15]。
|
图 8 CdS/TiO2空穴和电子传输的机理图 Fig.8 Mechanism diagram of hole and electron transport in CdS/TiO2 |
本文利用阳极氧化法和连续离子层吸附反应法,制备出了CdS/TiO2复合纳米材料,并借助多种方法对它进行了形貌结构的表征和光电性能的测试,可得以下结论:(1)与未修饰的TiO2纳米网相比,CdS/TiO2复合纳米材料对光的吸收范围增宽至可见光区且光吸收强度增大,说明窄禁带半导体CdS的修饰显著提高了材料对光的吸收能力;(2)通过光电流测试,发现沉积15圈CdS后的CdS/TiO2复合纳米材料的光电性能最强,其光电流最大为0.35 mA/cm2。以上实验结果说明,修饰过CdS的复合纳米材料更有利于对可见光的吸收,并且有效地抑制了光生电子和空穴的复合率。因此,复合材料表现出更优异的光催化降解有机污染物MB的能力。
| [1] | Ooka Chihiro, Yoshida Hisao, Suzuki Kenzi, Hattori T. Highly hydrophobic TiO2 pillared clay for photocatalytic degradation of organic compounds in water[J]. Microporous and Mesoporous Materials, 2004, 67(2-3): 143–150. DOI:10.1016/j.micromeso.2003.10.011 |
| [2] | Su Z, Zhou W. Pore diameter control in anodic titanium and aluminium oxides[J]. Journal of Materials Chemistry, 2011, 21(2): 357–362. DOI:10.1039/C0JM02521F |
| [3] | Su Z, Zhou W, Jiang F, Hong M. Anodic formation of nanoporous and nanotubular metal oxides[J]. Journal of Materials Chemistry, 2012, 22(2): 535–544. DOI:10.1039/C1JM13338A |
| [4] | Linsebigler A L, Lu G, Yates Jr J T. Photocatalysis on TiO2 surfaces:principles, mechanisms, and selected results[J]. Chemical Reviews, 1995, 95(3): 735–758. DOI:10.1021/cr00035a013 |
| [5] | Liao J J, Lin S W, Zhang L, Pan N, Cao X, Li J. Photoca-talytic degradation of methyl orange using a TiO2/Ti electrode with 3-D nanotube arrays[J]. ACS Applied Materials & Interfaces, 2012, 4(1): 171–177. |
| [6] |
杨小龙, 潘月, 邢明阳, 张金龙. TiO2-SiO2二维大孔薄膜的制备及其光催化活性研究[J]. 影像科学与光化学, 2015, 33(5): 383–393.
Yang X L, Pan Y, Xing M Y, Zhang J L. Preparation and photocatalytic study of TiO2-SiO2 macroporous film[J]. Imaging Science and Photochemistry, 2015, 33(5): 383–393. DOI:10.7517/j.issn.1674-0475.2015.05.383 |
| [7] | Fei J, Li J. Controlled preparation of porous TiO2-Ag nanostructures through supramolecular assembly for plasmon-enhanced photocatalysis[J]. Advanced Materials, 2015, 27(2): 1521–4095. |
| [8] |
景明俊, 王岩, 张敏, 杨建军. 负载金的掺氮二氧化钛的制备及其可见光催化性能[J]. 影像科学与光化学, 2011, 29(5): 353–363.
Jing M J, Wang Y, Zhang M, Yang J J. Preparation of gold-modified nitrogen-doped TiO2 and its visible light photocatalytic activity[J]. Imaging Science and Photochemistry, 2011, 29(5): 353–363. DOI:10.7517/j.issn.1674-0475.2011.05.353 |
| [9] | Asahi R, Morikawa T, Ohwaki T, Aoki K, Taga Y. Visible-light photocatalysis in nitrogen-doped titanium oxides[J]. Science, 2001, 293(5528): 269–271. DOI:10.1126/science.1061051 |
| [10] | Qian S, Wang C, Liu W, Zhu Y, Yao W, Lu X. An enhanced CdS/TiO2 photocatalyst with high stability and activity:effect of mesoporous substrate and bifunctional linking molecule[J]. Journal of Materials Chemistry, 2011, 21(13): 4945–4952. DOI:10.1039/c0jm03508d |
| [11] | Bessekhouad Y, Robert D, Weber J V. Bi2S3/TiO2 and CdS/TiO2 heterojunctions as an available configuration for photocatalytic degradation of organic pollutant[J]. Journal of Photochemistry and Photobiology A:Chemistry, 2004, 163(3): 569–580. DOI:10.1016/j.jphotochem.2004.02.006 |
| [12] | Li Y, Luo S, Wei Z, Meng D, Ding M, Liu C. Electrodeposition technique-dependent photoelectrochemical and photocatalytic properties of an In2S3/TiO2 nanotube array[J]. Physical Chemistry Chemical Physics, 2014, 16(9): 4361–4368. DOI:10.1039/c3cp54675f |
| [13] | Tian M, Wu G, Chen A. Unique electrochemical catalytic behavior of Pt nanoparticles deposited on TiO2 nanotubes[J]. ACS Catalysis, 2012, 2(3): 425–432. DOI:10.1021/cs200691a |
| [14] | Gao X, Sun W, Hu Z, Ai G, Zhang Y, Feng S, Li F, Peng L. An efficient method to form heterojunction CdS/TiO2 photoelectrodes using highly ordered TiO2 nanotube array films[J]. The Journal of Physical Chemistry C, 2009, 113(47): 20481–20485. DOI:10.1021/jp904320d |
| [15] | Wei Z, Li Y, Luo S, Liu C, Meng D, Ding M, Zeng G. Hierarchical heterostructure of CdS nanoparticles sensitized electrospun TiO2 nanofibers with enhanced photocatalytic activity[J]. Separation & Purification Technology, 2014, 122(3): 60–66. |




