2. 湖北固润科技股份有限公司, 湖北 荆门 448000
2. Hubei Gurun Technology Corporation, Jingmen 448000, Hubei, P. R. China
光固化体系主要由光引发剂、低聚物和活性稀释剂组成,活性稀释剂占整个体系质量分数的40%~60%。常用的阳离子UV固化活性树脂有环氧化合物、乙烯基醚和氧杂环丁烷。脂肪族环氧化合物具有聚合速度快、固化制件耐候性好等特点,且具有良好的电绝缘性能,已成为阳离子固化体系中主要的反应原料。但该类化合物合成工艺复杂,成本较高。乙烯基醚类化合物也可作为阳离子光固化预聚物或活性稀释单体进行阳离子聚合,具有速度快、粘度低等优点。但该类化合物易挥发、气味较大,环境污染严重。
近年来,氧杂环丁烷活性稀释剂发展迅猛[1-3],这些化合物具有粘度低、固化收缩率低、粘接强度高、聚合速度快、毒性低和不易挥发等特点,广泛用于紫外光固化材料。其主要种类有:单官能团氧杂环丁烷、双官能团氧杂环丁烷、杂化氧杂环丁烷。
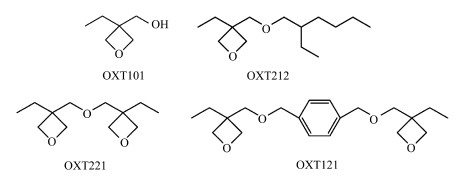
单官能团和双官能团的代表性品种见式1。
|
式1 单官能团和双官能团代表品种 Monofunctional and bisfuncational groups of oxetane varieties |
杂化氧杂环丁烷活性稀释剂的结构特点主要是将自由基聚合单体如丙烯酸和含氟/含硅基团引入到氧杂环丁烷上。其主要品种见式2。

|
式2 杂化氧杂环丁烷的代表品种 Hybrid oxetane varieties |
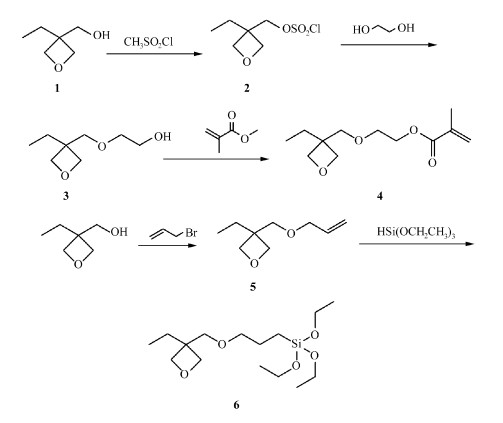
丙烯酸改性氧杂环丁烷同时可以参与自由基聚合和阳离子聚合,国内报道比较少。在文献[4-8]的基础上,本文合成了两种杂化氧杂环丁烷,并对其结构进行了核磁表征。其合成路线见图 1。
|
图 1 杂化氧杂环丁烷的合成路线 The synthesis route of oxetane |
试剂:3-乙基-3-羟甲基氧杂环丁烷,工业品,湖北固润科技股份有限公司;乙二醇,化学纯,国药集团化学试剂有限公司;甲基磺酰氯,工业品,湖北孝昌金鸡化工厂;甲基丙烯酸甲酯,分析纯,天津市福晨化学试剂厂;三乙氧基硅烷,工业级,曲阜晨光化工。
仪器:瑞士BrukerAvance 400NMR型核磁共振仪。
1.2 3-乙基-3-甲磺酰基甲基氧杂环丁烷(2)的合成在装有温度计、搅拌器和滴液漏斗的500 mL三口反应瓶中,加入139.2 g(1.2 mol)的3-乙基-3-羟甲基氧杂环丁烷和200 mL甲苯,冷却至-10~-15 ℃,在-10 ℃以下滴加137.4 g(1.2 mol)甲烷磺酰氯。滴加完毕,升至室温继续反应2 h。加入200 mL蒸馏水至反应瓶中,分层,有机层用3×150 mL 5%的NaCl水溶液洗涤,再用蒸馏水洗至中性,浓缩得棕红色液体。产物不必提纯,可直接用于下一步反应。
1.3 2-[(3-乙基-3-氧杂环丁基)甲氧基]乙醇(3)的合成在带有温度计、搅拌器、回流冷凝管的250 mL反应瓶中加入58.2 g(0.3 mol)的3-乙基-3-甲磺酰基甲基氧杂环丁烷(2)、乙二醇18.6 g(0.3 mol)、80 mL甲苯、24 g质量浓度50%的氢氧化钾溶液和0.1 g相转移催化剂PEG600,升温回流搅拌3 h,冷却后加水、分层,用甲苯萃取水相3次,合并有机层,无水硫酸镁干燥浓缩,减压蒸馏收集107~109 ℃/2 mmHg馏分33.2 g, 收率69.1%,含量98.2%。
1.4 2-[(3-乙基-3-氧杂环丁烷)甲氧基]甲基丙烯酸乙酯(4)的合成在装有温度计、搅拌器、蒸馏装置的250 mL反应瓶中加入64.08 g(0.4 mol)的2-[(3-乙基-3-氧杂环丁基)甲氧基]乙醇(3)、40.0 g(0.4 mol)甲基丙烯酸甲酯(MMA)、0.01 g阻聚剂对苯二酚和催化剂,升温,及时蒸出生成的甲醇,用GC监测。反应完成后,减压蒸馏收集120~122 ℃/2 mmHg馏分,得73.0 g无色油状物,收率80%,含量98.9%。
1.5 3-乙基-3-[(2-丙烯-1-基氧基)甲基]氧杂环丁烷(5)的合成在装有温度计、搅拌器、冷凝回流管的250 mL反应瓶中加入58.1 g(0.5 mol)的3-乙基-3-羟甲基氧杂环丁烷、40 g质量浓度为50%的氢氧化钠溶液、0.1 g相转移催化剂四丁基溴化铵,在0 ℃下滴加60.5 g(0.5 mol) 3-溴丙烯,滴加完毕升至室温搅拌,GC监测。反应完成用甲苯萃取,水洗、干燥浓缩,减压蒸馏收集55~57 ℃/2 mmHg馏分,得72.3 g无色油状物,收率90%,含量99.7%。
1.6 3-乙基-3-[[3-(三乙氧基硅)丙氧基]甲基]氧杂环丁烷(OXT610)的合成在装有温度计、搅拌器、冷凝回流管的250 mL反应瓶中加入无水甲苯80 mL、三乙氧基硅烷32.86 g(0.2 mol)和适量铂金催化剂,在室温下滴加31.2 g(0.2 mol)的3-乙基-3-[(2-丙烯-1-基氧基)甲基]氧杂环丁烷(5),滴加完毕后,升温至80℃继续反应2 h,GC监测。反应完成后浓缩蒸出甲苯,然后减压蒸馏,收集123~124 ℃/2 mmHg馏分,得51.3 g无色油状物,收率80%,含量98.5%。
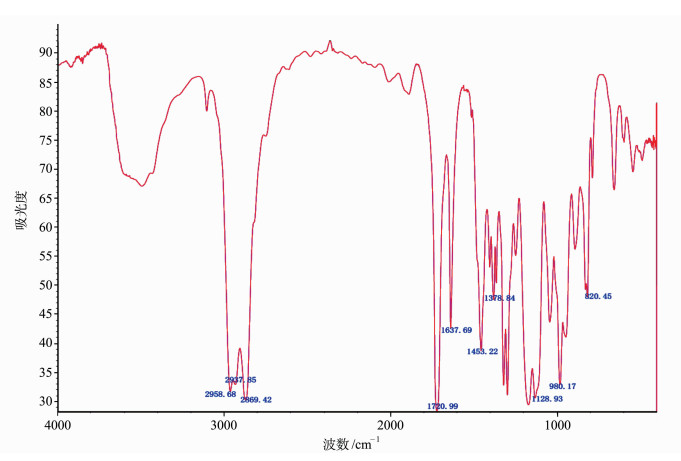
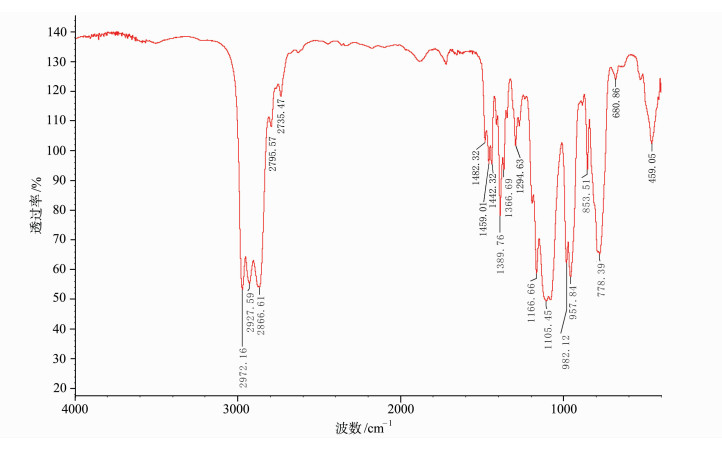
2 结果与讨论 2.1 红外光谱分析图 2为2-[(3-乙基-3-氧杂环丁烷)甲氧基]甲基丙烯酸乙酯(4)红外光谱图,从图可以看到红外吸收IR(cm-1):碳碳双键吸收峰: 1637.69;甲基C—H吸收峰:2958.68,2937.85,1453.22,1378.84;亚甲基C—H吸收峰:2869.42;酯键羰基吸收峰:1720.99;非四元环C—O—C吸收峰:1128.93;四元环C—O—C吸收峰:980.17,820.45。图 3为3-乙基-3-[[3-(三乙氧基硅)丙氧基]甲基]氧杂环丁烷(OXT610)红外光谱图IR(cm-1):硅氧烷红外吸收峰:1166.66,957.84;甲基C—H吸收峰:2972.16,2927.59,1480.32,1389.76;亚甲基C—H吸收峰:2866.61;非四元环C—O—C吸收峰:1105.45;四元环C—O—C吸收峰:982.12,788.39。从图 2和图 3可以知道,所合成的氧杂环丁烷的结构与目标化合物的结构一致。
|
图 2 2-[(3-乙基-3-氧杂环丁烷)甲氧基]甲基丙烯酸乙酯(4)红外光谱图 The infrared spectrum of 2-propenoic acid, 2-methyl-2-[(3-ethyl-3-oxetanyl)methoxy]ethyl ester |
|
图 3 3-乙基-3-[[3-(三乙氧基硅)丙氧基]甲基]氧杂环丁烷(OXT610)红外光谱图 The infrared spectrum of 3-ethyl-3-[[3-(triethoxysilyl)propoxy]methyl]-oxetane(OXT610) |
使用瓦瑞安公司的Varian VA400 MHZ型核磁共振仪分别测试了所合成样品的氢谱来确定单体的结构,测试所用内标为四甲基硅烷(TMS),溶剂为氘代氯仿(CDCl3),频率400 MHz。
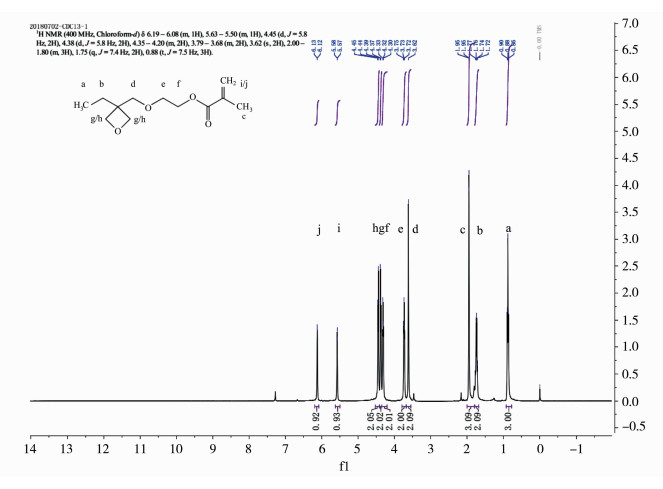
图 4是2-[(3-乙基-3-氧杂环丁烷)甲氧基]甲基丙烯酸乙酯(4)的核磁共振氢谱:0.88(t, 3H, CH3);1.75(q, 2H, CH2);2.00~1.80(m, 3H, CH3);3.62(s, 2H, CH2);3.79~3.68 (m, 2H, CH2);4.35~4.20(m, 2H, CH2);4.38(d, 2H, CH2);4.45(d, 2H, CH2);5.63~5.50 (m, 1H, CCH);6.19~6.08(m, 1H, CCH)。由谱图可知总共20个氢,和2-[(3-乙基-3-氧杂环丁烷)甲氧基]甲基丙烯酸乙酯的总氢个数符合,氢原子种类数目及个数比均与结构相符,可确定该样品与目标结构一致。
|
图 4 2-[(3-乙基-3-氧杂环丁烷)甲氧基]甲基丙烯酸乙酯核磁共振谱图 The NMR spectrum of 2-propenoic acid, 2-methyl-2-[(3-ethyl-3-oxetanyl)methoxy]ethyl ester |
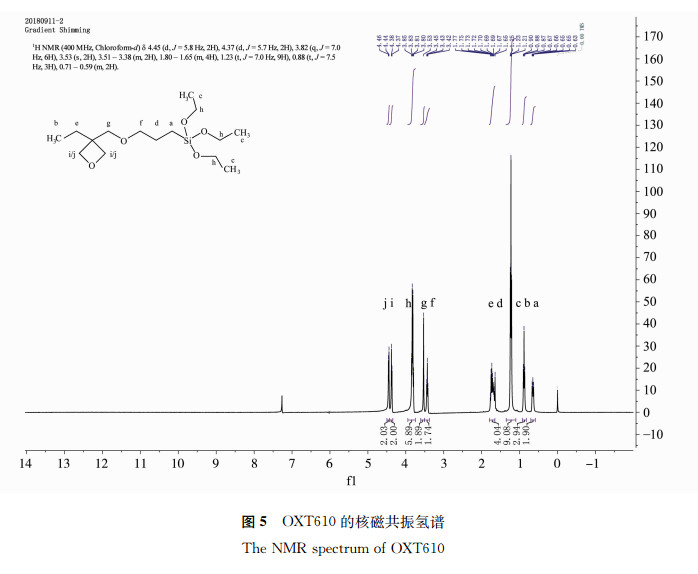
图 5是3-乙基-3-[[3-(三乙氧基硅)丙氧基]甲基]氧杂环丁烷(OXT610)的核磁共振氢谱:0.71~0.59(m, 2H, CH2);0.88(t, 3H, CH3);1.23(t, 9H, CH3);1.80~1.65(m, 4H, CH2);3.51~3.38(m, 2H, CH2);3.53(s, 2H, CH2);3.82(q, 6H);4.37(d, 2H, OCH2, ring);4.45(d,2H, OCH2, ring)。由谱图可以看到总共32个氢,和OXT610的总氢个数符合,氢原子种类数目及个数比均与结构相符,可确定该样品与目标结构一致。
|
图 5 OXT610的核磁共振氢谱 The NMR spectrum of OXT610 |
(1) 以3-乙基-3-羟甲基氧杂环丁烷为原料,与甲基磺酰氯磺酰化,得到3-乙基-3-甲磺酰基甲基氧杂环丁烷;在碱性条件下,以PEG600作相转移催化剂,3-乙基-3-甲磺酰基甲基氧杂环丁烷与乙二醇醚化得到2-[(3-乙基-3-氧杂环丁基)甲氧基]乙醇;然后与甲基丙烯酸甲酯进行酯交换得目的产物2-[(3-乙基-3-氧杂环丁烷)甲氧基]甲基丙烯酸乙酯;
(2) 3-乙基-3-羟甲基氧杂环丁烷与3-溴丙烯反应,然后在氯铂酸的催化下,与三乙氧基硅烷反应得到3-乙基-3-[[3-(三乙氧基硅)丙氧基]甲基]氧杂环丁烷;
(3) 产物经红外光谱和核磁共振谱表征得到确证。
| [1] |
张娜, 陈媛, 聂俊, 杨金梁. 光固化阳离子活性稀释剂研究进展[J]. 影像科学与光化学, 2016, 34(6): 491-504. Zhang N, Chen Y, Nie J, Yang J L. Research progress of cationic reactive diluents for photopolymerization[J]. Imaging Science and Photochemistry, 2016, 34(6): 491-504. |
| [2] |
苏建宇, 汪鲁焱, 郑怡倩, 刘敏, 卜凡乐, 刘安昌. 新型阳离子光固化活性单体3, 3-[氧基双亚甲基]-双[3-甲基]氧杂环丁烷的合成[J]. 武汉工程大学学报, 2018, 40(3): 263-266. Su J Y, Wang L Y, Zheng Y Q, Liu M, Bu F L, Liu A C. Synthesis of bis(3-methyloxetan-3-yl)methyl ether for novel cationic photocuringmonomer[J]. Journal of Wuhan Institute of Technology, 2018, 40(3): 263-266. DOI:10.3969/j.issn.1674-2869.2018.03.006 |
| [3] |
Crivello J V. Investigations of the reactivity of "kick-started" oxetanes in photoinitiated cationic polymerization[J]. Journal of Polymer Science Part A Polymer Chemistry, 2015, 53(4): 586-593. DOI:10.1002/pola.v53.4 |
| [4] |
Qian X C. Preparation of oxetan containing ester compounds[P]. WO2016066146, 2016-05-06.
|
| [5] |
El-Ghayoury A, Boukaftane C, De Ruiter B, Van Der Linde R. Ultraviolet-ultraviolet dual-cure process based on acrylate oxetane monomers[J]. Journal of Polymer Science, Part A:Polymer Chemistry, 2003, 41(4): 469-475. DOI:10.1002/(ISSN)1099-0518 |
| [6] |
Suzuki H, Goto K, Washimi A. Preparation of silylpro-poxyoxetanes for cationically photocurable polymer compositions[P]. JP2000247981, 2000-9-12.
|
| [7] |
Schulte B, Dannenberg C A, Keul H, Moeller M. Formation of linear and cyclic polyoxetanes in the cationic ring-opening polymerization of 3-allyloxymethyl-3-ethyloxetane and subsequent postpolymerization modification of poly(3-allyloxymethyl-3-ethyloxetane)[J]. Journal of Polymer Science, Part A:Polymer Chemistry, 2013, 51(5): 1243-1254. DOI:10.1002/pola.26494 |
| [8] |
Yeong C H, Su L J. Photosensitive resin composition with good adhesion[P]. KR2015081581, 2015-01-15.
|




