非酒精性脂肪肝(NAFLD)是世界范围内最常见的疾病之一,是因肝脏脂肪堆积过多而引起的慢性肝脏疾病,在一般人口中的估计流行率为10%~24%,在患有2型糖尿病或代谢综合征(如中心性肥胖、胰岛素抵抗等)的人群中更常见,且50%以上存在非酒精性脂肪肝的患者可进展为肝纤维化、肝硬化,甚至是肝细胞癌[1, 2]。近几年,NAFLD患病率逐年上升,其发病平均年龄在40~60岁,但随着儿童肥胖症的流行,现已逐渐年轻化,早期的诊断和治疗至关重要[3]。目前,NAFLD诊断的“金标准”是肝脏活检,但在大量高危患者中进行肝活检是不可行的,侵入性检查可对患者机体造成一定的损伤,因此,选择一种简单、方便、成本效益高、无创性的检测方法是非常迫切的,瞬时弹性成像技术(TE)是美国肝脏病研究协会(AASLD)推荐的评估肝脏疾病的重要手段,因其具有简便、快捷、无创、安全性和准确性高等多种优势而在临床上广泛应用[4, 5]。本文主要探讨NAFLD患者TE成像特点,并分析其与患者病情严重程度以及胰岛素抵抗之间的关系。
1 资料与标准选择2017年2月~2019年6月在我院进行体检的人群,选择经超声诊断的非酒精性脂肪肝患者112例,设为NAFLD组,另选择同期在本院进行健康体检的患者108例,设为对照组。NAFLD组,男53例、女59例,年龄(54.47±10.12)岁;对照组,男52例、女56例,年龄(53.89±10.03)岁。两组患者间性别、年龄差异无统计学意义,具有可比性。
纳入标准:①NAFLD组患者符合NAFLD诊断标准[6];②超声检查肝脏的近场回声较脾脏、肾脏弥漫性增强;肝脏管道结构紊乱;肝脏的远场回声衰减(以上异常具备任意两项或以上)。
排除标准:①合并有严重的冠心病、糖尿病、高血压等慢性基础性疾病;②长期酗酒史;③妊娠状态或哺乳期妇女或未成年人;④明确有病毒性肝炎、自身免疫性肝脏疾病、药物性肝病、失代偿期肝病、代谢性肝病等肝脏疾病;⑤艾滋或梅毒患者。
2 方法所有入选患者均常规测量身高体重,计算BMI(体重指数)指数,空腹抽血检查(包括肝功能、血常规、血脂、甲胎蛋白、血清胰岛素等),肝脏CT和瞬时弹性成像检查。
2.1 肝脏CT脂肪肝诊断标准选取门静脉主支进入肝脏时的层面,测量肝脏、脾脏CT值,并按照其比值确定,1.0≤无脂肪肝,0.7<轻度脂肪肝<1.0, 0.5<中度脂肪肝≤0.7,重度脂肪肝≤0.5。
2.2 血清学检查方法所有患者采血前一晚10:00以后禁食禁水,晨起抽空腹血,采用全自动生化分析仪和相关配套试剂检测肝功能等相关指标,操作过程严格按照操作规程进行。
2.3 瞬时弹性成像检查采用迈瑞公司提供的DC-85测量仪测量肝脏硬度以及CAP(受控衰减参数),按照用户说明手册进行操作。
2.4 统计学处理采用SPSS 22.0软件进行数据处理,以(x±s)表示定量资料,以t检验进行组间比较,以百分率表示计数资料,并以卡方检验进行组间比较,采用Spearman相关分析对CAP、HOMA-IR与NAFLD病情严重程度的相关性进行分析,均以P<0.05表示差异显著。
3 结果 3.1 脂肪肝组与健康对照患者基线资料比较两组患者年龄、性别比例、CAP、BMI、WBC(白细胞)、HGB(血红蛋白)、PLT(血小板)、TG(甘油三酯)、GHOL(胆固醇)、FBG(空腹血糖)、AFP(甲胎蛋白)等指标差异无统计学意义(P>0.05);NAFLD组AST(谷草转氨酶)、ALT(谷丙转氨酶)、肝脏硬度、血清胰岛素、HOMA-IR显著高于对照组,差异显著(P<0.05)。数据见表 1。
| 表 1 脂肪肝组与健康对照患者基线资料比较 |
不同程度脂肪肝患者之间性别比例、年龄、肝脏硬度、CAP、HGB、ALT、AST、FINS和HOMA-IR均差异显著(P<0.05)。见表 2。
| 表 2 不同程度脂肪肝组之间相关指标比较 |
分别采用ROC曲线分析TE成像对轻度、中度、重度NAFLD患者的诊断价值,结果表明CAP对轻度、中度和重度NAFLD均有较高的诊断价值,灵敏度分别为0.865、0.861、0.931,特异度分别为0.614、0.819、0.822。见表 3、图 1~3。
| 表 3 CAP对不同程度脂肪肝诊断价值比较 |

|
图 1 CAP诊断轻度NAFLD的ROC曲线 |
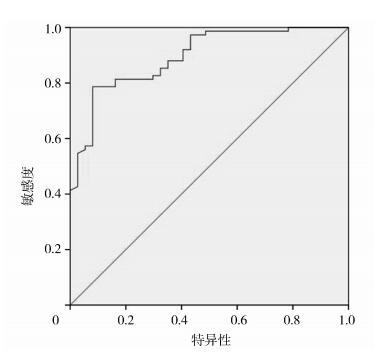
|
图 2 CAP诊断中度NAFLD的ROC曲线 |
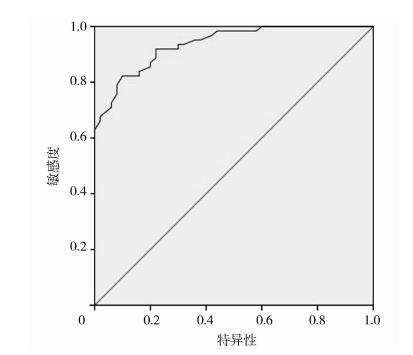
|
图 3 CAP诊断重度NAFLD的ROC曲线 |
CAP与NAFLD病情严重程度呈显著正相关(r=0.536);HOMA-IR与NAFLD病情严重程度呈显著正相关(r=0.479), 见表 4。
| 表 4 CAP及胰岛素抵抗与病情严重程度的相关性分析 |
NAFLD是全球最常见的肝脏疾病,影响约17%~46%的成年人,根据组织学分析,其特点是肝脏脂肪堆积过多,肝细胞脂肪变性超过5%,且伴有胰岛素抵抗,临床以肝脏转氨酶的升高和(或)超声检查异常为主要表现,随着发病时间的增长,可显著增加患者罹患肝硬化、肝功能衰竭和肝细胞癌的风险。
有研究表明,胰岛素抵抗是NAFLD发病的重要因素[7, 8]。肝脏是合成脂肪和糖异生的重要场所,当患者发生胰岛素抵抗时,机体内脂肪酸出现代谢失衡,甘油三酯合成过多且无法及时输出,进而堆积于肝脏,导致肝脏出现脂肪变性。目前,肝活检被认为是一种安全的手术方法,已用于肝脏一级的筛选、评分和解释,可辅助临床医生明确患者病情诊断,但由于是侵袭性检查,它可能伴随着一些不良反应,包括疼痛、感染、出血等[9, 10]。TE是一种新的声波测量成像技术,通过测量肝硬度判断肝纤维化分期,检查快速便捷,近年来探头的更新研制大大降低了体重指数(BMI)>28 kg/m2患者的检查失败率,在临床广泛使用[11]。Koch等[12]通过对非酒精性脂肪肝的诊断研究发现,TE对NAFLD有着较高的敏感性,诊断准确率高,可辅助临床医师对病情分期作出准确判断。本研究中,健康人群与NAFLD组患者对比发现,NAFLD患者肝功能指标、肝脏硬度以及胰岛素水平较正常人有明显差异,且随着脂肪肝程度的增加,患者年龄普遍偏高,男性多于女性,肝脏硬度、肝功能指标以及胰岛素水平均明显升高,同时发现,CAP对轻度、中度和重度NAFLD均有较高的诊断价值,且随着病情严重程度的加深,CAP的值也逐渐升高。
目前,“二次打击”(two-hit hypothesis)学说在NAFLD发病机制中广受关注:当机体出现胰岛素抵抗时,肝内脂质过度蓄积,人体内源性细胞损害因子致敏性提高,此为第一次打击,与此同时,在炎性、氧化应激反应作用下,出现第二次打击,被激活的损害因子导致肝细胞进一步受损,炎性反应加剧,甚至出现肝纤维化、坏死等[13, 14]。本研究中,NAFLD组患者出现胰岛素抵抗,其空腹血糖水平的升高,表明其胰岛素抵抗进一步加重,且胰岛β细胞增加无明显补偿作用。同时,胰岛素抵抗在使肝脏脂肪合成增多的同时,也促进了人体内氧化应激反应,加重NAFLD患者体内坏死炎症反应物的生成。因此,早期评估胰岛素抵抗风险值并合理干预对NAFLD患者至关重要。Sree等[15]通过对60例存在胰岛素抵抗的患者研究发现,NAFLD发病率明显升高,且肝脏纤维化程度普遍偏高,胰岛素抵抗与肝脏病变存在明显的相互作用。本研究中,随着脂肪肝严重程度的加深,患者FINS、HOMA-IR水平也逐渐升高。
本研究主要通过TE检测患者肝脏的脂肪沉积情况,由于常规肝脏超声检查结果与检查者密切相关,无法保证客观性,而肝脏穿刺成本昂贵,且为侵入性检查,并发症发生率高,可重复性差,无法有效评价患者肝脏脂肪转归情况。TE作为相对成熟的无创检查,对10%以上的肝脏脂肪病变可准确测量区分,成本低廉,可反复使用,且不受检查者主观性干扰,可对肝脏纤维化程度、脂肪病变定量检测以及肝脏二维状态同时检测,使用前景良好,是我国慢性乙型肝炎防治指南中肝纤维化评估的重要推荐检查手段,TE成像特点对于NAFLD病情的评估具有重要意义[16, 17]。
综上所述,NAFLD患者TE成像与不同程度NAFLD密切相关,胰岛素抵抗可临床辅助诊断NAFLD。
| [1] |
Kan C, Jianbo M, Xiaoyuan J, et al. Advancing the understanding of NAFLD to hepatocellular carcinoma development:From experimental models to humans[J]. Biochimica et Biophysica Acta (BBA)-Reviews on Cancer, 2019, 1871(1): 117-125. |
| [2] |
Cyrielle C, Jun C, Mosab H A, et al. Association between obesity and discordance in fibrosis stage determination by magnetic resonance vs transient elastography in patients with nonalcoholic liver disease[J]. Clinical Gastroenterology and Hepatology, 2018, 16(12): 1974-1982. |
| [3] |
Cynthia H, Cyrielle C, Kento I, et al. Magnetic resonance vs transient elastography analysis of patients with nonalcoholic fatty liver disease:a systematic review and pooled analysis of individual participants[J]. Clinical Gastroenterology and Hepatology, 2019, 17(4): 630-637. |
| [4] |
中华医学会肝病学分会脂肪肝和酒精性肝病学组. 2010非酒精性脂肪性肝病诊疗指南(2010年修订版)[J]. 胃肠病学和肝脏病学杂志, 2010, 19(6): 483-487. The Chinese National Work-shop on Fatty Liver and Alcoholic Liver Disease for the Chinese Liver Disease Association. Guidelines for management of nonalcoholic fatty liver disease:updated and revised edition[J]. Chinese Journal of Gastroenterology and Hepatology, 2010, 19(6): 483-487. |
| [5] |
Ahmad H, Dyah P, Kemal F K, et al. The influence of insulin resistance in the occurence of non-alcoholic fatty liver disease among first degree relatives of type 2 diabetes[J]. Diabetes & Metabolic Syndrome-Clinical Research & Reviews, 2019, 13(2): 1431-1435. |
| [6] |
Zobair M Y. Non-alcoholic fatty liver disease-a global public health perspective[J]. Journal of Hepatology, 2019, 70(3): 531-544. |
| [7] |
Christian B, Luisa S, Sophie S, et al. Elevated hepatic DPP4 activity promotes insulin resistance and non-alcoholic fatty liver disease[J]. Molecular Metabolism, 2017, 6(10): 1254-1263. |
| [8] |
Sanjay R, Patricia M. Non-alcoholic fatty liver disease[J]. Paediatrics and Child Health, 2017, 27(12): 556-560. |
| [9] |
南月敏, 付娜, 李文聪, 等. 2017美国非酒精性脂肪性肝病诊断与管理指南解读[J]. 中华肝脏病杂志, 2017, 25(9): 687-694. Nan Y M, Fu N, Li W C, et al. An interpretation of the AASLD practice guideline on the diagnosis and management of nonalcoholic fatty liver disease in 2017[J]. Chinese Journal of Hepatology, 2017, 25(9): 687-694. |
| [10] |
中华医学会肝病学分会脂肪肝和酒精性肝病学组. 非酒精性脂肪性肝病防治指南(2018更新版)[J]. 现代医药卫生, 2018, 34(5): 641-649. Fatty Liver and Alcoholic Liver Disease Group, Chineses Society of Hepatology. Guideline of prevention and treatment for nonalcoholic fatty liver disease:a 2018 update[J]. Modern Medicine & Health, 2018, 34(5): 641-649. |
| [11] |
曾静, 范建高, 爱肝联盟. 弹性成像技术在慢性肝病诊断中应用的美国共识[J]. 实用肝脏病杂志, 2018, 21(1): 32-33. Zeng J, Fan J G, Love Liver Alliance. American consensus on the application of elastography in the diagnosis of chronic liver disease[J]. Journal of Clinical Hepatology, 2018, 21(1): 32-33. |
| [12] |
Koch L K, Yeh M M. Nonalcoholic fatty liver disease (NAFLD):diagnosis, pitfalls, and staging[J]. Annals of Diagnostic Pathology, 2018, 37: 83-90. |
| [13] |
中国中西医结合学会消化系统疾病专业委员会. 非酒精性脂肪性肝病中西医结合诊疗共识意见(2017年)[J]. 中国中西医结合消化杂志, 2017, 25(11): 805-901. Digestive Diseases Committee of Chinese Society of Integrated Traditional and Western Medicine. Consensus opinions on the diagnosis and treatment of non-alcoholic fatty liver disease with integrated Chinese and western medicine (2017)[J]. Chinese Journal of Integrated Traditional and Western Medicine on Digestion, 2017, 25(11): 805-901. |
| [14] |
中华医学会内分泌学分会. 非酒精性脂肪性肝病与相关代谢紊乱诊疗共识(第二版)[J]. 中华内分泌代谢杂志, 2018, 34(7): 549-554. Chinese Societyof Endocrinology, Chinese Medical Association. Consensus for diagnosis and treatment of nonalcoholic fatty liver disease and metabolic disorders(2nd Edition)[J]. Chinese Journal of Endocrinology and Metabolism, 2018, 34(7): 549-554. |
| [15] |
Sree H V, Sunanda T, Pradeep T V S, et al. Insulin resistance and hyperandrogenemia independently predict nonalcoholic fatty liver disease in women with polycystic ovary syndrome[J]. Diabetes & Metabolic Syndrome:Clinical Research & Reviews, 2019, 13(2): 1065-1069. |
| [16] |
张霞霞, 徐有青. 《2018年国际肝移植协会意见:非酒精性脂肪性肝炎的管理和治疗》摘译[J]. 临床肝胆病杂志, 2019, 35(1): 64-66. Zhang X X, Xu Y Q. An excerpt of the recommendations of international liver transplantation society for management and treatment of nonalcoholic steatohepatitis (2018)[J]. Journal of Clinical Hepatology, 2019, 35(1): 64-66. |
| [17] |
瞬时弹性成像技术(TE)临床应用共识专家委员会. 瞬时弹性成像技术(TE)临床应用专家共识(2015年)[J]. 中国肝脏病杂志(电子版), 2015, 7(2): 12-18. Consensus Expert Committee on Clinical Applications of Transient Elastography (TE). Consensus of experts on the clinical application of instantaneous elastic imaging technology(TE)(2015)[J]. Chinese Journal of Liver Diseases(Electronic Version), 2015, 7(2): 12-18. |



