乳腺癌是困扰女性健康的恶性肿瘤, 2017年美国癌症协会发布的数据显示, 乳腺癌居女性恶性肿瘤发病率的首位[1]。而致密型乳腺是乳腺癌的独立危险因子, 尤其东方女性腺体大多较致密。目前临床广泛应用于乳腺疾病诊断的全视野数字化乳腺摄影(full-field digital mammography, FFDM), 具有操作简单、便捷的特点。有研究报道FFDM检测乳腺癌的灵敏度为75%~85%[2],但在致密乳腺腺体组织中诊断效能可降低至50%[3]。对比增强能谱乳腺X线摄影(contrast enhanced specral mammography, CESM)是在FFDM基础上衍生的一项新技术,该技术利用碘的K缘效应(33.2 keV),注射碘对比剂后, 对同一体位进行高能(45~49 kVp)和低能(26~31 kVp)图像采集,通过融合和减影获得低能图像和减影图像。本文通过对比分析CESM和FFDM两种检查方法在致密型乳腺疾病中的诊断效能,探讨CESM在致密型乳腺疾病中的临床应用价值。
1 资料与方法 1.1 临床资料回顾性分析了2017年3月~2018年12月在我院乳腺外科就诊并经病理证实的137例患者,所选患者均为女性且纤维腺体为致密型,年龄23岁~77岁,平均(44.12±11.39)岁。纳入标准:(1)患者5年内未做过乳腺手术;(2)在一周内行FFDM和CESM两种检查;(3)根据美国放射学院(American College of Radiology, ACR)建立并推荐的乳腺影像报告和数据系统(breast imaging reporting and date system, BI-RADS)的标准[4],乳腺密度为c型的患者有108例(78.83%),d型有29例(21.17%);(4)最终诊断结果经病理证实。排除标准:(1)既往有乳腺手术史或接受过乳腺治疗; (2)备孕、妊娠和哺乳期女性;(3)对碘对比剂过敏、肾脏功能不全的患者。检查前充分告知患者或其监护人对比剂使用的适应症、禁忌症、可能发生的不良反应和注意事项,并签署“碘对比剂使用患者知情同意书”。
1.2 检查仪器与方法FFDM检查采用GE Senographe Essential全数字化乳腺机,摄取常规头尾位(craniocaudal,CC)、内外斜位(mediolateral oblique,MLO)图像。CESM检查采用GE Senographe Essential CESM钼靶机。检查前于站立位经患者前臂静脉注射对比剂碘海醇(300 mg/mL),剂量为1.5 mL/kg, 速率为2.0~ 3.0 mL/s。注入对比剂2 min后开始摄影,7 min内完成双乳CC位和MLO位的屏气摄影。
1.3 图像分析由两名放射科医师(分别有15年和7年的乳腺影像诊断经验)采用双盲法对CESM和FFDM图像进行评价。由于目前尚无CESM图像的判读标准,需结合低能图并分析减影图上病灶是否强化以及强化的形态特征,并参照BI-RADS分类标准对病灶特征进行描述和分类。术前判定为BI-RADS 1、2类为无病灶,BI-RADS 3类及以上为有病灶,BI-RADS 4C类以下为良性,BI-RADS 4C类及以上为恶性,影像诊断结果均与病理结果对照,主要分析乳腺腺体类型,观察整体病灶及病灶边缘情况,计算并比较CESM与FFDM诊断致密型乳腺疾病的敏感度、特异度、阳性预测值、阴性预测值和准确率。
1.4 统计学方法使用SPSS 20.0统计软件进行分析,采用χ2检验比较CESM与FFDM在致密型乳腺疾病中的诊断效能,P < 0.05认为差异有统计学意义。
2 结果 2.1 病理诊断137例患者经病理证实共检测出140个病灶,病灶位于左乳70例,右乳62例,双乳均有的4例。其中良性病灶105个(囊性伴纤维瘤32个、腺病伴纤维腺瘤28个、纤维腺瘤23个、腺病15个、纤维性导管内乳头状瘤3个、囊肿伴炎症3个、纤维组织增生1个);恶性病灶35个(浸润性癌11个、导管原位癌9个、浸润性导管癌9个、原位癌2个、浸润性小叶癌1个、淋巴转移癌1个、皮肤Paget病1个、浸润性导管癌伴导管原位癌1个)。
2.2 影像检查方法对病灶的检验结果采用CESM与FFDM检出病灶(BI-RADS分类3、4、5型)分别为137和125个(详见表 1)。
| 表 1 采用不同影像检查方法对病灶进行BI-RADS分类的结果(个) |
CESM除3个未检出的病灶(1个纤维囊性乳腺病、1个纤维瘤、1个腺病)之外,共检出137个病灶。减影图上肿块样强化有99个,非肿块样强化有38个。其中FFDM检出的125个病灶在CESM的低能图和减影图像上均可见异常,12个病灶仅可在减影图上被检出,这12个病灶中,10个表现为肿块样强化,2个表现为非肿块样强化;恶性病灶5个(浸润性癌2个、导管原位癌2个、浸润性小叶癌1个),良性病灶7个(腺病3个、纤维瘤2个、囊性伴纤维瘤2个)。FFDM检出的125个病灶中,其中肿块不伴钙化的有74个,肿块伴钙化的有13个,单纯钙化的有16个,结构扭曲的有15个,其他7个。
CESM和FFDM的诊断效能详见表 2所示。CESM和FFDM对图像的错误判读: CESM错误判读病灶5个,其中恶性病灶2个,1个导管原位癌在减影图上表现为中央区0.7 cm强化结节影,诊断为BI-RADS 4A类;另1个浸润性癌在减影图上呈明显片团状强化,诊断为BI-RADS 4B类。3个良性病灶被错误判读,其中2个纤维腺瘤在减影图上表现为强化结节影,诊断为BI-RADS 4C类;1个腺病伴导管上皮普通型增生在减影图上表现为肿块样明显强化,诊断为BI-RADS 4C类。FFDM错误判读病灶38个,其中恶性病灶13个(诊断为BI-RADS 1类5个、3类3个、4A类3个、4B类2个),良性病灶25个(诊断为BI-RADS 4C类18个、5类7个)。
| 表 2 采用不同的影像检查方法对140个病灶的诊断效能 |
CESM在致密型乳腺疾病诊断方面的特异度、阳性预测率和准确率均高于FFDM且存在显著差异(χ2=16.003、14.083、25.445;P=0.00),敏感度和阴性预测率的差异无统计学意义(χ2=6.563、6.887;P=0.10、0.09)。
3 讨论FFDM是一项临床广泛应用于乳腺疾病的检测方法[5]。由于FFDM获得的是乳腺纤维腺体组织重叠图像,对于腺体较致密的患者,重叠的腺体对病灶显示的影响较大,容易造成病灶的漏诊和误诊。CESM是基于常规乳腺X线摄影技术、使用对比剂显影的一项新型成像技术,经过系统后处理可得到低能图和减影图像,且低能图与FFDM图像质量相当[6], 而减影图剔除了乳腺正常软组织且额外提供了病灶的血供信息,可以显著减少假阳性和假阴性结果,提高了特异性和灵敏度,评价病变的准确性更高[7, 8]。有研究[9, 10]表明CESM诊断乳腺癌的敏感度约为91%~100%,与动态对比增强磁共振成像的敏感度79%~98%相似。由于CESM检查时间短,因此对于有磁共振检查禁忌的患者,可作为一种替代的检查方法,有潜力在乳腺癌的检测和分期中发挥重要的作用[11, 12]。
本研究对137例患者的140个乳腺病灶进行回顾性分析,比较了CESM和FFDM对致密型乳腺疾病的诊断效能,结果显示CESM比FFDM的敏感度提高了28.57%(91.42% vs. 62.85%),特异度提高了20.72%(96.91% vs. 76.91%), 阳性预测值提高了42.07%(88.88% vs. 46.81%),阴性预测值提高了11.09%(97.11% vs. 86.02%),准确率提高了22.15%(95% vs. 72.85%), 与Cheung等[13]的研究结果基本相符。
Houben等[14]研究显示,CESM在乳腺癌筛查召回患者中可以检测出更多的病灶,本研究结果与之一致,CESM检出137个病灶,多于FFDM检出的125个病灶,证明CESM对致密型乳腺疾病的检出率高于FFDM。仅被CESM减影图检出的12个病灶中,其中5个恶性病变灶均表现为肿块样强化(见图 1), 7个良性病灶中5个表现为肿块样强化,2个表现为环形强化结节影。Badr等[15]报道恶性肿瘤新生血管较多,在减影图上往往表现为重度或中度肿块样强化,而良性病灶往往显示为无强化,但俞敏秋等[16]发现早期低度恶性肿瘤也表现为明显或者轻度强化,Petal等[17]研究显示良性病灶也会表现为肿块样轻中度强化,说明我们不能仅凭病灶是否强化和病灶的强化程度来判别良恶性。比如本研究中一例浸润性小叶癌(见图 2)表现为轻中度强化,易与良性病灶混淆,我们应该进一步对病灶强化特征进行定性分析,以探索不同类型乳腺疾病的强化特征。未被CESM检出的3个良性病灶,病灶直径均小于1 mm,在注射对比剂后,由于正常的乳腺腺体在减影图像上也会产生强化,实质背景明显强化会对较小的病灶产生遮挡,造成漏诊和误诊。有研究显示[18]背景实质强化程度可能与绝经、放疗前、激素治疗前、乳腺纤维腺体密度具有相关性,因此临床工作中应反复仔细阅片,并对照对侧乳腺图像,尽可能减少误诊或漏诊。由于CESM需要注射碘对比剂,比FFDM增加了碘过敏的风险[19],所以CESM更适用于临床或相关检查已发现肿块、可疑恶性钙化、结构异常、多灶病变者以及手术后、放疗或化疗患者复查等,可提供更多的信息便于临床诊断。本研究存在的不足之处:CESM应用于临床的时间较短,诊断老师的经验不够丰富,在强化的判读上仍有一些困难;敏感性差异无统计学意义,可能是样本中恶性病灶较少的原因,在以后的研究中需要多收集一些恶性病灶来进一步论证。

|
图 1 36岁女性的全视野数字化乳腺X摄影(FFDM)和对比增强能谱乳腺X线摄影(CESM) 图a和b为左乳FFDM的CC位和MLO位图像,显示乳腺纤维腺体组织呈ACR C型,且未见异常征像,诊断为BI-RADS 3类;图c和e为CESM低能图像,CC位和MLO位未见异常征像;图d和f中CESM减影图像CC位和MLO位发现异常强化灶,诊断为BI-RADS 4C类,病理证实为导管内癌 |
|
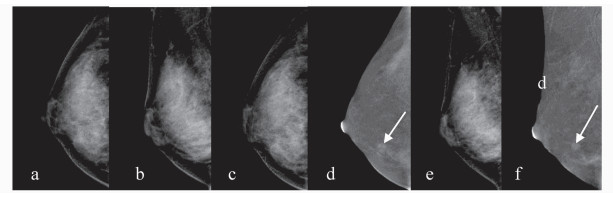
图 2 38岁女性的全视野数字化乳腺X摄影(FFDM)和对比增强能谱乳腺X线摄影(CESM) 图a和b为右乳FFDM的CC位和MLO位图像,显示乳腺纤维腺体组织呈ACR d类,未见异常征像;图c和e为CESM低能图像CC位和MLO位未见异常征像,诊断为BI-RADS 3类;图d和f为CESM减影图的CC位和MLO位,右乳内下象限见1.2×1.2 cm2轻中度强化肿块影,诊断为BI-RADS 4C类,病理证实为浸润性小叶癌 |
综上所述,与FFDM相比,CESM可以提高对致密型乳腺疾病的诊断效能,因此CESM更适用于对致密型乳腺疾病的筛查,具有较高的临床应用价值。
| [1] |
Siegel R L, Miller K D, Jemal A. Cancer statistics, 2017[J]. CA: A Cancer Journal for Clinicians, 2017, 67(1): 7-30. DOI:10.3322/caac.21387 |
| [2] |
Shetty M K. Screening for breast cancer with mammography: current status and an overview[J]. Indian Indian Journal of Surgical Oncology, 2010, 1(3): 218-223. DOI:10.1007/s13193-010-0014-x |
| [3] |
Mori M, Akashi-Tanaka S, Suzuki S, et al. Diagnostic accuracy of contrast-enhanced spectral mammography in comparison to conventional full-field digital mammography in a population of women with dense breasts[J]. Breast Cancer, 2017, 24(1): 104-110. |
| [4] |
D'Orsi C J, Sickles E A, Mendelson E B, et al. ACR BI-RADSⓇ Atlas, Breast Imaging Reporting and Data System[M]. Reston, VA: American College of Radiology, 2013.
|
| [5] |
Marmot M G, Altman D G, Cameron D A, et al. The benefits and harms of breast cancer screening: an independent review[J]. British Journal of Cancer, 2013, 108(11): 2205-2240. DOI:10.1038/bjc.2013.177 |
| [6] |
Francescone M A, Jochelson M S, Dershaw D D, et al. Low energy mammogram obtained in contrast-enhanced digital mammography (CEDM) is comparable to routine full-field digital mammography (FFDM)[J]. European Journal of Radiology, 2014, 83(8): 1350-1355. DOI:10.1016/j.ejrad.2014.05.015 |
| [7] |
Bhimani C, Li L, Liao L, et al. Contrast-enhanced spectral mammography: modality-specific artifacts and other factors which may interfere with image quality[J]. Academic Radio-logy, 2017, 24(1): 89-94. DOI:10.1016/j.acra.2016.08.024 |
| [8] |
姜婷婷, 张盛箭, 李瑞敏, 等. 对比增强能谱X线摄影对乳腺疾病的诊断价值[J]. 中华放射学杂志, 2017, 51(4): 273-278. Jiang T T, Zhang S J, Li R M, et al. Diagnostic performance of contrast-enhanced spectral mammography[J]. Chinese Journal of Radiology, 2017, 51(4): 273-278. |
| [9] |
Lobbes M B, Lalji U, Houwers J, et al. Contrast-enhanced spectral mammography in patients referred from the breast cancer screening programme[J]. European Radiology, 2014, 24(7): 1668-1676. |
| [10] |
Fallenberg E M, Dromain C, Diekmann F, et al. Contrast-enhanced spectral mammography versus MRI: initial results in the detection of breastcancer and assessment of tumour size[J]. European Radiology, 2014, 24(1): 256-264. |
| [11] |
Iotti V, Ravaioli S, Vacondio R, et al. Contrast-enhanced spectral mammography in neoadjuvant chemotherapy monitoring: a comparison with breast magnetic resonance imaging[J]. Breast Cancer Research, 2017, 19(1): 106. |
| [12] |
Barra F R, de Souza F F, Camelo REFA, et al. Accuracy of contrast-enhanced spectral mammography for estimating residual tumor size after neoadjuvant chemotherapy in patients with breast cancer: a feasibility study[J]. Radiologia Brasileira, 2017, 50(4): 224-230. DOI:10.1590/0100-3984.2016-0029 |
| [13] |
Cheung Y C, Lin Y C, Wan Y L, et al. Diagnostic performance of dual-energy contrast-enhanced subtracted mammography in dense breasts compared to mammography alone: interobserver blind-reading analysis[J]. European Radiology, 2014, 24(10): 2394-2403. DOI:10.1007/s00330-014-3271-1 |
| [14] |
Houben I P L, Van de Voorde P, Jeukens C R L P N, et al. Contrast-enhanced spectral mammography as work-up tool in patients recalled from breast cancer screening has low risks and might hold clinical benefits[J]. European Journal of Radiology, 2017, 94: 31-37. DOI:10.1016/j.ejrad.2017.07.004 |
| [15] |
Badr S, Laurent N, Régis C, et al. Dual-energy contrast-enhanced digital mammography in routine clinical practice in 2013[J]. Diagnostic Interventional Imaging, 2014, 95(3): 245-258. DOI:10.1016/j.diii.2013.10.002 |
| [16] |
俞敏秋, 李俊晨. 对比增强能谱成像与动态增强磁共振成像诊断乳腺癌的对比研究[J]. 中国医疗设备, 2017, 32(11): 74-77. YU M Q, LI J C. Comparative study of contrast-enhanced spectral mammography and dynamic contrast-enhanced magnetic resonance imaging in diagnosis of breast cancer[J]. China Medical Devices, 2017, 32(11): 74-77. DOI:10.3969/j.issn.1674-1633.2017.11.018 |
| [17] |
Patel B K, Hilal T, Covington M, et al. Contrast-enhanced spectral mammography is comparable to MRI in the assessment of residual breast cancer following neoadjuvant systemic therapy[J]. Annals of Surgical Oncology, 2018, 25(5): 1350-1356. DOI:10.1245/s10434-018-6413-x |
| [18] |
Sogani J, Morris E A, Kaplan J B, et al. Comparison of background parenchymal enhancement at contrast-enhanced spectral mammography and breast MR imaging[J]. Radiology, 2017, 282(1): 63-73. DOI:10.1148/radiol.2016160284 |
| [19] |
Patel B K, Lobbes M B I, Lewin J, et al. Contrast enhanced spectral mammography: a review[J]. Semin Ultrasound CT MR, 2018, 39(1): 70-79. DOI:10.1053/j.sult.2017.08.005 |



