2. 重庆市中医院 放射科, 重庆 400021
2. Department of Radiology, Chongqing Traditional Chinese Medicine Hospital, Chongqing 400021, P. R. China
乳腺癌作为恶性肿瘤,具有较高发病率,近年来发展呈年轻化趋势,严重威胁妇女生命健康[1]。乳腺癌患者早期临床症状多表现为乳痛、可偶然触及肿块、乳头糜烂或溢液等[2],不具有典型特征,难以确诊。早期诊断对提高临床治疗效果和改善患者预后具有积极意义。磁共振(magnetic resonance, MRI)技术对软组织分辨率较高,其中包括MRI增强扫描(dynamic contrast-enhanced magnetic resonance imaging, DCE-MRI)、磁共振扩散加权成像(diffusion weighted imaging, DWI)等,具有无辐射、成像清晰等特点,明显优于其他影像学检查方式[3]。由于单一诊断可能导致部分漏诊或误诊发生,影响后期治疗,本研究对乳腺癌患者行DCE-MRI与DWI联合检测,以探究二者在乳腺癌诊断中的临床应用价值。
1 资料和方法 1.1 一般资料回顾性分析2015年8月~2017年8月于本院收治的经手术病理证实的乳腺癌患者81例,纳入标准:(1)患者均为首次入院,经手术病理证实为乳腺癌;(2)术前接受MRI检查,且未经放化疗及介入治疗;(3)经伦理会批准及患者同意。排除标准:(1)合并其他恶性肿瘤者;(2)不宜行MRI扫描者;(3)影像学资料不完整或图像质量较差者。
患者年龄21~75岁,平均年龄(40.95±5.74)岁;病灶大小0.5 mm×0.6 cm~1.5 mm×2.0 cm,平均病灶大小0.8 mm×1.2 cm;病灶位置:左侧37例、右侧44例;类型:浸润性导管癌32例、乳腺纤维瘤24例、黏液癌11例、浸润性小叶癌8例,导管内乳头状瘤6例。
1.2 检查方法仪器:美国GE HD 1.5T磁共振扫描仪,使用8通道专用乳腺线圈进行信号采集。所有患者均呈俯卧位,头先进,充分暴露双侧乳房并自然下垂于线圈当中,保持自然呼吸。设置扫描序列为横断面T1WI、T2WI和矢状面T1WI、T2WI+脂肪抑制序列,对患者进行常规扫描,获取形态学信息。
1.2.1 DCE-MRI检测与图像分析设置层厚5.0 mm,层距1.0 mm,TE 4.6 ms,TR 1.8 ms,FOV 30 mm×30 mm。先进行平扫,随后增强扫描,建立手背静脉通道,给患者注射钆喷替酸葡甲胺(Gd-DPTA)对比剂(剂量为0.2 mmol/kg体质量,速率为2.5 mL/s),然后使用20~30 mL生理盐水冲洗。间隔8 s后再连续无间隔扫描7次,30 s/次。扫描结束后,将后7次图像与首次扫描图像自动减影,并进行多平面重建处理与最大密度投影,得到病灶部位时间-信号强度曲线(time signalintensity curves,TIC)。
依据Kuhl分型进行良/恶性鉴别[4]:Ⅰ型即持续上升型,信号强度持续性增强,可作为良性诊断依据;Ⅱ型即平台型,信号早期强化,中后期维持信号强度;Ⅲ型即流出或轮廓型,信号早期强化,中后期信号逐步降低。Ⅱ型与Ⅲ型可作为恶性诊断依据。
1.2.2 DWI检测与图像分析采用单次激发回波平面成像技术(SE-EPI)轴位扫描+脂肪抑制,取b值1000 s/mm2,层厚4 mm,层距1.0 mm。所有图像均上传至GE Advantage Workstation工作站,对阈值进行调节并定义感兴趣区(ROI),ROI面积≥5 mm2,避开血管坏死区域及囊变部位,选择准备分析图像。在b=1000 s/mm2条件下,消除伪影并计算扩散系数(apparent diffusion coeffcient,ADC),反复测量3次后取平均值,即为该病灶ADC值。
乳腺癌良/恶性病灶鉴别结果由2名具有10年临床经验医师进行独立分析判断,意见不一致时可共同讨论以得出结论。
1.3 统计学方法使用四格表对诊断数据进行统计,并计算各检测方式敏感度、特异度、准确度、阳性预测值及阴性预测值。采用统计学软件SPSS 22.0分析数据,计数资料用n(%)描述,计量资料用(x±s)描述,两组比较分别采用χ2及t检验,采用受试者作业特征曲线(ROC)分析ADC值诊断乳腺癌良/恶性的效果,以P<0.05为差异有统计学意义。
2 结果 2.1 不同检查方法与病理结果的比较经手术病理诊断,81例乳腺癌患者中良性37例、恶性44例。以病理结果为金标准,DCE-MRI检测、DWI检测和联合检测的结果详见表 1。
| 表 1 不同检查方法与病理结果的比较 |
DCE-MRI与DWI联合检测的敏感度与准确度显著高于单一检测(P<0.05),详见表 2。
| 表 2 3种检查方法的数据比较 |
恶性病灶以Ⅲ型为主,良性病灶以Ⅰ型为主,良/恶性病灶TIC分型分布比较,差异具有统计学意义(P<0.05),详见表 3。
| 表 3 良/恶性病灶TIC分型比较 |
恶性病灶的ADC值显著低于良性病灶(P<0.05),详见表 4。
| 表 4 良/恶性病灶的ADC值比较(x±s,×10-3 mm2/s) |
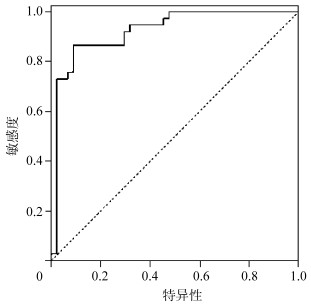
在b=1000 s/mm2条件下,ROC曲线结果显示,ADC值诊断乳腺癌良/恶性AUC为0.923(95%置信区间为0.862~0.984,P=0.000),最佳界限值为1.28×10-3 mm2/s,此时灵敏度为86.5%、特异度为90.9%,约登指数为0.774。见图 1。
|
图 1 ADC值诊断乳腺癌良/恶性的ROC曲线 |
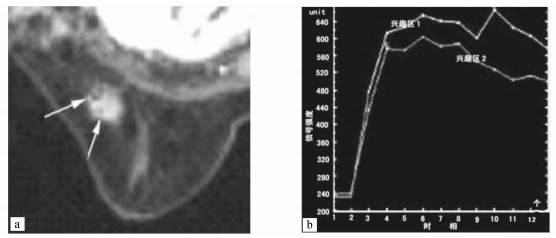
典型病例1:患者45岁,乳腺纤维瘤,经MRI显示病灶边缘不光滑,可见短毛刺征,以较高血流信号为主,DCE-MRI扫描ROI两区(箭头所示),其TIC为Ⅱ型,如图 2所示。
|
图 2 典型病例1的MRI成像结果 a. DCE-MRI扫描ROI两区;b. TIC为Ⅱ型 |
典型病例2:患者53岁,浸润性导管癌,经MRI显示病灶边缘不光滑,可见毛刺,T1脂肪抑制序列左侧乳腺上象限部位可见不规则肿块(箭头所示),DWI检测在ADC图呈低信号,如图 3所示。

|
图 3 典型病例2的MRI成像结果 a. T1脂肪抑制序列见不规则肿块;b. ADC呈低信号 |
乳腺癌是女性高发恶性肿瘤,目前虽可通过乳腺癌根治术、保乳术、术后放化疗等手段治疗[5],但早期若不能及时发现并进行有效治疗,肿瘤易发生全身转移,导致患者病情恶化,生存率及生存质量明显降低[6]。影像学检查对乳腺癌早期诊断与分期具有重要价值[7],其中X线钼靶、超声等传统检查方式虽可发现病灶[8],但难以有效区分良/恶性病变,导致乳腺癌漏诊或误诊较多,患者易错过最佳治疗时机。近年来随影像学技术不断发展,MRI作为集多层面、多参数、多技术的成像方法,对软组织分辨率极高,可清晰观察和收集患者病灶形状、强化方式、信号特点等信息,广泛应用于临床多种疾病诊断。有研究证实,MRI对乳腺癌诊断具有较高敏感性及准确度,还可有效鉴别良/恶性病灶,具有重要临床应用价值[9]。
DCE-MRI和DWI为常见的两种MRI技术检查手段,可为诊断乳腺癌及鉴别良/恶性病变提供重要数据信息。DCE-MRI可在任意角度断层,进行三维重建,因此其定位病灶更加准确,能够直接观察病灶特点。良/恶性病变组织在血管通透性、间隙结构及微循环等方面存在明显差异[10],而DCE-MRI可较好显示深部病灶、精确判断病灶强化程度,因此可提高良/恶性病灶诊断的准确率[11-13]。此外,在应用对比剂条件下,绘制不同TIC曲线并观察信号变化情况,可对病变性质进行划分[14]。但因DCE-MRI技术主要通过TIC及形态学综合分析鉴别,多依赖于医师临床经验与主观判断,对医师水平要求较高,存在一定应用限制[15, 16]。不同病理状态下,水分子运动受弥散系数、生物膜等因素影响,存在明显差异[17]。DWI作为一种新型成像技术,可精确检测水分子运动微小变化情况,而且采集图像清晰显示,便于定位病灶,可为临床疾病诊断与鉴别提供依据,具有检测时间短等优点[18]。DWI在检测方式方面优于DCE-MRI,该技术图像采集时间短,可避免使用造影剂,对人体无创,不良反应较少且适用范围更广。此外,DWI技术利用ADC值作定量分析,准确性较高,受到患者及医师高度认可,具有临床应用推广的优势[19]。
本研究结果显示,DCE-MRI、DWI及联合检测的准确度分别为80.25%、83.95%、95.06%,且DCE-MRI与DWI联合检测敏感度与准确度显著高于单一检测,表明DCE-MRI及DWI单一检测在一定程度上虽可较为准确地鉴别乳腺癌良/恶性病变,但敏感度与特异度均较低,不利于临床早期发现和治疗,而DCE-MRI与DWI联合检测取得了满意成果,显著提高了对乳腺癌的临床诊断效能,该研究结果与彭建波等[20]认为DCE-MRI联合DWI可提高对乳腺癌良/恶性病变诊断特异度的结果相一致。本研究结果还显示,良/恶性病灶的TIC分型分布相比较,差异具有统计学意义,其中恶性病灶以Ⅲ型为主,良性病灶以Ⅰ型为主,进一步证明了DCE-MRI在乳腺癌早期诊断与术前检查中可发挥重要作用。推测良/恶性病灶分型存在差异的原因为恶性病变组织代谢较高,微血管明显多于良性病变,且其血管内皮尚未成熟,血管通透性较高,使其表现为早期、快速及明显强化等特点。但在临床应用过程中,Ⅱ型曲线良/恶性病灶存在有重叠现象,影响医师诊断与治疗,因此还应结合其他方式联合诊断以提高对乳腺病变鉴别诊断的准确率。临床应用ADC值代替扩散强度[20],本研究检测了在b=1000 s/mm2时的ADC值,结果显示恶性病灶ADC值显著低于良性病灶,提示ADC值对鉴别乳腺癌良/恶性病变性质具有重要作用。可能原因为恶性病灶增殖较快,细胞密度高于良性病灶,容积减少,水分子运动受限,使ADC值有所降低。另行ROC分析ADC值诊断效能,结果显示ADC值诊断乳腺癌良/恶性截断值为1.28×10-3 mm2/s,灵敏度为86.5%,特异度为90.9%,表明ADC值具有良好诊断效果,当ADC<1.28×10-3 mm2/s时可判断病灶为恶性。
综上所述,DCE-MRI与DWI检测在乳腺癌诊断中具有重要价值,可通过分析TIC及ADC值进行良/恶性病变鉴别,为临床诊断与治疗提供重要数据支持。但由于MRI检查价格昂贵、限制条件较多,在实际应用中还应谨慎选择,必要时可结合其他手段联合检查,以提高乳腺癌诊断的准确性,协助制定手术方案。
| [1] |
闫贻忠. 2010~2017年新疆石河子市女性乳腺癌流行趋势分析[J]. 中国肿瘤, 2019, 28(9): 689-693. Yan Y Z. Time trend of female breast cancer in Xinjiang Shihezi region, 2010~2017[J]. China Cancer, 2019, 28(9): 689-693. |
| [2] |
中华人民共和国卫生部医政司. 乳腺癌诊疗规范(2011年版)[J]. 中国实用外科杂志, 2011, 31(10): 902-907. Department of Medical Administration, Ministry of Health. Standard for diagnosis and treatment of breast cancer (2011 Edition)[J]. Chinese Journal of Practical Surgery, 2011, 31(10): 902-907. |
| [3] |
阳君. 钼靶和超声及MRI对乳腺癌的诊断价值多中心研究及卫生经济学评价[J]. 放射学实践, 2018, 33(6): 579-581. Yang J. The multi-center research on diagnostic value and health economic evaluation of MRI, ultrasonography, and X-ray mammography in breast cancer[J]. Radiologic Practice, 2018, 33(6): 579-581. |
| [4] |
Kuhl C K, Mielcareck P, Klaschik S, et al. Dynamic breast MR imaging:are signal intensity time course data useful for differential diagnosis of enhancing lesions?[J]. Radiology, 1999, 211(1): 101. DOI:10.1148/radiology.211.1.r99ap38101 |
| [5] |
左文述, 郑美珠, 韩超. 新辅助化疗对可手术乳腺癌患者总体治疗策略影响的思考[J]. 中华肿瘤杂志, 2017, 39(12): 952-957. Zuo W S, Zheng M Z, Han C. Effect of neoadjuvant chemotherapy on the overall treatment strategy in operable breast cancer[J]. Chinese Journal of Oncology, 2017, 39(12): 952-957. DOI:10.3760/cma.j.issn.0253-3766.2017.12.014 |
| [6] |
欧开萍, 罗扬, 吕剑虹, 等. HER2阳性早期乳腺癌患者的预后分析[J]. 癌症进展, 2019, 17(16): 1935-1938, 1966. Ou K P, Luo Y, Lyu J H, et al. Prognostic analysis of the patients with early HER2 postive breast cancer[J]. Oncology Progress, 2019, 17(16): 1935-1938, 1966. |
| [7] |
王思佳, 吴金萍. 彩色多普勒超声成像和乳腺X线摄影对早期乳腺癌诊断价值的对比[J]. 河北医学, 2016, 22(1): 78-81. Wang S J, Wu J P. Comparison of color Doppler ultrasonography and mammography in the diagnosis of early breast cancer[J]. Hebei Medicine, 2016, 22(1): 78-81. |
| [8] |
何洁, 黄伟俊, 徐志锋, 等. 乳腺癌患者活检术后残瘤灶的超声与钼靶X线成像对比研究[J]. 临床放射学杂志, 2018, 37(6): 926-929. He J, Huang W J, Xu Z F, et al. Comparison of ultrasound and mammography in detecting residual disease following bioptic lumpectomy in breast cancer patients[J]. Journal of Clinical Radiology, 2018, 37(6): 926-929. |
| [9] |
Ashirbani S, Yu X, Sahoo D, et al. Effect of MRI scanner parameters on breast cancer radiomics[J]. Expert Systems with Applications, 2017, 87(1): 384-391. |
| [10] |
李相生, 宋云龙, 李德昌, 等. 术前MRI动态增强扫描可降低早期非肿块型乳腺癌保乳术切缘阳性率[J]. 中华肿瘤杂志, 2017, 39(10): 768-774. Li X S, Song Y L, Li D C, et al. Preoperative dynamic contrast-enhanced MRI can reduce the rate of tumor-positive resection margins after breast conserving surgery in patients with early non-mass breast carcinoma[J]. Chinese Journal of Oncology, 2017, 39(10): 768-774. DOI:10.3760/cma.j.issn.0253-3766.2017.10.010 |
| [11] |
Levman J E, Warner E, Causer P, et al. A vector machine formulation with application to the computer-aided diagnosis of breast cancer from DCE-MRI screening examinations[J]. Journal of Digital Imaging, 2014, 27(1): 145-151. |
| [12] |
杨露, 毛伟明. MRI增强扫描与ADC序列观察肿瘤退缩率对乳腺癌化疗疗效的评估价值[J]. 中国CT和MRI杂志, 2016, 14(5): 62-64. Yang L, Mao W M. Value of MRI enhanced scan and ADC sequence observing tumor regression rate in evaluating the curative effect of chemotherapy in breast cancer[J]. Chinese Journal of CT and MRI, 2016, 14(5): 62-64. DOI:10.3969/j.issn.1672-5131.2016.05.020 |
| [13] |
冯莉莉, 周红悦, 麻增林. 动态增强扫描MR及弥散加权MRI在监测乳腺癌保乳术后肿瘤复发中的价值[J]. 广东医学, 2017, 38(10): 1561-1564. Feng L L, Zhou H Y, Ma Z L. The value of dynamic contrast-enhanced MR and diffusion-weighted MRI in monitoring the recurrence of breast cancer after breast conserving surgery[J]. Guangdong Medical Journal, 2017, 38(10): 1561-1564. DOI:10.3969/j.issn.1001-9448.2017.10.025 |
| [14] |
Kostopoulos S A, Vassiou K G, Lavdas E, et al. Computer-based automated estimation of breast vascularity and correlation with breast cancer in DCE-MRI images[J]. Magnetic Resonance Imaging, 2017, 26(35): 39-45. |
| [15] |
朱辉严, 谌力群. 乳腺癌DCE-MR征象分析及其与微血管密度的关系研究[J]. 中国CT和MRI杂志, 2016, 14(5): 71-74. Zhu H Y, Chen L Q. DCE-MR appearances of breast cancer and its relationship with microvessel density[J]. Chinese Journal of CT and MRI, 2016, 14(5): 71-74. DOI:10.3969/j.issn.1672-5131.2016.05.023 |
| [16] |
罗红兵, 王闽, 周鹏, 等. 乳腺癌DCE-MRI量化参数与组织病理相关性分析[J]. 临床放射学杂志, 2017, 36(7): 952-957. Luo H B, Wang M, Zhou P, et al. The correlation of quantitative and semi-quantitative parameters obtained from dyna-mic contrast-enhanced magnetic resonance imaging with histopathology in human breast cancer[J]. Journal of Clinical Radiology, 2017, 36(7): 952-957. |
| [17] |
Li X, Petrovi S, Harrison D J. A novel spectroscopic me-thod to image H2O distribution in ion-selective membranes[J]. Sensors and Actuators B (Chemical), 1990, 1(1-6): 275-280. DOI:10.1016/0925-4005(90)80215-L |
| [18] |
Dijkstra H, Dorrius M D, Wielema M, et al. Quantitative DWI implemented after DCE-MRI yields increased specificity for BI-RADS 3 and 4 breast lesions[J]. Journal of Magnetic Resonance Imaging, 2016, 44(6): 1642-1649. DOI:10.1002/jmri.25331 |
| [19] |
李向阳, 刘灵灵, 倪毅. 乳腺癌1.5T MRI动态增强扫描及DWI与免疫组化指标相关性分析[J]. 中国CT和MRI杂志, 2017, 15(9): 37-39. Li X Y, Liu L L, Ni Y. Correlation analysis of 1.5TMRI dynamic contrast-enhanced MR imaging and DWI and immunohistochemistry in breast cancer[J]. Chinese Journal of CT and MRI, 2017, 15(9): 37-39. DOI:10.3969/j.issn.1672-5131.2017.09.012 |
| [20] |
彭建波, 李文武, 范小涛, 等. 磁共振动态增强扫描及弥散加权成像在乳腺癌诊断中的应用价值[J]. 河北医学, 2016, 22(10): 1626-1629. Peng J B, Li W W, Fan X T, et al. The application value of dynamic enhanced MRI and diffusion weighted imaging in the diagnosis of breast cancer[J]. Hebei Medicine, 2016, 22(10): 1626-1629. DOI:10.3969/j.issn.1006-6233.2016.10.017 |



