风湿性心脏病(rheumatic heart disease,RHD)是人体感染A组乙型溶血性链球菌后炎症反复发作导致心肌损害和结缔组织纤维化的自身免疫性疾病[1]。RHD可发生于任何年龄段,具有较高致死率和致残率,即便是接受手术治疗的重度RHD患者术后6年死亡率仍高达10%[1, 2]。RHD早期症状不典型,心脏损害一般发现较晚,因此,早期诊断RHD对于临床治疗具有重要意义。经胸超声心动图(transthoracic echocardiography,TTE)是无创诊断RHD的重要影像方法[3, 4]。为明确TTE对RHD的诊断效果,本研究回顾性分析了112例慢性RHD患者的临床资料,观察了TTE诊断RHD与介入/术中所见/术后病理结果的符合情况。
1 资料与方法 1.1 临床资料选择2016年8月~2019年1月我院心内科收治的112例RHD患者,均为窦性心律。纳入标准:①有心悸、气短、心前区不适等临床表现,听诊得心前区杂音,经超声心动图检查瓣膜病变,经介入、术中探查或术后病理证实为RHD,符合2012年世界心脏联合会RHD标准[5];②均行TTE检查,资料完整;③美国纽约心脏病协会(New York Heart Association,NYHA)分级Ⅱ~Ⅲ级。
排除标准:①合并冠状动脉粥样硬化性心脏病、先天性心脏病、感染性心内膜炎、胸主动脉疾病等;②临床资料缺失;③NYHA分级Ⅳ级。其中男51例、女61例,年龄42~62岁,平均(51.94±6.37)岁;NYHA分级:Ⅱ级69例,Ⅲ级43例;临床表现:心悸27例、乏力45例、气短23例、心前区不适35例、双下肢水肿12例。本研究获得我院伦理会批准。
1.2 检查方法采用美国GE Vivid E9心脏超声诊断仪,二维探头频率2.0~5.0 mHz,三维矩阵探头频率1.5~3.5 mHz,帧频25~40帧/s。患者左侧卧位,平静呼吸,同步连接心电图,先于心尖位置进行二维模式扫查,启动M型模式依次从胸骨旁左室长轴切面、心尖五腔切面、心尖四腔切面、胸骨上窝主动脉弓切面观察二尖瓣、主动脉瓣、三尖瓣的形态、狭窄程度、活动情况、反流程度等,测量瓣膜跨瓣压差和瓣口面积。于大动脉短轴切面观察左心耳和左房结构、左房自发性回声、左心耳血栓回声以及左房血栓回声。采集图像经Echo PAC离线图像处理软件进行图像处理和分析。
1.3 图像分析 1.3.1 瓣叶分类按照瓣叶形态和活动状态对瓣膜分类。瓣叶钙化:局部增强但活动正常;瓣叶粘连:瓣叶厚度增加, 连接处粘连,活动功能受限;混合型瓣叶:瓣叶回声增厚和增强,活动受限。
1.3.2 瓣膜狭窄或关闭不全(1) 二尖瓣狭窄:轻度:二尖瓣跨瓣压差≤10 mmHg,瓣口面积1.50~2.00 cm2;中度:跨瓣压差10~20 mmHg,瓣口面积1~1.5 cm2; 重度:跨瓣压差>20 mmHg,瓣口面积<1.0 cm2。
(2) 二尖瓣关闭不全:轻度:反流束面积<3 cm2; 中度: 3~6 cm2; 重度:>6 cm2。
(3) 主动脉瓣狭窄:轻度:主动脉瓣跨瓣压差≤25 mmHg,瓣口面积1~1.5 cm2; 中度:跨瓣压差25~50 mmHg,瓣口面积0.75~1 cm2; 重度:跨瓣压差>50 mmHg,瓣口面积<0.75 cm2。
(4) 主动脉瓣关闭不全:轻度:反流<25.00%;中度:25.00%~65.00%;重度:反流>65.00%。
(5) 三尖瓣关闭不全:轻度:三尖瓣反流长度<1.5 cm; 中度:1.5~3 cm之间; 重度:>3 cm[5-7]。
1.3.3 左房血栓诊断标准未检测到密度较高、界线清楚团块影,左房内飘动旋转的烟雾状回声。
1.4 统计学分析用SPSS 25.0进行数据分析,基线资料采用统计学描述,符合率以率(%)表示。用Kappa一致性检验来验证TTE与临床诊断结果的一致性,Kappa值0.41~0.60认为一致性中等,0.61~0.80为高度一致。所有统计均采用双侧检验,检验水准α=0.05。
2 结果 2.1 TTE诊断慢性RHD瓣膜类型的结果以介入/术中所见/病理结果为准,TTE诊断RHD瓣膜类型的整体符合率为92.86%(104/112),瓣叶钙化符合率91.18%(31/34),瓣叶粘连符合率86.96%(20/23),混合型瓣叶符合率96.36%(53/55)。TTE与介入/术中所见/病理结果一致性较高(Kappa值=0.731,P<0.05),详见表 1。RHD患者二尖瓣叶形态改变见图 1a。
| 表 1 TTE诊断慢性RHD瓣膜类型与介入/术中所见/病理结果对比 |
|
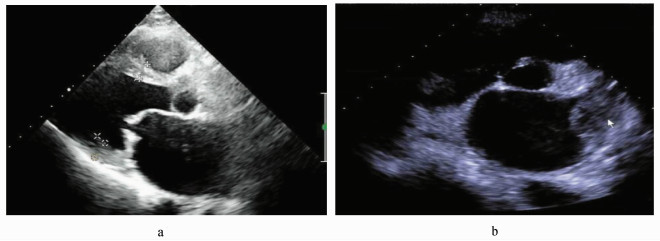
图 1 风湿性心脏病典型超声征象 a.胸骨旁长轴切面示二尖瓣叶增厚,钙化,回声增强,瓣叶活动受限;b.大动脉短轴切面示左心耳附壁血栓(白色箭头所指) |
TTE诊断RHD瓣膜狭窄总体符合率为94.44%(85/90),其中二尖瓣狭窄符合率95.83%(69/72),主动脉瓣狭窄符合率88.89%(16/18)。TTE诊断二尖瓣狭窄和主动脉瓣狭窄与介入/术中所见/病理结果的一致性系数分别为0.757和0.703,P均<0.05,详见表 2。
| 表 2 TTE诊断慢性RHD瓣膜狭窄与介入/术中所见/病理结果对比 |
TTE诊断RHD瓣膜关闭不全总体符合率为91.67%(44/47),其中二尖瓣关闭不全符合率96.55%(28/29),主动脉瓣关闭不全符合率88.89%(8/9),三尖瓣关闭不全例符合率85.71%(6/7),肺动脉瓣关闭不全例符合率100.00%(2/2)。TTE诊断二尖瓣关闭不全与介入/术中所见/病理结果的一致性系数为0.775,诊断主动脉瓣关闭不全的一致性系数为0.693,诊断三尖瓣关闭不全的一致性系数为0.681,诊断肺动脉瓣关闭不全的一致性系数为0.867,P均<0.05,详见表 3。
| 表 3 TTE诊断慢性RHD瓣膜关闭不全与介入/术中所见/病理结果对比 |
TTE检出左房血栓位于左心耳14例(87.50%),位于左心房房腔1例(6.25%),左心房和左心耳共存1例(6.25%),左心耳血栓见图 1b。TTE诊断RHD合并左房血栓与介入/术中所见/病理结果符合率为94.12%(16/17),一致性较高(Kappa值=0.752,P<0.05),见表 4。
| 表 4 TTE诊断慢性RHD合并左房血栓与介入/术中所见/病理结果对比 |
RHD是急性风湿热后遗症,好发于青少年和老年,初次感染后引起瓣膜病变和明显临床症状需要漫长的过程。症状轻微或不典型RHD不易被发现,患者就诊时往往已经出现典型的心脏结构和功能改变。瓣膜病变是RHD主要病理基础,感染溶血性链球菌后心脏瓣膜基底和边缘部位发生水肿,引起炎性反应和纤维化,导致瓣膜交界区腱索和瓣叶融合,瓣叶发生钙化、变形、僵硬和纤维化,最终引起瓣膜关闭不全或狭窄。超声心动图是世界心脏联合会推荐的RHD筛查和诊断方法[8],通过三维容积测量,可真实、立体展示心脏形态和结构,具有重复性好、准确度高等优势[9]。本研究从瓣叶类型、瓣膜狭窄和关闭不全、左房血栓的检出结果几方面评价TTE诊断RHD的准确性。
RHD导致的瓣膜病变是血流动力学改变和瓣膜形态改变的基础,瓣膜病变类型、程度与患者预后密切相关[10]。本研究观察到的RHD瓣膜常见病变类型分钙化、粘连和钙化与粘连同时存在的混合型改变,其中以混合型瓣叶为主,占49.11%。TTE诊断瓣膜病变类型与实际结果符合率达92.86%,与介入/术中所见/病理结果一致性系数较高(0.731),与赖炳煌[11]报道结果接近,提示TTE对RHD瓣膜病变类型具有准确鉴别的能力。RHD最常累及的瓣膜是二尖瓣,其次为主动脉瓣、三尖瓣和肺动脉瓣。二尖瓣狭窄超声表现为二尖瓣瓣叶增粗回声增强,瓣膜增厚钙化,瓣口开放受限,腱索僵硬。本研究中TTE对二尖瓣狭窄和(或)关闭不全的检出率为86.61%(97/112),其中单纯二尖瓣狭窄69例,占72.63%,与陈东琳[12]报道一致。严春苗等[13]也报道超声心动图对RHD二尖瓣狭窄、二尖瓣关闭不全、二尖瓣狭窄合并关闭不全的检出率分别为7.50%、25.00%、40.00%,灵敏度62.35%、特异度74.11%,准确率92.94%,高于心电图检查效能。本文中TTE诊断RHD二尖瓣狭窄符合率为95.83%,二尖瓣关闭不全符合率96.55%,均与介入/术中所见/病理结果高度一致。
主动脉瓣狭窄或关闭不全多见于年龄相关的退化性瓣膜疾病,与主动脉钙化有关[14, 15],但也有约20%为RHD引起。RHD患者主动脉瓣狭窄多与二尖瓣狭窄或关闭不全等同时存在。主动脉瓣狭窄时瓣口开放幅度可由正常16~26 mm缩至15 mm以下,瓣口面积减少至2 cm2以下。本研究中TTE诊断主动脉瓣狭窄和(或)关闭不全的检出率为21.43%(24/112),与介入/术中所见/病理结果符合率都为88.89%,一致性较好。RHD患者三尖瓣狭窄极少见,肺动脉瓣狭窄主要见于先天性心脏病。三尖瓣关闭不全病变特点为三尖瓣瓣环结构和完整性遭到破坏,出现瓣环扩张、瓣叶增厚粘连挛缩、腱索短缩或活动受限等[16]。三尖瓣关闭不全、肺动脉瓣关闭不全多为功能性,风湿性病因占比较低[17]。本研究中TTE三尖瓣关闭不全检出率为5.36%(6/112)、肺动脉瓣关闭不全为1.79%(2/112),与介入/术中所见/病理结果符合率分别为85.71%和100.00%。
左房血栓是RHD二尖瓣狭窄的常见并发症,可导致脑、肾、下肢动脉栓塞等严重并发症,临床致残致死率高[18]。左房血栓形成与血流动力学改变、血液粘滞度增加有关,RHD二尖瓣机械性狭窄,随心房规律性收缩运动,房内血液形成涡流,易导致左房血栓形成[19]。缓慢回旋活动烟雾样低回声影是左心房血栓形成的典型超声表现[20],Solie[20]报道指出TTE是诊断左房血栓的理想方法,可用于指导心内血栓预防和治疗。本研究中TTE对左房血栓病例的检出率为14.29%(16/112),多数血栓位于左心耳处,与实际结果符合率达94.12%。
Beaton等[21]采用便携式超声心动图筛查儿童RHD,结果显示超声心动图诊断RHD的敏感性为78.9%,特异性为87.2%,明确诊断RHD敏感度达97.9%。本研究中TTE对RHD瓣叶类型、狭窄、关闭不全以及左房血栓诊断符合率均在90%以上,强烈提示TTE可作为RHD诊断的首选影像检查方法。但是临床中慢性RHD病情复杂,部分伴心脏扩大、心律失常、肺动脉高压、左心功能不全等表现,给临床诊断带来难度,应详细了解患者年龄、基础疾病、现病史、既往病史等信息,熟练掌握瓣膜形态分析技术,提高操作技能及对声像图的主观判断水平,以提高对RHD瓣膜损伤的诊断效能,更好地指导临床治疗。
综上,TTE诊断RHD具有较高临床应用价值,与实际诊断结果符合率高,可作为RHD瓣膜病变及其并发症诊断的主要检查手段。
| [1] |
Cannon J, Roberts K, Milne C, et al. Rheumatic heart disease severity, progression and outcomes:a multi-state model[J]. Journal of the American Heart Association, 2017, 6(3): e003498. |
| [2] |
Watkins D A, Johnson C O, Colquhoun S M, et al. Global, regional, and national burden of rheumatic heart disease, 1990-2015[J]. New England Journal of Medicine, 2017, 377(8): 713-722. DOI:10.1056/NEJMoa1603693 |
| [3] |
Yanagawa B, Butany J, Verma S. Update on rheumatic heart disease[J]. Current Opinion in Cardiology, 2016, 31(2): 162-168. DOI:10.1097/HCO.0000000000000269 |
| [4] |
Çal K, Gölbaş Z. How to diagnose rheumatic heart disease with echocardiography[J]. Turki Kardiyoloji Dernfgi Arsivi, 2016, 44(5): 440-444. DOI:10.5543/tkda.2016.18055 |
| [5] |
Reményi B, Wilson N, Steer A, et al. World Heart Federation criteria for echocardiographic diagnosis of rheumatic heart disease:an evidence-based guideline[J]. Nature Reviews Cardiology, 2012, 9: 297-309. DOI:10.1038/nrcardio.2012.7 |
| [6] |
郭艳燕. 经胸超声对风湿性心脏病的诊断价值[J]. 现代诊断与治疗, 2015, 26(2): 452-453. Guo Y Y. The diagnostic value of transthoracic ultrasound in rheumatic heart disease[J]. Modern Diagnosis & Treatment, 2015, 26(2): 452-453. |
| [7] |
高金霞. 慢性风湿性心脏联合瓣膜病的超声诊断探讨[J]. 当代医学, 2014, 20(12): 24-25. Gao J X. Ultrasonic diagnosis of chronic rheumatic heart disease with valvular disease[J]. Contemporary Medicine, 2014, 20(12): 24-25. DOI:10.3969/j.issn.1009-4393.2014.12.016 |
| [8] |
Remenyi B, Carapetis J, Stirling J W, et al. Inter-rater and intra-rater reliability and agreement of echocardiographic diagnosis of rheumatic heart disease using the World Heart Federation evidence-based criteria[J]. Heart Asia, 2019, 11(2): e011233. DOI:10.1136/heartasia-2019-011233 |
| [9] |
Gregory A T, Stanton T, Thomas L, et al. Echocardiography:navigating complexities to provide many useful applications in contemporary clinical cardiology[J]. Heart Lung and Circulation, 2019, 28(9): 1303-1306. DOI:10.1016/j.hlc.2019.07.001 |
| [10] |
Chen J, Wang H, Zhao L. Long-term outcomes of radiofrequency catheter ablation for atrial fibrillation in rheumatic heart disease patients with mild mitral stenosis[J]. Journal of Interventional Cardiac Electrophysiology, 2019, 56(3): 313-319. DOI:10.1007/s10840-019-00538-7 |
| [11] |
赖炳煌. 超声心动图在慢性风湿性心脏病诊断中的应用价值[J]. 医疗装备, 2018, 31(24): 37-38. Lai B H. The value of echocardiography in the diagnosis of chronic rheumatic heart disease[J]. Chinese Journal of Medical Device, 2018, 31(24): 37-38. DOI:10.3969/j.issn.1002-2376.2018.24.025 |
| [12] |
陈东琳.常见老年心脏瓣膜病的临床特点分析[D].南宁: 广西医科大学, 2017. Chen D L. Analysis of clinical features of valvular heart disease in the elderly[D]. Nanning: Guangxi Medical University, 2017. |
| [13] |
严春苗, 黄旴宁, 周德兴. 心脏彩色多普勒超声联合心电图在风湿性心脏瓣膜病诊断中的应用价值[J]. 河北医药, 2018, 40(18): 2812-2813, 2818. Yan C M, Huang Y N, Zhou D X. Application value of color Doppler ultrasound combined with electrocardiogram in diagnosis of rheumatic valvular disease[J]. Hebei Medical Journal, 2018, 40(18): 2812-2813, 2818. |
| [14] |
Joseph J, Naqvi S Y, Giri J, et al. Aortic stenosis:pathophysiology, diagnosis, and therapy[J]. American Journal of Chinese Medicine, 2017, 130(3): 253-263. DOI:10.4103/0366-6999.198936 |
| [15] |
Fukuhara S, Ikegami H, Polanco A R, et al. Concomitant repair for mild aortic insufficiency and continuous-flow left ventricular assist devices[J]. European Journal of Cardio-thoracic Surgery, 2017, 52(6): 1062-1068. DOI:10.1093/ejcts/ezx150 |
| [16] |
陈宗辉, 付亮, 倪寅凯, 等. 三尖瓣关闭不全的诊治进展[J]. 国际心血管病杂志, 2018, 45(1): 20-23. Chen Z H, Fu L, Ni Y K, et al. Diagnosis and treatment of tricuspid insufficiency[J]. International Journal of Cardio-logy, 2018, 45(1): 20-23. |
| [17] |
Said S M, Mainwaring R D, Ma M, et al. Pulmonary valve repair for patients with acquired pulmonary valve insufficiency[J]. Annals of Thoracic Surgery, 2016, 101(6): 2294-2301. DOI:10.1016/j.athoracsur.2016.01.035 |
| [18] |
王刚, 刘强. 心房颤动患者左心房血栓形成机制及中西医结合防治的研究进展[J]. 浙江中西医结合杂志, 2017, 27(3): 254-259. Wang G, Liu Q. The mechanism of left atrial thrombosis in patients with atrial fibrillation and its prevention and treatment by integrated Chinese and western medicine[J]. Zhejiang Journal of Integrated Traditional Chinese and Western Medicine, 2017, 27(3): 254-259. DOI:10.3969/j.issn.1005-4561.2017.03.034 |
| [19] |
Yang Y, Du X, Dong J, et al. Outcome of anticoagulation therapy of left atrial thrombus or sludge in patients with nonvalvular atrial fibrillation or flutter[J]. American Journal of the Medical Sciences, 2019, 358(4): 273-278. DOI:10.1016/j.amjms.2019.07.013 |
| [20] |
Solie C J, Mohr N M, Runde D P. Can multidetector computed tomography rule out left atrial thrombus in patients with atrial fibrillation?[J]. Annals of Emergency Medicine, 2018, 71(4): 480-481. DOI:10.1016/j.annemergmed.2017.09.012 |
| [21] |
Beaton A, Lu J C, Aliku T, et al. The utility of handheld echocardiography for early rheumatic heart disease diagnosis:a field study[J]. European Heart Journal Cardiovascular Imaging, 2015, 16(5): 475-482. DOI:10.1093/ehjci/jeu296 |



