胰腺癌是临床常见消化系统恶性肿瘤,其早期症状缺乏特异性,起病隐匿,加之胰腺癌病灶位置较深,易被腹腔组织器官遮盖,导致胰腺癌诊断延误,影响预后[1]。因此,寻找一种合理有效的胰腺癌诊断方法,完善早期检测方案是临床研究的重点环节之一。目前, CT是临床诊断腹腔疾病主要影像学手段,随着多层螺旋CT(multilayer spiral CT,MSCT)灌注成像技术的发展,可为分析组织器官血流动力学提供影像参数,便于从血流动力学方面定性判断正常组织或恶变组织,为胰腺癌良恶性诊断提供依据[2]。临床研究已证实,肿瘤属血管依赖性疾病,其中微血管密度(microvascular density,MVD)是反映肿瘤血管生成效应的主要参数,被作为判定肿瘤血管生成的“金标准”,且与肿瘤侵袭性和预后关系密切[3, 4]。基于此,本研究对MSCT灌注成像参数对胰腺癌鉴别诊断效果及与肿瘤恶性生物学行为、微血管密度的关系进行探讨,旨在为临床早期诊断提供参考。
1 资料与方法 1.1 一般资料选取2016年7月~2019年8月我院胰腺癌患者68例为胰腺癌组,同期行手术治疗的68例急性胰腺炎患者为胰腺炎组。均经病理诊断确诊胰腺癌/胰腺炎;首次发病;既往无腹部手术史;知情本研究并签署同意书。排除标准:无法耐受手术者;恶液体征者;合并其他疾病致全身感染者;伴凝血功能障碍者。2组年龄、性别、体质量指数、症状等基础资料见表 1,具有可比性(P>0.05)。
| 表 1 一般资料 |
飞利浦Brilliance32多层螺旋CT机首先平扫,再行CT灌注扫描,最后完成胰腺多期扫描。检查当天禁食,检查前饮温水800 mL充盈胃、小肠。
扫描方式:(1)平扫,范围膈顶-肝下缘,参数110 kV,200 mA, 螺距1.0,层厚5 mm。(2) CT灌注扫描,检查前训练呼吸,告知造影剂可能引起的发热反应,以5 mL/s注入50 mL造影剂,延迟8 s,120 kV,60 mA,5 mm,间隔1 s,周期1.0 s,采集数据时间45 s,扫描22次,8层/次,共生成重建图像176帧。(3)多期增强扫描,灌注扫描完成后追加70 mL造影剂,速度2.5 mL/s,扫描动脉期25 s,胰腺期45 s,门脉期70 s,层厚5 mm,重建层厚0.625,多角度观察病变。
1.2.2 分析平扫和多期图像分析:全部图像均于工作站(ADW4.2)处理,分析轴状位、冠状位、矢状位、斜位MPR图像或VR重建图像。
CT灌注图像分析:采取Perfusion 2软件包分析数据,腹主动脉作为流入血管,从单层连续动态图内病灶组织、胰腺组织及腹主动脉感兴趣区获取血流血容量(BV)、平均通过时间(MTT)、血流量(BF)、表面通透性(PS)彩色灌注图。
数据资料处理:由2位或以上高级职称影像科医师分别分析图像,判定病灶性质、强化程度,结论不一致时经讨论达成一致结果。
1.2.3 微血管密度(MVD)值检查获取标本时标记方位,结合CT扫描位置尽量在CT灌注靶平面感兴趣位置取材,甲醛(40 g/L)固定,脱水,透明处理,石蜡包埋制蜡块备用;采取链霉菌抗生物蛋白-过氧化酶免疫组化(SP)法试剂盒、鼠抗人CD34检查MVD。MVD计数:任何被CD34抗体染色为棕黄孤立的内皮细胞簇团或内皮细胞,与周围恶性细胞、微血管或其他芥蒂组织分开者属一个微血管,若结构未相连,其分支同样为一个微血管,排除血管内径可容纳8个及以上红细胞及存在肌肉细胞的血管;首先×40低倍镜扫视切片,确认高密度区(3个),切换×200高倍镜,计数取平均值。
1.2.4 基因检测以实时荧光定量PCR(polymerase chain reaction)技术测目标基因表达量,包括肿瘤侵袭基因(HOXB7、Twist)、增殖基因(FOXC1、Bmi-1)。
具体操作:裂解标本细胞,实施两相分离,取无色水相上层,移至离心管内,加等体积异丙醇沉淀RNA,清洗RNA凝胶块,室温干燥,加水40 μL制成RNA溶液,冷冻备用;紫外线吸收法测RNA纯度;采取反转录试剂盒制成样品cDNA;待测样品试管实施PCR检测,设置良性组织内目标基因表达量作为标准值100,计算标本组织内目标基因相对表达量。
1.3 观察指标(1) 对比2组胰腺组织MSCT灌注成像参数(BV、BF、PS、MTT); (2) ROC曲线分析MSCT灌注成像参数(BV、BF、PS、MTT)诊断胰腺癌的价值; (3)对比不同临床分期胰腺癌患者胰腺组织MSCT灌注成像参数(BV、BF、PS、MTT); (4)对比不同临床分期胰腺癌患者组织中肿瘤侵袭基因(HOXB7、Twist)、增殖基因(FOXC1、Bmi-1)表达量; (5)对比不同临床分期胰腺癌患者组织中MVD值; (6)分析MSCT灌注成像参数(BV、BF、PS、MTT)与胰腺癌肿瘤侵袭、增殖基因、MVD值的相关性。
1.4 统计学处理采用SPSS 22.0统计分析软件,计数资料以率表示,2组间比较采用χ2检验;相关性以Pearson相关性系数分析;符合正态分布的计量资料以(x±s)表示,2组间比较采用t检验;ROC曲线评估MSCT灌注成像参数对胰腺癌的诊断价值。P<0.05为差异有统计学意义。
2 结果 2.1 2组胰腺组织MSCT灌注成像参数胰腺癌组BV、BF及PS水平低于胰腺炎组,MTT高于胰腺炎组(P<0.05)。见表 2。
| 表 2 2组胰腺组织MSCT灌注成像参数对比(x±s) |
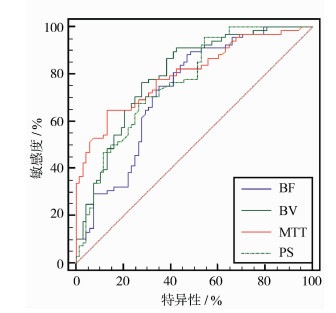
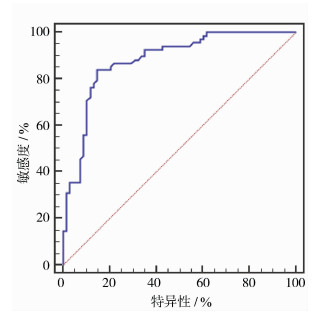
BV、MTT、BF及PS联合诊断胰腺癌的AUC为0.881,均高于BV、MTT、BF及PS单一指标诊断的0.796、0.801、0.730、0.766,联合诊断敏感度为83.82%,特异度为85.29%。见表 3、图 1、图 2。
| 表 3 MSCT灌注成像参数诊断胰腺癌的ROC曲线 |
|
图 1 单一指标诊断ROC曲线 |
|
图 2 各指标联合诊断ROC曲线 |
胰腺癌组临床分期为Ⅲ~Ⅳ期的患者,其BV、BF及PS水平低于Ⅰ~Ⅱ期患者,MTT高于Ⅰ~Ⅱ期患者(P<0.05)。见表 4。
| 表 4 胰腺癌组不同临床分期患者胰腺组织MSCT灌注成像参数对比(x±s) |
胰腺癌组临床分期为Ⅲ~Ⅳ期患者组织标本中FOXC1、Bmi-1、HOXB7、Twist mRNA表达量高于Ⅰ~Ⅱ期患者(P<0.05)。见表 5。
| 表 5 胰腺癌组不同临床分期患者组织中肿瘤侵袭、增殖基因表达量比较(x±s) |
胰腺癌组临床分期为Ⅲ~Ⅳ期患者组织标本中MVD值平均为(58.72±10.83)条,Ⅰ~Ⅱ期患者为(43.67±5.38)条,组间比较,Ⅲ~Ⅳ期患者高于Ⅰ~Ⅱ期患者(t=7.038, P<0.001)。
2.6 MSCT灌注成像参数与患者肿瘤侵袭、增殖基因、MVD值的相关性胰腺癌患者MSCT灌注成像参数的BV、BF、PS与FOXC1、Bmi-1、HOXB7、Twist mRNA表达量、MVD值呈明显负相关,MSCT灌注成像参数的MTT与FOXC1、Bmi-1、HOXB7、Twist mRNA表达量、MVD值呈明显正相关(P<0.05)。见表 6。
| 表 6 MSCT灌注成像参数与患者肿瘤侵袭、增殖基因、MVD值的相关性(n=68) |
胰腺血流丰富,其病变会直接影响胰腺实质血流灌注[5]。MSCT灌注成像技术能反映器官实质水平血供状态,胰腺癌为低血供病灶,此特征决定实质功能学变化早于形态学变化[6]。因此,理论上检测其异常情况对早期诊断胰腺癌具有重要作用。
西方学者最早应用胰腺MSCT灌注成像诊断胰腺疾病,发现胰腺正常患者胰腺灌注量为1.25~1.66 mL/(min·mL)[7]。国内学者测得胰腺灌注值为(90.6±29.25)mL/(100 mL·min)[8]。本研究显示,胰腺癌患者BV值为(7.96±2.85)mL/kg,与上述研究存在较大偏差,可能与应用数学模型及灌注软件不同有关。本研究还显示,与急性胰腺炎患者相比,胰腺癌患者BV、BF及PS水平显著降低(P<0.05),与胰腺癌低血供这一生理特点相符,且与学者雷江侠[9]研究结果一致。本研究测得胰腺癌组MTT高于胰腺炎组(P<0.05),可能与胰腺癌病灶血管壁不完整有关。基于上述研究,MSCT灌注成像参数BV、BF、PS、MTT可为胰腺癌早期鉴别诊断提供新方向。但有学者指出,胰腺体积小,相对而言胰腺癌病灶体积更小,MSCT检测对层厚选择要求高,层厚太大易受容积效应影响,层厚太薄会增加图像噪声[10]。临床胰腺扫描常采取5~10 mm层厚,赵常红等[11]所采取灌注扫描层厚为10 mm,本研究所用灌注扫描层厚为5 mm,结果显示,本研究测得结果标准差绝对值为同类研究最低,说明本研究准确性更高,进一步ROC曲线分析显示,BV、MTT、BF及PS联合诊断胰腺癌的AUC值最大0.881,敏感度为83.82%,特异度为85.29%,具有较高诊断价值。
恶性肿瘤生长依赖于新生血管形成,MVD值高低可间接反映病灶恶性程度[12]。但有报道显示,大肠癌患者MVD值与淋巴结转移、肿瘤分期、预后无相关性[13]。黄婷等[14]的研究表明,胰腺炎、胰腺癌患者间MVD值有差异,即胰腺癌组织微血管分布更密集,本研究结果与之一致。此外,MSCT灌注成像参数值与恶性病灶病理改变有关,揭示参数值改变属新生血管显微解剖学变化的副本[15, 16],MSCT灌注成像参数可用于评估病灶血管新生状态。有研究显示,恶性病灶新生血管形成不仅会刺激病灶生长、转移,还可造成灌注量、血容量、毛细血管通透性改变[17]。本研究胰腺癌患者FOXC1、Bmi-1、HOXB7、Twist mRNA表达量、MVD值与MSCT灌注成像参数BV、BF、PS呈负相关,与MTT呈正相关(P<0.05)。正常胰腺组织细胞存在增殖/凋亡平衡状态,在癌变发生早期即存在细胞凋亡抑制、增殖活性增强现象,二者协同作用加重病情进展[18],随胰腺癌病情加重,病灶组织内FOXC1、Bmi-1、HOXB7、Twist基因表达呈升高趋势(P<0.05)。FOXC1、Bmi-1、HOXB7、Twist在不同研究中均被证实与胰腺癌细胞增殖活性密切相关,其中FOXC1基因过表达能直接抑制胰腺癌细胞凋亡,并促进恶性细胞G0/G1期进展;HOXB7基因过表达可直接增加恶性细胞侵袭活性[19]。上述结果表明,肿瘤侵袭、增殖基因过表达及MVD值升高共同促进胰腺癌分期进展,此与恶性肿瘤基因学演进特征吻合,临床可通过MSCT灌注成像参数值变化评估胰腺癌患者病情特征及预后转归。
综上可知,MSCT灌注成像参数对胰腺癌鉴别诊断有一定临床价值,BV、BF、PS、MTT参数值与肿瘤侵袭基因、增殖基因、MVD值关系密切,可为临床病情及预后评估提供理论依据。
| [1] |
Sohal D P, Mangu P B, Laheru D. Metastatic pancreatic cancer:American Society of Clinical Oncology Clinical Practice guideline summary[J]. Journal of Oncology Practice, 2017, 13(4): 261-264. |
| [2] |
Yin Y, Jiang J. JOG technique versus nonspiral axial scan in pancreatic perfusion computed tomography imaging and their preliminary application[J]. Journal of Computer Assisted Tomography, 2016, 40(6): 880-885. |
| [3] |
Stojanovic D, Milenkovic S M, Mitrovic N, et al. Clinical significance of neoangiogenesis and index of proliferation in the signet ring type of gastric adenocarcinoma[J]. Journal of the Balkan Union of Oncology, 2018, 23(4): 992-1003. |
| [4] |
陈小华, 李佳音, 李莉明, 等. 感兴趣区选择对胃癌能谱CT测量结果可重复性的影响及与微血管密度的关系[J]. 中华放射学杂志, 2018, 52(1): 24-29. |
| [5] |
Eriksson E, Wenthe J, Irenaeus S, et al. Gemcitabine reduces MDSCs, tregs and TGFβ-1 while restoring the teff/treg ratio in patients with pancreatic cancer[J]. Journal of Translational Medicine, 2016, 14(1): 282. |
| [6] |
毛卫霞, 韩文. 增强CT定量参数与胰腺癌病灶内增殖、侵袭基因表达量的相关性[J]. 海南医学院学报, 2017, 23(21): 3025-3027, 3031. |
| [7] |
Guo L, Akahori H, Harari E, et al. CD163+ macrophages promote angiogenesis and vascular permeability accompanied by inflammation in atherosclerosis[J]. Journal of Clinical Investigation, 2018, 128(3): 1106-1124. |
| [8] |
陈小龙, 寇明清, 冯永恒, 等. 胰腺癌微循环CT灌注成像分析[J]. 陕西医学杂志, 2015, 44(11): 1478-1480. |
| [9] |
雷江侠. 胰腺CT灌注扫描量化指标对胰腺癌恶性程度的评估价值[J]. 海南医学院学报, 2016, 22(19): 2346-2349. |
| [10] |
陆娜, 邸悦, 强金伟, 等. 胰腺导管腺癌CT灌注成像与HIF-1α表达相关性研究[J]. 中国医学计算机成像杂志, 2016, 22(2): 143-147. |
| [11] |
赵常红, 郝粉娥, 刘挨师. 胰腺癌定量双能CT碘图与CT灌注参数相关性研究[J]. 放射学实践, 2018, 33(6): 587-592. |
| [12] |
Atkins M, Potier D, Romanelli L, et al. An ectopic network of transcription factors regulated by hippo signaling drives growth and invasion of a malignant tumor model[J]. Current Biology, 2016, 26(16): 2101-2113. |
| [13] |
唐广义, 殷东风. 益气健脾抗癌法对大肠癌组织微血管密度及细胞凋亡影响的实验研究[J]. 世界中西医结合杂志, 2016, 11(5): 601-604. |
| [14] |
黄婷, 郑许强, 肖桂卿. 多层螺旋CT与MR显像在胰腺肿块患者中的诊断价值的对比[J]. 黑龙江医药, 2019, 32(5): 1160-1161. |
| [15] |
Araujo Neto S A, Franca H A, de Mello Júnior C F, et al. Anatomical variations of the celiac trunk and hepatic arterial system:an analysis using multidetector computed tomography angiography[J]. Radiologia Brasileira, 2015, 48(6): 358-362. |
| [16] |
宋丹, 许红旗, 李力. 不同级别脑胶质瘤MSCT灌注成像参数比较及与VEGF表达相关性探讨[J]. 中国CT和MRI杂志, 2019, 17(6): 18-20. |
| [17] |
Mains J R, Donskov F, Pedersen E M, et al. Dynamic contrast-enhanced computed tomography-derived blood volume and blood flow correlate with patient outcome in metastatic renal cell carcinoma[J]. Investigative Radiology, 2017, 52(2): 103-110. |
| [18] |
唐优仕, 王龙, 马浩文, 等. 瑞芬太尼对胰腺癌BxPC-3细胞增殖、凋亡的影响及其机制[J]. 中国热带医学, 2017, 17(12): 1193-1197. |
| [19] |
刘畅, 田兴, 郭雷鸣, 等. miR-15a负调控Bmi-1对胰腺癌细胞系PANC-1放射敏感性影响[J]. 中华放射肿瘤学杂志, 2017, 26(5): 572-574. |



