2. 荆州市中心医院 放射科, 湖北 荆州 434020
2. Department of Radiology, Jingzhou Central Hospital, Jingzhou 434020, Hubei, P. R. China
肝纤维化是指在饮酒、病毒性肝炎及自身免疫性肝病等多种因素影响下发生的慢性肝脏损伤,以肝脏慢性持续性炎症导致的损伤-愈合反应持续激活为主要病理表现。多种细胞介质参与该过程,肝脏中纤维化反应引起细胞外基质成分积累,导致纤维性瘢痕形成,而纤维性疤痕的存在破坏了肝脏的结构,导致肝细胞坏死及肝脏功能失调,最终导致肝功能衰竭[1]。所有慢性肝病均可导致肝纤维化,而肝纤维化严重程度的评估对于制定治疗及管理策略至关重要。肝活检是目前评估肝纤维化的金标准,但肝活检会对肝脏造成损伤,并可导致肝实质中的纤维化改变。且肝纤维化晚期患者存在营养不良、凝血障碍及致命性肝衰竭的潜在风险,因此对其行侵入性检查需非常慎重。此外,肝活检还存在合并多种并发症及取样错误的风险,使其临床应用具有一定局限性[2, 3]。目前Tc-99m-二亚乙基三胺-五乙酸-半乳糖基人血清白蛋白(99mTc-GSA)单光子发射计算机断层扫描(SPECT)/CT融合成像已被常规应用于肝切除术中,用以评估肝脏功能[4]。99mTc-GSA仅由肝脏吸收,并可与肝细胞上的去唾液酸糖蛋白特异性结合,而肝损伤患者肝细胞表面的去唾液酸糖蛋白受体数量减少,提示99mTc-GSA闪烁显像可以用以评估肝细胞功能。本文旨在分析该技术评估肝纤维化及其严重程度的临床意义。
1 资料及方法 1.1 一般资料将2017年1月~2019年12月于荆州市中心医院就诊的124例需行肝脏活检的患者纳入研究,纳入标准:①需行肝脏病理活检的患者;②自愿参与本试验研究;③临床资料完整。排除标准:①合并严重心、脑、肾功能不全者;②合并血液、肿瘤及自身免疫系统疾病;③合并大量腹水;④过度肥胖者;⑤妊娠、哺乳期女性。所有患者均在行肝脏活检前1周内完善SPECT/CT检查,并在行肝脏活检前1天抽取空腹静脉血,对患者体内的肝脏功能指标进行检验。根据患者病理活检结果,将患者分为纤维化组(n=51)及非纤维化组(n=73)。纤维化组有36例男性,15例女性,平均年龄(51.78±8.45)岁,平均BMI(24.01±2.89)kg/m2,有29例病毒性肝炎、6例酒精性肝病、11例非酒精脂肪性肝病及5例自身免疫性肝炎。两组患者的年龄、性别等一般资料无明显差异。
1.2 实验方法和研究指标 1.2.1 SPECT/CT检查检查仪器为Symbia T6扫描仪(德国,西门子)。所有患者行检查前需禁食一夜,检查时嘱患者仰卧位,双手置于头侧,在图像采集前休息并缓慢呼吸。经肘静脉注射99mTc-GSA 185 MBq,20 min后使用低能量、高分辨率准直仪采集SPECT数据,SPECT断层采集矩阵为128×128,上下探头各围绕肝脏旋转180°,每6°一帧,每帧采集30 s。以SPECT检查结果定位选择扫描范围,确定后行CT扫描,扫描参数为:管电压120 kV、管电流35 mA、扫描厚度3 mm,以肝脏为中心,扫描长度与核医学准直器扫描范围相同,螺距及进床速度为系统自动生成。获得CT图像后,使用嵌入式西门子通用平台软件Syngo MI工作区自动融合SPECT和CT图像:通过医学数字成像和通信检索SPECT切片数据,并将SPECT切片转换为类似CT的数据量以融合SPECT和CT图像。
1.2.2 图像处理利用GI-BONE软件(日本AZE公司产品)处理获得的图像,生成冠状面、矢状面及横轴面图像,并在肝脏横断面图像上勾画感兴趣区域(region of interest,ROI)。采用LHL15评价肝纤维化区域的放射性,LHL15值是由注射99mTc-GSA 15 min后肝脏ROI的放射性计数除以心脏ROI放射性计数(H15)与肝脏ROI放射性计数(L15)之和得出的,计算公式为LHL15=L15/(L15+H15);采用SUV值评估肝脏中99mTc-GSA的积累程度,因为99mTc-GSA仅在肝脏摄取,故采用肝脏体积对放射性活性进行标准化,肝脏体积由VINCRNT工作站(日本FUJIFILM公司)自动计算,公式为SUVmean=[肝感兴趣体积放射性活性(Bq/mL)]/[扫描起始注射剂量(Bq)/肝体积(mL)×10]。
1.2.3 实验室指标检查采用多功能全自动全血细胞分析仪(Sysmex XS-5000)对患者体内的血小板计数进行检测;采用全自动血凝仪(Sysmex CA-1500)对患者体内的凝血酶原活动度进行检测;采用全自动生化分析仪(OLYMPUS AU-2700)对患者体内的谷丙转氨酶(alanine aminotransferase,ALT)、谷草转氨酶(aspartate aminotransferase,AST)及白蛋白(albumin,Alb)水平进行检测。
1.2.4 Child-Pugh评分[5]分值5~15分,分数越高,肝脏储备功能越差。
1.3 研究指标比较并分析两组患者肝功能相关指标;采用多因素Logistic回归模型对影响肝纤维化的指标进行分析;应用ROC曲线分析上述影响因素预测肝纤维化的诊断价值;根据患者病理结果将肝纤维化患者进行分级,比较轻度纤维化(S0~S1级)及重度纤维化(S2~S4级)患者的LHL15、SUVmean及Child-Pugh评分;对SUVmean与Child-Pugh评分的相关性进行分析。
1.4 统计学方法所有数据使用SPSS 22.0进行分析,服从正态分布的计量资料以均数±标准差(x±s)表示,组间比较采用t检验;计数资料采用例数(n)的形式表示,用χ2检验比较组间差异;应用多因素Logistic回归模型分析危险因素;采用Pearson相关分析对指标的相关性进行分析;应用受试者工作曲线(ROC)评估不同指标预测的诊断效能,并计算其曲线下面积(AUC);DeLong法比较曲线下面积的差异,以P<0.05为差异有统计学意义。
2 结果 2.1 非纤维化组与纤维化组各指标检测结果比较非纤维化组患者的血小板计数、LHL15及SUVmean明显高于纤维化组,凝血酶原活动度明显低于纤维化组(均P<0.05),数据详见表 1。
| 表 1 两组患者肝功能相关指标比较(x±s) |
多因素Logistic分析示高血小板计数、LHL15及SUVmean是肝纤维化的保护因素(均P<0.05),高凝血酶原活动度是独立危险因素(OR=1.495,P=0.002),数据详见表 2。
| 表 2 预测肝纤维化因素的多因素Logistic分析 |
ROC曲线显示(图 1),SUVmean预测肝纤维化的AUC为0.862,明显高于LHL15、凝血酶原活动度及血小板计数(均P<0.05),其诊断的最佳截点为≤6.48,此时敏感度为87.7%,特异度为72.5%,详见表 3。

|
图 1 不同指标预测肝纤维化的ROC曲线 |
| 表 3 不同指标预测肝纤维化的诊断效能 |
肝纤维化S0~S1级患者的LHL15及SUVmean明显高于S2~S4级患者,而Child-Pugh评分明显低于S2~S4级患者(均P<0.05),数据详见表 4。
| 表 4 不同肝纤维化程度患者的LHL15及SUVmean比较(x±s) |
SUVmean与肝纤维化程度呈明显负相关(ρ=-0.873,P=0.000),数据详见图 2。
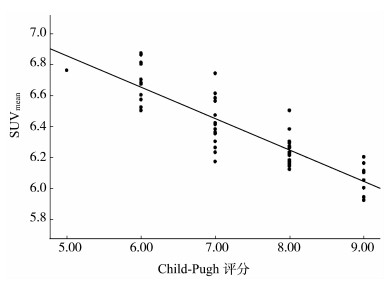
|
图 2 SUVmean与Child-Pugh评分的相关性 |
肝纤维化是慢性肝病的标志,其特征是细胞外基质蛋白的过度积累。尽管肝活检是肝纤维化的诊断和分期的参考标准,但其因存在潜在伤害和疼痛、采样变异及患者接受度较低等缺点,使其临床应用具有局限性[6]。而非侵入性指标,如透明质酸、龙脑酸、Ⅲ型胶原、Ⅳ型胶原是纤维化的有效标志物,但因其缺乏肝脏特异性,故临床应用亦具有一定局限性[7, 8]。
目前临床常用凝血酶原活动度、血清白蛋白等指标对肝病患者肝脏储备功能进行评估[9],上述指标反映了肝脏的合成能力。在肝纤维化过程中,会出现较明显的血清凝血酶原拮抗作用,导致患者存在出血倾向,而存在出血倾向及腹水则标志着患者接近肝功能失代偿阶段。白蛋白作为体内营养状态的重要反应指标,其水平下降提示患者营养状态长期不良[10]。基于这些指标制定的Child-Pugh评分可对患者晚期肝硬化情况进行预测,但上述指标通常会受药物、其他原因导致的营养不良及胆道狭窄等因素影响,使其临床应用价值受到影响[11]。
SPECT/CT是一种功能强大的计算机成像系统,其可反映整体及残余肝功能。肝功能与去唾液酸糖蛋白(ASGP)受体表达及受体介导的内吞作用直接相关[12]。而由tech 99标记的ASGO类似物(血清半乳糖末端糖蛋白,99mTc-GSA)与ASGP受体结合,可在Gamma Camera跟踪下通过闪烁显像(SPECT)进行定量分析,可用于评估相应的肝功能。且ASGP受体仅在肝细胞上特异性表达,故基于99mTc-GSA的SPECT/CT检查基本不受其他因素影响,可作为评价肝功能的特异性指标。因此,3D CT与SPECT扫描的融合图像能够同时显示肝脏解剖细节及肝脏任何特定区域的功能[13]。
本研究结果发现SUVmean是肝纤维化的独立预测指标,在诊断肝纤维化方面具有较高的诊断效能,且SUVmean值与肝纤维化严重程度呈明显负相关。这一结果提示SPECT/CT定量分析能有效诊断肝纤维化,并对其严重程度进行评估。这是由于99mTc-GSA仅在肝脏吸收,随着患者肝功能的不断降低,因严重肝纤维化所致的功能性肝细胞数量减少,且表面的GSA受体减少,故而使99mTc-GSA在肝脏中积累下降,SUVmean值也随之降低。因此,SUVmean不仅能有效反映患者肝纤维化程度,并能对患者肝功能进行评估,且操作无创,易于为患者接受。
综上,SPECT/CT定量分析可对患者肝纤维化发生情况及严重程度进行评估,且操作简单易行。但本研究仍存在一定不足,首先是纳入样本量较小,研究因素较少,使其具有一定局限性;其次,SUVmean主要是用于评估功能正常的肝细胞,而并非直接评估肝脏纤维化严重程度的手段;此外,对于SUVmean值与患者远期预后的相关性,本研究并未探及,故应进一步对SPECT/CT技术在诊断及评估肝纤维化方面的作用进行深入研究。
| [1] |
Aydın M M, Akçalı K C. Liver fibrosis[J]. Turkish Journal of Gastroenterology, 2018, 29(1): 14-21. DOI:10.5152/tjg.2018.17330 |
| [2] |
Lai M, Afdhal N H. Liver fibrosis determination[J]. Gast-roenterology Clinics of North America, 2019, 48(2): 281-289. DOI:10.1016/j.gtc.2019.02.002 |
| [3] |
Tokorodani R, Sumiyoshi T, Okabayashi T, et al. Liver fibrosis assessment using 99mTc-GSA SPECT/CT fusion imaging[J]. Japanese Journal of Radiology, 2019, 37(4): 315-320. |
| [4] |
Sumiyoshi T, Shima Y, Okabayashi T, et al. Functional discrepancy between two liver lobes after hemilobe biliary drai-nage in patients with jaundice and bile duct cancer:an apprai-sal using (99m)Tc-GSA SPECT/CT fusion imaging[J]. Radiology, 2014, 273(2): 444-451. |
| [5] |
van den Broek M A J, olde Damink S W M, Dejong C H C, et al. Liver failure after partial hepatic resection:definition, pathophysiology, risk factors and treatment[J]. Liver International, 2008, 28(6): 767-780. DOI:10.1111/j.1478-3231.2008.01777.x |
| [6] |
Petitclerc L, Gilbert G, Nguyen B N, et al. Liver fibrosis quantification by magnetic resonance imaging[J]. Topic Magnetic Resonance Imaging, 2017, 26(6): 229-241. |
| [7] |
Jabor A, Kubíek Z, Fraňková S, et al. Enhanced liver fibrosis (ELF) score:reference ranges, biological variation in healthy subjects, and analytical considerations[J]. Clinica Chimica Acta, 2018, 483(2): 291-295. |
| [8] |
Gudowska M, Cylwik B, Chrostek L. The role of serum hyaluronic acid determination in the diagnosis of liver fibrosis[J]. Acta Biochimica Polonica, 2017, 64(3): 451-457. DOI:10.18388/abp.2016_1443 |
| [9] |
郭长峰, 陈艳清, 周海东, 等. 乙型肝炎肝硬化代偿期患者外周血小板计数和病毒血清标志物变化及与肝纤维化程度的线性关系[J]. 肝脏, 2017, 22(2): 125-128. DOI:10.3969/j.issn.1008-1704.2017.02.011 |
| [10] |
王超秀, 陈炘, 刘发彬, 等. 血清凝血酶原活动度及相关因素对重度慢性肝炎肝纤维化患者预后的影响分析[J]. 川北医学院学报, 2019, 34(3): 441-444. |
| [11] |
Kotani K, Kawabe J, Higashiyama S, et al. Heterogeneous liver uptake of Tc-99m-GSA as quantified through SPECT/CT helps to evaluate the degree of liver fibrosis:A retrospective observational study[J]. Medicine (Baltimore), 2018, 97(31): e11765. DOI:10.1097/MD.0000000000011765 |
| [12] |
胡楠, 程午樱, 李方, 等. 99mTc-GSA SPECT/CT肝脏功能显像中肝占位性病变的图像特征[J]. 现代仪器与医疗, 2017, 23(2): 1-3. DOI:10.11876/mimt201704001 |
| [13] |
Mao Y, Du S, Ba J, et al. Using Dynamic 99mT c-GSA SPECT/CT fusion images for hepatectomy planning and postoperative liver failure prediction[J]. Annals of Surgical Oncology, 2015, 22(4): 1301-1307. DOI:10.1245/s10434-014-4117-4 |



