2. 鄞州区第二医院 呼吸科, 浙江 宁波 315100;
3. 鄞州区第二医院 影像科, 浙江 宁波 315100
2. Department of Respiratory Medicine, Second Hospital of Yinzhou District, Ningbo 315100, Zhejiang, P. R. China;
3. Department of Imaging, Second Hospital of Yinzhou District, Ningbo 315100, Zhejiang, P. R. China
孤立性肺结节[1-3](solitary pulmonary nodules,SPN)是一种类圆形的肺内病灶,直径一般在3 cm以内,边界清晰,但无局部淋巴结肿大、肺不张、胸腔积液等表现。在肺内形态上,常呈现结节状良性及恶性病变[4]。有研究[5]发现超五成SPN会产生恶性病变,对于早期肺癌患者行手术切除后,其5年生存率超过90%,而中晚期却不足5%,因此,临床初期检测肺部结节,准确判断其组织学特性意义重大。现阶段,鉴别诊断良恶性SPN仍是胸部影像学研究的重点和难点。CT纹理分析能够对病灶内的组织结构异质性及其内部潜在信息进行更深入发掘和掌握[6],从而提高诊断科学性及准确性,在胸部检查中,多层螺旋CT(multislice spiral CT,MSCT)应用逐渐广泛,进一步提高了SPN良恶性鉴别诊断准确率[7],但对于孤立性肺结节良恶性的鉴别诊断,有关二者诊断效能的对比研究尚缺乏,鉴于此,本研究选取100例SPN患者,对比CT纹理分析与MSCT三维重建对孤立性肺结节良恶性鉴别的诊断效能,以期为提高临床诊治精准性提供参考依据。
1 资料与方法 1.1 一般资料从2017年1月~2019年12月于宁波市鄞州区第二医院就诊的SPN患者中,选取100例为研究对象。其中,男53例、女47例;年龄26~78岁,平均(58.43±13.82)岁;结节大小0.7~3.6 cm,平均(2.1±0.7)cm。100例中有炎性结节16例、结核球28例、恶性肿瘤56例,均经医院穿刺及手术病理证实。根据病理类型划分为良性组与恶性组,良性组44例:男25例、女19例;年龄26~77岁,平均(57.32±13.26)岁;炎性肉芽肿22例、活动性炎性结节9例、结核球13例。恶性组56例:男34例、22例;年龄27~78岁,平均(58.84±14.06)岁;腺癌38例、鳞癌18例。两组性别、年龄等一般资料比较,无统计学意义(P>0.05)。本研究经医院医学伦理委员会批准,患者家属均知情且签署同意书。
1.2 纳入标准与排除标准纳入标准:(1)病灶与SPN定义相符;(2)肺内单发;(3)SPN直径小于3 mm;(4)心肾功能正常;(5)结节内钙化及脂肪成分不明显。
排除标准:(1)已行放化疗患者;(2)磨玻璃密度结节;(3)穿刺后结节;(4)结节内伴有空洞形成。
1.3 方法采用美国GE公司的64排MSCT,对患者胸廓入口至肋膈角水平范围行平扫及增强薄层扫描。全胸平扫以确定大致范围,扫描参数:球管电压120 kV、电流110~240 mA,启动Care-Dose 4D(实时动态曝光计量调节),扫描层面5 mm,0.5 s/圈,准直0.6×128 mm。并采用纵膈窗方式(窗宽350 HU,窗位50 HU)对图像进行观察,以选取能够显示结节最大径的轴位图像,测量结节最大径及CT值,再经开源后处理软件MaZda(Version 4.6)对病灶中心层面及其上下临近间隔5 mm的两层面进行纹理分析。
在发现SPN后,对SPN局部范围行高分辨率增强扫描。扫描参数:层厚1 mm,球管电压120~140 kV、电流150~250 mA,矩阵512×512,扫描时间1.2 s,采用1 mm间隔距离在不同视野下进行图像重建,后期经GE公司aw 4.4网络工作站,以容积显示重建法(VR)进行三维重建。
1.4 观察指标CT纹理分析及MSCT三维重建技术操作、分析均由2名放射诊断医师(主治医师及以上)单独进行,若两者意见未达成一致,则经协商确定。提取SPN三个层面的熵、熵和、熵差、对比度、相关性、均和等纹理特征值,取均值并作对比分析。统计MSCT扫描及MSCT三维重建技术对SPN形态特征显示率,形态特征主要有分叶征、毛刺征、血管集束征、胸膜牵拉征、空泡征,并以分叶征和毛刺征作为主诊断征象,其余为次诊断征象。评估SPN良恶性,恶性:2项主诊断征象,或1项主诊断征象且具2项及以上次诊断征象,良性:与SPN恶性诊断条件不相符的为SPN良性。
1.5 统计学处理采取SPSS 22.0软件进行统计分析,计数资料用(n,%)表示,行χ2检验;计量资料用( x ±s)表示,行t检验。对差异显著的纹理参数及联合指标建立受试者工作特征(ROC)曲线,评价其鉴别诊断SPN良恶性的敏感度与特异度。P < 0.05为差异具有统计学意义。
2 结果 2.1 CT纹理分析结果比较CT纹理分析两组的纹理特征参数,详见表 1,结果显示,恶性组熵、熵和、熵差均明显高于良性组,差异具有统计学意义(P < 0.05)。
| 表 1 CT纹理分析两组纹理特征参数比较( x ±s) |
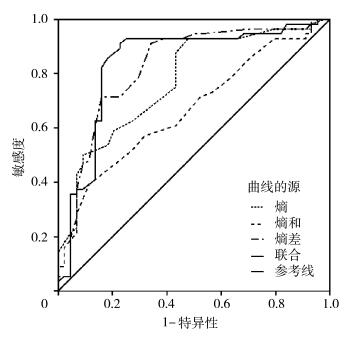
基于上述具有统计学意义的熵、熵和、熵差参数指标,采用二元Logistic回归分析计算三者联合指标,建立ROC曲线(图 1),ROC曲线分析结果、鉴别诊断SPN良恶性效能分析详见表 2、表 3。熵、熵和、熵差及三项联合鉴别诊断SPN良恶性的AUC分别为0.790、0.677、0.821、0.841。熵差、三项联合鉴别诊断SPN良恶性准确性高,二者AUC比较无显著差异。根据约登指数计算最佳临界值发现,当熵差高于0.965时,其敏感度为85.7%,特异度为70.5%;当三项联合高于2.9096时,其敏感度为94.6%,特异度为65.9%。
|
图 1 熵、熵和、熵差及联合特征参数的ROC曲线图 |
| 表 2 CT纹理分析各特征参数ROC曲线下面积AUC分析 |
| 表 3 CT分析各参数特征及联合指标鉴别诊断SPN良恶性效能分析 |
表 4为MSCT三维重建和CT平扫对SPN征象的显示率,由表 4可知,在SPN征象方面,除胸膜牵拉征外,MSCT三维重建技术在分叶征、毛刺征、血管集束征、空泡征等SPN形态特征显示率均明显高于CT平扫,差异均有统计学意义(P < 0.05)。
| 表 4 MSCT三维重建技术与CT平扫对SPN征象的显示率比较(n,%) |
MSCT三维重建技术与CT平扫鉴别SPN的诊断结果及效能分析列于表 5、表 6,由表中可知,MSCT三维重建对SPN的诊断准确率、灵敏度、特异度、阳性预测率、阴性预测率,分别为86.0%、88.9%、82.6%、85.7%、86.4%,各诊断效能指标均高于CT平扫。
| 表 5 MSCT三维重建与CT平扫鉴别SPN的诊断结果比较(例) |
| 表 6 MSCT三维重建与CT平扫鉴别诊断SPN的效能(%) |
肺癌高发病率及高死亡率特征明显[8, 9],患者5年生存率低于5%[10]。因此,早期诊断与及时治疗尤为重要。CT纹理技术属图像后处理技术,可根据组织纹理特征揭示其内在异质性,基于CT图像表现,可有效提升SPN鉴别诊断能力,从而更精准地鉴别诊断早期肺癌[11]。肿瘤异质性与新血管生成密切相关,是恶性肿瘤重要特征之一[12]。而对肺癌而言,坏死为其主要CT表现,朱胜康等[12]研究发现,肺癌病灶内坏死发生率与病灶体积成正相关。孔令重等[13]研究发现,良恶性SPN在CT值与结节最大径方面存在差异但不显著,表明CT平扫难以有效鉴别诊断SPN良恶性。在CT图像表现中,熵与其纹理非均匀程度成正相关,熵越大,纹理越复杂[14, 15]。迟淑萍[16]的研究结果显示恶性结节熵值明显高于良性。本研究中,恶性组熵、熵和、熵差均明显高于良性组,与上述结论一致。ROC曲线分析结果显示,熵、熵和、熵差、以及三项联合鉴别诊断SPN良恶性的AUC分别为0.79、0.677、0.821、0.841,根据得到的最佳临界值、敏感度、特异度分析可知,三项联合鉴别诊断SPN良恶性准确性高,效能更优。
随着多层螺旋CT逐渐推广应用,三维重建成像技术所具备的高辨析度优势日益凸显,逐渐广泛应用于临床。基于性质及部位,SPN在MSCT三维成像上可呈现出多种表现,其形态学征象细微但独特,以此为根据,可对SPN良恶性进行有效鉴别诊断[17]。SPN恶性病变其形态学征象主要以病灶背部结构特征方式表现,包括胸膜牵拉征、毛刺征、空泡征、分叶征、血管集束征等,其中,分叶征与毛刺征为SPN恶性病变主要鉴别诊断依据。本研究中,在SPN征象方面,除胸膜牵拉征外,MSCT三维重建技术在分叶征、毛刺征、血管集束征、空泡征等SPN形态特征显示率均明显高于CT平扫。此外,对SPN诊断准确率、灵敏度、特异度、阳性预测率、阴性预测率而言,MSCT三维重建各诊断效能指标均高于CT平扫,表明MSCT三维重建技术提高了SPN良恶性鉴别准确率,对SPN临床初期诊断更为有利。
综上所述,CT纹理分析与MSCT三维重建技术均有利于SPN良恶性鉴别诊断,CT纹理分析熵、熵和、熵差联合诊断敏感度更高,为94.6%,而MSCT三维重建特异度更高,为82.6%,因此,还需结合临床情况进行科学选择。
| [1] |
Marukawa M, Taniguchi A, Kimura G, et al. Solitary pulmonary nodules caused by Mycobacterium avium complex[J]. Respiratory Investigation, 2019, 57(6): 566-573. |
| [2] |
闾少冬, 陆文博, 楼良潮. 孤立性肺结节123例诊治体会[J]. 贵州医药, 2019, 43(9): 1406-1407. |
| [3] |
许海柱, 祝佳佳, 张栩. 孤立性肺结节诊断和治疗进展[J]. 长春中医药大学学报, 2019, 35(5): 1002-1006. |
| [4] |
张崴琪, 王一卓, 王晓慧, 等. 基于CT后处理重组技术的孤立性肺结节良恶性危险因素[J]. 放射学实践, 2019, 34(10): 1102-1107. |
| [5] |
张振显, 杨爱莲, 吴爱军, 等. 多层螺旋CT动脉扫描及三维重建在孤立性肺小结节诊断中的应用比较[J]. 中国医学装备, 2018, 15(9): 62-65. |
| [6] |
You S, Kim E Y, Park K J, et al. Visual assessment of calcification in solitary pulmonary nodules on chest radiography:correlation with volumetric quantification of calcification[J]. European Radiology, 2019, 29(8): 4324-4332. |
| [7] |
Nasim F, Ost D E. Management of the solitary pulmonary nodule[J]. Current Opinion in Pulmonary Medicine, 2019, 25(4): 344-353. |
| [8] |
王霞, 孙琼芳, 涂蓉, 等. 螺旋CT三维重建技术对孤立性肺结节征象的研究进展[J]. 海南医学, 2014, 25(14): 2105-2108. |
| [9] |
王拢拢, 李静. 孤立性肺结节的活检方式进展[J]. 临床肺科杂志, 2018. |
| [10] |
余翔, 张敏, 刘建光. 孤立性肺结节影像学特征的logistic回归分析[J]. 蚌埠医学院学报, 2019, 44(7): 936-939. |
| [11] |
张娜, 鄂林宁, 吴山, 等. CT纹理分析技术鉴别良恶性孤立性肺结节[J]. 中国医学影像技术, 2018, 34(8): 1211-1215. |
| [12] |
朱胜康, 翟荣存, 李年春, 等. 多层螺旋计算机断层扫描在鉴别良恶性肺部孤立性结节中的应用[J]. 癌症进展, 2019, 17(15): 1771-1773. |
| [13] |
孔令重, 姜壮国, 曹小江, 等. Logistic回归分析高分别率CT的纹理特征对孤立性肺结节诊断价值[J]. 新疆医科大学学报, 2019, 42(2): 198-202. |
| [14] |
鄂林宁, 张娜, 王荣华, 等. 计算机体层摄影术纹理分析对孤立性肺结节良恶性鉴别诊断的价值[J]. 中华肿瘤杂志, 2018, 40(11): 847-850. |
| [15] |
张泽文, 张才擎, 王广丽, 等. 孤立性肺结节在HDCT的计算机辅助诊断[J]. 医学影像学杂志, 2015, 25(6): 993-997. |
| [16] |
迟淑萍. CT图像纹理分析在鉴别良恶性肺结节中的价值[J]. 实用放射学杂志, 2016, 32(11): 1789-1792. |
| [17] |
柯君, 马亚宁. 螺旋CT三维重建对孤立性肺结节良恶性的诊断价值分析[J]. 中国CT和MRI杂志, 2019, 17(5): 55-58. |



