2. 东华理工大学, 化学生物与材料科学学院, 江西 南昌 330013
2. School of Chemistry, Biology and Material Science, East China University of Technology, Nanchang 330013, Jiangxi, P. R. China
三磷酸腺苷(adenosine triphosphate, ATP)是各种活细胞内普遍存在的一种高能化合物,是各种生物活动的直接能量来源,在光合、酶催化、生物合成、DNA复制、细胞呼吸等各种生物过程中,ATP还是一种重要的信号分子[1, 2],ATP水平的异常变化可用于指示疾病及病变的程度。此外,ATP含量与活细胞数目有着线性关系,可间接表达样品中细菌数量。因此,ATP快速检测可在临床诊断、药物筛选、食品卫生、环境监测等领域发挥重要作用[3-5]。
目前,已报道的ATP检测方法主要包括电泳分析法[6, 7]、色谱分析法[8]、光学分析法[9]和生物传感器法[10, 11]等。其中,光学分析法中的荧光分析在检测生物分子方面显示出独特的优势,有灵敏度高、选择性好等特点,是目前公认的较为理想的检测方法之一。常见的荧光探针有贵金属纳米团簇、有机染料、量子点(QDs)。相比较而言,QDs具有荧光产率高、激发光谱宽、荧光光谱窄的特点,因此QDs的应用受到越来越多的关注,尤其是在化学及生物分析领域。如Tedsana等[12]将半胱胺修饰CdS量子点(Cys-CdS QDs)的荧光强度与ATP呈正比关系用于ATP的高选择性检测。Shi等[13]采用Cys-CdTe QDs为荧光团,Zn2+为猝灭剂,添加ATP,荧光性能恢复,实现了“off-on”模式的ATP检测。但重金属型量子点因毒性较大,在生物医学尤其是活体检测中难以展开应用[14]。因此,研究者开始尝试探寻低毒或无毒性的量子点。如胡先运等[15]以氧化石墨烯(GO)为猝灭剂,ATP适配体标记InP/ZnS量子点(ABA-QDs),通过GO与ABA-QDs之间的长程共振能量转移(LrRET),对ATP进行检测。Xiong等[16]用MPA-Mn:ZnS QDs为荧光探针,采用ATP适配体为猝灭剂,实现生物体液中ATP的检测。但是,这些量子点荧光探针的合成过程要求严格,工艺偏复杂,且制备成本偏高。
氧化物钼是一种过渡金属半导体,其自然资源丰富、价廉、低毒,且有独特的电子、光学和力学性能[17, 18];在气体传感、催化剂、光致变色等领域备受关注[19-21]。本课题组采用常温一步法制备出低毒性的荧光氧化钼量子点(MoOx QDs),目前已将基于MoOx QDs的荧光探针用于对卡托普利、2, 4, 6-三硝基苯、乙酰胆碱酯酶的快速检测[22, 23]。本文以MoOx QDs为荧光探针,Cu2+为荧光猝灭剂,建立一种简单、快速、高灵敏的ATP检测方法。
1 实验部分 1.1 试剂与仪器寡三磷酸腺苷(ATP)、三磷酸胞嘧啶(CTP)、牛血清白蛋白(BSA),上海生工生物工程有限公司;二硫化钼粉末(MoS2),美国Sigma-Aldrach公司;氢氧化钠(NaOH)、30%双氧水(30% H2O2)、浓盐酸(HCl)、氯化铜(CuCl2)、乙二胺四乙酸二胺(EDTA)、硫酸铁[Fe2(SO4)3]、氯化钙(CaCl2)、氯化镍(NiCl2)、氯化钴(CoCl2)、硫酸锰(MnSO4),均购于西陇化工股份有限公司;磷酸钠、磷酸氢二钠、磷酸二氢钠、焦磷酸钠,国药集团化学试剂有限公司;Tris缓冲液(C4H11O3),美国Solarbio公司。实验中所用试剂均为分析纯,使用前未经纯化,所有溶液均采用二次蒸馏水配制。
JEM-2010透射电子显微镜(日立公司,日本),USB-4000荧光分光光谱仪(海洋光谱,美国),F-7000荧光分光光度计(日立公司,日本)。
1.2 实验方法 1.2.1 氧化钼荧光量子点的制备氧化钼荧光量子点(MoOx QDs)的制备方法参考文献[22]。200 mg MoS2粉末和16 mL 30% H2O2、6 mL H2O在40 ℃水浴反应4 h,加入NaOH调至pH中性,然后8000 r/min离心10 min,所得上清液即为氧化钼荧光量子点。
1.2.2 Cu2+对MoOx QDs荧光猝灭的影响在离心管中加入20 L 1 mg/mL MoOx QDs溶液、40 L 50 mmol//L Tris-HCl缓冲溶液、不同体积的1 mmol/L CuCl2溶液,最后用去离子水定容至400 L,充分振荡后静置,10 min后在405 nm下测定溶液荧光光谱。
在离心管中加入20 L 1 mg/mL MoOx QDs溶液、40 L 50 mmol/L Tris-HCl,20 L 1 mmol/L CuCl2溶液,以及不同体积的1 mmol/L EDTA溶液,最后用去离子水定容至400 L,充分振荡后静置,10 min后在405 nm下测定溶液荧光光谱。
1.2.3 ATP测定方法在离心管中加入20 L 1 mg/mL MoOx QDs溶液、40 L 50 mmol/L Tris-HCl缓冲溶液、20 L 1 mmol/L CuCl2溶液,以及不同浓度ATP溶液,最后用去离子水定容至400 L,充分振荡后静置,10 min后在405 nm下测定溶液荧光光谱,用520 nm处最强发射峰的荧光强度(FL)定量分析ATP含量。
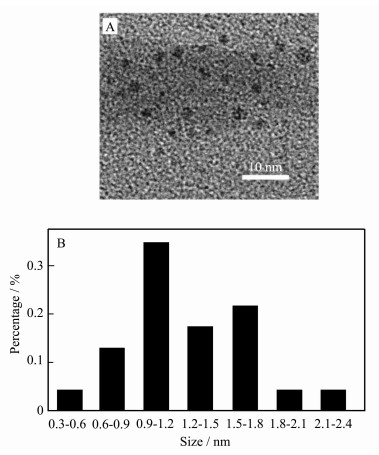
2 结果与讨论 2.1 MoOx QDs的表征通过TEM对MoOx QDs进行扫描测试可知,合成的MoOx QDs外貌为类球形,颗粒分散性能较好,粒径分布范围较窄,平均粒径约为1.7 nm(见图 1)。
|
图 1 MoOx QDs的TEM图(A)和粒径分布图(B) |
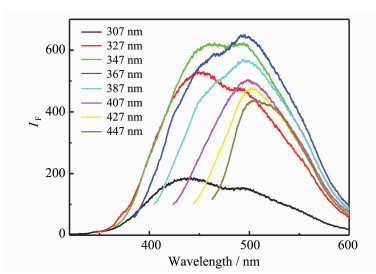
在307~447 nm不同激发光照射下,MoOx QDs均具有很强的荧光发光性能(图 2),且在367nm激发波下,于495 nm处产生最强的荧光信号;不同激发光下,发射峰位置随着激发波长变长而发生红移,说明MoOxQDs的荧光性能具有连续性和可调性。本文合成量子点的基本荧光性能与文献[22]报道基本吻合。
|
图 2 不同激发光下MoOx QDs荧光发射光谱 |
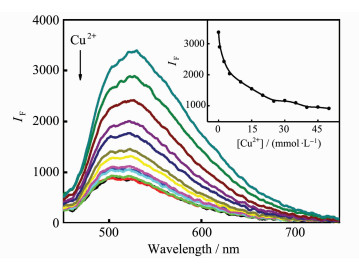
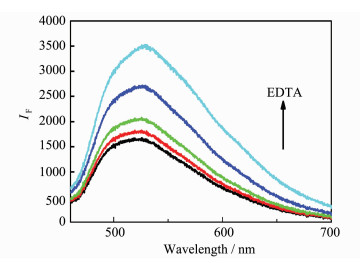
为考察Cu2+对MoOx QDs荧光猝灭的动力学特征,研究了Cu2+和EDTA共同加入量对荧光强度的影响。图 3显示,Cu2+浓度变化不影响荧光发射峰的形状,它们的最大发射波长均在520 nm,这表明Cu2+与MoOx QDs作用不会改变其晶体结构。当[Cu2+]为5~50 mol/L时,体系的荧光峰强度会随着Cu2+加入量增加而迅速下降(图 3内插图),35~50 mol/L时,荧光猝灭率可达70%。本试验选择50 mol/L Cu2+溶液作为猝灭剂。如图 4,在MoOx QDs-Cu2+体系中继续添加EDTA时,体系的荧光峰强度会随EDTA浓度增大而逐渐增强,即产生荧光恢复。当[EDTA]:[Cu2+]=1时,体系荧光强度可恢复到初始的95%以上。说明Cu2+对MoOx QDs的荧光猝灭性是可逆的。
|
图 3 Cu2+浓度对MoOx QDs荧光发射光谱的影响 插图为520nm处Cu2+浓度与荧光发射强度关系曲线 (实验条件:0.05 mg/mL MoOx QDs,pH 7.5,Cu2+浓度从上到下为0、0.5、2.5、5、10、15、20、25、30、35、40、45、50 mol/L) |
|
图 4 EDTA对MoOx QDs-Cu2+荧光发射光谱的影响 (实验条件:0.05 mg/mL MoOx QDs,[Cu2+]=50mol/L, pH 7.5, EDTA的浓度从下到上分别为0、12.5、25、37.5、50 mol/L) |
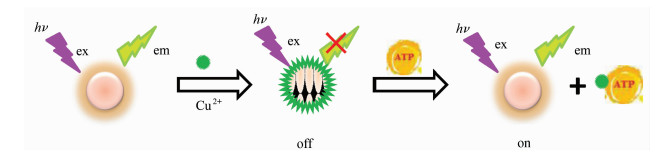
Cu2+对MoOx QDs的荧光猝灭作用机理大致为:Cu2+通过弱键与MoOx QDs之间发生结合作用形成了非荧光的基态化合物,产生静态荧光猝灭,即“off”状态。与Cu2+能产生强亲和作用的化合物,将Cu2+从MoOx QDs上分离并释放出MoOx QDs,体系荧光性能得到恢复,即“on”状态。ATP是一种典型的磷酸化合物,其磷酸基团可通过P-O-与Cu2+产生强烈作用。向MoOx QDs-Cu2+体系加入ATP时,Cu2+会从MoOx QDs表面分离下来,重新释放量子点,从而使猝灭的荧光性能得到恢复,如图 5所示。基于上述分析,本文构建“off-on”型MoOx QDs-Cu2+检测平台用于ATP检测。
|
图 5 检测ATP原理示意图 |
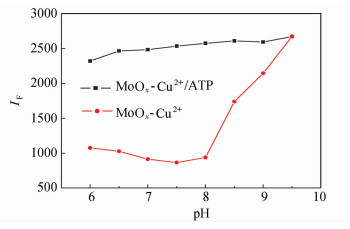
一般情况下,检测环境的pH值对检测效果影响很大,为了增强MoOx QDs-Cu2+检测平台的稳定性和选择性,优化检测方法,实验考察了溶液pH值对MoOxQDs荧光猝灭及荧光恢复的影响。如图 6所示,在弱酸性条件下,荧光强度较低,且酸性越强荧光强度越弱。当pH 7.5时,荧光强度最弱。在pH 8.0~9.5碱性性条件下,荧光强度随碱性的显著增强。这可能是在碱性条件下-OH与Cu2+作用的几率增大,从而抑制了Cu2+对MoOxQDs的结合,导致荧光猝灭不完全,甚至无荧光猝灭产生。ATP对MoOx QDs的荧光恢复性在pH 6.0~9.5时,变化幅度不大。当Cu2+与MoOx QDs的作用完全被抑制时,MoOx QDs的荧光强度可恢复到初始状态。为使检测的“off-on”过程明显,本试验pH值优化为7.5。
|
图 6 pH对MoOx QDs-Cu2+和MoOx QDs-Cu2+/ATP对520 nm处荧光发射性能的影响 (实验条件:0.05 mg/mL MoOx QDs,[Cu2+]=50mol/L,或ATP:200mol/L) |
如图 7所示,在优化后的实验条件下,荧光强度随着ATP浓度的增大而不断增强;且ATP浓度为25~250 mol/L时,荧光强度(F)与ATP浓度(c,μmol/L)呈现良好的线性关系(图 7插图),拟合线性方程为F=785.40+9.05c,相关系数R=0.993,该线性使用范围比文献[12]中的20~80mol/L宽。

|
图 7 ATP对MoOx QDs-Cu2+荧光发射光谱的影响 插图为520 nm处ATP浓度与荧光发射强度关系曲线 (实验条件:0.05 mg/mL MoOx QDs,[Cu2+]=50 mol/L,pH 7.5,ATP浓度自下而上依次为0、25、50、75、100、125、150、175、200、250 mol/L) |
为进一步验证MoOx QDs-Cu2+检测平台对ATP荧光检测方法的灵敏性,本文考察了BSA、Ni2+、Mn2+、Fe3+、Co2+、Ca2+等可能共存物对量子点荧光的影响,见图 8。当干扰物为非磷酸盐化合物时,对应的荧光恢复程度不及ATP的1/10;当干扰物为含磷酸盐的CTP时,其荧光恢复程度仅为ATP的1/2。所以,该检测方法在无磷酸盐干扰时检测灵敏性高,由于该荧光检测的机理主要为离子间键的相互作用,该作用没有方向性,但在含磷酸盐干扰环境下可进行半定量分析。

|
图 8 MoOx QDs荧光探针对ATP的选择性 (实验条件:0.05 mg/mL MoOx QDs,[Cu2+]=50 mol/L,pH 7.5,ATP:250 mol/L,Ni2+、Mn2+、Fe3+、Co2+、Ca2+、BSA、H2PO4-、HPO42-、PO43-浓度均为500 mol/L) |
本文以MoOx QDs为荧光探针,Cu2+为猝灭剂,构建新型“off-on”荧光传感器用于ATP快速检测,该检测响应时间快,荧光性能强且稳定。在1 mg/mL MoOx QDs,50mol/L CuCl2,Tris-HCl缓冲pH 7.5、ATP浓度为25~250 mol/L优化条件时,体系荧光强度与ATP浓度呈线性关系,相关系数为0.993;除含磷酸盐化合物外,该检测方法的抗干扰性高。因此,本文的ATP检测方法具有制备技术简单、性能稳定、检测时间短、灵敏度高,且线性使用范围宽等特点,可为环境及食品等领域的品质评价提供一种新的快捷检测方法。
| [1] |
Gourine A V, Llaudet E, Dale N, et al. ATP is a mediator of chemosensory transduction in the central nervous system[J]. Nature, 2005, 436(7047): 108-111. DOI:10.1038/nature03690 |
| [2] |
Lian Y K, Jiang H, Feng J Z, et al. Direct and simultaneous quantification of ATP, ADP and AMP by 1H and 31P nuclear magnetic resonance spectroscopy[J]. Talanta, 2016, 150: 485-492. DOI:10.1016/j.talanta.2015.12.051 |
| [3] |
Cheng J H, Sun D W, Zeng X A, et al. Recent advances in methods and techniques for freshness quality determination and evaluation of fish and fish fillets:a review[J]. Critical Reviews in Food Science & Nutrition, 2015, 55(7): 1012-1225. |
| [4] |
Pistelok F, Pohl A, Stuczynski T, et al. Strengths and weaknesses in the determination of Saccharomyces cerevisiae cell viability by ATP-based bioluminescence assay[J]. Ecological Chemistry & Engineering S, 2016, 23(2): 259-270. |
| [5] |
Han T, Wren M, Dubois K, et al. Application of ATP-based bioluminescence for bioaerosol quantification:effect of sampling method[J]. Journal of Aerosol Science, 2015, 90: 114-123. DOI:10.1016/j.jaerosci.2015.08.003 |
| [6] |
周春喜, 郁荣, 吕海燕, 等. 三磷酸腺苷、二磷酸腺苷和一磷酸腺苷的毛细管电泳分析研究[J]. 分析科学学报, 2003(5): 433-434. |
| [7] |
Liebers V, Bachmann D, Franke G, et al. Determination of ATP-activity as a useful tool for monitoring microbial load in aqueous humidifier samples[J]. International Journal of Hygiene and Environmental Health, 2015, 218(2): 246-253. DOI:10.1016/j.ijheh.2014.11.004 |
| [8] |
Zhou L, Xue X X, Zhou J Hi, et al. Fast determination of adenosine 5'-triphosphate (ATP) and its catabolites in royal jelly using ultraperformance liquid chromatography[J]. Journal of Agricultural and Food Chemistry, 2012, 60(36): 8994-8999. DOI:10.1021/jf3022805 |
| [9] |
Wu H Q, Wu Q P, Zhang J M, et al. Study on rapid quantitative detection of total bacterial counts by the ATP-bioluminescence and application in probiotic products[J]. International Journal of Food Science and Technology, 2011, 46(5): 921-929. DOI:10.1111/j.1365-2621.2010.02531.x |
| [10] |
Srivastava P, Razi S S, Ali R, et al. Highly sensitive cell im-aging "off-on" fluorescent probe for mitochondria and ATP[J]. Biosensors and Bioelectronics, 2015, 69: 179-185. DOI:10.1016/j.bios.2015.02.028 |
| [11] |
Wang W, Zhao N, Li X X, et al. Isothermal amplified detection of ATP using Au nanocages capped with a DNA molecular gate and its application in cell lysates[J]. The Analyst, 2015, 140(5): 1672-1677. DOI:10.1039/C4AN02202E |
| [12] |
Tedsana W, Tuntulani T, Ngeontae W. A highly selective turn-on ATP fluorescence sensor based on unmodified cysteamine capped CdS quantum dots[J]. Analytica Chimica Acta, 2013, 783(11): 65-73. |
| [13] |
Shi F P, Li Y, Lin Z H, et al. A novel fluorescent probe for adenosine 5-triphosphate detection based on Zn2+-modulated l-cysteine capped CdTe quantum dots[J]. Sensors and Actuators B:Chemical, 2015, 220: 433-440. DOI:10.1016/j.snb.2015.05.087 |
| [14] |
Derfus A M, Chan W C W, Bhatia S N. Probing the cytotoxicity of semiconductor quantum dots[J]. Nano Letters, 2004, 4(1): 11-18. DOI:10.1021/nl0347334 |
| [15] |
胡先运, 江家志, 王传明, 等. 氧化石墨烯/适配体-量子点荧光探针用于ATP检测[J]. 分析试验室, 2018, 37(9): 1003-1007. |
| [16] |
Xiong Y, Cheng Y, Wang L, et al. An "off-on" phosphorescent aptasensor switch for the detection of ATP[J]. Talanta, 2018, 190: 226-234. DOI:10.1016/j.talanta.2018.07.060 |
| [17] |
Anh Tran T, Krishnamoorthy K, Song Y W, et al. Toxicity of nano molybdenum trioxide toward invasive breast cancer cells[J]. ACS Applied Materials & Interface, 2014, 6(4): 2980-2986. |
| [18] |
Krishnamoorthy K, Premanathan M, Veerapandian M, et al. Nanostructured molybdenum oxide-based antibacterial paint:effective growth inhibition of various pathogenic bacteria[J]. Nanotechnology, 2014, 25(31): 596-606. |
| [19] |
Illyaskutty N, Sreedhar S, Kumar G S, et al. Alteration of architecture of MoO3 nanostructures on arbitrary substrates:growth kinetics, spectroscopic and gas sensing properties[J]. Nanoscale, 2014, 6: 13882-13894. DOI:10.1039/C4NR04529G |
| [20] |
Wang Y X, Zhang X, Luo Z M, et al. Liquid-phase growth of platinum nanoparticles on molybdenum trioxide nanosheets:an enhanced catalyst with intrinsic peroxidase-like catalytic activity[J]. Nanoscale, 2014, 6(21): 12340-12344. DOI:10.1039/C4NR04115A |
| [21] |
Yi Q H, Zhai P F, Sun Y H, et al. Aqueous solution-deposited molybdenum oxide films as an anode interfacial layer for organic solar cells[J]. ACS Applied Materials & Interfaces, 2015, 7: 18218-18224. |
| [22] |
Xiao S J, Zhao X J, Chu Z J, et al. New off-on sensor for captopril sensing based on photoluminescent MoOx quantum Dots[J]. ACS Omega, 2017, 2: 1666-1671. DOI:10.1021/acsomega.7b00088 |
| [23] |
Xiao S J, Zhao X J, Chu Z J, et al. Highly photoluminescent molybdenum oxide quantum dots:one pot synthesis and application in 2, 4, 6-trinitrotoluene determination[J]. ACS Applied Materials & Interfaces, 2016, 8(12): 8184-8191. |



