2. 北京交通大学 理学院 发光与光信息技术教育部重点实验室, 北京 100044
2. Key Laboratory of Luminescence and Optical Information, Ministry of Education, School of Science, Beijing Jiaotong University, Beijing 10044, P. R. China
随着全球能源短缺的日益加剧,白光LED的开发与研究成为照明产业的一大热点,LED作为一种新型的绿色环保型固体照明光源,必将成为未来发展的趋势.白光LED与目前广泛应用的传统照明光源和显示设备相比较,具有发光效率高、光色纯、光线质量 高、能耗小、寿命长、无污染、应用灵活、控制灵活、响应快等优点.基于LED的种种优点,未来白光LED的应用将非常广泛,如液晶屏背光灯光源、汽车前灯、室外及室内照明设备等,其中最大的市场,还是取代白炽钨丝灯泡及荧光灯的照明替换市场.
白光LED可以通过以下3种方法得到:(1)红、绿、蓝3种LED组合得到白光;(2)蓝光LED和黄色荧光粉组合得到白光;(3)紫光LED和RGB(红绿蓝)荧光粉组合得到白光.目前,利用蓝色芯片和黄色YAG∶Ce荧光粉组成的白光LED在发光效率等方面取得了明显的进步.但是,该方法组合产生的白光LED至少存在两方面的缺陷:一是色温偏高,降低色温会使发光效率明显降低;二是这种所谓的白光缺少可见光的红色光谱部分,为了弥补色平衡方面的不足,需在黄色荧光粉中加入一种能够被蓝色LED有效激发的红色荧光粉.在该模式产生的白光LED中,高效的红色荧光粉是不可或缺的部分.
长期以来,人们在改进红色荧光粉的基质方面做了大量工作,例如硫化物、硅酸盐、钛酸盐、氧化物、硫氧化物和铝酸盐等体系的开发和研究.在钼、钨酸盐基质的开发上也取得了一定成果.Neeraj等[1]研究发现,NaY0.95Eu0.05(WO4)(MoO4)在393 nm光激发下发射615 nm的红光,在该波段激发下发光强度是传统硫化物的7.28倍.Hu等[2]制备了Ca(MoO4)∶Eu3+,在394 nm光激发下发射616 nm的红光,其强度是传统硫化物红粉的5倍.还可以掺杂Li+、Na+或K+以实现电荷补偿,发光强度可提高至以前的3倍[3].近年来,稀土离子作为激活剂的荧光粉得到了广泛的研究[4,5].由于三价Eu3+离子掺杂的材料对蓝色LED的蓝光发射有很好的吸收,而且在紫外激发下也有很高的量子效率;尤其是Eu3+离子在基质中占据非对称中心位置时,它的5D0→7F2跃迁在红光范围内有很强的发射,所以,Eu3+是一种很好的红色荧光粉激活剂[6,7,8].我们利用高温固相反应法合成R2-x(MoO4)3∶xEu3+(R=Y,Gd)红色荧光粉,通过调节煅烧温度、助熔剂的含量和Eu3+离子的掺杂量来制备高亮度、高稳定性的钼酸盐红色荧光粉,并对样品的物相组成、激发和发射光谱进行分析. 1 实验部分
通过高温固相法合成名义成分为Gd2-x(MoO4)3∶xEu3+(x=0.4、0.6、0.8、1.0、1.2、1.4、1.6、1.8)和Y2-y(MoO4)3∶yEu3+(y=0.4、0.6、0.8、1.0、1.2、1.4、1.6、1.8)的红色荧光粉.按化学计量比称取一定量的Y2O3(99.99%),Gd2O3(99.99%),(NH4)6Mo7O24· 4H2O(AR),Eu2O3(99.99%)和适量助熔剂.将上述混合物在玛瑙研钵中充分混合均匀,装入氧化铝坩埚,放入KSF1700X型箱式电阻炉在空气气氛下800 ℃—1100 ℃煅烧3 h即得所需样品.
样品经过再次研磨得到粒度分布均匀的红色粉末,用X射线衍射仪(XRD,Rigaku D/max-Rb,Cu-Kα,λ=0.1542 nm)分析确定样品的相组分.样品的激发和发射光谱通过EX-1000荧光粉激发光谱与热猝灭分析系统(杭州远方科技)测量,激发光源为Xe灯,入射和出射狭缝均为2.5 nm,扫描速率1200 nm/min,激发发射光谱范围200 nm—800 nm,所有测量在室温下进行. 2 结果与讨论 2.1 Eu3+离子的浓度和煅烧温度对样品发光强度的影响
图1和图2分别给出样品Gd2-x(MoO4)3∶xEu3+和Y2-y(MoO4)3∶yEu3+在1000 ℃下煅烧3 h所得荧光粉的相对发光亮度随Eu3+离子含量的变化关系.从图1中可以看出,样品Gd2-x(MoO4)3∶xEu3+和Y2-y(MoO4)3∶yEu3+的相对亮度随Eu3+离子含量的增加呈上升趋势,当x=1.4时,样品Gd2-x(MoO4)3∶xEu3+的相对亮度达到最佳(图1),Eu3+离子的浓度继续增加,样品的相对亮度趋于下降.在图2中,当y=1.8时,样品Y2-y(MoO4)3∶yEu3+的相对亮度达到最佳(图2).两个系列配方的样品在465 nm激发下的相对亮度要比在395 nm激发下的高,说明该基质的红色荧光粉更适合蓝光芯片(465 nm)的激发.
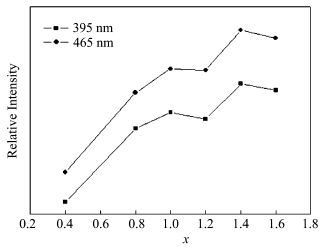 | 图1 样品Gd2-x(MoO4)3∶xEu3+在1000 ℃下煅烧所得荧光粉的相对亮度随Eu3+离子含量的变化关系 variation of the emission intensity with Eu3+ concentration for Gd2-x(MoO4)3∶xEu3+ prepared at 1000 ℃ |
 | 图2 样品Y2-y(MoO4)3∶yEu3+在1000 ℃下煅烧所得荧光粉的相对亮度随Eu3+离子含量的变化关系 The variation of the emission intensity with Eu3+ concentration for Y2-y(MoO4)3∶yEu3+ prepared at 1000 ℃ |
图3为样品Gd0.6(MoO4)3∶1.4Eu3+(a)和Y0.2(MoO4)3∶1.8Eu3+(b)在不同的煅烧温度下的相对亮度变化关系图.从图中可以看出在1000 ℃以下,样品的相对亮度随煅烧温度的提高而逐渐增加,表明随着温度的提高样品结晶更完全,合成了单一的相,有利于发光性能的改善和提高.在1000 ℃煅烧得到的样品的发光性能达到最佳,之后随着煅烧温度的提高,样品的相对发光亮度下降.
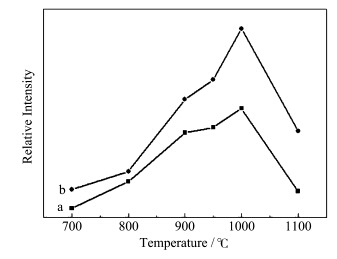 | 图3 Gd0.6(MoO4)3∶1.4Eu3+(a)和Y0.2(MoO4)3∶1.8Eu3+(b)在不同的煅烧温度下的相对亮度变化关系图 The variation of emission intensity for Gd0.6(MoO4)3∶1.4Eu3+ (a) and Y0.2(MoO4)3∶1.8Eu3+ (b) prepared at different temperature |
图4和图5分别给出了样品Gd0.6(MoO4)3∶1.4Eu3+在800 ℃和1000 ℃下煅烧3 h所得荧光粉的XRD图谱.图4中在800 ℃下把衍射图谱与XRD标准卡片JCPDS 25-0338相比较,只观察到了单斜晶系的Gd2(MoO4)3,没有其它的相出现.说明Eu3+的掺杂对样品的相结构影响不大,其晶格常数为a=0.7575 nm,c=1.1424 nm.随着煅烧温度的提高,样品的相结构发生了变化,图5中样品在1000 ℃下煅烧,其衍射图谱与XRD标准卡片JCPDS 20-0408相比较,观察到了不同于在800 ℃下煅烧后样品的相结构,样品呈正交结构,其晶格常数为a=1.038 nm,c=1.0697 nm.可以看出样品随着煅烧温度的提高,相结构发生了明显的变化,Eu3+的掺杂对样品的相结构几乎没有影响,Eu3+离子能够很好地取代Gd3+离子的位置,在改变其晶格常数的同时,提高了样品的发光性能.
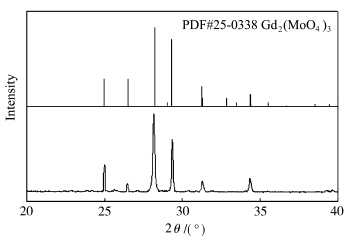 | 图4 Gd0.6(MoO4)3∶1.4Eu3+在800 ℃下煅烧的XRD图谱 The XRD patterns of Gd0.6(MoO4)3∶1.4Eu3+ prepared at 800 ℃/span> |
 | 图5 Gd0.6(MoO4)3∶1.4Eu3+在1000 ℃下煅烧的XRD图谱 The XRD patterns of Gd0.6(MoO4)3∶1.4Eu3+ prepared at 1000 ℃ |
图6给出了样品Y0.2(MoO4)3∶1.8Eu3+分别在800℃和1000℃下煅烧3 h所得荧光粉的XRD图谱.样品Y0.2(MoO4)3∶1.8Eu3+在800 ℃下的衍射图谱中各衍射峰与样品Gd0.6(MoO4)3∶1.4Eu3+在1000 ℃下的衍射峰位置相同,表明样品Y0.2(MoO4)3∶1.8Eu3+在800 ℃下已经完全形成了正交结构,且Y0.2(MoO4)3∶1.8Eu3+与Gd0.6(MoO4)3∶1.4Eu3+具有相同的正交结构,当煅烧温度升高到1000 ℃时,其正交结构仍可保持,没有发生相变.
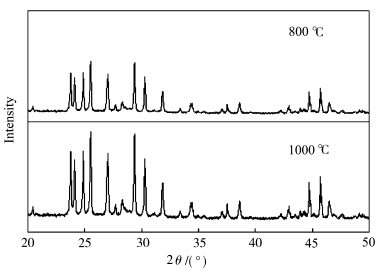 | 图6 Y0.2(MoO4)3∶1.8Eu3+分别在800 ℃和1000 ℃下煅烧的XRD图谱 The XRD patterns of Y0.2(MoO4)3∶1.8Eu3+ prepared at 800 ℃ and 1000 ℃ |
由图4、图5、图6的相结构分析,结合图3中两样品在不同温度下的相对发光亮度,可以看出1000 ℃下煅烧3 h样品的相对发光亮度最高,样品形成正交斜晶结构是其发光亮度提高的主要原因之一.晶格常数及晶胞结构的变化使得作为发光中心的Eu3+与其周围的氧离子的密排程度增加,在接受外界能量后不易引起氧离子严重偏离平衡位置,从而影响Eu3+发生无辐射能量跃迁的几率.晶胞的改变使得Eu3+在荧光粉晶格的距离减小,原子之间更容易发生能量转移.因此,正交斜晶结构的形成能使Eu3+充分进入晶格而形成有效的发光中心,提高发光亮度. 2.3 激发光谱和发射光谱
图7和图8分别是样品Gd0.6(MoO4)3∶1.4Eu3+和Y0.2(MoO4)3∶1.8Eu3+在395 nm(a)和465 nm(b)激发下的发射光谱.由图可知,Gd0.6(MoO4)3∶1.4Eu3+和Y0.2(MoO4)3∶1.8Eu3+的发射光谱都是由几组尖锐的峰组成,属于Eu3+的特征发射峰,分别对应于Eu3+的不同激发态5DJ(J=0、1)到基态7FJ(J=1、2、3、4)的跃迁(部分跃迁标于图中).
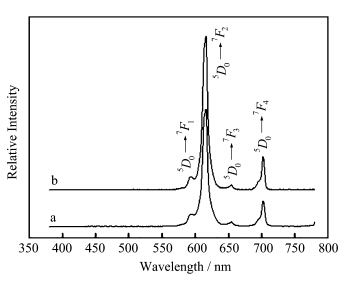 | 图7 样品Gd0.6(MoO4)3∶1.4Eu3+在395 nm(a)和465 nm(b)激发下的发射光谱 TThe emission spectra of Gd0.6(MoO4)3∶1.4Eu3+ excited by 395 nm (a) and 465 nm (b) |
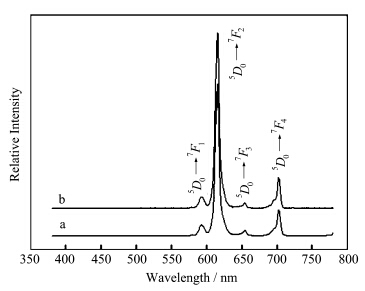 | 图8 样品Y0.2(MoO4)3∶1.8Eu3+Eu3+在395 nm(a)和465 nm(b)激发下的发射光谱 The emission spectra of Y0.2(MoO4)3∶1.8Eu3+excited by 395 nm (a) and 465 nm (b) |
位于591 nm附近较弱的发射峰对应的是Eu3+离子的5D0→7F1跃迁,位于612 nm附近的发射峰对应于Eu3+离子的5D0→7F2的跃迁发射,5D0→7F2的跃迁比5D0→7F1跃迁强,说明Eu3+离子占据非反演对称中心的位置[9].在紫外或蓝光激发下能发出很好的红光,是一种非常合适的蓝+黄体系获取白光LED的红色补光材料和紫外激发的红色转光材料.
图9为Gd0.6(MoO4)3∶1.4Eu3+(a)和Y0.2(MoO4)3∶1.8Eu3+(b)的激发光谱,检测波长612 nm,在图中350 nm之前低而宽的激发带来自电荷迁移带,350 nm后窄而强的峰属于Eu3+离子的f—f跃迁(395nm处的激发峰对应于Eu3+离子的7F0→5L6,465nm处的激发峰对应于Eu3+离子的7F0→5D2,535nm处的激发峰对应于Eu3+离子的7F0→5D1跃迁).3个主要的f—f跃迁的强度都高于电荷迁移带,对于一般的Eu3+激活的材料,激发谱中电荷迁移带的强度都高于Eu3+的f—f跃迁的强度,但钼酸盐基质例外,这可能是MoO42- 特有的性质.
 | 图9 样品Gd0.6(MoO4)3∶1.4Eu3+(a)和Y0.2(MoO4)3∶1.8Eu3+(b)的激发光谱 The excitation spectrum of Gd0.6(MoO4)3∶1.4Eu3+ (a) and Y0.2(MoO4)3∶1.8Eu3+ (b) monitored at 612 nm |
助熔剂在样品制备的过程中起着重要的作用,助熔剂的加入使激活剂容易进入基质,并促使基质形成微小颗粒,有利于煅烧物的相生成和转变,也更容易保持晶格的完整性,可以缩短反应时间,提高样品的结晶质量.利用助熔剂提高样品的发光效率是目前荧光粉制备过程中常用的一种方法.在该系列样品的制备过程中,我们尝试添加不同的助熔剂来研究它们对样品发光性能的影响.表1给出了样品Y0.2(MoO4)3∶1.8Eu3+在相同的反应条件下,加入不同种类助熔剂时的发光强度.从表中数据可以看出,样品Y0.2(MoO4)3∶1.8Eu3+在加入3%(质量分数)的NH4Cl作为助熔剂对其相对发光亮度的提高最大,说明NH4Cl在钼酸盐基质结晶过程中能够很好地提高结晶质量,是一种合适的助熔剂,适量加入可以提高样品的发光性能.
| 表1 不同助熔剂对样品Y0.2(MoO4)3∶1.8Eu3+发光性能的影响 The influence of different fluxes on the luminescent property of the samples Y0.2(MoO4)3∶1.8Eu3+ |
通过高温固相法合成了Gd0.6(MoO4)3∶1.4Eu3+和Y0.2(MoO4)3∶1.8Eu3+红色荧光粉,该荧光粉可以被近紫外光(395 nm)和蓝光(465 nm)有效激发,发射峰值位于612 nm的红光,是一种较好的产生白光LED的红色荧光粉.煅烧过程中的温度和时间是影响样品性能的主要因素,我们选择的两个系列样品在1000 ℃下煅烧3 h,样品的发光性能最佳.助熔剂的加入对样品的发光强度也有一定影响,当NH4Cl作为助熔剂加入3%时,样品分散性好,结晶完全,发光强度较高.
| [1] | Neeraj S, Kijima N, Cheetham A K. Novel red phosphors for solid-state lighting the system NaM(WO4)2-x(MoO4)x:Eu3+(M=Gd, Y, Bi) [J]. Chem. Phy. Lett., 2004, 387(1-3): 2-6. |
| [2] | Hu Y S, Zhuang W D, Ye H Q, et al. A novel red phosphor for white light emitting diodes [J]. J. Alloys Comp., 2005, 390(1-2): 226-229. |
| [3] | Wang J G, Jing X P, Yan C H, et al. Ca1-2xEuxLixMoO4: a novel red phosphor for solid-state lighting based on a GaN LED [J].J. Electrochem. Soc., 2005, 152(3): G186-G188. |
| [4] | 吴 亮, 刘光华, 李江涛. Eu3+掺杂Y2O3-Al2O3-SiO2玻璃的制备与荧光性能研究[J]. 影像科学与光化学, 2011, 29(4): 287-296. Wu L, Liu G H, Li J T Preparation and characterization of Eu3+: Y2O3-Al2O3-SiO2 glass[J]. Imaging Science and Photochemistry, 2011, 29(4): 287-296. |
| [5] | 莎 仁, 王喜贵. 纳米晶LaAlO3掺Eu3+的复合沉淀法制备及发光性质[J]. 影像科学与光化学, 2009, 27(6): 435-441. Sha R, Wang X G. Preparation and luminescence properties of LaAlO3:Eu3+ nanocrystals by complex precipate method[J]. Imaging Science and Photochemistry, 2009,27(6): 435-441. |
| [6] | Zeng X Q, Im S J, Jang S H, et al. Luminescent properties of (Y,Gd)BO3:Bi3+,RE3+ (RE=Eu,Tb) phosphor under VUV/UV excitation [J]. Journal of Luminescence, 2006, 121(1): 1-6. |
| [7] | Jong S B, Byung S Y, Jung H K. Luminescence characteristics of pulsed-laser-ablated Y1.35Gd0.6O3:Eu3+ thin-film phosphors [J]. J. Appl. Phys., 2005, 98(4): 043513-1-5. |
| [8] | Dorenbos P. The Eu3+ charge transfer energy and the relation with the band gap of compounds [J]. J. Lumin., 2005, 111(1-2): 89-104. |
| [9] | 刘晃清,秦伟平,张继森. ZrO2中Eu3+的发光特性 [J]. 光谱与光谱分析, 2005, 25(1): 19. Liu H Q, Qin W P, Zhang J S. Luminescence properties of Eu3+ ions in nanocrystalline Zirconia[J]. Spectroscopy and Spectral Analysis, 2005, 25(1): 19. |




