2. 聊城市中医医院 脾胃科, 山东 聊城, 252000
2. Department of Spleen and Stomach, Liaocheng Hospital of Traditional Chinese Medicine, Liaocheng 252000, Shandong, P. R. China
急性胰腺炎是因胰酶异常激活造成胰腺出现局部炎症反应的严重疾病,患者临床表现为持续性、急性腹痛、恶心、呕吐、发热等症状,轻型急性胰腺炎患者经治疗后可恢复健康,但重型急性胰腺炎患者死亡率高达15%~30%[1]。因此,早期诊断急性胰腺炎、准确判定病情,对患者的临床治疗及预后评估具有十分重要的作用。目前,血淀粉酶(SAMY)是临床诊断急性胰腺炎的最常用生化检测指标,SAMY在发病早期即可升高,而尿淀粉酶(UAMY)升高比SAMY晚,但也呈现逐渐升高趋势[2]。胰脂肪酶(LPS)主要来源于胰腺的腺泡细胞,它是唯一合成LPS的场所,LPS是一种比淀粉酶更特异的急性胰腺炎诊断指标[3]。但生化指标容易受其他疾病等影响,其检查结果缺乏一定的特异性[4]。近年来,随着影像学技术的不断发展,多层螺旋CT(MSCT)检查逐渐广泛应用于多种胃肠道疾病的临床诊疗中[5], MSCT检查通过对胰腺及周围情况进行扫描,同时对其他器官进行检查,可有效提高急性胰腺炎的诊断准确率[6]。为此,本研究对我院收治的80例急性胰腺炎患者均给予MSCT平扫、动态增强扫描检查及生化指标检测,分析检查结果并探讨MSCT检查联合SAMY、UAMY、LPS检测对急性胰腺炎的诊断价值。
1 资料与方法 1.1 一般资料选取2018年6月~2019年6月我院收治的80例急性胰腺炎患者作为观察对象,其中,男48例、女32例;年龄25~67岁,平均(41.3±3.4)岁。纳入标准:①所有患者均符合《中国诊治指南》(2014版)[7]中关于急性胰腺炎的诊断标准:患者出现急性持续性的腹痛、腹胀、恶心、呕吐;血清淀粉酶或脂肪酶浓度高于正常上限值3倍以上;腹部影像学检查可见胰形态影像学改变;符合2项以上指征者可诊断为急性胰腺炎;②临床病例资料完整,均行MSCT检查和生化指标检测;③患者及家属均知情并签署知情同意书。排除标准:①有腹部手术史;②合并严重感染性疾病;③严重肝肾功能不全;④合并腹腔、腹膜后间隙肿瘤;⑤人血白蛋白 < 30 g/L。另选取同期健康体检者80例作为对照组:男52例、女28例;年龄26~70岁,平均(42.8±3.7)岁。本研究经我院医学伦理委员会批准,两组患者一般资料比较差异均无统计学意义(P>0.05),具有可比性。
1.2 方法 1.2.1 生化指标检测所有受试者均抽取静脉血并留取新鲜尿液标本5 mL,血液标本室温静置凝血后分离血清。采用速率法检测SAMY、UAMY和LPS水平。检测试剂盒由宁波美康生物科技有限公司提供,所有操作均严格按照试剂说明书进行。若SAMY水平>220 U/L判定为阳性,UAMY水平>500 U/L判定为阳性,LPS水平>51.3 U/L判定为阳性[8]。
1.2.2 MSCT检查采用西门子Sensation 64排螺旋CT扫描仪对患者进行平扫和动态增强扫描检查。患者检查前4~6 h均保持空腹,于检查前0.5 h口服2%~3%的泛影葡胺500 mL,并于扫描前口服相同剂量和浓度的造影剂,保证患者胃肠等充分充盈,暴露胰腺轮廓,以便清晰观测。扫描参数:螺距1.0,电压120 V,电流80~259 mA,重建层厚度2~5 mm。患者取仰卧位后进行屏气,扫描范围自膈顶开始至双肾以下,注意胰腺要扫描完全。平扫结束后,以3.0 mL/s的速率,利用高压注射器经肘静脉注对比剂碘海醇,浓度300 mgI/mL,对比剂用量100 mL。动态增强扫描动脉期开始时间为静脉注射后25~30 s,专扫描胰腺,门静脉期扫描开始时60 s后,扫描范围自膈顶开始向下至胰腺各部显示为止。将获取图像分析处理成像。
1.3 观察指标观测急性胰腺炎MSCT影像学表现;比较观察组和对照组患者SAMY、UAMY、LPS水平;比较不同检查方式诊断急性胰腺炎的灵敏度和特异性。
1.4 统计学方法采用SPSS 18.0软件进行数据分析,计量资料以(x±s)表示,采用t检验,计数资料以百分率(%)表示,采用χ2检验,P < 0.05为差异有统计学意义。
2 结果 2.1 急性胰腺炎MSCT影像学表现MSCT检出急性水肿型胰腺炎53例、急性坏死型胰腺炎27例。急性水肿型胰腺炎,MSCT表现为胰腺体积可见正常或轻度局限性/弥漫性增大,且基本均匀性强化,胰腺密度可表现为正常或轻度降低,以均匀或不均匀形式呈现(图 1),且胰腺轮廓清楚或模糊,部分可见胰周积液和肾前筋膜增厚。急性坏死型胰腺炎,MSCT表现为胰腺体积明显增大,且表现为散在点状、斑片状或大片状低密度灶或在密度减低区夹杂密度增高影,形态不规则,胰腺轮廓模糊,而渗出水肿区的CT值可降低,坏死区CT值降低更为明显,当出现出血时可表现为CT值升高(图 2)。动态增强扫描可见急性水肿型胰腺炎增强呈现均匀性强化,而急性坏死型胰腺炎表现为不均匀强化,其中坏死区不强化,而胰腺正常组织强化。

|
图 1 男,31岁,MSCT扫描示胰腺形态正常,密度无明显改变,仅有胰周少量渗出,左肾前筋膜增厚 |
|
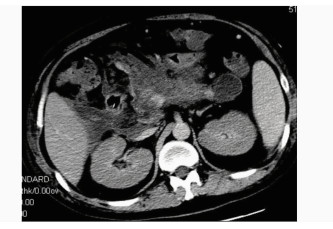
图 2 男,41岁,MSCT扫描示胰腺明显肿大,胰腺水肿、坏死,实质密度减低,胰周脂肪间隙模糊、密度增高,左侧肾筋膜增厚 |
观察组患者SAMY、UAMY、LPS水平均明显高于对照组,差异有统计学意义(P < 0.05),详见表 1。
| 表 1 两组患者生化指标检测结果(x±s) |
MSCT检查联合SAMY、UAMY、LPS检测诊断急性胰腺炎的灵敏度和特异性均明显高于各单项及多项结合检查,差异有统计学意义(P < 0.05),详见表 2。
| 表 2 不同检查方式诊断急性胰腺炎的灵敏度和特异性(%) |
急性胰腺炎是临床常见的急腹症,具有发病急、进展快、易恶化的特点,如不及时治疗患者死亡率较高[9]。急性胰腺炎的致病因素较多,如药物、酗酒、胆总管结石、内分泌异常等,在这些因素的影响下机体内胰酶被大量激活,导致胰腺组织自身消化、胰腺及周围组织出现水肿、出血或坏死等[10]。在胰腺组织出现炎症反应的同时,炎症因子还可通过淋巴道及血管流到其他组织,引发胸腔积液、心包积液、脏器损伤等并发症,严重者可导致多系统器官功能衰竭,甚至患者死亡[11]。因此,对于急性胰腺炎的早期筛查、快速诊断和及时治疗尤为重要。
目前,临床诊断急性胰腺炎常用的生化检测指标仍然是SAMY和UAMY[12]。急性胰腺炎发病后2 h,SAMY活性迅速上升,12~24 h达最高峰[13];而UAMY则大约于发病后12~24 h始升高,而且下降比SAMY慢,因而在急性胰腺炎后期更有价值[14]。但淀粉酶的合成除胰腺外,还有其他组织器官来源,如某些胆管疾病、肠道梗阻等患者的SAMY、UAMY也会增加,而且当胰腺组织广泛坏死时,急性胰腺炎患者的SAMY水平反而会正常甚至下降,因此,仅仅依靠SAMY、UAMY来诊断急性胰腺炎是不可靠的[15]。当发生急性胰腺炎时,腺泡细胞损伤会导致LPS分泌剧烈增加,且其活性维持升高的时间较淀粉酶更长,故更易检测到LPS水平变化[16]。本研究结果显示,观察组患者SAMY、UAMY、LPS水平均明显高于对照组(P < 0.05),且SAMY联合UAMY、LPS检测诊断急性胰腺炎的灵敏度和特异性分别为90.2%、89.4%,表明生化指标检测能够有效诊断急性胰腺炎。
超声、CT及MRI是临床诊断急性胰腺炎的主要影像学检查手段,超声检查通过观察胰头、胰尾、胰体厚度及回声情况诊断急性胰腺炎,经济方便,但由于容易受到胃肠道积气、腹壁脂肪等因素的影响,超声检查的诊断准确率较低[17]。MRI的诊断准确率高、特异性强,但是MRI检查时间长,危重患者难以坚持,并且MRI机房磁场较强,一些含金属的抢救设备不能进入,影响患者的救治[18]。MSCT的空间分辨率高,可对细微结构进行观察,并且不受气体、脂肪的影响,可快速确定胰腺病变程度和病变范围,是临床诊断急性胰腺炎的有效影像学方法,对于评估患者的病情及预后具有重要作用[19]。由于MSCT具有更快的扫描速度和更高的空间及密度分辨率,还可对不同病理类型胰腺炎的组织学结构进行清晰显示,有助于急性胰腺炎的早期定性诊断[20]。如对于急性水肿型胰腺炎,MSCT扫描表现为胰腺体积基本正常,胰腺密度可未见明显改变或轻度降低,且胰腺轮廓清楚或模糊,部分可见胰周积液和肾前筋膜增厚。对于急性坏死型胰腺炎,MSCT扫描表现为胰腺体积明显增大,且表现为散在点状、斑片状或大片状低密度灶或在密度减低区夹杂密度增高影,形态不规则,胰腺轮廓模糊。进一步增强扫描可见急性水肿型胰腺炎增强呈现均匀性强化,而急性坏死型胰腺炎表现为不均匀强化,其中坏死区不强化,而胰腺正常组织强化。本研究结果显示,MSCT检查联合SAMY、UAMY、LPS检测诊断急性胰腺炎的灵敏度和特异性均明显高于各单项及多项结合检查(P < 0.05),表明MSCT检查联合生化指标检测可提高诊断急性胰腺炎的灵敏度和特异性,有助于临床早期诊断急性胰腺炎。
综上所述,MSCT检查可准确显示胰腺病灶部位、病变范围及程度,有助于急性胰腺炎的早期定性诊断,联合生化指标检测,可提高诊断急性胰腺炎的灵敏度和特异性,具有重要的临床应用价值。
| [1] |
杨珠莹, 谢齐贵, 陈湛蕾, 等. 血清CRP与PCT及脂肪酶对重症急性胰腺炎患者发生感染性胰腺坏死的预测[J]. 中华医院感染学杂志, 2018, 28(11): 1693-1696. |
| [2] |
朱红梅. 急性胰腺炎患者S-Amy、U-Amy、LPS、TAP及CRP水平检测的临床价值评估[J]. 河北医药, 2016, 38(1): 81-83. |
| [3] |
张振. 血淀粉酶、尿淀粉酶、胰脂肪酶和降钙素原的检测对急性胰腺炎的诊断价值[J]. 国际检验医学杂志, 2015, 36(10): 1444-1445. |
| [4] |
夏艳丽. MSCT联合血清AMY、LPS水平检测在急性胰腺炎患者病情评估中的应用价值[J]. 现代医用影像学, 2018, 27(2): 539-540. |
| [5] |
李嫚华, 张文, 向晓辉, 等. 胸腹并发症CT征象、血钙、血清C反应蛋白对急性胰腺炎患者病情严重程度的评估价值[J]. 临床肝胆病杂志, 2019, 35(8): 1766-1769. |
| [6] |
林凌霄, 施洪, 陶超超, 等. 胰腺增强CT实质期与门静脉期联合评估对急性坏死性胰腺炎的早期诊断价值[J]. 临床与病理杂志, 2018, 38(8): 1687-1692. |
| [7] |
刘希龙, 刘日旭. 淀粉酶、脂肪酶和C反应蛋白联合检测在急性胰腺炎早期诊断中的价值[J]. 国际检验医学杂志, 2017, 38(21): 2979-2981. |
| [8] |
穆峰, 王一民, 何文进, 等. 多层CT联合血清淀粉酶、脂肪酶浓度检测在急性胰腺炎诊断中的应用[J]. 河北医药, 2016, 38(12): 1775-1778. |
| [9] |
Wang J, Zhang C, Xu P, et al. Phosphoinositide 3-kinase/protein kinase B regulates inflammation severity via signaling of Toll-like receptor 4 in severe acute pancreatitis[J]. Molecular Medicine Reports, 2018, 17(6): 7835-7844. |
| [10] |
张剑, 魏殿军. 血淀粉酶、胰脂肪酶、PCT、CRP联合检测在急性胰腺炎中的诊断价值[J]. 中国实验诊断学, 2017, 21(5): 778-780. |
| [11] |
Dixit A K, Sarver A E, Yuan Z, et al. Comprehensive analysis of microRNA signature of mouse pancreatic acini:overexpression of miR-21-3p in acute pancreatitis[J]. American Journal of Physiology Gastrointestinal and Liver Physiology, 2016, 311(5): 974-980. |
| [12] |
陈翠连, 王明林, 袁启奎, 等. 常见生化指标联合检测对急性胰腺炎病情严重程度的评估价值[J]. 重庆医学, 2017, 46(31): 4402-4404. |
| [13] |
高娟, 刘静. 急性胰腺炎早期诊断中血清脂肪酶、淀粉酶、C反应蛋白联合检验的临床价值[J]. 现代消化及介入诊疗, 2017, 22(3): 325-327. |
| [14] |
党云超, 许红梅. 螺旋CT灌注技术联合生化指标检测在急性胰腺炎诊断及病情评估中的应用研究[J]. 中国CT和MRI杂志, 2018, 16(6): 71-73, 80. |
| [15] |
张颖惠. S-Amy、U-Amy、LPS、TAP及CRP联合检测诊断急性胰腺炎患者的实效性评价[J]. 中国民康医学, 2015, 27(9): 85-93. |
| [16] |
孙广晓, 陈勉, 洗丽娜, 等. 血清C反应蛋白、降钙素原及脂肪酶联合检测对重症急性胰腺炎发生后期感染性胰腺坏死的预判价值[J]. 广东医学, 2016, 37(18): 2768-2770. |
| [17] |
黄莺, 李奇林, 张存程, 等. 老年急性胰腺炎彩色多普勒超声和多层螺旋CT检查的影像学表现及检出率比较[J]. 中国老年学杂志, 2018, 38(8): 1854-1856. |
| [18] |
韩高飞, 卫一宾, 张炽, 等. 磁共振弥散加权成像联合CT检测在急性胰腺炎中的诊断价值研究[J]. 中国医学装备, 2019, 16(1): 61-64. |
| [19] |
徐婷婷, 张珂珂. 多层螺旋CT检查联合血清淀粉酶、脂肪酶检测在诊断急性胰腺炎中的应用价值[J]. 当代医药论丛, 2019, 17(9): 179-180. |
| [20] |
钟燕, 陈兵阳. 多层螺旋CT联合S-Amy、U-Amy及LPS生化指标检测对急性胰腺炎的诊断价值研究[J]. 中国CT和MRI杂志, 2019, 17(7): 92-95. |



